
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
MINISTERSTWO EDUKACJI
NARODOWEJ
Jolanta Łagan
Józefa Wójcik
Badanie toksyn w środowisku naturalnym
i przemysłowym 311[02].Z3.02
Poradnik dla nauczyciela
Wydawca
Instytut Technologii Eksploatacji – Państwowy Instytut Badawczy
Radom 2007

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
1
Recenzenci:
mgr Urszula Ciosk-Rawluk
dr Robert Rochel
Opracowanie redakcyjne:
mgr Jolanta Łagan
Konsultacja metodyczna:
mgr inż. Gabriela Poloczek
Poradnik stanowi obudowę dydaktyczn
ą
programu jednostki modułowej 311[02].Z3.03,
„Badanie toksyn w środowisku naturalnym i przemysłowym”, zawartego w modułowym
programie nauczania dla zawodu technik analityk.
Wydawca
Instytut Technologii Eksploatacji – Państwowy Instytut Badawczy, Radom 2007

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
2
SPIS TREŚCI
1.
Wprowadzenie
3
2.
Wymagania wstępne
5
3.
Cele kształcenia
6
4.
Przykładowe scenariusze zajęć
7
5.
Ćwiczenia
13
5.1. Skażenie środowiska naturalnego
13
5.1.1. Ćwiczenia
13
5.2. Szkodliwe działanie promieniowania
17
5.2.1. Ćwiczenia
17
5.3. Bezpieczeństwo chemiczne
20
5.3.1. Ćwiczenia
20
5.4. Choroby zawodowe w świetle oceny ryzyka zawodowego
22
5.4.1. Ćwiczenia
22
6. Ewaluacja osiągnięć ucznia
24
7. Literatura
38

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
3
1. WPROWADZENIE
Przekazujemy Państwu Poradnik dla nauczyciela „Badanie toksyn w środowisku
naturalnym i przemysłowym”, który będzie pomocny w prowadzeniu zajęć dydaktycznych
w szkole kształcącej w zawodzie technik analityk 311[02].
W poradniku zamieszczono:
−
wymagania wstępne – wykaz umiejętności, jakie uczeń powinien mieć już ukształtowane,
aby bez problemów mógł korzystać z poradnika,
−
cele kształcenia – wykaz umiejętności jakie uczeń ukształtuje podczas pracy
z poradnikiem,
−
przykładowe scenariusze zajęć,
−
ć
wiczenia – przykładowe ćwiczenia ze wskazówkami do realizacji, zalecanymi metodami
nauczania – uczenia oraz środkami dydaktycznymi,
−
ewaluację osiągnięć ucznia – przykładowe narzędzie pomiaru dydaktycznego,
−
literaturę.
Wskazane jest, aby zajęcia dydaktyczne były prowadzone różnymi metodami ze
szczególnym uwzględnieniem aktywizujących metod nauczania:
−
tekstu przewodniego,
−
ć
wiczeń laboratoryjnych,
−
gier dydaktycznych,
−
metody projektów,
−
dyskusji dydaktycznej.
Formy organizacyjne pracy uczniów mogą być zróżnicowane, począwszy od
samodzielnej pracy uczniów do pracy zespołowej.
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
4
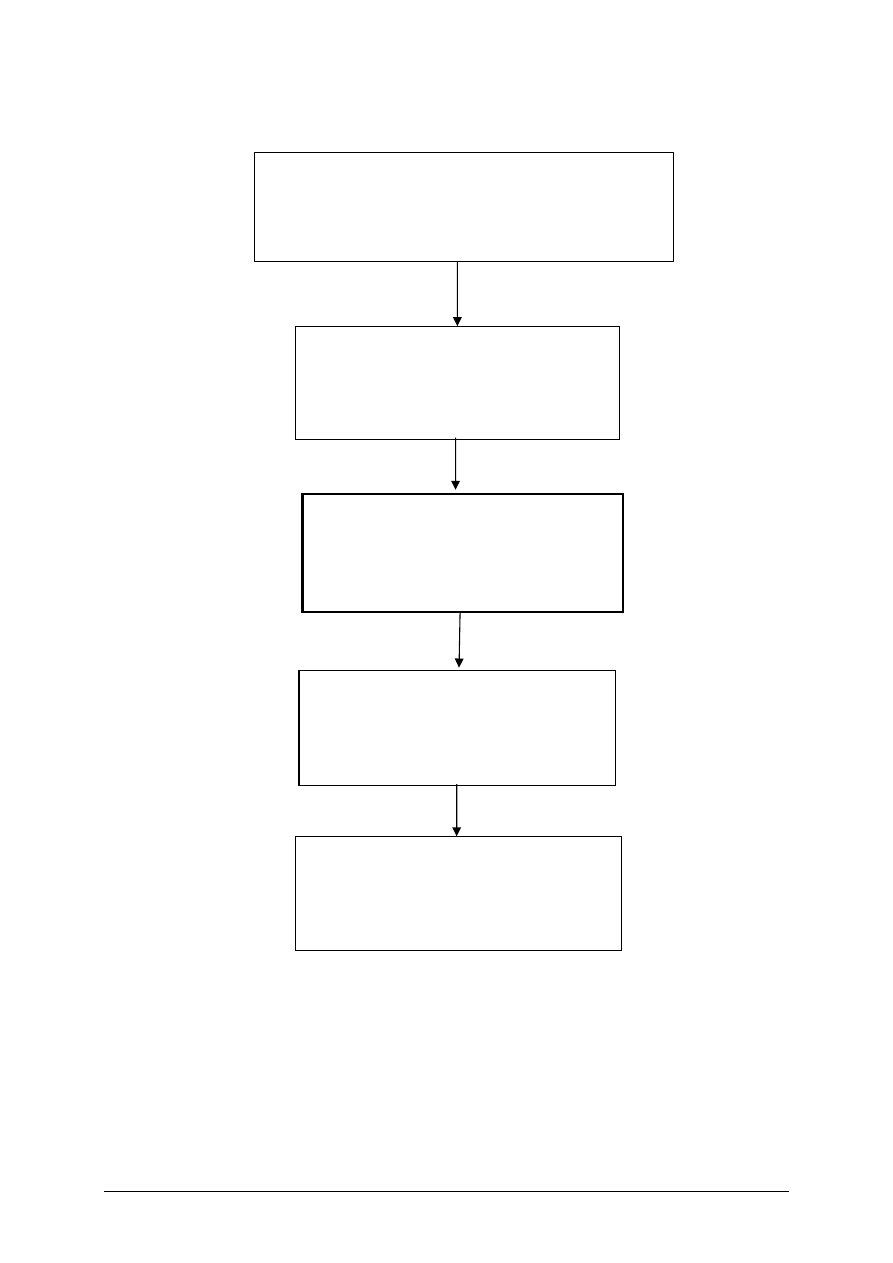
Schemat układu jednostek modułowych
311[02] Z3
Podstawowe badania toksykologiczne
311[02].Z3.02
Badanie toksyn w środowisku
naturalnym i przemysłowym
311[02].Z3.01
Stosowanie podstawowych zasad
toksykologii
311[02].Z3.03
Badanie substancji toksycznych
w żywności i w środkach codziennego
użytku
311[02].Z3.04
Określanie wpływu leków i substancji
toksycznych na organizm

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
5
2. WYMAGANIA WSTĘPNE
Przystępując do realizacji programu jednostki modułowej uczeń powinien umieć:
−
przestrzegać przepisów bezpieczeństwa i higieny pracy, ochrony przeciwpożarowej
i bezpieczeństwa zdrowotnego,
−
przestrzegać zasad dobrej techniki laboratoryjnej,
−
przestrzegać zasad bezpieczeństwa podczas badania analitycznego,
−
posługiwać się nomenklaturą związków nieorganicznych i organicznych,
−
określać właściwości fizykochemiczne substancji nieorganicznych i organicznych,
−
sporządzać roztwory o określonym stężeniu,
−
przygotowywać próbki do analizy,
−
przygotowywać sprzęt laboratoryjny, aparaturę, odczynniki,
−
rozpoznawać rodzaje zatruć,
−
określać grupy nawozów stosowanych w rolnictwie do użyźniania gleby,
−
posługiwać się wiadomościami z zakresu przemian jądrowych,
−
korzystać z kart charakterystyk substancji niebezpiecznych,
−
korzystać z norm, przepisów, procedur i dostępnych instrukcji,
−
dokonywać oceny stopnia szkodliwości substancji zawartych w środowisku naturalnym.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
6
3. CELE KSZTAŁCENIA
W wyniku realizacji programu jednostki modułowej uczeń powinien umieć:
−
sklasyfikować i scharakteryzować trucizny i substancje niebezpieczne stosowane
w przemyśle i rolnictwie,
−
przewidzieć toksyczne działanie najgroźniejszych trucizn przemysłowych i substancji
niebezpiecznych,
−
ocenić stopień narażenia pracowników zakładu przemysłowego na substancje toksyczne
i związki niebezpieczne,
−
scharakteryzować metody kontroli i monitorowania środowiska,
−
scharakteryzować metody zapobiegania skażeniom środowiska,
−
zidentyfikować substancje toksyczne i środki niebezpieczne, zastosować środki
ostrożności,
−
przeprowadzić analizę substancji celem ustalenia stopnia czystości z zastosowaniem
metod analitycznych,
−
zastosować przepisy i normy bezpiecznego użytkowania, przechowywania i transportu
substancji chemicznych,
−
skorzystać z informacji zamieszczanych w kartach charakterystyk, normach, przepisach,
etykietach dotyczących wpływu substancji szkodliwych na organizm oraz oceny ryzyka
pracy na określonych stanowiskach,
−
rozpoznać objawy najczęstszych zatruć w praktyce przemysłowej oraz zastosować
procedury udzielania pierwszej pomocy,
−
zastosować przepisy prawa oraz bezpieczeństwa i higieny pracy dotyczące ochrony
ś
rodowiska.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
7
4. PRZYKŁADOWE SCENARIUSZE ZAJĘĆ
Scenariusz zajęć 1
Osoba prowadząca:
…………………………………………
Modułowy program nauczania:
Technik analityk 311[02]
Moduł:
Podstawowe badania toksykologiczne 311[02].Z3
Jednostka modułowa:
Badanie toksyn w środowisku naturalnym
i przemysłowym 311[02].Z3.02
Temat: Oznaczanie i znaczenie tlenu zawartego w wodzie.
Cel ogólny: Kształtowanie postawy odpowiedzialności za stan jakości zbiorników wodnych.
Po zakończeniu zajęć edukacyjnych uczeń powinien umieć:
−
określić źródła zanieczyszczenia zbiorników wodnych,
−
określić wpływ czynników fizycznych na rozpuszczalność tlenu w wodzie,
−
zdefiniować jednostki określające zawartość tlenu w wodzie,
−
podać metody oznaczania tlenu zawartego i rozpuszczonego w wodzie,
−
określić znaczenie tlenu zawartego w wodzie,
−
określić przemiany chemiczne zachodzące w wodzie z udziałem tlenu,
−
wymienić i opisać sposoby oznaczania tlenu w wodzie i ściekach,
−
wykonać oznaczanie tlenu w wodzie,
−
wykonać obliczenia dla określenia zawartości tlenu w wodzie.
Metody nauczania–uczenia się:
−
dyskusja dydaktyczna,
−
ć
wiczenie praktyczne.
Formy organizacyjne pracy uczniów:
–
praca indywidualna,
–
praca zespołowa.
Czas: 180 minut.
Uczestnicy:
−
uczniowie szkoły kształcącej w zawodzie technik analityk.
Środki dydaktyczne:
−
foliogramy,
−
prezentacja multimedialna,
−
szkło laboratoryjne,
−
odczynniki,
−
instrukcje do ćwiczeń.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
8
Przebieg zajęć:
1.
Wprowadzenie.
2.
Dyskusja na temat zanieczyszczenia wód.
3.
Prezentacja pt. Badania jakości wody w stacji Sanepidu.
4.
Foliogramy prezentujące informacje dotyczące oznaczania tlenu w wodzie (metoda
Winklera, oznaczanie chemicznego zapotrzebowania na tlen ChZT, oznaczanie
biochemicznego zapotrzebowania na tlen BZT
5
).
5.
Ć
wiczenia praktyczne.
Wskazówki do realizacji:
–
zalecana praca w grupach 2 - 3 osobowych,
–
każda grupa wykonuje oznaczenie tej samej próbki wody ale w innej temperaturze,
nauczyciel koordynuje pracę zespołową.
Ć
wiczenie 1
Oznaczanie zawartości rozpuszczonego tlenu w wodzie metodą Winklera.
Sposób wykonania ćwiczenia
Aby wykonać ćwiczenie, powinieneś:
1)
pobrać wodę (ze studni lub rzeki) do butelki,
2)
dodać 2 cm
3
roztworu MnSO
4
i 2 cm
3
zasadowego roztworu KI,
3)
zatkać szczelnie korkiem butelkę (bez pęcherzyków powietrza),
4)
wymieszać dokładnie zawartość butelki,
5)
pozostawić butelkę w ciemnym miejscu do opadnięcia osadu,
6)
dodać pod powierzchnię cieczy 1 cm
3
stężonego H
2
SO
4
tak, aby nie było pęcherzyków
powietrza,
7)
zamknąć butelkę korkiem,
8)
wymieszać do całkowitego rozpuszczenia osadu,
9)
pozostawić do wydzielenia wolnego jodu (od 5–10 minut),
10)
pobrać do kolby stożkowej 100 cm
3
roztworu,
11)
miareczkować roztworem Na
2
S
2
O
3
do jasno słomkowego zabarwienia,
12)
dodać 1 cm
3
roztworu skrobi,
13)
miareczkować do odbarwienia roztworu,
14)
odczytać i zapisać objętość zużytego Na
2
S
2
O
3,
15)
obliczyć zawartość tlenu rozpuszczonego w wodzie korzystając ze wzoru:
x =
V
V 1000
2
,
0
1
⋅
⋅
[mgO
2
/dm
3
]
V
1
– objętość roztworu 0,025 mol/dm
3
Na
2
S
2
O
3
zużyta do miareczkowania
wydzielonego I
2
[cm
3
],
0,2 – ilość tlenu odpowiadająca 1 cm
3
roztworu Na
2
S
2
O
3
[mg],
V – objętość próbki wody użytej do miareczkowania [cm
3
],
16)
obliczyć zawartość rozpuszczonego tlenu w wodzie w procentach masowych nasycenia
tlenem x
n
w zadanej temperaturze ze wzoru:
x
n
=
t
x
x 100
⋅
[%]

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
9
x – ilość tlenu oznaczona w mgO
2
/dm
3
x
t
– maksymalna zawartość tlenu w wodzie destylowanej w danej temperaturze
(odczytać z odpowiedniej tabeli chemicznej)
17)
zapisać wnioski z ćwiczenia.
Ś
rodki dydaktyczne:
–
szkło laboratoryjne: butelka z korkiem, pipeta, kolba miarowa, kolba stożkowa, biureta,
lejek do biurety,
–
odczynniki: roztwór zasadowy KI, roztwór MnSO
4
(rozpuścić 519 g MnSO
4
⋅
5H
2
O
w kolbie miarowej o pojemności 1 dm
3
), H
2
SO
4
cz.d.a. roztwór 0,025 mol/dm
3
Na
2
S
2
O
3,
0,5% roztwór skrobii,
–
tablica rozpuszczalności tlenu w wodzie w zależności od temperatury,
–
PN – C – 04545.
6.
Prezentacja wyników przez poszczególne grupy i zapis do zbiorczej tabeli.
7.
Analiza otrzymanych wyników i sprecyzowanie wpływu temperatury na jakość wody.
8.
Burza mózgu „Znaczenie tlenu w wodzie”.
9.
Weryfikacja prezentowanych odpowiedzi.
10.
Modelowanie pozytywnych i negatywnych skutków obecności tlenu w wodzie.
11.
Synteza poznanych wiadomości – uczeń samodzielnie wypełnia kartę pracy.
12.
Podsumowanie pracy zespołu.
Zakończenie zajęć
–
wypełnianie karty pracy ucznia.
Praca domowa
Dopuszczalne stężenie fenolu w wodzie do picia wynosi 1
⋅
10
-8
mol/dm
3
. Do zbiornika
wodnego o pojemności 10
5
m
3
przedostało się z wodami ściekowymi 1 kg fenolu. Oblicz, ile
razy stężenie fenolu w ściekach zostało przekroczone.
Sposób uzyskania informacji zwrotnej od ucznia po zakończonych zajęciach:
–
anonimowe ankiety dotyczące oceny zajęć i trudności podczas realizowania zadania.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
10
Scenariusz zajęć 2
Osoba prowadząca:
…………………………………………..
Modułowy program nauczania:
Technik analityk 311[02]
Moduł:
Podstawowe badania toksykologiczne 311[02].Z3
Jednostka modułowa:
Badanie toksyn w środowisku naturalnym
i przemysłowym 311[02].Z3.02
Temat: Zanieczyszczenia litosfery.
Cel ogólny: Kształtowanie umiejętności oceny zagrożenia wynikającego z zanieczyszczenia
gleby.
Po zakończeniu zajęć edukacyjnych uczeń powinien umieć:
−
wymienić czynniki zanieczyszczające litosferę,
−
określić rolę pestycydów stosowanych do użyźniania gleby,
−
omówić procesy niszczące glebę,
−
określić sposoby ochrony gleby,
−
rozwiązywać problemy i w twórczy sposób efektywnie współdziałać w grupie,
−
posługiwać się zasadami prawidłowej komunikacji interpersonalnej,
−
prezentować znaczenie wiedzy chemicznej w rozwoju cywilizacji.
Metody nauczania–uczenia się:
−
dyskusja dydaktyczna,
−
ć
wiczenie dydaktyczne.
Ćwiczenia z zakresu analizy gleby:
Ć
wiczenie 1
Badanie odczynu gleby za pomocą papierka wskaźnikowego.
Sposób wykonania ćwiczenia
Aby wykonać ćwiczenie, powinieneś:
1)
umieścić próbki badanej gleby w probówce,
2)
dodać niewielką ilość wody destylowanej,
3)
zatkać probówkę korkiem i wstrząsać jej zawartość przez 5 minut,
4)
pozostawić probówkę do sklarowania cieczy,
5)
nanieś kroplę cieczy na papierek uniwersalny o zawężonym zakresie pH,
6)
porównać uzyskana barwę papierka z skalą,
7)
odczytać i zapisać pH.
Ś
rodki dydaktyczne:
–
próbki gleby,
–
papierek wskaźnikowy,
–
szkło laboratoryjne: probówki, korki, bagietka.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
11
Ć
wiczenie 2
Badanie przepuszczalności gleb.
Sposób wykonania ćwiczenia
Aby wykonać ćwiczenie, powinieneś:
1)
umieścić lejki w statywach,
2)
nałożyć na lejki grubą warstwę ligniny,
3)
nasypać na ligninę jednakowe próbki gleby, do każdego lejka inny rodzaj,
4)
umieścić pod lejkami zlewki,
5)
nalać na każdą próbkę gleby jednakową ilość wody,
6)
obserwować przepuszczalność gleb,
7)
zanotować obserwacje.
Ś
rodki dydaktyczne:
–
odczynniki: próbki gleby (np. glinowa, ilasta, piaskowa, torfowa),
–
szkło laboratoryjne; lejki, zlewki, bagietki,
–
lignina.
Ć
wiczenie 3
Wykrywanie zawartości węglanów w glebie.
Sposób wykonania ćwiczenia
Aby wykonać ćwiczenie, powinieneś:
1)
umieścić w parownicy kilka grudek ziemi,
2)
zwilżyć ziemię rozcieńczonym kwasem solnym,
3)
obserwować zachodzące zmiany,
4)
zanotować obserwacje,
5)
zanotować wnioski.
Ś
rodki dydaktyczne:
–
odczynniki: próbki gleby, rozcieńczony kwas solny (1:3),
–
sprzęt laboratoryjny: parownice, pipeta.
Ć
wiczenie 4
Badanie właściwości sorpcyjnych gleb.
Sposób wykonania ćwiczenia
Aby wykonać ćwiczenie, powinieneś:
1)
wlać do 3 probówek po 3 cm
3
wody zabarwionej atramentem,
2)
wsypać do 1 probówki 2 cm
3
gleby lessowej,
3)
wsypać do 2 probówki 2 cm
3
piasku kwarcowego,
4)
wymieszać zawartość probówki 1 i 2,
5)
pozostawić probówki do rozdziału,
6)
porównać barwę cieczy nad osadem z roztworem w 3 probówce,
7)
zapisać obserwacje.
Ś
rodki dydaktyczne:
–
odczynniki: woda destylowana, próbka gleby, piasek kwarcowy, atrament,
–
szkło laboratoryjne: probówki,

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
12
Formy organizacyjne pracy uczniów:
–
praca grupowa i indywidualna.
Czas:
90minut.
Uczestnicy:
−
uczniowie szkoły kształcącej w zawodzie technik analityk.
Środki dydaktyczne:
−
foliogramy,
−
prezentacja multimedialna „ Gleba – fizykochemiczna struktura”,
−
próbki gleb, glina, piasek,
−
odczynniki chemiczne,
−
sprzęt laboratoryjny.
Przebieg zajęć:
1.
Wprowadzenie do tematu.
2.
Obejrzenie prezentacji multimedialnej – „Struktura i skład gleby”.
3.
Praca w grupach, uczniowie wykonują ćwiczenia z zakresu analizy gleby.
4.
Prezentacja wyników poszczególnych grup ćwiczeniowych.
5.
Omówienie procesów niszczących glebę z wykorzystaniem foliogramów.
6.
Burza mózgów dotycząca zagadnienia - „Sposoby ochrony gleb”.
7.
Weryfikacja udzielonych odpowiedzi.
8.
Synteza nowych treści – uczeń wypełnia kartę pracy.
9.
Podsumowanie zajęć.
Zakończenie zajęć
−
wypełnianie kart pracy ucznia,
−
synteza nowych treści,
−
ocena pracy uczniów.
Praca domowa
1. Wyszukaj informacje na temat gospodarstw ekologicznych w Polsce.
2. Dokonaj oceny wpływu stężenia soli kuchennej na wzrost rzeżuchy. W tym celu wykonaj
ć
wiczenie.
Sposób wykonania ćwiczenia:
1)
posiej rzeżuchę na pięciu szalkach Petriego wyłożonych wilgotną ligniną,
2)
podlewaj wszystkie próbki wodą do momentu wykiełkowania,
3)
jedną próbkę podlewaj cały czas wodą,
4)
każdą z próbek podlewaj przez 10 dni roztworem soli kuchennej o innym stężeniu, np.:
0,1%, 0,4%, 0,7%, 1,0%, 1,3%,
5)
dokonuj systematycznie pomiaru wzrostu rośliny,
6)
zanotuj obserwacje, sporządź wykres dla poszczególnych próbek zależności wysokości
roślin od kolejnego dnia wzrostu. Wyciągnij wnioski z przeprowadzonych badań.
Sposób uzyskania informacji zwrotnej od ucznia po zakończonych zajęciach:
–
anonimowe ankiety dotyczące oceny zajęć i trudności podczas realizowania zadania.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
13
5. ĆWICZENIA
5.1. Skażenie środowiska naturalnego
5.1.1. Ćwiczenia
Ćwiczenie 1
Oznacz metodą amerykańską związki organiczne zawarte w wodzie i w ściekach (ChZT).
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia nauczyciel powinien omówić zakres
i technikę wykonania ćwiczenia. Ćwiczenie wykonujemy w grupach dwuosobowych.
Nauczyciel koordynuje pracę grup. W oparciu o uzyskane wyniki badań należy zestawić
z uczniami zbiorczą tabelę i przeanalizować z wynikami normatywnymi. Przewidywany czas
trwania ćwiczenia 135 minut.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
zorganizować stanowisko pracy zgodnie z wymaganiami bezpieczeństwa i higieny pracy,
2)
odmierzyć 10 cm
3
badanych ścieków do kolby miarowej o pojemności 125 cm
3
,
3)
dodać do kolby 25 cm
3
mieszaniny utleniającej,
4)
dodać 0,5 g siarczanu (VI) srebra i 0,5 g siarczanu (VI) rtęci,
5)
ogrzać mieszaninę do 168ºC,
6)
ochłodzić mieszaninę,
7)
dodać 25 cm
3
wody destylowanej i ochłodzić do temperatury pokojowej,
8)
dodać 2–3 cm
3
wskaźnika ferroiny,
9)
miareczkować solą Mohra do zmiany zabarwienia z niebiesko – zielonego na czerwono –
niebieski,
10)
powtórzyć czynności dla kolejnych próbek ścieków,
11)
wykonać ślepą próbę z 10 cm
3
wody destylowanej,
12)
wyznaczyć stężenie soli Mohra:
–
miareczkować ślepą próbę,
–
dodać 10 cm
3
dichromianu (VI) potasu do zmiany barwy na zielono – żółtą,
–
miareczkować solą Mohra (nie dodawać wskaźnika),
–
obliczyć stężenie molowe korzystając ze wzoru:
c
x
=
k
V
V
1
10
⋅
c
x
– poszukiwane stężenie molowe [mol/dm
3
]
V
k
– objętość roztworu, którego miano nastawiamy [cm
3
]
V
1
–objętość roztworu o znanym mianie [cm
3
]
13)
powtórzyć czynności dla próbki wody,
14)
obliczyć ChZT dla wody i ścieków ze wzoru:
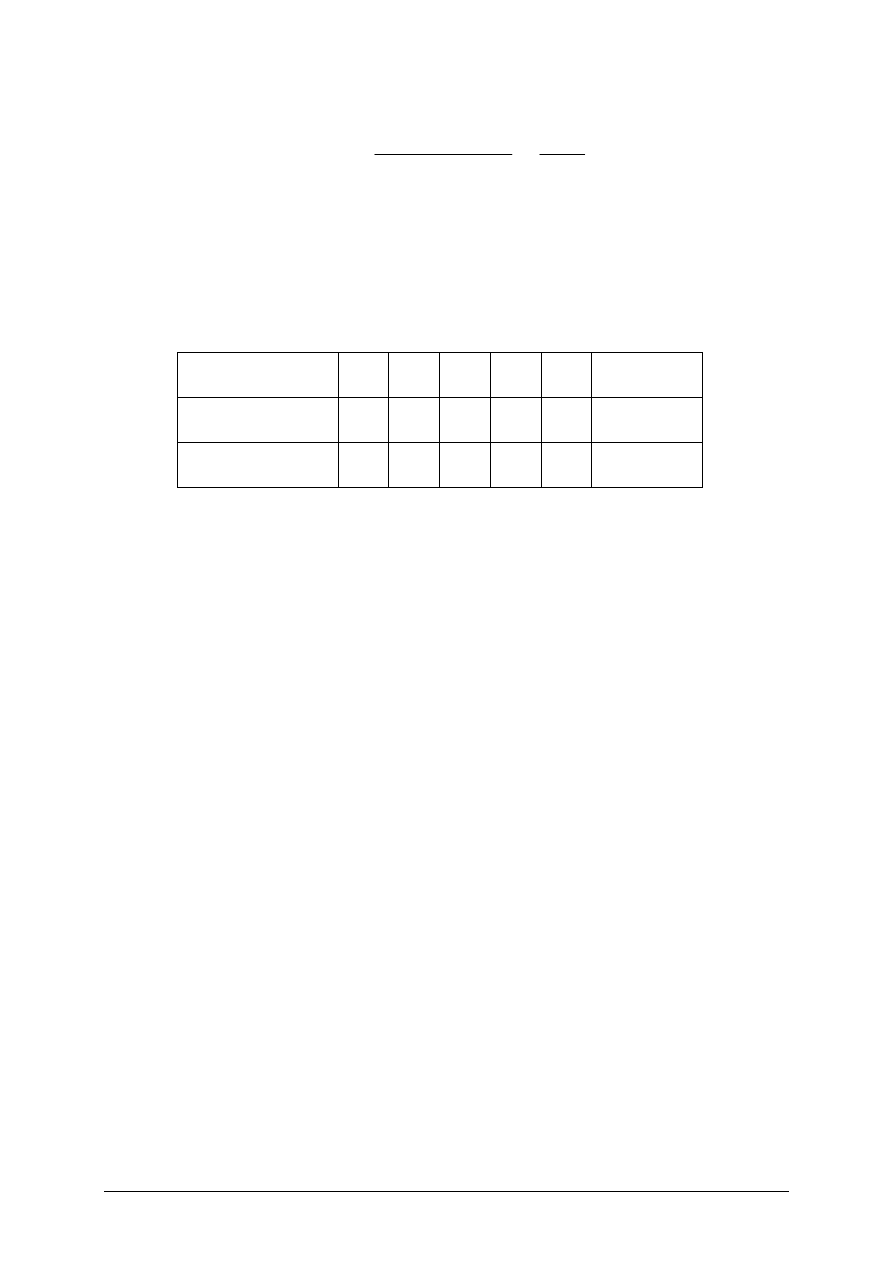
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
14
ChZT =
V
c
a
b
x
1000
8
)
(
⋅
⋅
⋅
−
3
2
dm
mgO
V – obj
ę
to
ść
próbki pobranej do analizy [cm
3
]
a – obj
ę
to
ść
soli Mohra zu
ż
yta na miareczkowanie badanej próbki [cm
3
]
b – obj
ę
to
ść
soli Mohra zu
ż
yta na miareczkowanie
ś
lepej próby [cm
3
]
c
x
– st
ęż
enie soli Mohra [mol/dm
3
]
8 – współczynnik przeliczeniowy wyniku na mg tlenu
15)
zestawi
ć
wyniki w tabeli,
Rodzaj próbki
V
1
V
2
V
3
V
śr
b–a
ChZT
[mgO
2
/dm
3
]
Próbka badana (a)
Ś
lepa próba (b)
16)
dokona
ć
oceny ilo
ś
ciowej badanej próbki z wymogami normatywnymi,
17)
dokona
ć
neutralizacji odczynników i uporzadkowa
ć
stanowisko pracy.
Zalecane metody nauczania–uczenia si
ę
:
–
ć
wiczenie laboratoryjne,
–
dyskusja dydaktyczna.
Ś
rodki dydaktyczne:
–
szkło laboratoryjne: cylindry, kolbki sto
ż
kowe, zlewka, biureta, lejek do biurety, pipety,
–
sprz
ę
t laboratoryjny: łapa do biurety, gruszka, tryskawka, termometr, waga analityczna,
–
sprz
ę
t ochrony indywidualnej: r
ę
kawice, okulary ochronne, fartuch ochronny,
–
odczynniki: mieszanina utleniaj
ą
ca: 2,4518 g K
2
Cr
2
O
7
rozpu
ś
ci
ć
w 1 dm
3
st
ęż
onego
H
2
SO
4,
doda
ć
1 cm
3
st
ęż
onego H
3
PO
4
, roztwór 0,05 mol/dm
3
soli Mohra, roztwór
0,05 mol/dm
3
dichromianu (VI) potasu (K
2
Cr
2
O
7
), siarczan (VI) srebra, siarczan (VI)
rt
ę
ci, 1% roztwór 1,1 – siarczanu ferroiny (wska
ź
nik), woda destylowana bez w
ę
glanów,
–
próbka wody i
ś
cieków,
–
norma badania wody PN: C – 04578.
Ćwiczenie 2
Oznacz w nawozach fosforowych zawarto
ś
ci fosforu obecnego w postaci zwi
ą
zków
rozpuszczalnych w wodzie.
Wskazówki do realizacji
Przed przyst
ą
pieniem do realizacji
ć
wiczenia nauczyciel powinien omówi
ć
zakres
i technik
ę
wykonania
ć
wiczenia.
Ć
wiczenie wykonujemy w grupach dwuosobowych.
Nauczyciel koordynuje prac
ą
grup. Przewidywany czas trwania
ć
wiczenia 135 minut.
Sposób wykonania
ć
wiczenia
Ucze
ń
powinien:
1)
zorganizowa
ć
stanowisko pracy zgodnie z wymaganiami bezpiecze
ń
stwa i higieny pracy,

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
15
2)
utrzeć próbkę nawozu w moździerzu,
3)
przesiać próbkę przez sito o średnicy oczek 0,5 mm,
4)
odważyć na wadze analitycznej około 5 g rozdrobnionej próbki,
5)
przenieść odważkę nawozu do zlewki,
6)
dodać do zlewki 200 cm
3
wody destylowanej (odmierzonej cylindrze miarowym),
7)
przykryć zlewkę szkiełkiem zegarkowym,
8)
zmieszać zawartość zlewki mieszadełkiem na mieszadle magnetycznym przez 30 minut,
9)
pozostawić zlewkę do sedymentacji,
10)
przesączyć roztwór do suchej zlewki,
11)
pobrać pipetą 50 cm
3
przesączu do kolbki stożkowej o pojemności 500 cm
3
,
12)
dodać do kolbki stożkowej 150 cm
3
wody destylowanej i 3 krople oranżu metylowego,
13)
miareczkować roztworem 0,1 mol/dm
3
NaOH do zmiany barwy wskaźnika z czerwonej
na żółtą,
14)
dodać 50 cm
3
roztworu chlorku wapnia, 3 krople fenoloftaleiny,
15)
oziębić zlewkę do temperatury 14ºC,
16)
miareczkować roztworem 0,5 mol/dm
3
NaOH do wyraźnej zmiany barwy roztworu na
kolor malinowy,
17)
powtórzyć czynności dla kolejnych próbek,
18)
obliczyć zawartość w procentach masowych wolnego kwasu ortofosforowego
w przeliczeniu na P
2
O
5
według wzoru:
x
1
=
50
250
007098
,
0
⋅
⋅
⋅
m
V
⋅
100%
x
1
– zawarto
ść
wolnego H
3
PO
4
w przeliczeniu na P
2
O
5
V – obj
ę
to
ść
roztworu NaOH o st
ęż
eniu 0,1 mol/dm
3
zu
ż
yta na miareczkowanie
wobec oran
ż
u metylowego [cm
3
]
0,007098 – ilo
ść
P
2
O
5
odpowiadaj
ą
ca 1 cm
3
roztworu NaOH o st
ęż
eniu
0,1 mol/dm
3
[g/cm
3
]
m – masa badanej próbki, odwa
ż
onej do ekstrakcji [g]
19)
obliczy
ć
w procentach masowych, ł
ą
czn
ą
zawarto
ść
H
3
PO
4
i Ca(H
2
PO
4
)
2
w przeliczeniu
na P
2
O
5
według wzoru:
x
2
=
50
250
017745
,
0
⋅
⋅
⋅
m
V
·
100%
V – obj
ę
to
ść
roztworu NaOH o st
ęż
eniu 0,5 mol/dm
3
, zu
ż
yta na miareczkowanie
wobec fenoloftaleiny [cm
3
]
0, 017745 – masa P
2
O
5
odpowiadaj
ą
ca 1 cm
3
roztworu NaOH o st
ęż
eniu
0,5 mol/dm
3
[g/cm
3
]
m – masa badanej próbki, odwa
ż
onej do ekstrakcji [g]
20)
zestawi
ć
wyniki w tabeli,
21)
zaprezentowa
ć
, korzystaj
ą
c z pozycji literaturowej wpływ zawarto
ś
ci fosforu w nawozie
na uzyskiwane plony.
Zalecane metody nauczania–uczenia si
ę
:
–
ć
wiczenie laboratoryjne,
–
dyskusja dydaktyczna.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
16
Ś
rodki dydaktyczne:
–
szkło laboratoryjne: zlewka, szkiełko zegarkowe, kolba miarowa (200 cm
3
), kolba
stożkowa, lejek zwykły, pipeta, biureta, cylinder miarowy, sączek,
–
sprzęt laboratoryjny: moździerz, mieszadło magnetyczne, sito o średnicy oczek 0,5 mm,
waga analityczna,
–
odczynniki: roztwór 0,5 mol/dm
3
i 0,1 mol/dm
3
NaOH, fenoloftaleina, oranż metylowy,
roztwór 30% CaCl
2
,
–
próbki nawozu fosforowego,
–
literatura wskazana przez nauczyciela,
–
PN – C – 05537.
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
17
5.2. Szkodliwe działanie promieniowania
5.2.1. Ćwiczenia
Ćwiczenie 1
Okres połowicznego rozpadu izotopu
Po
209
84
wynosi 102 lata. Sporządź wykres zależności
masy pierwiastka od czasu i odczytaj z wykresu:
–
masę pierwiastka, który powstanie z próbki o masie 100 mg po upływie 155 lat,
–
czas, po którym z próbki o masie 100 mg pozostało 12,5 mg pierwiastka.
Przedstaw zastosowanie okresu półtrwania w metodach radioizotopowych.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia nauczyciel powinien omówić zakres
i sposób wykonania ćwiczenia. Ćwiczenie wykonujemy w grupach dwuosobowych.
Nauczyciel koordynuje pracą grup. W oparciu o zaprezentowane przykłady zastosowania
radioizotopów należy przedyskutować z uczniami znaczenie izotopów w medycynie.
Przewidywany czas trwania ćwiczenia 45 minut.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
uzupełnić tabelę odpowiednimi wartościami,
Tabela do ćwiczenia 1
2)
dobrać jednostkę i nanieś na osie współrzędnych wartości z tabeli,
3)
wykreślić krzywą zależności m = f(
τ
1/2
),
4)
znaleźć na osi czasu wartość t = 155 lat,
5)
odczytać z osi masy wartość dla 155 lat i zaznaczyć punkt,
6)
znaleźć na osi masy wartość m = 12,5 mg,
7)
odczytać z osi czasu wartość dla 12,5 mg i zaznaczyć punkt,
8)
zobaczyć film o zastosowaniu w badaniach radioizotopowych okresu półtrwania,
9)
zanotować przykłady zastosowania czasu półtrwania w badaniach radioizotopowych.
Zalecane metody nauczania–uczenia się:
–
zadanie praktyczne,
–
dyskusja dydaktyczna.
Ś
rodki dydaktyczne:
–
film,
–
przybory papiernicze,
–
kalkulator.
Okres półtrwania
Lata
Masa pierwiastka
τ
1/2
2
τ
1/2
3
τ
1/2
4
τ
1/2
5
τ
1/2

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
18
Ćwiczenie 2
Podczas badania szczątków tkaniny znalezionych w starożytnym grobowcu stwierdzono,
ż
e zmierzona intensywność rozpadu promieniotwórczego
14
C
jest ośmiokrotnie niższa niż
w przypadku świeżo sporządzonej tkaniny. Oblicz wiek znaleziska i zapoznaj się z metodą
radiowęglową stosowaną w badaniach archeologicznych.
Skorzystaj ze standardowego wzoru związanego z obliczeniami dotyczącymi okresu czasu
półtrwania.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia nauczyciel powinien omówić zakres
i sposób wykonania ćwiczenia. Ćwiczenie wykonujemy w grupach dwuosobowych.
Nauczyciel koordynuje pracą grup. W oparciu o zaprezentowane wyniki przedyskutować
z uczniami celowość prowadzenia badań radiowęglowych. Przewidywany czas trwania
ć
wiczenia 45 minut.
I
=
2
1
2
1
0
τ
t
I
⋅
I – intensywność rozpadu
I
o
– intensywność początkowa
t – czas
τ
– okres półtrwania
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
wypisać dane z ćwiczenia,
2)
odszukać wartość półtrwania
14
C,
3)
zapisać odpowiedni wzór,
4)
wstawić wartości do wzoru,
5)
rozwiązać równanie wykładnicze,
6)
zapisać odpowiedź do ćwiczenia,
7)
przedstawić istotę metody radiowęglowej.
Zalecane metody nauczania–uczenia się:
–
ć
wiczenie praktyczne,
–
dyskusja dydaktyczna.
Ś
rodki dydaktyczne:
–
poradnik fizykochemiczny,
–
literatura wskazana przez nauczyciela.
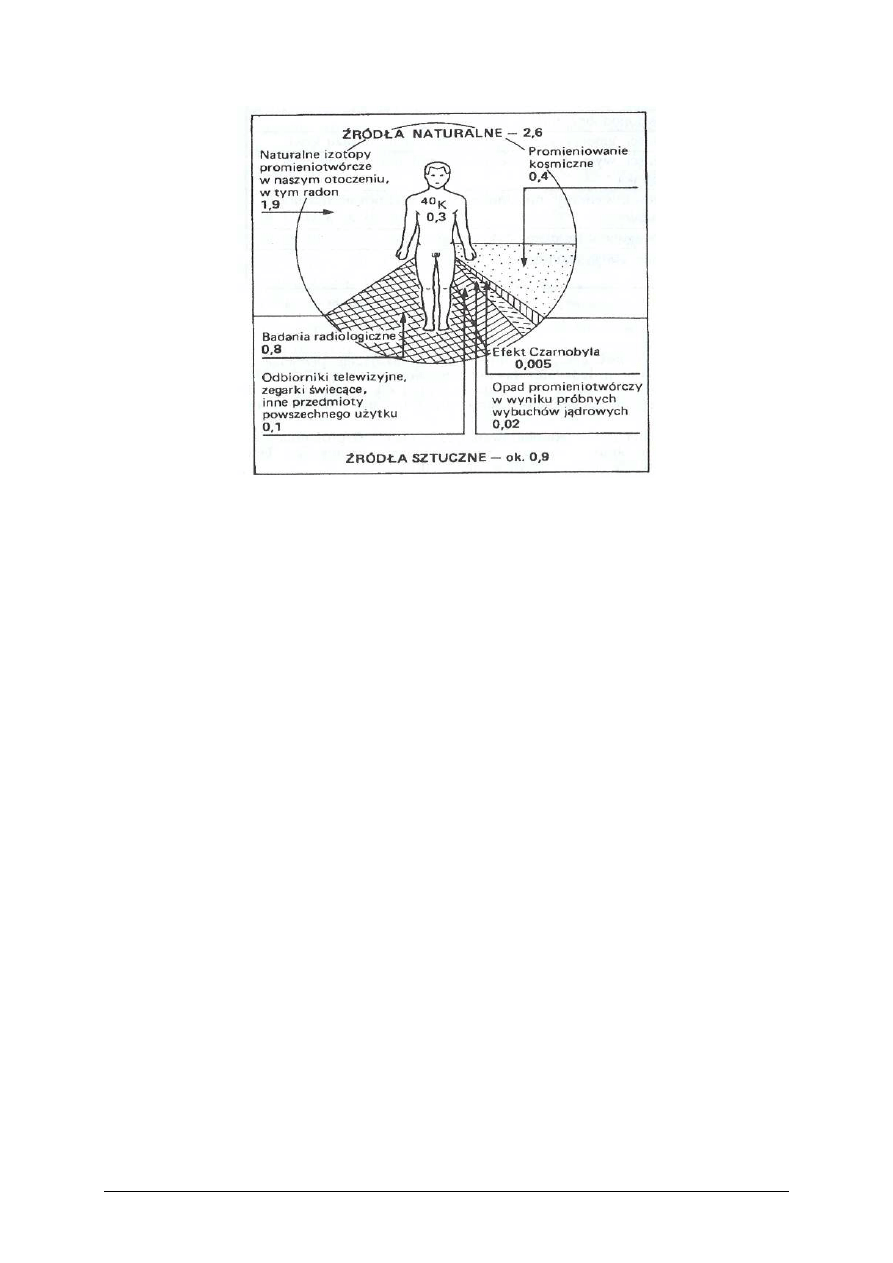
Ćwiczenie 3
Promieniowanie jonizujące oddziaływuje na człowieka z różnych źródeł. Analizując
roczne dawki (w mSv) promieniowania (rysunek do ćwiczenia), oblicz dawkę jaką otrzymuje
w ciągu roku statystyczny Polak. Określ procentowy udział promieniowania pochodzenia
naturalnego i sztucznego. Podaj przykłady katastrof jądrowych, jakie wydarzyły się na
ś
wiecie i oceń ich wpływ na środowisko i poszczególne organy wewnętrzne człowieka.
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
19
Rysunek 1 do ćwiczenia 3. Orientacyjne dawki roczne, jakie otrzymuje
człowiek z różnych źródeł promieniowania
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia nauczyciel powinien omówić zakres
i sposób wykonania ćwiczenia. Ćwiczenie wykonujemy w grupach dwuosobowych.
Nauczyciel koordynuje pracą grup. W oparciu o zebrane wiadomości przedyskutować
z uczniami szkodliwość badań jądrowych dla środowiska. Przewidywany czas trwania
ć
wiczenia 45 minut.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
zapoznać się z dołączonym rysunkiem do ćwiczenia,
2)
zsumować wartości dawek z poszczególnych źródeł promieniowania,
3)
obliczyć procent udziału promieniowania naturalnego,
4)
obliczyć procent udziału promieniowania sztucznego,
5)
odszukać wiadomości dotyczące katastrof ekologicznych,
6)
wybrać przykłady katastrof jądrowych mających miejsce na świecie,
7)
zaprezentować skutki oddziaływania odszukanych katastrof na środowisko,
8)
zaprezentować skutki oddziaływania odszukanych katastrof na organizm człowieka,
9)
wykreślić na podstawie zebranych danych diagram pokazujący opad substancji
promieniotwórczej na tereny skażone w zależności od roku wydarzenia,
10)
dokonać oceny rozwoju radioaktywności we współczesnym świecie.
Zalecane metody nauczania–uczenia się:
–
ć
wiczenie praktyczne,
–
dyskusja dydaktyczna.
Ś
rodki dydaktyczne:
–
Internet,
–
literatura,
–
kalkulator.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
20
5.3. Bezpieczeństwo chemiczne
5.3.1. Ćwiczenia
Ćwiczenie 1
Roztwór amoniaku z zakładu produkcyjnego należy przetransportować do innych
zakładów w których amoniak jest surowcem do otrzymywania tworzyw sztucznych.
Zaproponuj bezpieczny przewóz amoniaku. Określ rodzaje zagrożenia dla organizmu
i środowiska w przypadku wycieku substancji.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia nauczyciel powinien omówić zakres
i sposób wykonania ćwiczenia. Ćwiczenie wykonujemy w grupach dwuosobowych.
Nauczyciel koordynuje pracą grup. W oparciu o zaprezentowany dobór środków ochrony
indywidualnej przeanalizować z uczniami właściwy dobór środków ochrony indywidualnej.
Przewidywany czas trwania ćwiczenia 45 minut.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
skorzystać z dostępnych źródeł informacji na temat amoniaku,
2)
zaproponować opis zgodnie z wymogami określonymi w umowie Europejskiej ADR
transportu amoniaku,
3)
ocenić drogi narażenia organizmu na amoniak,
4)
określić objawy toksyczne w przypadku narażenia amoniakiem,
5)
dobrać środki ochrony indywidualnej dla ochrony zdrowia w kontakcie z amoniakiem,
6)
oznakować substancje odpowiednimi symbolami.
Zalecane metody nauczania–uczenia się:
–
ć
wiczenie praktyczne,
–
dyskusja dydaktyczna.
Ś
rodki dydaktyczne:
–
znaki ADR,
–
symbole oznakowania substancji niebezpiecznych,
–
Karta Charakterystyki amoniaku,
–
Internet.
Ćwiczenie 2
W laboratorium do analizy powietrza kopalnianego stosuje się analizator SRG składający
się ze szklanych płuczek zawierających: rtęć, P
2
O
5
i inne substancje chemiczne. Podczas
sprawdzania szczelności aparatury płuczka z rtęcią uległa stłuczeniu. Płuczka zawierała
25 cm
3
rtęci. Oceń narażenie pracownika – laboranta na pary rtęci w ciągu 8 godzinnego dnia
pracy. Zaproponuj sposób neutralizacji i usunięcia rozlanej cieczy.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia nauczyciel powinien omówić zakres
i sposób wykonania ćwiczenia. Ćwiczenie wykonujemy w grupach dwuosobowych.
Nauczyciel koordynuje pracą grup. W oparciu o zebrane wiadomości przedyskutować

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
21
z uczniami szkodliwość działania substancji toksycznych stosowanych w analizach
chemicznych na zdrowie pracownika. Przewidywany czas trwania ćwiczenia 45 minut.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
skorzystać z dostępnych źródeł na temat bezpieczeństwa pracy z rtęcią,
2)
ocenić drogi narażenia organizmu na rtęć,
3)
określić objawy toksyczne działania rtęci na organizm,
4)
dobrać środki ochrony indywidualnej do likwidacji rtęci,
5)
dobrać bezpieczny sposób neutralizacji likwidacji rozlanej rtęci,
6)
dokonać oszacowania pochłoniętej dawki rtęci w godzinach pracy.
Zalecane metody nauczania–uczenia się:
–
ć
wiczenie praktyczne,
–
dyskusja dydaktyczna.
Ś
rodki dydaktyczne:
–
Karta Charakterystyki rtęci,
–
literatura,
–
Internet.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
22
5.4. Choroby zawodowe w świetle oceny ryzyka zawodowego
5.4.1. Ćwiczenia
Ćwiczenie 1
Dokonaj opisu stanowiska pracy dla zawodu – spawacz w celu oceny narażenia
zawodowego.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia nauczyciel powinien omówić zakres
i sposób wykonania. Praca przebiega indywidualnie. W oparciu o zebrane wiadomości
uczniowie dokonują wnikliwej analizy. Czas wykonania ćwiczenia 45 minut.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
zebrać informacje dotyczące rodzaju i przebiegu procesu spawania,
2)
sporządzić listę stosowanych substancji i preparatów chemicznych,
3)
zapoznać się z chronometrażem pracy poszczególnych pracowników,
4)
wykonać zestawienie liczby pracowników, w tym kobiet i mężczyzn,
5)
zaproponować zestaw środków ochrony indywidualnej i zbiorowej,
6)
zapoznać się z chorobami zawodowymi występującymi u spawaczy,
7)
zgłosić potrzebę profilaktycznych zaleceń medycznych,
8)
zaproponować rozwiązania organizacyjne na stanowisku spawacza,
9)
prześledzić wyniki pomiarów substancji szkodliwych na stanowisku pracy,
10)
ocenić szkodliwość warunków pracy na zdrowie pracownika,
11)
sporządzić protokół analizy stanowiska pracy.
Zalecane metody nauczania–uczenia się:
–
ć
wiczenie praktyczne,
–
dyskusja dydaktyczna.
Ś
rodki dydaktyczne:
–
dokumentacja lekarska,
–
wywiad z pracownikami,
–
raport z obserwacji stanowiska pracy,
–
karty substancji szkodliwych,
–
znaki bezpieczeństwa substancji szkodliwych,
–
normy oznaczeń substancji szkodliwych.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
23
Ćwiczenie 2
Pyły występujące na różnych stanowiskach pracy mogą wykazywać szkodliwe działanie
na organizm pracownika. Dokonaj analizy działania pyłów na układ oddechowy człowieka na
podstawie informacji zawartych w tabeli.
Tabela do ćwiczenia 2
Zawód pracownika
Czynnik toksyczny
Obraz kliniczny
Choroba zawodowa
drewno
zapalenie płuc
rozedma
węglik krzemu
mika
górnik dołowy
nafta, benzyna
nauczyciel
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia nauczyciel powinien omówić zakres
i sposób wykonania. Ćwiczenie przeprowadzamy w grupach dwuosobowych. W oparciu
o zebrane wiadomości uczniowie dokonują wnikliwej analizy. Czas wykonania ćwiczenia 20
minut.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
prześledzić budowę i choroby układu oddechowego,
2)
sporządzić listę zawodów, w których zachorowalność pracownika w ciągu 5 lat pracy
według badań statystycznych była największa,
3)
skorzystać z literatury lub poradnika medycznego w celu odszukania objawów
klinicznych towarzyszących przykładowym chorobom zawodowym,
4)
przeanalizować Karty Charakterystyk substancji szkodliwych,
5)
prześledzić listę chorób zawodowych,
6)
uzupełnić tabelę wpisując w puste miejsca odpowiednie wiadomości,
7)
zaprezentować wyniki ćwiczenia.
Zalecane metody nauczania–uczenia się:
–
ć
wiczenie praktyczne,
–
dyskusja dydaktyczna.
Ś
rodki dydaktyczne:
–
literatura medyczna: Vademecum zatruć, Poradnik medyczny, Słownik medyczny,
–
karty charakterystyk substancji szkodliwych,
–
lista chorób zawodowych.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
24
6. EWALUACJA OSIĄGNIĘĆ UCZNIA
Przykłady narzędzi pomiaru dydaktycznego
Test 1
Test dwustopniowy do jednostki modułowej „Badanie toksyn w środowisku
naturalnym i przemysłowym”
Test składa się z 22 zadań wielokrotnego wyboru, z których:
−
zadania 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 15, 16, 18 są z poziomu podstawowego,
−
zadania 13, 14, 17, 19, 20, 21, 22 są z poziomu ponadpodstawowego.
Punktacja zadań: 0 lub 1 punkt
Za każdą prawidłową odpowiedź uczeń otrzymuje 1 punkt. Za złą odpowiedź lub jej brak
uczeń otrzymuje 0 punktów.
Proponuje się następujące normy wymagań – uczeń otrzyma następujące
oceny szkolne:
−
dopuszczający – za rozwiązanie co najmniej 10 zadań z poziomu podstawowego,
−
dostateczny – za rozwiązanie co najmniej 12 zadań z poziomu podstawowego,
−
dobry – za rozwiązanie 16 zadań, w tym co najmniej 3 z poziomu ponadpodstawowego,
−
bardzo dobry – za rozwiązanie 20 zadań, w tym co najmniej 5 z poziomu
ponadpodstawowego.
Klucz odpowiedzi: 1. c, 2. d, 3. b, 4. a, 5. b, 6. b, 7. b, 8. c, 9. c, 10. d, 11. a,
12. d, 13. c, 14. a, 15. d, 16. b, 17. a, 18. a, 19. d, 20. b, 21. d, 22. b.
Plan testu
Nr
zad.
Cel operacyjny
(mierzone osiągnięcia ucznia)
Kategoria
celu
Poziom
wymagań
Poprawna
odpowiedź
1
Przedstawić cechy chorobowe układów
człowieka
B
P
c
2
Rozróżnić rodzaj pyłu wywołującego
chorobę zawodową
B
P
d
3
Przedstawić istotę zjawiska
zachodzącego w zanieczyszczonym
ś
rodowisku
B
P
b
4
Nazwać proces powstający w wyniku
działalności człowieka
A
P
a
5
Znać instytucje zajmujące się
określaniem normatywów wody
A
P
b
6
Rozróżnić pyły stanowiące składnik
zanieczyszczenia atmosfery
B
P
b

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
25
7
Wymienić substancję będącą
przyczyną skażeń radioaktywnych
A
P
b
8
Znać źródła zanieczyszczenia
powietrza
A
P
c
9
Nazwać substancje powodujące trwałe
zanieczyszczenie wód
A
P
c
10
Wymienić metody oznaczania tlenu w
wodzie
A
P
d
11
Wyjaśnić wpływ substancji
toksycznych w wodzie na ich stan
chemiczny
B
P
a
12
Rozróżnić czynniki chemiczne mające
wpływ na stan gleb
B
P
d
13
Obliczyć zadanie z zakresu
promieniotwórczości
C
PP
c
14
Ocenić szkodliwość dawki
promieniowania
D
PP
a
15
Przedstawić zastosowanie
radioizotopów
B
P
d
16
Rozróżnić czynniki oddziaływujące na
zdrowie człowieka
B
P
b
17
Obliczyć czas połowicznego rozpadu
pierwiastka promieniotwórczego
C
PP
a
18
Wyjaśnić określenie metody badania
fizykochemicznego wody
B
P
a
19
Ocenić wpływ zanieczyszczeń
ś
rodowiska na zdrowie
D
PP
d
20
Zanalizować przyczynę ujemnego
działania substancji w środowisku
D
PP
b
21
Zaproponować sposób zmniejszania
emisji zanieczyszczeń
D
PP
d
22
Zanalizować wiadomości potrzebne do
oceny ryzyka zawodowego
D
PP
b

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
26
Przebieg testowania
Instrukcja dla nauczyciela
1.
Ustal z uczniami termin przeprowadzenia sprawdzianu z wyprzedzeniem co najmniej
jednotygodniowym.
2.
Przygotuj odpowiednią liczbę testów.
3.
Zapewnij samodzielność podczas rozwiązywania zadań.
4.
Przed rozpoczęciem testu przeczytaj instrukcję dla ucznia.
5.
Zapytaj czy uczniowie wszystko zrozumieli.
6.
Nie przekraczaj przeznaczonego czasu na test.
Instrukcja dla ucznia
1.
Przeczytaj uważnie instrukcję.
2.
Podpisz imieniem i nazwiskiem kartę odpowiedzi.
3.
Zapoznaj się z zestawem zadań testowych.
4.
Udzielaj odpowiedzi na załączonej karcie odpowiedzi, wstawiając w odpowiedniej
rubryce znak X. W przypadku pomyłki należy błędną odpowiedź zaznaczyć kółkiem
a następnie ponownie zaznaczyć odpowiedź prawidłową.
5.
Test zawiera 22 zadań o różnym stopniu trudności.
6.
Do każdego zadania dołączone są 4 możliwe odpowiedzi. Tylko jedna jest prawdziwa.
7.
Pracuj samodzielnie, bo tylko wtedy będziesz miał satysfakcję z wykonanego zadania.
8.
Kiedy udzielanie odpowiedzi będzie Ci sprawiało trudność, wtedy odłóż jego
rozwiązanie na później i wróć do niego, gdy zostanie Ci wolny czas.
9.
Na rozwiązanie testu masz 40 min.
Powodzenia
Materiały dla ucznia:
–
instrukcja,
–
zestaw zadań testowych,
–
karta odpowiedzi.
ZESTAW ZADAŃ TESTOWYCH
1.
Pylica to
a)
choroba wątroby powodująca marskość narządu.
b)
choroba układu krwiotwórczego, polegająca na uszkodzeniu krwinek czerwonych
przez pył dostający się do organizmu człowieka.
c)
choroba układu oddechowego, powodująca jego przewlekłe stany zapalne.
d)
choroba układu pokarmowego, powodująca zapalenie dwunastnicy.
2.
Krzemica to choroba wywołana przez pył
a)
gipsowy.
b)
drzewny.
c)
wapienny.
d)
kwarcowy.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
27
3.
Biodegradacja oznacza
a)
zanik przemian metabolicznych u roślin.
b)
naturalny rozkład substancji organicznych przez mikroorganizmy.
c)
anomalie rozwojowe u zwierząt pod wpływem zanieczyszczenia powietrza.
d)
wynaturzenie zwierząt pod wpływem zanieczyszczeń gazowych.
4.
Proces wzmożenia organicznego wzbogacania wód przez działalność gospodarczą
człowieka określa się mianem
a)
eutrofizacji.
b)
jarowizacji.
c)
humifikacji.
d)
nitrofizacji.
5.
O dopuszczeniu wody do celów pitnych decyduje
a)
Wydział
Ochrony
Ś
rodowiska
Gospodarki
Wodnej
i
Geologii
Urzędu
Wojewódzkiego.
b)
Stacja Sanitarno – Epidemiologiczna.
c)
Ośrodek Badań i Kontroli Środowiska.
d)
Ośrodek Kontroli Przestrzegania Dopuszczalnych Stężeń.
6.
Ze względu na oddziaływanie na ludzki organizm pyły dzielimy na
a)
pochodzenia organicznego i nieorganicznego.
b)
toksyczne, pylicotwórcze, uczulające, drażniące.
c)
drobnoziarniste i gruboziarniste.
d)
mineralne i kopalniane.
7.
Pierwiastkiem, który wskazuje na skażenie środowiska po katastrofie w Czarnobylu jest
a)
ołów.
b)
cez.
c)
jod.
d)
potas.
8.
Wśród zanieczyszczeń powietrza są węglowodory, których źródłem są
a)
gazy spalinowe i gazy koksownicze.
b)
pyły przemysłowe i surowce energetyczne.
c)
gazy spalinowe i surowce energetyczne.
d)
gazy przemysłowe i gazy spalinowe.
9.
Trwałe zanieczyszczenia wód są spowodowane przez
a)
rozpuszczony tlen.
b)
obecność glonów.
c)
sole metali ciężkich.
d)
butwiejące szczątki organiczne.
10.
Zawartość tlenu w wodzie można oznaczyć metodą
a)
tylko Winklera.
b)
tylko ChZT.
c)
tylko BZT
5
.
d)
Winklera, ChZT oraz BZT
5
.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
28
11.
Fenole przedostające się do wód są niebezpieczne z powodu
a)
reaktywności z zawartym w wodzie wodociągowej chlorem.
b)
zmiany składu substancji mineralnych stałych wody.
c)
aktywności chemicznej z zawartym w wodzie tlenem.
d)
zasadowości wody.
12.
Zakwaszenie gleb nie jest spowodowane
a)
hydrolizą zawartych w glebie soli.
b)
nitryfikacją związków zawartych w glebie.
c)
kwaśnymi opadami deszczu.
d)
dysocjacją stosowanych nawozów sztucznych.
13.
Z 1 g radu o okresie połowicznego rozpadu równym 1600 lat pozostanie po upływie
8000 lat około
a)
1 mg.
b)
3 mg.
c)
30 mg.
d)
5 mg.
14.
Ś
miertelna dawka promieniowania LD
30
50
dla człowieka waha się w granicach od 3–4 Gy.
Późniejsze skutki takiego promieniowania mogą spowodować u człowieka
a)
uszkodzenie szpiku kostnego.
b)
zaburzenia układu pokarmowego.
c)
egzemę skóry.
d)
zmiany w narządzie słuchu.
15.
Radioizotopy mają szerokie zastosowanie, wykorzystuje się je
a)
tylko medycynie podczas sterylizacji sprzętu medycznego.
b)
tylko geologii przy badaniu wieku skał.
c)
tylko radiacyjnej konserwacji żywności.
d)
medycynie podczas sterylizacji sprzętu medycznego, geologii przy badaniu wieku
skał, radiacyjnej konserwacji żywności.
16.
Bezpośrednie oddziaływanie pyłów na układy i narządy ludzkie nie zależy od
a)
rodzaju pyłów.
b)
wilgotności powietrza.
c)
wielkości cząstek.
d)
składu chemicznego pyłów.
17.
Z próbki o masie początkowej 0,16 g próbki po upływie 176 dni zostało 0,04 g próbki.
Czas połowicznego rozpadu pewnego pierwiastka wynosi
a)
88 dni.
b)
58 dni.
c)
28 dni.
d)
68 dni.
18.
BZT
5
to
a)
biochemiczne zapotrzebowanie na tlen w ciągu 5 dni.
b)
biologiczne zapotrzebowanie na tlen w ciągu 5 dni.
c)
biochemiczne zapotrzebowanie na tlen w ciągu 5 minut.
d)
biologiczne zapotrzebowanie na tlen w ciągu 5 godzin.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
29
19.
Zanieczyszczenia środowiska są powodem wzrostu zachorowań na
a)
białaczkę, rozedmę płuc.
b)
ołowicę, grypę.
c)
gruźlicę, białaczkę.
d)
ołowicę, zapalenie płuc.
20.
Freony stanowią zagrożenie dla biosfery ze względu na
a)
przynależność do pochodnych węglowodorów.
b)
powstający chlor pełniący rolę katalizatora w reakcjach rodnikowych.
c)
szerokie zastosowanie w urządzeniach chłodniczych.
d)
wzrost produkcji tych związków.
21.
Nieprawidłowy sposób zmniejszania emisji zanieczyszczeń podczas spalania paliw to
a)
zmiana technologii.
b)
oczyszczenie paliwa.
c)
oczyszczanie spalin.
d)
stosowanie surowców zawierających domieszki.
22.
Dla oceny ryzyka zawodowego zbędne są informacje o
a)
opisie stanowiska pracy.
b)
chronometrażu pracy pracowników.
c)
pomiarze stężeń substancji chemicznych.
d)
wskaźnikach narażenia.
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
30
KARTA ODPOWIEDZI
Imię i nazwisko..........................................................................................
Badanie toksyn w środowisku naturalnym i przemysłowym
Zakreśl poprawną odpowiedź
.
Nr
zadania
Odpowiedź
Punkty
1.
a
b
c
d
2.
a
b
c
d
3.
a
b
c
d
4.
a
b
c
d
5.
a
b
c
d
6.
a
b
c
d
7.
a
b
c
d
8.
a
b
c
d
9.
a
b
c
d
10.
a
b
c
d
11.
a
b
c
d
12.
a
b
c
d
13.
a
b
c
d
14.
a
b
c
d
15.
a
b
c
d
16.
a
b
c
d
17.
a
b
c
d
18.
a
b
c
d
19.
a
b
c
d
20.
a
b
c
d
21.
a
b
c
d
22.
a
b
c
d
Razem:

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
31
Test 2
Test dwustopniowy do jednostki modułowej „Badanie toksyn w środowisku
naturalnym i przemysłowym”
Test składa się z 22 zadań wielokrotnego wyboru, z których:
−
zadania 2, 3, 4, 5, 6, 7, 9, 10, 12, 13, 14, 17, 19, 21, 22 są z poziomu podstawowego,
−
zadania 1, 8, 11, 15, 16, 18, 20 są z poziomu ponadpodstawowego.
Punktacja zadań: 0 lub 1 punkt
Za każdą prawidłową odpowiedź uczeń otrzymuje 1 punkt. Za złą odpowiedź lub jej brak
uczeń otrzymuje 0 punktów.
Proponuje się następujące normy wymagań – uczeń otrzyma następujące
oceny szkolne:
−
dopuszczający – za rozwiązanie co najmniej 10 zadań z poziomu podstawowego,
−
dostateczny – za rozwiązanie co najmniej 12 zadań z poziomu podstawowego,
−
dobry – za rozwiązanie 16 zadań, w tym co najmniej 3 z poziomu ponadpodstawowego,
−
bardzo dobry – za rozwiązanie 20 zadań, w tym co najmniej 5 z poziomu
ponadpodstawowego.
Klucz odpowiedzi: 1. c, 2. b, 3. b, 4. d, 5. a, 6. b, 7. c, 8. b, 9. a, 10. d, 11. a,
12. a, 13. b, 14. d, 15. c, 16. c, 17. d, 18. b, 19. d, 20. b, 21. c, 22. a
Plan testu
Nr
zad.
Cel operacyjny
(mierzone osiągnięcia ucznia)
Kategoria
celu
Poziom
wymagań
Poprawna
odpowiedź
1
Obliczyć masę pierwiastka
promieniotwórczego po upływie
określonego czasu rozpadu.
C
PP
c
2
Wyliczyć czynniki wywołujące zmiany
skórne.
A
P
b
3
Przedstawić zjawiska powstające w
zanieczyszczonych zbiornikach
wodnych
B
P
b
4
Rozróżnić rodzaj pyłu wywołującego
chorobę zawodową
B
P
d
5
Rozróżnić jednostkę odpowiedniej
dawki
B
P
a
6
Znać źródła powstawania
zanieczyszczeń w powietrzu
A
P
b
7
Rozróżnić substancje o działaniu
rakotwórczym
B
P
c
8
Obliczyć zadanie z zakresu
promieniotwórczości
C
PP
b

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
32
9
Wyjaśnić zapis metody oznaczania
tlenu w wodzie
B
P
a
10
Przedstawić drogi przedostawania się
do organizmu promieniowania
B
P
d
11
Ocenić czynniki prowadzące do
degradacji wód
D
PP
a
12
Rozróżnić parametry określające klasy
wód
B
P
a
13
Wyliczyć substancje gazowe
stanowiące zanieczyszczenie powietrza
A
P
b
14
Przedstawić działanie ozonu na
biosferę
B
P
d
15
Ocenić szkodliwość substancji na
podstawie opisu opakowania
D
PP
c
16
Zanalizować opis materiału na
transporcie
D
PP
c
17
Znać zasady ryzyka pracy w
laboratorium
A
P
d
18
Zanalizować ryzyko zachorowania na
danym stanowisku pracy
D
PP
b
19
Rozróżnić właściwy wariant
wskazujący na bezpieczeństwo w
ś
rodowisku pracy
B
P
d
20
Zanalizować działanie substancji
szkodliwej na organizm
D
PP
b
21
Rozróżnić utleniacz do metody analizy
chemicznej
B
P
c
22
Rozróżnić substancje o działaniu
drażniącym
B
P
a

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
33
Przebieg testowania
Instrukcja dla nauczyciela
1.
Ustal z uczniami termin przeprowadzenia sprawdzianu z wyprzedzeniem co najmniej
jednotygodniowym.
2.
Przygotuj odpowiednią liczbę testów.
3.
Zapewnij samodzielność podczas rozwiązywania zadań.
4.
Przed rozpoczęciem testu przeczytaj instrukcję dla ucznia.
5.
Zapytaj czy uczniowie wszystko zrozumieli.
6.
Nie przekraczaj przeznaczonego czasu na test.
Instrukcja dla ucznia
1.
Przeczytaj uważnie instrukcję.
2.
Podpisz imieniem i nazwiskiem kartę odpowiedzi.
3.
Zapoznaj się z zestawem zadań testowych.
4.
Udzielaj odpowiedzi na załączonej karcie odpowiedzi, wstawiając w odpowiedniej
rubryce znak X. W przypadku pomyłki należy błędną odpowiedź zaznaczyć kółkiem
a następnie ponownie zaznaczyć odpowiedź prawidłową.
5.
Test zawiera 22 zadań o różnym stopniu trudności.
6.
Do każdego zadania dołączone są 4 możliwe odpowiedzi. Tylko jedna jest prawdziwa.
7.
Pracuj samodzielnie, bo tylko wtedy będziesz miał satysfakcję z wykonanego zadania.
8.
Kiedy udzielanie odpowiedzi będzie Ci sprawiało trudność, wtedy odłóż jego
rozwiązanie.
9.
na później i wróć do niego, gdy zostanie Ci wolny czas.
10.
Na rozwiązanie testu masz 40 min.
Powodzenia
Materiały dla ucznia:
–
instrukcja,
–
zestaw zadań testowych,
–
karta odpowiedzi.
ZESTAW ZADAŃ TESTOWYCH
1. Paliwo atomowe zawiera 10 g radioaktywnego izotopu o okresie półtrwania równym
2 miesiące. Po dwóch latach ilość izotopu w paliwie będzie wynosić
a)
1,560 g.
b)
0,160 g.
c)
0,156 g.
d)
2,655 g.
2. Czynnikami chemicznymi wywołującymi choroby skóry są
a)
metale, detergenty, pyły.
b)
ś
rodki czyszczące, pochodne węglowodorów, metaloidy.
c)
barwniki, pestycydy, alergeny zapachowe.
d)
gazy drażniące, cement, alergeny zwierzęce.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
34
3. Eutrofizacja polega na
a)
niedoborze substancji pokarmowych w wodach.
b)
organicznym wzbogacaniu wód powierzchniowych przez działalność gospodarczą
człowieka.
c)
nadmiernym zarastaniu zbiorników wodnych i tworzeniu zbiorowisk lądowych.
d)
powstawaniu w zbiornikach wodnych gazu błotnego.
4.
Krzemica to choroba wywołana przez pył
a)
gipsowy.
b)
drzewny.
c)
wapienny.
d)
kwarcowy.
5. Jednostką dawki równoważnej jest
a)
silvert (Sv).
b)
grej (Gy).
c)
dżul (J).
d)
J
⋅
kg
-1
.
6. Za obecność w atmosferze tlenków azotu odpowiedzialne są
a)
spalanie koksu, spalanie gazu ziemnego.
b)
wyładowania atmosferyczne, rozpad substancji organicznych.
c)
oddychanie ludzi i zwierząt, wybuchy wulkanów.
d)
wybuchy wulkanów, spalanie węgla.
7.
Niebezpieczną substancją rakotwórczą powstającą wskutek rozwoju transportu
samochodowego jest
a)
1,3 – dichlorobenzen.
b)
orto – ksylen.
c)
3,4 – benzopiren.
d)
meta – ksylen.
8. Stwierdzono, że w pewnej próbce organicznej jest 60mg izotopu
14
C. Po 22920 latach
ilość izotopu w próbce będzie wynosić
a)
2,56 mg.
b)
1,56 mg.
c)
2,65 mg.
d)
1,05 mg.
9. BZT
5
– to wskaźnik jakości wody, który informuje
a)
o ilości tlenu niezbędnego do utleniania zawartych w wodzie substancji organicznych
w ciągu 5 dób.
b)
o ilości tlenu wprowadzonego do wody w celu dotlenienia organizmów żywych.
c)
o ilości tlenu powstającego na drodze redukcji substancji organicznych zawartych
w wodzie w ciągu 5 dób.
d)
o ilości tlenu otrzymanego w reakcjach redukcji substancji nieorganicznych zawartych
w wodzie.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
35
10.
90
Sr emitując promieniowanie
β
działa jonizująco na żywe komórki krwi powodując
zmiany nowotworowe w tkance kostnej i szpiku kostnym. Przenikanie strontu do
organizmu odbywa się drogą
a)
tylko pokarmową.
b)
tylko skórną.
c)
tylko oddechową.
d)
pokarmową, skórną, oddechową.
11. Degradacja wód prowadzi do powstawania ścieków, które są wynikiem
a)
spływu z pól substancji biogenicznych, środków ochrony roślin oraz przenikania
zanieczyszczeń z powietrza.
b)
działalności człowieka w gospodarstwie domowym.
c)
opadów atmosferycznych.
d)
rozwoju organizmów wodnych.
12. Wody I klasy czystości powinny służyć
a)
zaopatrzeniu ludności w wodę do picia.
b)
zaopatrzeniu hodowli zwierząt gospodarskich.
c)
nawadnianiu upraw ogrodniczych.
d)
hodowli ryb z wyjątkiem łososiowatych.
13. Najczęściej występujące gazowe skażenia atmosfery wymieniono prawidłowo w punkcie
a)
SO
2
, H
2
S, CO
2
, HCl.
b)
SO
2
, CO
2
, NO
x
.
c)
SO
2
, O
3
, CO
2
, HCl.
d)
CO
2,
NO
2
, O
3
, SO
2
.
14. Zagrożeniem dla biosfery spowodowanym zanikaniem ozonu nie jest
a)
wzrost ilości promieniowania ultrafioletowego.
b)
wzrost niebezpiecznych chorób.
c)
brak odporności w chorobach skórnych.
d)
wzrost gazów cieplarnianych.
15.
Opakowanie z substancją szkodliwą opisano R22, co oznacza że
a)
może być przyczyną raka.
b)
może upośledzić płodność.
c)
działa szkodliwe w przypadku spożycia.
d)
działa bardzo toksycznie w przypadku spożycia.
16. ADR reguluje transport towarów występujący przed numerem rozpoznawczym
niebezpieczeństwa informuje o
a)
materiale trującym.
b)
materiale łatwopalnym.
c)
materiale reagującym z wodą.
d)
materiale wybuchowym.
17. Laboratorium, w którym odbywają się ćwiczenia może funkcjonować pomimo braku:
a)
regulaminu i przepisów bezpieczeństwa i higieny pracy.
b)
Kart Charakterystyk substancji niebezpiecznych.
c)
oznakowania substancji chemicznych.
d)
wykazu sprzętu i szkła chemicznego.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
36
18. Pracownikowi na stanowisku pracy zostały przedstawione najwłaściwsze choroby
zawodowe. Błędne przyporządkowanie przedstawia
a)
rozedma płuc – muzyk instrumentów dętych.
b)
alergiczny nieżyt nosa – malarz.
c)
pylica – szlifierz.
d)
niedowład strun głosowych – nauczyciel.
19. Ryzyko średnie narażenia na substancje chemiczne w środowisku pracy cechuje
a)
wskaźniki narażenia są równe wartości dopuszczalnych NDS, NDSCh, NDSP.
b)
wskaźniki narażenia są zgodne z wartościami dopuszczalnych NDS, NDSCh, NDSP.
c)
wskaźniki narażenia są mniejsze od 0,5 wartości dopuszczalnych NDS, NDSCh,
NDSP.
d)
wskaźniki narażenia są równe lub większe od 0,5 wartości dopuszczalnych NDS,
NDSCh, NDSP.
20. Błędną informację na temat benzopirenu podaje zdanie
a)
produkt niecałkowitego spalania paliw.
b)
niebezpieczny ze względu na przedostanie się do organizmu człowieka przez skórę.
c)
przemieszcza się wraz z pyłem i wodą.
d)
pod wpływem światła, tlenu i temperatury ulega biotransformacji.
21. W oznaczaniu chemicznego zapotrzebowania na tlen (ChZT) jako utleniacza stosujemy
a)
manganian (VII) potasu.
b)
azotan (V) potasu.
c)
chromian (VI) potasu.
d)
chloran (VII) potasu.
22. Działanie drażniące na organizm człowieka wykazują
a)
amoniak, siarkowodór, kwas siarkowy(VI).
b)
chlor, fenol, tlenek siarki(IV).
c)
siarkowodór, tlenek węgla(II), chlor.
d)
chlor, kwas siarkowy(IV), tlenek węgla(IV).
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
37
KARTA ODPOWIEDZI
Imię i nazwisko..........................................................................................
Badanie toksyn w środowisku naturalnym i przemysłowym
Zakreśl poprawną odpowiedź
.
Nr
zadania
Odpowiedź
Punkty
1.
a
b
c
d
2.
a
b
c
d
3.
a
b
c
d
4.
a
b
c
d
5.
a
b
c
d
6.
a
b
c
d
7.
a
b
c
d
8.
a
b
c
d
9.
a
b
c
d
10.
a
b
c
d
11.
a
b
c
d
12.
a
b
c
d
13.
a
b
c
d
14.
a
b
c
d
15.
a
b
c
d
16.
a
b
c
d
17.
a
b
c
d
18.
a
b
c
d
19.
a
b
c
d
20.
a
b
c
d
21.
a
b
c
d
22.
a
b
c
d
Razem:

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
38
7. LITERATURA
1.
Bodzek D.: Chemia i fizykochemia substancji toksycznych i niebezpiecznych. ŚAM,
Katowice 2003
2.
Dreisbach R. H., Robertson W. O.: Vademecum zatruć. Wydawnictwo Lekarskie. PZWL,
Warszawa 1995
3.
Górny M.: Ekologia i ochrona środowiska. Polski Klub Ekologiczny, Gliwice 1996
4.
Hassa R., Mrzigod A, Mrzigod J, Sułkowski W.: Chemia. Wydawnictwo M. Rożak
Sp.z o.o. 2002
5.
Jasińska – Zubelewicz E.: Ergonomia. Toksykologia przemysłowa i środowiskowa.
OWPW, Warszawa 1996
6.
Klepaczko – Filipek B., Łoin J.: Analiza techniczna. WSiP, Warszawa 1994
7.
Lipkowska – Grabowska K.: Analiza wody i ścieków WSiP, Warszawa 1998
8.
Łopata K.: Chemia a środowiska. WSIP, Warszawa 1994
9.
Piotrowski J.: Podstawy toksykologii. WNT, Warszawa 2006
10.
Pyłka – Gutowska E.: Ekologia z ochroną środowiska. Wydawnictwo Oświata,
Warszawa 1997
11.
Rączkowski B.: BHP w praktyce. Ośrodek Doradztwa i Doskonalenia Kadr Sp.z.o.o,
Gdańsk 2000
12.
Seńczuk W.: Toksykologia. Wyd. Lekarskie PZWL, Warszawa 1999
13.
Wiśniewski H., Kowalewski G.: Ekologia z ochroną i kształtowaniem środowiska. Wyd.
AGMEN, Warszawa 2000
14.
Zawieski M. W.: Ocena ryzyka zawodowego. CIOP PIB, Warszawa 2004
15.
www.komers-
bhp.pl/substancjeniebezpieczne.html
16.
www.techem.com.pl/category_sign.php?categoryId=chemost
Literatura metodyczna:
1.
Jeruszka U., Niemierko B.: Zastosowania pomiaru sprawdzającego w kształceniu
zawodowym. MEN, Warszawa 1997
2.
Szlosek F.: Wstęp do dydaktyki przedmiotów zawodowych. ITE, Radom 1998
Wyszukiwarka
Podobne podstrony:
08 Badanie toksyn w środowisku naturalnym
08 Badanie toksyn w środowisku naturalnym
08 Badanie toksyn w środowisku naturalnym
01Higiena- wstęp,czynniki chemicznedoc, Higiena - dział medycyny zajmujący się badaniem wpływu środo
ekologia, wytyczne do referatow z ekologii 2007 08, Przedmiot: Ekologia zasobów naturalnych i ochron
08 Kubiak J i inni Badania wplywu srodowiska chlorkowego na trwalosc konstrukcji zelbetowej hali prz
2 23 lutego 2011 Izolowanie mikroorganizmów z różnych środowisk naturalnych
Higiena środowisko naturalne
sr test5, PWr, Środowisko naturalne człowieka
Ochrona środowiska naturalnego oraz utylizacja odpadów chemicznych
Srodowisko naturalne spr końcowy
rozkłady przestrzenne liczenia populacji, Ochrona środowiska, Natura 2000
śliwińska, środowisko naturalne człowieka, pytania i odpowiedzi ,Grawitaja, rodowisko?ryczne
Ściągi z fizyki-2003 r, Wpływ produkcji wytwarzania energii na środowisko naturalne
sprawdziany, Środowisko naturalne Polski B, SPRAWDZIAN WIADOMOŚCI - Środowisko naturalne Polski
Zanieczyszczenie środowiska naturalnego
więcej podobnych podstron