
„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
MINISTERSTWO EDUKACJI
NARODOWEJ
Kazimierz Olszewski
Wytwarzanie podstawowych półproduktów i produktów
organicznych 815[01].Z2.03
Poradnik dla nauczyciela
Wydawca
Instytut Technologii Eksploatacji
–
Państwowy Instytut Badawczy
Radom 2007

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
1
Recenzenci:
dr inż. Jarosław Religa
mgr Urszula Ciosk Rawluk
Opracowanie redakcyjne:
mgr inż. Kazimierz Olszewski
Konsultacja:
mgr inż. Halina Bielecka
Poradnik stanowi obudowę dydaktyczną programu jednostki modułowej 815[01].Z2.03
„Wytwarzanie podstawowych półproduktów i produktów organicznych”, zawartego
w modułowym programie nauczania dla zawodu operator urządzeń przemysłu chemicznego.
Wydawca
Instytut Technologii Eksploatacji – Państwowy Instytut Badawczy, Radom 2007

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
2
SPIS TREŚCI
1.
Wprowadzenie
3
2.
Wymagania wstępne
5
3.
Cele kształcenia
6
4.
Przykładowe scenariusze zajęć
7
5.
Ćwiczenia
11
5.1.
Technologia przerobu surowców energetycznych
11
5.1.1.
Ć
wiczenia
11
5.2.
Przemysł tłuszczowy
14
5.2.1.
Ć
wiczenia
14
5.3.
Procesy jednostkowe w syntezie organicznej
17
5.3.1.
Ć
wiczenia
17
5.4.
Przemysł tworzyw sztucznych
20
5.4.1.
Ć
wiczenia
20
5.5.
Syntezy organiczne z gazu syntezowego
24
5.5.1.
Ć
wiczenia
24
6.
Ewaluacja osiągnięć uczniów
27
7.
Literatura
40

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
3
1. WPROWADZENIE
Przekazujemy Państwu Poradnik dla nauczyciela, który będzie pomocny w prowadzeniu
zajęć dydaktycznych w szkole kształcącej w zawodzie operator urządzeń przemysłu
chemicznego
w jednostce
modułowej
„Wytwarzanie
podstawowych
półproduktów
i produktów organicznych”
W poradniku zamieszczono:
−
wymagania wstępne,
−
wykaz umiejętności, jakie uczeń opanuje podczas zajęć,
−
przykładowe scenariusze zajęć,
−
propozycje ćwiczeń, które mają na celu ukształtowanie umiejętności praktycznych
uczniów,
−
wykaz literatury, z jakiej uczniowie mogą korzystać podczas nauki.
Wskazane jest, aby zajęcia dydaktyczne były prowadzone różnymi metodami ze
szczególnym uwzględnieniem:
−
tekstu przewodniego,
−
metody projektów,
−
ć
wiczeń praktycznych.
Formy organizacyjne pracy uczniów mogą być zróżnicowane, począwszy od
samodzielnej pracy uczniów do pracy zespołowej.
Z powodu obszernego materiału nauczania objętego programem jednostki modułowej
815[01].Z2.03 w poradnikach zawarto tylko wybrane ćwiczenia zawarte w programie
jednostki jako najbardziej reprezentatywne dla specyfiki nauczania przedstawionych
w Materiale nauczania jednostki zagadnień.
W celu przeprowadzenia sprawdzianu wiadomości i umiejętności ucznia, nauczyciel
może posłużyć się zamieszczonym w rozdziale 6 zestawem zadań testowych i sprawdzianem
praktycznym. W rozdziale 6 podano również:
−
plan testu,
−
punktację zadań,
−
propozycje norm wymagań,
−
instrukcję dla nauczyciela,
−
instrukcję dla ucznia,
−
kartę odpowiedzi,
−
zestaw zadań testowych.

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
4
Schemat układu jednostek modułowych
815[01].Z2
Technologie wytwarzania
półproduktów i produktów
przemysłu chemicznego
815[01].Z2.02
Wytwarzanie podstawowych
półproduktów i produktów
nieorganicznych
815[01].Z2.03
Wytwarzanie podstawowych
półproduktów i produktów
organicznych
815[01].Z2.01
Stosowanie zasad prowadzenia
procesów produkcyjnych

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
5
2. WYMAGANIA WSTĘPNE
Przystępując do realizacji programu jednostki modułowej uczeń powinien umieć:
–
korzystać z różnych źródeł informacji,
–
wykonywać podstawowe czynności laboratoryjne,
–
posługiwać się podstawowy pojęciami i wzorami z zakresu chemii organicznej,
–
wykonywać podstawowe obliczenia chemiczne,
–
rozróżniać symbole graficzne aparatów, maszyn i urządzeń przemysłu chemicznego,
–
charakteryzować wymagania dotyczące bezpieczeństwa pracy przy obsłudze aparatów,
maszyn i urządzeń przemysłu chemicznego,
–
charakteryzować budowę i zasadę działania podstawowych aparatów maszyn i urządzeń
przemysłu chemicznego,
–
posługiwać się podstawowymi pojęciami technologicznymi,
–
rozróżniać zastosowane zasady technologiczne,
–
posługiwać się normami, ustawami, rozporządzeniami,
–
obsługiwać komputer,
–
współpracować w grupie.

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
6
3. CELE KSZTAŁCENIA
W wyniku realizacji programu jednostki modułowej uczeń powinien umieć:
−
rozróżnić surowce energochemicznie,
−
rozróżnić procesy rafineryjne od petrochemicznych,
−
określić zadania procesów przygotowania ropy naftowej do przeróbki,
−
scharakteryzować właściwości i skład destylatów naftowych otrzymywanych z ropy
naftowej,
−
wskazać kierunki oczyszczania lub dalszej przeróbki destylatów naftowych,
−
scharakteryzować przemysłowe metody sulfonowania, nitrowania, chlorowania,
estryfikacji oraz hydrolizy i utwardzania tłuszczów,
−
rozróżnić symbole aparatury, punktów pomiaru parametrów, urządzeń regulacji
i sterowania stosowanych w procesach wytwarzania półproduktów i produktów
organicznych,
−
określić wpływ zmiany parametrów procesowych na przebieg procesów wytwarzania
produktów organicznych,
−
wskazać metody wytwarzania surowego gazu syntezowego z różnych surowców,
−
uzasadnić konieczność odsiarczania produktów przerobu gazu ziemnego, ropy naftowej
i węgla kamiennego,
−
scharakteryzować budowę i zasady działania aparatów i urządzeń stosowanych
w procesach przerobu węgla kamiennego, gazu ziemnego, ropy naftowej oraz
w procesach wytwarzania podstawowych grup związków organicznych,
−
posłużyć się uproszczonymi schematami technologicznymi procesów przerobu węgla
kamiennego, gazu ziemnego oraz ropy naftowej,
−
wskazać kierunki wykorzystywania poszczególnych składników surowego gazu
syntezowego,
−
ocenić stopień zagrożenia środowiska pracy podczas eksploatacji aparatów i urządzeń
stosowanych w procesach przerobu węgla kamiennego, gazu ziemnego, ropy naftowej
oraz w procesach wytwarzania podstawowych grup związków organicznych,
−
ocenić toksyczność substancji stosowanych w procesach wytwarzania produktów
organicznych na podstawie analizy karty charakterystyki substancji niebezpiecznych,
−
scharakteryzować skład i warunki pracy katalizatorów stosowanych w procesach
wytwarzania produktów organicznych,
−
wyjaśnić, w oparciu o schemat ideowy, chemiczną koncepcję procesu wytwarzania
produktów organicznych,
−
sporządzić schematy ideowe najważniejszych procesów wytwarzania produktów
organicznych,
−
wskazać stosowanie zasad technologicznych w procesach wytwarzania produktów
organicznych,
−
rozróżnić reakcje polimeryzacji i polikondensacji,
−
scharakteryzować stosowane w przemyśle sposoby prowadzenia polimeryzacji w: masie,
zawiesinie i emulsji,
−
odróżnić zasadnicze typy tworzyw polimeryzacyjnych,
−
scharakteryzować najważniejsze parametry jakościowe benzyn,
−
ocenić wpływ na środowisko procesów komponowania i zastosowania benzyn,
−
zastosować zasady bezpieczeństwa i higieny pracy, ochrony przeciwpożarowej oraz
ochrony środowiska obowiązujące na stanowiskach pracy.

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
7
4. PRZYKŁADOWE SCENARIUSZE ZAJĘĆ
Scenariusz zajęć 1
Osoba prowadząca
……………………………………….…………………
Modułowy program nauczania:
Operator urządzeń przemysłu chemicznego 815[01]
Moduł:
Technologie wytwarzania podstawowych półproduktów
i produktów przemysłu chemicznego 815[01].Z2
Jednostka modułowa:
Wytwarzanie podstawowych półproduktów i produktów
organicznych 815[01].Z2.03
Temat: Wpływ przemysłu koksochemicznego na środowisko naturalne.
Cel ogólny: Kształtowanie umiejętności określania wpływu instalacji produkcyjnej na
ś
rodowisko naturalne.
Po zakończeniu zajęć edukacyjnych uczeń potrafi:
−
ocenić toksyczność substancji powstających w procesie koksowania węgla,
−
skorzystać z kart charakterystyki substancji niebezpiecznych,
−
wskazać wpływ instalacji koksowania węgla oraz wydzielania produktów pirolizy na stan
ś
rodowiska naturalnego.
Metody nauczania–uczenia się:
−
tekstu przewodniego.
Formy organizacyjne pracy uczniów:
−
grupowa jednolita.
Czas trwania zajęć: 1 godzina dydaktyczna.
Środki dydaktyczne:
−
karty charakterystyki substancji niebezpiecznych,
−
uproszczony schemat technologiczny koksowania węgla oraz wydzielania produktów
pirolizy,
−
literatura z rozdziału 7 poradnika dla nauczyciela.
Zadanie dla ucznia
Określ wpływ przemysłu koksochemicznego na środowisko naturalne.
W tym celu:
−
określ wpływ substancji powstających w instalacji koksochemicznej na środowisko
naturalne,
−
wypisz wpływ substancji powstających w instalacji koksochemicznej na środowisko
naturalne,
−
wypisz
możliwe
sposoby
skażenia środowiska naturalnego przez przemysł
koksochemiczny.

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
8
Przebieg zajęć:
1.
Sprawy organizacyjne.
2.
Nawiązanie do tematu, omówienie celów zajęć.
3.
Zorganizowanie stanowiska pracy do wykonania ćwiczenia.
4.
Realizacja zajęć:
–
zapoznanie się z kartami charakterystyki substancji niebezpiecznych,
–
zapoznanie się z uproszczonym schematem koksowania węgla oraz wydzielania
produktów pirolizy,
–
określenie wpływu substancji powstających w procesie koksowania węgla oraz
wydzielania produktów pirolizy na środowisko naturalne,
–
wypisanie wpływu substancji powstających w procesie koksowania węgla oraz
wydzielania produktów pirolizy na środowisko naturalne,
–
określenie możliwych sposobów skażenia środowiska naturalnego przez przemysł
koksochemiczny,
–
wypisanie możliwych sposobów skażenia środowiska naturalnego przez przemysł
koksochemiczny.
5.
Po wykonaniu ćwiczenia uczeń określa, jakie zagrożenia stanowi przemysł
koksochemiczny.
6.
Nauczyciel analizuje prace uczniów.
7.
Grupa wspólnie z nauczycielem dokonuje oceny prac.
Zakończenie zajęć
Praca domowa
Odszukaj w literaturze informacji dotyczących zastosowań koksu.
Sposób uzyskania informacji zwrotnej od ucznia po zakończonych zajęciach:
−
anonimowe ankiety ewaluacyjne dotyczące sposobu prowadzenia zajęć i zdobytych
umiejętności.

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
9
Scenariusz zajęć 2
Osoba prowadząca
……………………………………….………………….
Modułowy program nauczania:
Operator urządzeń przemysłu chemicznego 815[01]
Moduł:
Technologie wytwarzania podstawowych półproduktów
i produktów przemysłu chemicznego 815[01].Z2
Jednostka modułowa:
Wytwarzanie podstawowych półproduktów i produktów
organicznych 815[01].Z2.03
Temat: Polimeryzacja styrenu w obecności nadtlenku wodoru.
Cel ogólny: Kształtowanie umiejętności przeprowadzenia reakcji polimeryzacji inicjowanej
nadtlenkiem wodoru.
Po zakończeniu zajęć edukacyjnych uczeń potrafi:
−
przeprowadzić proces polimeryzacji inicjowanej nadtlenkiem wodoru,
−
utrzymać warunki przebiegu reakcji,
−
przestrzegać przepisy bhp i ppoż.
Metody nauczania–uczenia się:
−
ć
wiczenie laboratoryjne.
Formy organizacyjne pracy uczniów:
−
grupowa jednolita.
Czas trwania zajęć: 2 godziny dydaktyczne.
Środki dydaktyczne:
−
styren,
−
roztwór nadtlenku wodoru o stężeniu 10 %,
−
zestaw do ogrzewania z pionową chłodnicą zwrotną,
−
płaszcz grzejny,
–
instrukcja otrzymywania polistyrenu w procesie polimeryzacji inicjowanej nadtlenkiem
wodoru,
–
ś
rodki ochrony indywidualnej.
Zadanie dla ucznia
Przeprowadź reakcję polimeryzacji styrenu inicjowaną nadtlenkiem wodoru.
W tym celu:
−
sporządź wykaz niezbędnego sprzętu laboratoryjnego i odczynników,
−
zaplanuj konieczne czynności laboratoryjne,
−
określ warunki bhp niezbędne do bezpiecznego wykonywania czynności laboratoryjnych,
−
pobierz od nauczyciela niezbędny sprzęt i odczynniki,
−
przeprowadź zaplanowane czynności laboratoryjne,
−
zapisz obserwacje w dzienniku laboratoryjnym.

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
10
Przebieg zajęć:
1.
Czynności porządkowe.
2.
Omówienie celów lekcji oraz przepisów bhp.
3.
Omówienie szczegółowych zasad sporządzania sprawozdania.
4.
Ć
wiczenia praktyczne:
−
zgromadzenie niezbędnego sprzętu i odczynników,
−
zaplanowanie czynności laboratoryjnych,
−
przeprowadzenie procesu polimeryzacji styrenu.
5.
Uporządkowanie stanowiska pracy.
Zakończenie zajęć
Praca domowa
Przygotuj sprawozdanie z dzisiejszego ćwiczenia.
Sposób uzyskania informacji zwrotnej od ucznia po zakończonych zajęciach:
−
anonimowe ankiety ewaluacyjne dotyczące sposobu prowadzenia zajęć, trudności
podczas realizowania zadania i zdobytych umiejętności.

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
11
5.
ĆWICZENIA
5.1. Technologia przerobu surowców energetycznych
5.1.1. Ćwiczenia
Ćwiczenie 1
Zaproponuj produkty powstające w wyniku krakingu heptanu. Zapisz równania reakcji,
które mogą zachodzić w czasie krakingu heptanu.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać fragment
rozdziału Materiał nauczania dotyczący technologii przerobu ropy naftowej. Należy zwrócić
szczególną uwagę na zagadnienia dotyczące krakingu. Ćwiczenie może być wykonywane
indywidualnie lub w grupach 2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
określić, jakim przemianom podlegają węglowodory w czasie krakingu,
2)
zapisać wzory przewidywanych produktów krakingu heptanu,
3)
zapisać równania reakcji, które mogą zachodzić w czasie krakingu heptanu.
Zalecane metody nauczania–uczenia się:
−
pogadanka,
−
ć
wiczenie praktyczne.
Ś
rodki dydaktyczne:
−
papier formatu A4,
−
kalkulator,
−
Poradnik dla ucznia.
Ćwiczenie 2
Zaproponuj produkty powstające w wyniku reformingu heptanu. Zapisz równania reakcji,
które mogą zachodzić w czasie reformingu heptanu.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać fragment
rozdziału Materiał nauczania dotyczący technologii przerobu ropy naftowej. Należy zwrócić
szczególną uwagę na zagadnienia dotyczące reformingu. Przed przystąpieniem do realizacji
ć
wiczenia nauczyciel powinien omówić jego zakres i sposób wykonania. Ćwiczenie może być
wykonywane indywidualnie lub w grupach 2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
określić, jakim przemianom podlegają węglowodory w czasie reformingu,
2)
zapisać wzory przewidywanych produktów reformingu heptanu,
„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
12
3)
zapisać reakcje, które mogą zachodzić w czasie reformingu heptanu.
Zalecane metody nauczania–uczenia się:
−
pogadanka,
−
ć
wiczenie praktyczne.
Ś
rodki dydaktyczne:
−
papier formatu A4,
−
kalkulator,
−
Poradnik dla ucznia.
Ćwiczenie 3
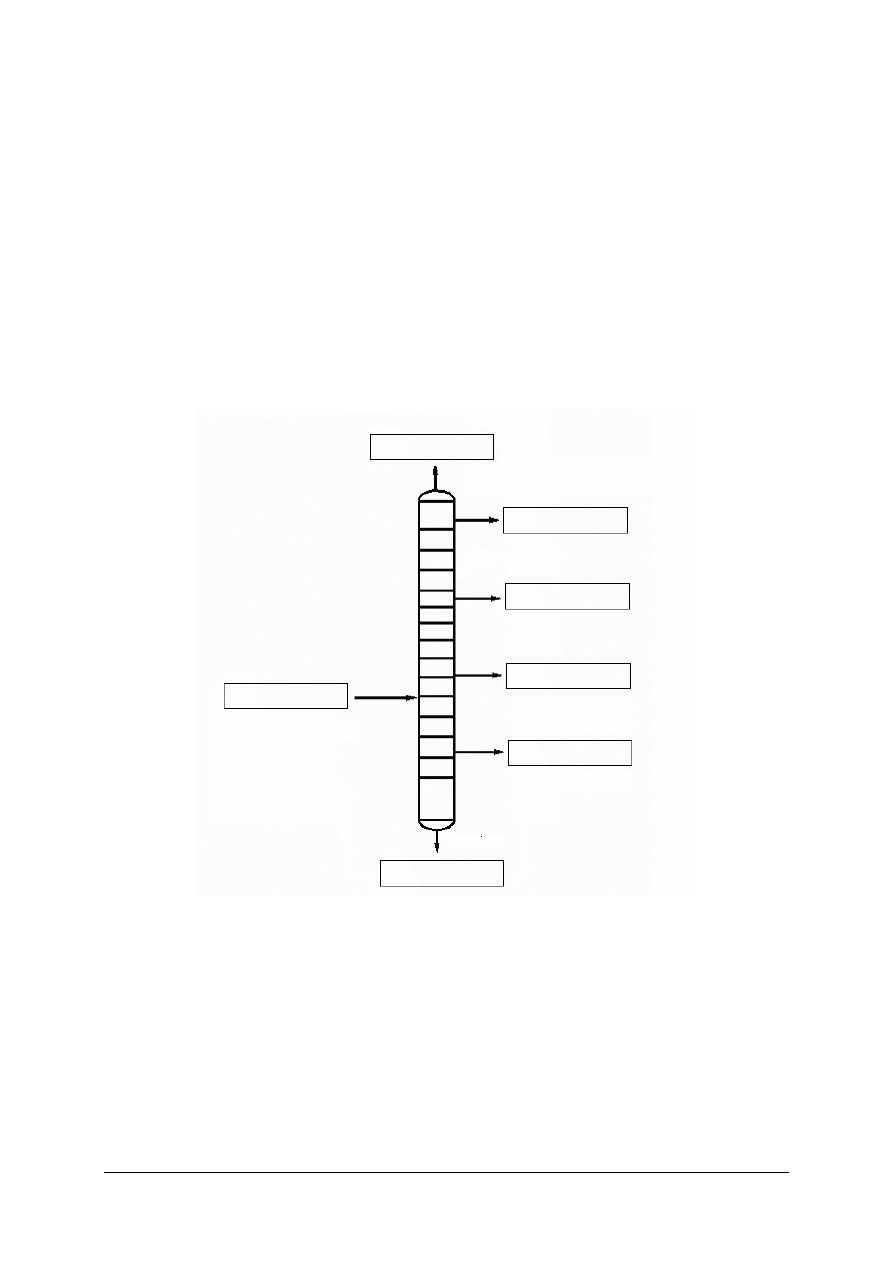
Uzupełnij puste miejsca (wpisz nazwy surowców i produktów) na uproszczonym
schemacie destylacji atmosferycznej ropy naftowej.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać fragment
rozdziału Materiał nauczania dotyczący technologii przerobu ropy naftowej. Należy zwrócić
szczególną uwagę na zagadnienia dotyczące destylacji rurowo-wieżowej. Przed
przystąpieniem do realizacji ćwiczenia nauczyciel powinien omówić jego zakres i sposób
wykonania. Ćwiczenie może być wykonywane indywidualnie lub w grupach 2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
odszukać informacje dotyczące atmosferycznej destylacji (rektyfikacji) ropy naftowej,

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
13
2)
określić surowce i produkty powstające w procesie atmosferycznej destylacji
(rektyfikacji) ropy naftowej,
3)
uzupełnić uproszczony schemat destylacji atmosferycznej ropy naftowej.
Zalecane metody nauczania–uczenia się:
−
pogadanka,
−
ć
wiczenie praktyczne.
Ś
rodki dydaktyczne:
−
papier formatu A4,
−
flamastry,
−
Poradnik dla ucznia,
−
literatura zgodna z punktem 7 poradnika dla nauczyciela.

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
14
5.2. Przemysł tłuszczowy
5.2.1. Ćwiczenia
Ćwiczenie 1
Określ wzory i nazwy produktów powstających w wyniku hydrolizy zasadowej
trioleinianu glicerolu. Zapisz równanie reakcji zasadowej hydrolizy trioleinianu glicerolu.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać fragment
rozdziału Materiał nauczania dotyczący produkcji mydeł. Przed przystąpieniem do realizacji
ć
wiczenia nauczyciel powinien omówić jego zakres i sposób wykonania. Ćwiczenie może być
wykonywane indywidualnie lub w grupach 2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
określić, jakim przemianom podlegają tłuszcze w środowisku zasadowym,
2)
zapisać wzory i nazwy przewidywanych produktów,
3)
zapisać równania reakcji, które mogą zachodzić w czasie zasadowej hydrolizy
trioleinianu glicerolu.
Zalecane metody nauczania–uczenia się:
−
pogadanka,
−
ć
wiczenie praktyczne.
Ś
rodki dydaktyczne:
−
papier formatu A4,
−
kalkulator,
−
Poradnik dla ucznia,
−
literatura zgodna z punktem 7 poradnika dla nauczyciela.
Ćwiczenie 2
Określ wzory i nazwy produktów powstających w wyniku całkowitego uwodornienia
trioleinianu glicerolu. Zapisz równanie reakcji całkowitego uwodornienia trioleinianu
glicerolu.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać fragment
rozdziału Materiał nauczania dotyczący przemysłu tłuszczowego. Należy zwrócić szczególną
uwagę zagadnienia dotyczące uwadarniania tłuszczów. Przed przystąpieniem do realizacji
ć
wiczenia nauczyciel powinien omówić jego zakres i sposób wykonania. Ćwiczenie może być
wykonywane indywidualnie lub w grupach 2–4-osobowych.

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
15
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
określić, jakim przemianom podlegają tłuszcze ciekłe (zawierają kwasy tłuszczowe
nienasycone) w obecności wodoru,
2)
zapisać wzory i nazwy przewidywanych produktów,
3)
zapisać równania reakcji, które mogą zachodzić w czasie całkowitego uwodornienia
trioleinianu glicerolu.
Zalecane metody nauczania–uczenia się:
−
pokaz z objaśnieniem,
−
tekstu przewodniego.
Ś
rodki dydaktyczne:
−
papier formatu A4,
−
kalkulator,
−
Poradnik dla ucznia,
−
literatura zgodna z punktem 7 poradnika dla nauczyciela.
Ćwiczenie 3
Otrzymaj mydło przez zmydlanie (hydroliza zasadowa) tłuszczu.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać fragment
rozdziału Materiał nauczania dotyczący produkcji mydeł. Należy zwrócić szczególną uwagę
na pracę z substancjami żrącymi lub parzącymi. Przed przystąpieniem do realizacji ćwiczenia
nauczyciel powinien omówić jego zakres i sposób wykonania. Ćwiczenie może być
wykonywane indywidualnie lub w grupach 2 - 4 osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
sporządzić wykaz niezbędnego sprzętu laboratoryjnego i odczynników,
2)
zaplanować konieczne czynności laboratoryjne,
3)
określić
warunki
bhp
niezbędne
do
bezpiecznego
wykonywania
czynności
laboratoryjnych,
4)
pobrać od nauczyciela niezbędny sprzęt i odczynniki,
5)
przeprowadzić zaplanowane czynności laboratoryjne,
6)
zapisać obserwacje w dzienniku laboratoryjnym.
Zalecane metody nauczania–uczenia się:
−
pogadanka,
−
ć
wiczenie praktyczne.

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
16
Ś
rodki dydaktyczne:
−
parownica
,
−
trójnóg,
−
palnik,
−
płytka metalowa,
−
bagietka,
−
cylinder miarowy o pojemności 100 cm
3
,
−
30 % roztwór NaOH,
−
etanol,
−
tłuszcz (smalec),
−
zestaw do filtracji.
Instrukcja wykonania ćwiczenia
1.
Odważ około 8 g tłuszczu i umieść go w parownicy.
2.
Ogrzej i roztop tłuszcz.
3.
Dodaj do roztopionego tłuszczu 20 cm
3
30 % roztworu NaOH oraz 20 cm
3
etanolu.
4.
Ogrzewaj łagodnie mieszając bagietką aż do utworzenia jednolitej masy mydlanej.
5.
Odfiltruj mydło.

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
17
5.3. Procesy jednostkowe w syntezie organicznej
5.3.1. Ćwiczenia
Ćwiczenie 1
Naszkicuj nitrator stosowany w okresowej produkcji nitrobenzenu. Podaj materiały,
z których można zbudować nitrator, w którym stosuje się mieszaninę nitrującą.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać fragment
rozdziału Materiał nauczania dotyczący nitrowania. Należy zwrócić szczególną uwagę na
pracę z substancjami żrącymi lub parzącymi. Przed przystąpieniem do realizacji ćwiczenia
nauczyciel powinien omówić jego zakres i sposób wykonania. Ćwiczenie może być
wykonywane indywidualnie lub w grupach 2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
wyszukać w materiałach dydaktycznych informacje dotyczące produkcji związków
nitrowych,
2)
określić, z jakich elementów powinien składać się nitrator, aby zapewnić jego bezpieczną
pracę,
3)
określić, z jakich materiałów można zbudować nitrator przystosowany do pracy
z mieszaniną nitrującą,
4)
naszkicować nitrator (rysunek w przekroju).
Zalecane metody nauczania–uczenia się:
−
metoda tekstu przewodniego.
Ś
rodki dydaktyczne:
−
papier formatu A4,
−
flamastry,
−
Poradnik dla ucznia,
−
literatura zgodna z punktem 7 poradnika dla nauczyciela.
Ćwiczenie 2
Produkcja nitrobenzenu polega na bezpośredniej reakcji benzenu z kwasem azotowym
(mieszanina nitrująca). Oblicz objętość benzenu niezbędną do uzyskania 100 kg nitrobenzenu,
jeżeli proces przebiega z wydajnością 80%. Gęstość benzenu w tych warunkach wynosi
0,877 g/cm
3
.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać fragment
rozdziału Materiał nauczania nitrowania.. Przed przystąpieniem do realizacji ćwiczenia
nauczyciel powinien przypomnieć uczniom podstawy obliczeń stechiometrycznych w zakresie
przewidzianym w ćwiczeniu. Ćwiczenie może być wykonywane indywidualnie lub w grupach
2–4-osobowych.
„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
18
Sposób wykonania ćwiczenia
Uczeń powinien:
1) zapisać równanie reakcji nitrowania benzenu,
2)
obliczyć masę czystego benzenu niezbędną do uzyskania 100 kg nitrobenzenu
wykorzystując zależność stechiometryczną pomiędzy benzenem a nitrobenzenem
przyjmując 100% wydajność reakcji,
3)
obliczyć masę czystego benzenu uwzględniając fakt, że proces przebiega z wydajnością
80%,
4)
obliczyć objętość benzenu na podstawie masy benzenu obliczonej w punkcie poprzednim
uwzględniając gęstość benzenu.
Zalecane metody nauczania–uczenia się:
−
ć
wiczenie praktyczne.
Ś
rodki dydaktyczne:
–
kalkulator,
–
papier formatu A4,
–
Poradnik dla ucznia,
–
literatura zgodna z punktem 7 poradnika dla nauczyciela.
Ćwiczenie 3
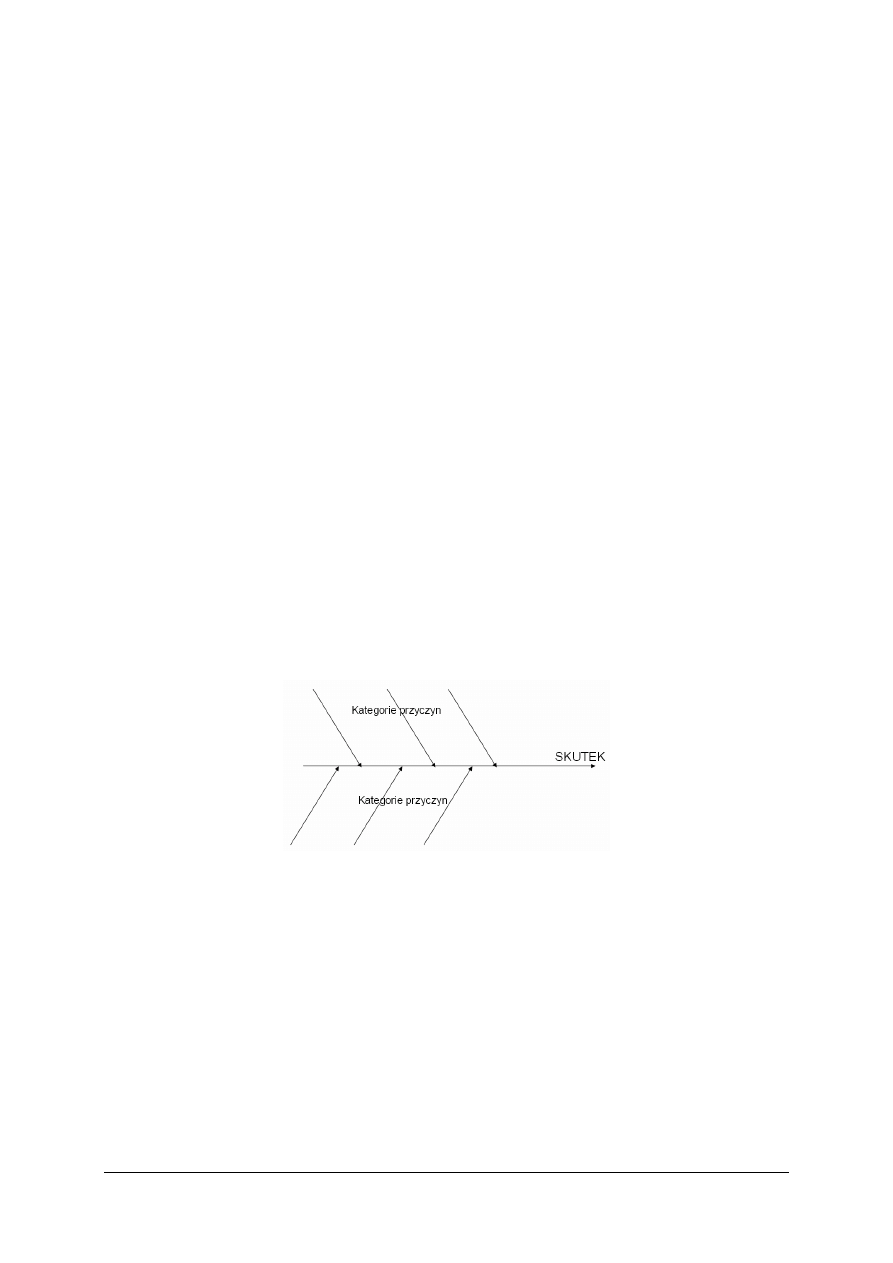
W reaktorach chemicznych, szeroko stosowanych w procesach przemysłowych, możliwe
są reakcje niekontrolowane. Badania wykazują, że awarie najczęściej wiążą się z reakcjami
polimeryzacji, nitrowania, sulfonowania, zobojętniania oraz chlorowania.
Określ przyczyny, które mogłyby spowodować powstanie niekontrolowanej reakcji
sulfonowania okresowego benzenu. Skorzystaj z metody Ishikawy.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać fragment
rozdziału Materiał nauczania dotyczący sulfonowania. Należy zwrócić szczególną uwagę na
pracę z substancjami żrącymi lub parzącymi. Przed przystąpieniem do realizacji ćwiczenia
nauczyciel powinien omówić metodę Ishikawy. Ćwiczenie może być wykonywane
indywidualnie lub w grupach 2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
wyszukać w materiałach dydaktycznych informacje dotyczące sulfonowania,
2)
określić przyczyny mogące doprowadzić do powstania niekontrolowanej reakcji
sulfonowania benzenu,

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
19
3)
uzupełnić wykres Ishikawy.
Zalecane metody nauczania–uczenia się:
−
ć
wiczenie praktyczne.
Ś
rodki dydaktyczne:
−
papier formatu A4,
−
flamastry,
−
Poradnik dla ucznia,
−
literatura zgodna z punktem 7 poradnika dla nauczyciela.
„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
20
5.4.
Przemysł tworzyw sztucznych
5.4.1. Ćwiczenia
Ćwiczenie 1
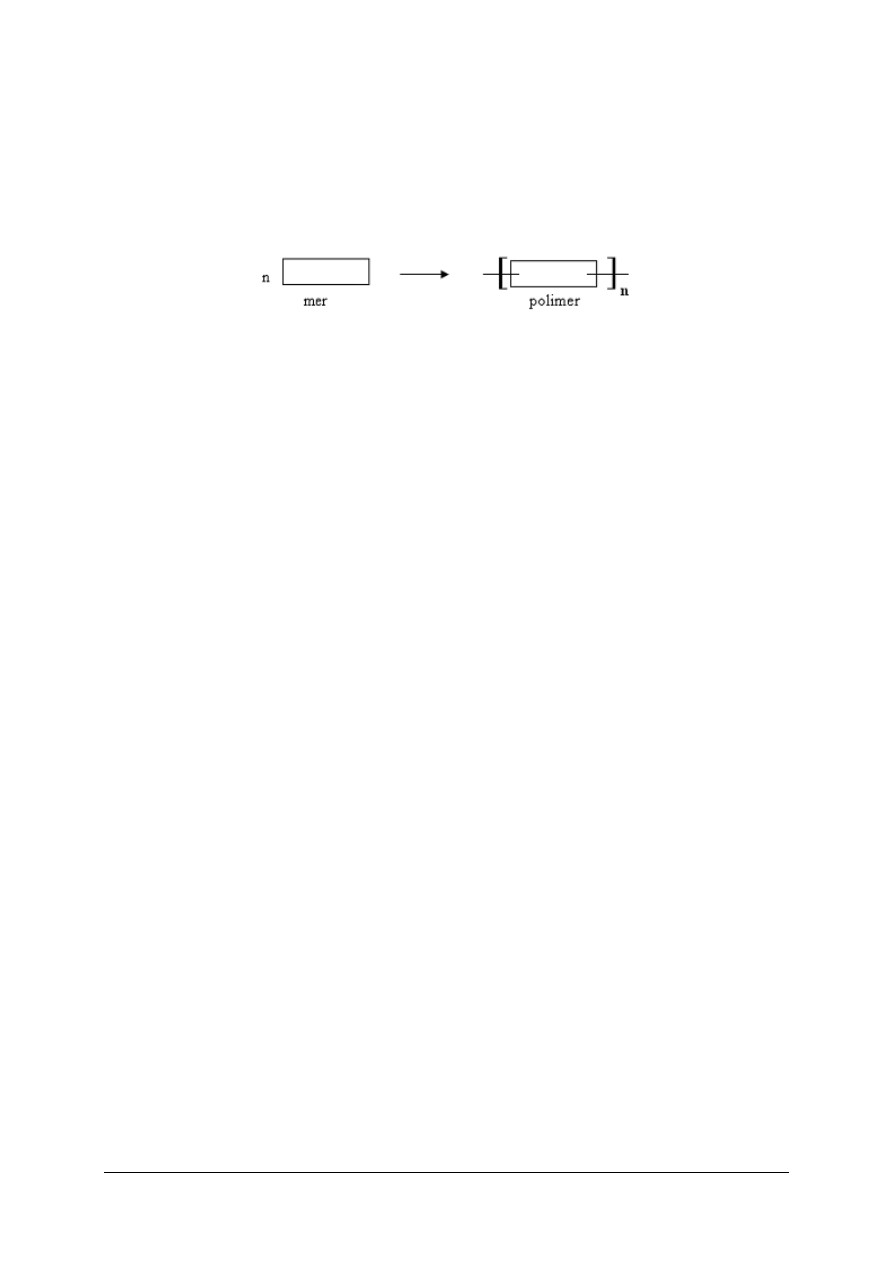
Reakcja polimeryzacji przebiega według schematu:
Zapisz równania reakcji polimeryzacji dla sześciu dowolnych tworzyw polimeryzacyjnych
oraz nazwij produkty reakcji.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać fragment
rozdziału Materiał nauczania dotyczący polimerów. Przed przystąpieniem do realizacji
ć
wiczenia nauczyciel powinien omówić jego zakres i sposób wykonania. Ćwiczenie może być
wykonywane indywidualnie lub w grupach 2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
wyszukać w materiałach dydaktycznych informacje dotyczące produkcji polimerów,
2)
zapisać równania polimeryzacji dla sześciu dowolnych tworzyw polimeryzacyjnych,
3)
zapisać nazwy produktów występujących w zapisanych równaniach reakcji.
Zalecane metody nauczania–uczenia się:
−
ć
wiczenie praktyczne.
Ś
rodki dydaktyczne:
−
papier formatu A4,
−
Poradnik dla ucznia,
−
literatura zgodna z punktem 7 poradnika dla nauczyciela.
Ćwiczenie 2
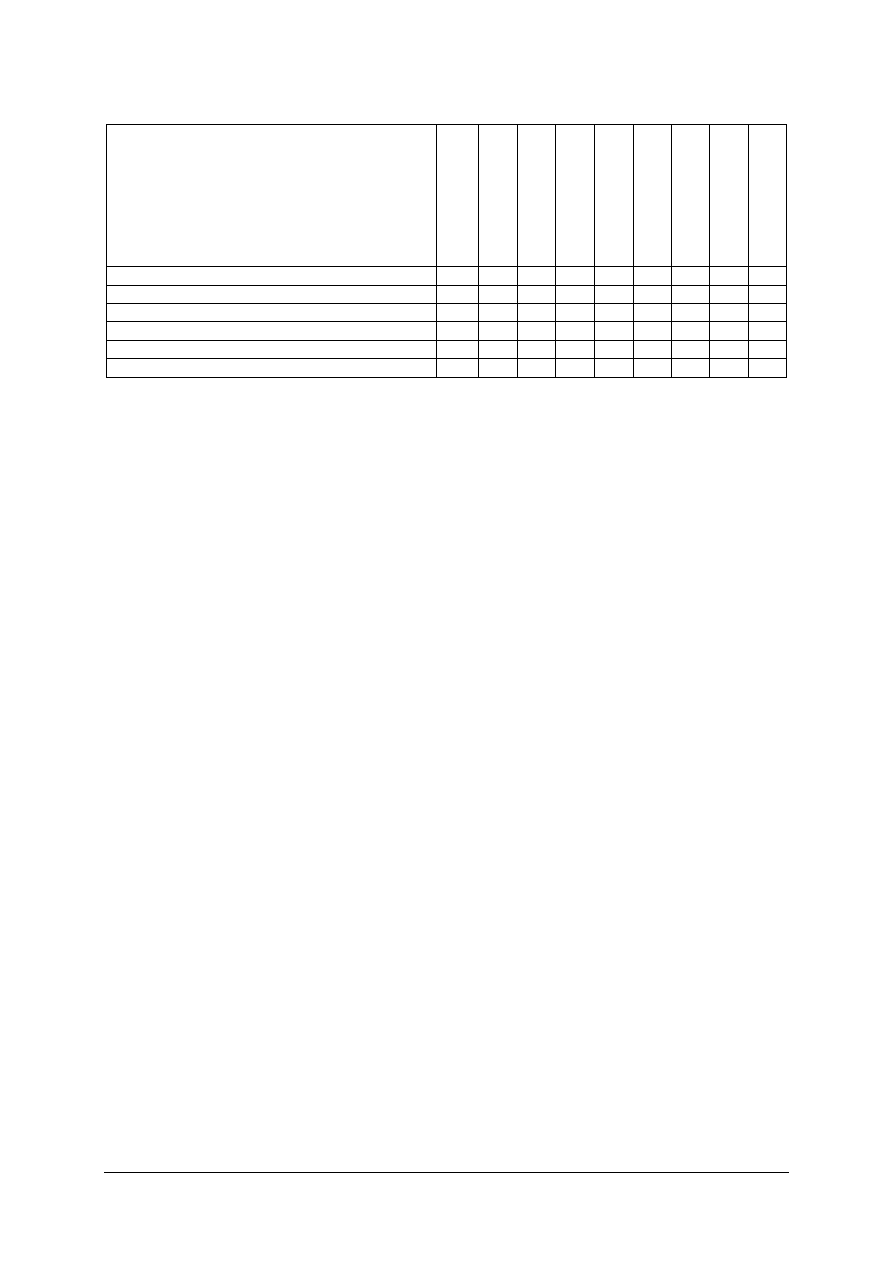
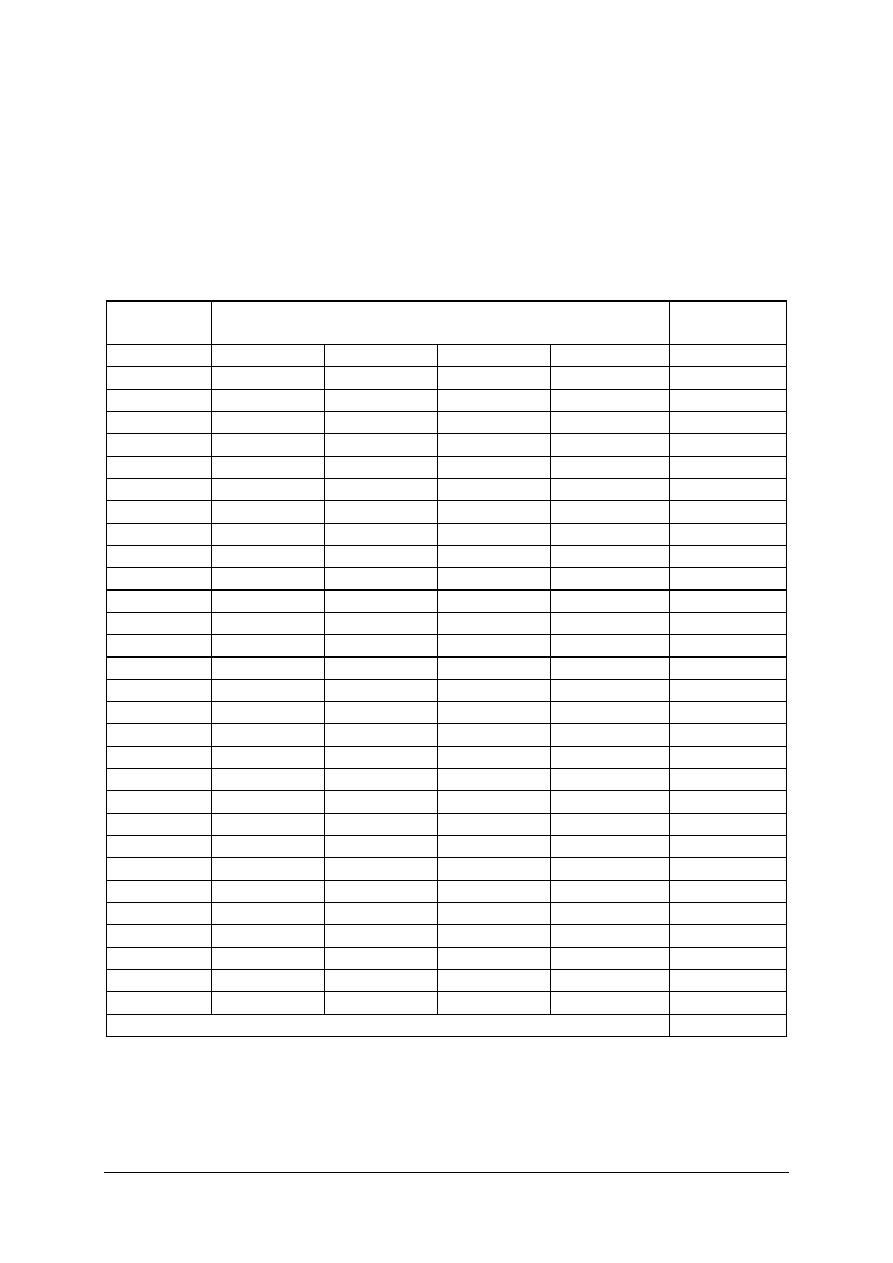
Na podstawie załączonej tabeli określ, z jakim tworzywem masz do czynienia. Twoja
próbka tworzywa (około 1 g) powinna Ci wystarczyć na przeprowadzenie kilku prób badania
rozpuszczalności tworzywa w różnych rozpuszczalnikach. Otrzymana próbka zawiera jedno
z tworzyw polimeryzacyjnych wymienionych w tabeli.
„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
21
Tabela do ćwiczenia 2
Polimer
W
o
d
a
A
ce
to
n
O
ct
an
e
ty
lu
D
io
k
sa
n
B
en
ze
n
C
h
lo
ro
fo
rm
E
te
r
et
y
lo
w
y
C
y
k
lo
h
ek
sa
n
o
l
T
et
ra
ch
lo
re
k
w
ę
g
la
Polialkohol winylowy
+
-
-
-
-
-
-
-
Polichlorek winylu
-
-
-
+
-
+
-
+
+
Polietylen
-
-
-
-
g
g
-
-
g
Polioctan winylu
-
+
+
+
+
+
p
+
+
Polipropylen
-
-
-
-
-
-
-
-
-
Polistyren
-
p
p
+
+
+
p
-
+
(+) – rozpuszczalny, (-) – nierozpuszczalny, (g) – rozpuszczalny na gorąco, (p) – pęcznieje.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać fragment
rozdziału Materiał nauczania dotyczący polimerów. Należy zwrócić szczególną uwagę na
zasady postępowania z substancjami łatwopalnymi (rozpuszczalnikami), szczególnie w czasie
ich ogrzewania. Przed przystąpieniem do realizacji ćwiczenia nauczyciel powinien omówić
jego zakres i sposób wykonania. Ćwiczenie może być wykonywane indywidualnie lub
w grupach 2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
wyszukać w Poradniku dla ucznia i w dostępnej literaturze informacje dotyczące tworzyw
polimeryzacyjnych,
2)
sporządzić wykaz niezbędnego sprzętu laboratoryjnego i odczynników,
3)
zaplanować konieczne czynności laboratoryjne,
4)
określić
warunki
bhp
niezbędne
do
bezpiecznego
wykonywania
czynności
laboratoryjnych,
5)
pobrać od nauczyciela niezbędny sprzęt i odczynniki,
6)
przeprowadzić zaplanowane czynności laboratoryjne,
7)
zapisać obserwacje w dzienniku laboratoryjnym.
Zalecane metody nauczania–uczenia się:
−
ć
wiczenie praktyczne.
Ś
rodki dydaktyczne:
−
rozpuszczalniki,
−
probówki,
−
łapa do probówek,
−
palnik denaturatowy,
−
Poradnik dla ucznia,
−
literatura zgodna z punktem 7 poradnika dla nauczyciela.
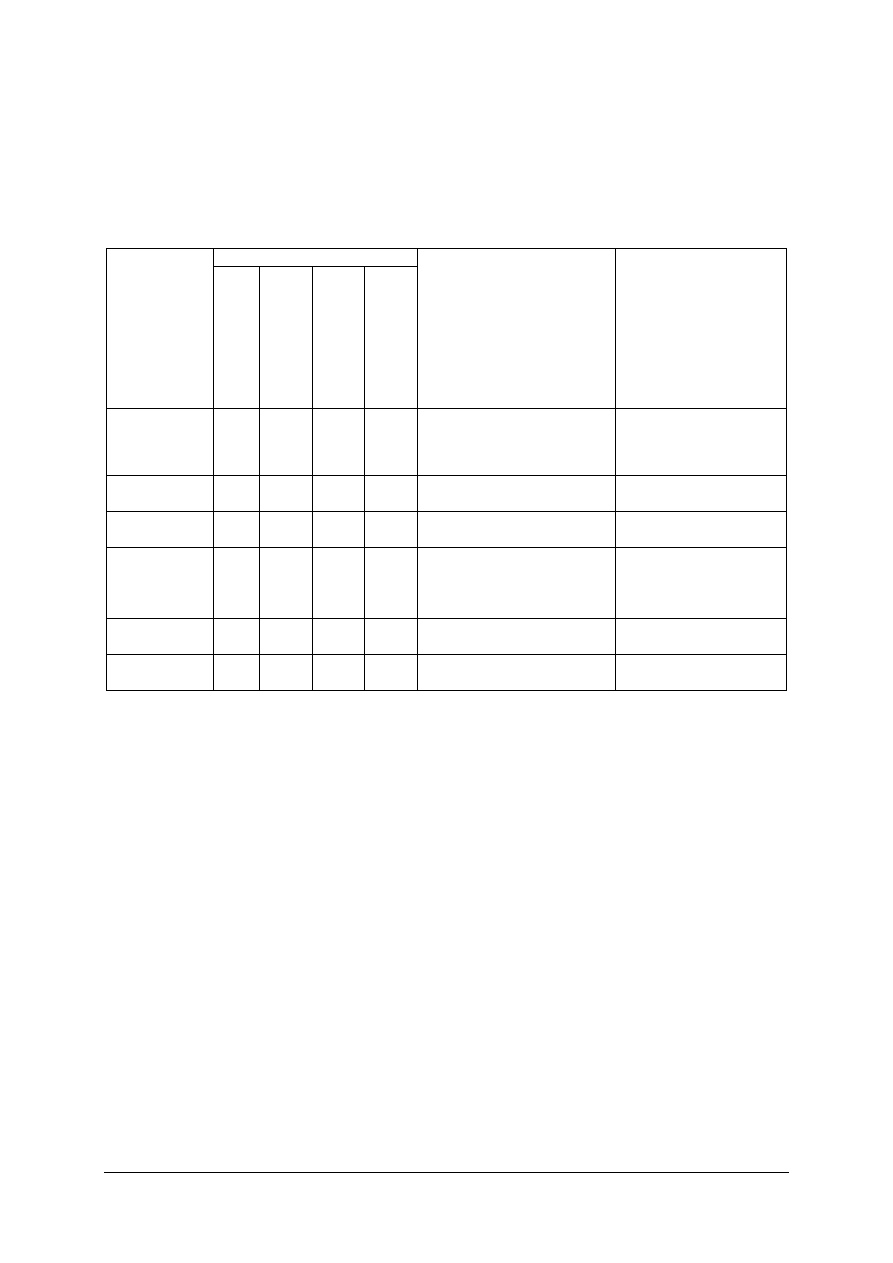
„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
22
Ćwiczenie 3
Na podstawie załączonej tabeli określ, z jakim tworzywem masz do czynienia. Twoja
próbka tworzywa (około 1 g) powinna Ci wystarczyć na przeprowadzenie kilku prób
płomieniowych. Otrzymana próbka zawiera jedno z tworzyw polimeryzacyjnych
wymienionych w tabeli.
Tabela do ćwiczenia 3
Palność próbki
Rodzaj
tworzywa
N
ie
p
al
i
si
ę
P
al
i
si
ę
t
y
lk
o
w
p
ło
m
ie
n
iu
P
o
z
ap
al
en
iu
p
al
i
si
ę
d
al
ej
s
am
o
P
al
i
si
ę
g
w
ał
to
w
n
ie
Wygląd płomienia
Zapach produktów
spalania
Polietylen
X
Ś
wiecący z niebieskim
ś
rodkiem, kapie kroplami.
Palącej się parafiny.
Polipropylen
X
Ś
wiecący z niebieskim
ś
rodkiem, kapie kroplami.
Palącej się parafiny.
Polistyren
X
Ś
wiecący, silnie kopcący,
powstają cząsteczki sadzy.
Słodkokwiatowy
(hiacynt)
Polichlorek
winylu
X
X
ś
ółto-zielony, na brzegach
białe dymy, czasem zielone
iskry, ewentualnie świecący
(plastyfikatory)
Kwasu solnego
Polioctan
winylu
X
Ś
wiecący, kopcący
Kwasu octowego
Polialkohol
winylowy
X
Ś
wiecący, kopcący
Drażniący
X – występowanie cechy
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać fragment
rozdziału Materiał nauczania dotyczący polimerów. Należy zwrócić szczególną uwagę na
zasady postępowania z substancjami łatwopalnymi, szczególnie w czasie ich spalania. Przed
przystąpieniem do realizacji ćwiczenia nauczyciel powinien omówić jego zakres i sposób
wykonania. Ćwiczenie może być wykonywane indywidualnie lub w grupach 2 - 4 osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
wyszukać w Poradniku dla ucznia i w dostępnej literaturze informacje dotyczące tworzyw
polimeryzacyjnych,
2)
sporządzić wykaz niezbędnego sprzętu laboratoryjnego i odczynników,
3)
zaplanować konieczne czynności laboratoryjne,
4)
określić
warunki
bhp
niezbędne
do
bezpiecznego
wykonywania
czynności
laboratoryjnych,
5)
pobrać od nauczyciela niezbędny sprzęt i odczynniki,
6)
przeprowadzić zaplanowane czynności laboratoryjne,
7)
zapisać obserwacje w dzienniku laboratoryjnym.

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
23
Zalecane metody nauczania–uczenia się:
−
ć
wiczenie praktyczne.
Ś
rodki dydaktyczne:
−
palniki,
−
łyżeczka do spalania,
−
próbki tworzyw
−
Poradnik dla ucznia,
−
literatura zgodna z punktem 7 poradnika dla nauczyciela.

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
24
5.5. Syntezy organiczne z gazu syntezowego
5.5.1. Ćwiczenia
Ćwiczenie 1
Etyn (acetylen) otrzymywano kiedyś głównie z karbidu w reakcji z wodą. Wyznacz
objętość acetylenu, jaką można maksymalnie (100% wydajność reakcji) uzyskać ze 100 kg
karbidu o czystości 80%.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać fragment
rozdziału Materiał nauczania dotyczący produkcji acetylenu. Przed przystąpieniem do
realizacji ćwiczenia nauczyciel powinien przypomnieć uczniom podstawy obliczeń
stechiometrycznych w zakresie przewidzianym w ćwiczeniu. Ćwiczenie może być
wykonywane indywidualnie lub w grupach 2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1) zapisać równanie reakcji karbidu z wodą,
2)
obliczyć masę czystego węglika wapnia znajdującego się w 100 kg karbidu (uwzględnij
czystość karbidu),
3)
obliczyć maksymalną objętość acetylenu wykorzystując zależność stechiometryczną
pomiędzy węglikiem wapnia a acetylenem przyjmując 100% wydajność reakcji.
Zalecane metody nauczania–uczenia się:
−
ć
wiczenie praktyczne.
Ś
rodki dydaktyczne:
–
kalkulator,
–
papier formatu A4,
–
Poradnik dla ucznia,
–
literatura zgodna z punktem 7 poradnika dla nauczyciela.
Ćwiczenie 2
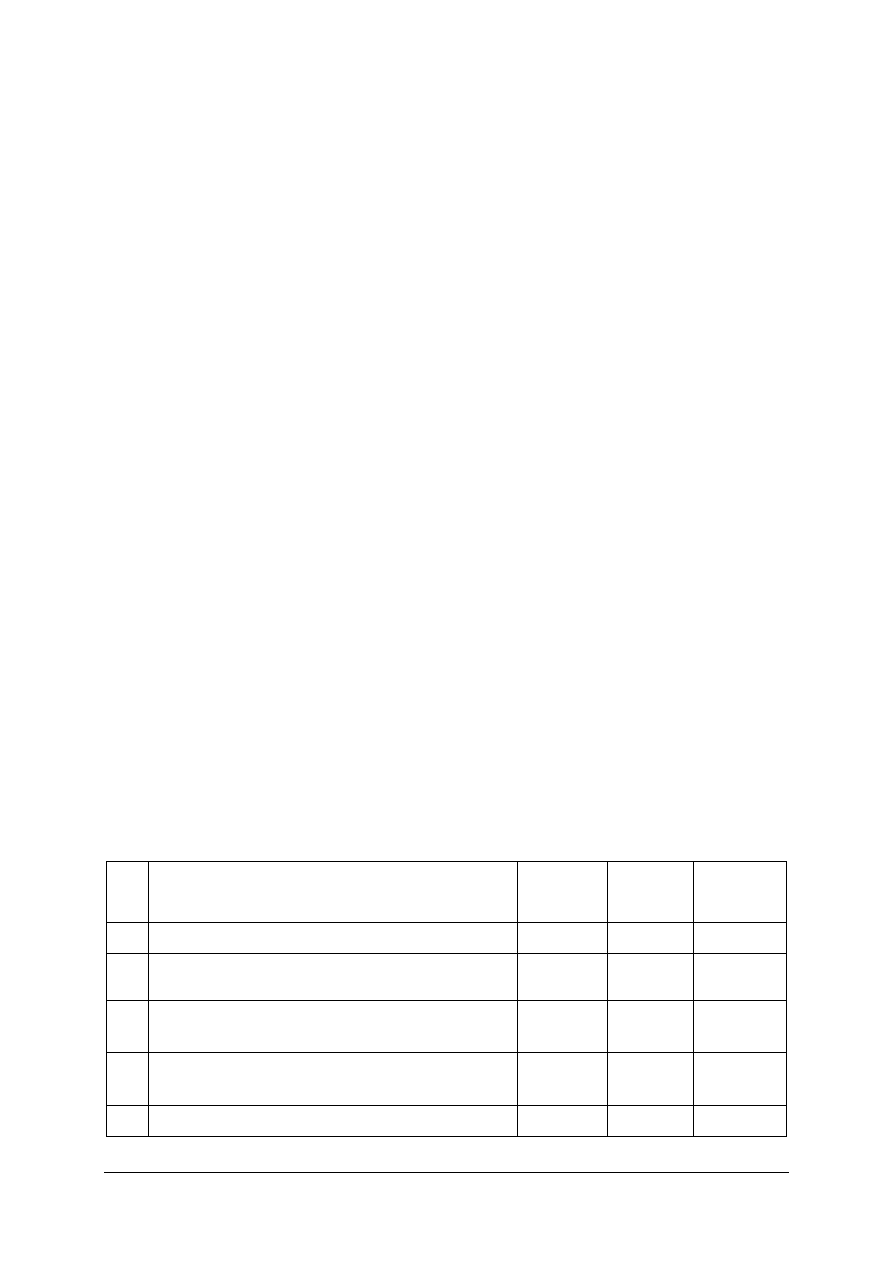
Wyznacz procentową zawartość gazu syntezowego otrzymanego w wyniku zgazowania
węgla kamiennego przegrzaną parą wodną. Do wykonania obliczeń przyjmij, że przereaguje
75% początkowej ilości węgla i pary wodnej. Uzupełnij tabelę przedstawioną poniżej.
Tabela do ćwiczenia 2
Substraty
Produkty
Substancje
Liczba moli
Substancje
Liczba moli
Zawartość procentowa
C
H
2
O
CO
H
2
1
1
0
0
C
H
2
O
CO
H
2
Razem:
2
Razem

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
25
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać fragment
rozdziału Materiał nauczania dotyczący produkcji gazu syntezowego. Przed przystąpieniem
do realizacji ćwiczenia nauczyciel powinien przypomnieć uczniom podstawy obliczeń
stechiometrycznych w zakresie przewidzianym w ćwiczeniu. Ćwiczenie może być
wykonywane indywidualnie lub w grupach 2 - 4 osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
wyszukać w materiałach dydaktycznych informacje dotyczące produkcji gazu
syntezowego,
2)
zapisać równanie reakcji zgazowania węgla przegrzaną parą wodną,
3)
obliczyć liczbę moli składników gazu po zajściu reakcji,
4)
obliczyć zawartość procentową składników gazu po reakcji.
Zalecane metody nauczania–uczenia się:
−
ć
wiczenie.
Ś
rodki dydaktyczne:
–
kalkulator,
–
papier formatu A4,
–
Poradnik dla ucznia,
–
literatura zgodna z punktem 6 poradnika.
Ćwiczenie 3
Z acetylenu można uzyskać wiele związków o znaczeniu przemysłowym. Zapisz
równania reakcji otrzymywania sześciu związków o znaczeniu przemysłowym, które można
uzyskać z acetylenu. Podaj nazwy tych związków.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać fragment
rozdziału Materiał nauczania dotyczący zastosowania przemysłowego acetylenu. Przed
przystąpieniem do realizacji ćwiczenia nauczyciel powinien omówić jego zakres i sposób
wykonania. Ćwiczenie może być wykonywane indywidualnie lub w grupach 2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
wyszukać w materiałach dydaktycznych informacje dotyczące przemysłowych
zastosowań acetylenu,
2)
zapisać równania otrzymywania sześciu związków o znaczeniu przemysłowym,
3)
zapisać nazwy produktów występujących w zapisanych równaniach reakcji.
Zalecane metody nauczania–uczenia się:
−
ć
wiczenie praktyczne.

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
26
Ś
rodki dydaktyczne:
−
papier formatu A4,
−
Poradnik dla ucznia,
−
literatura zgodna z punktem 7 poradnika dla nauczyciela.
„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
27
6. EWALUACJA OSIĄGNIĘĆ UCZNIA
Przykłady narzędzi pomiaru dydaktycznego
TEST 1
Test dwustopniowy do jednostki modułowej
„Wytwarzanie podstawowych
półproduktów i produktów organicznych”
Test składa się z 30 zadań wielokrotnego wyboru, z których:
−
zadania 1, 2, 3, 4, 5, 6, 7, 8, 9, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 24, 25, 26, 27, 28
są z poziomu podstawowego,
−
zadania 10, 22, 23, 29, 30 są z poziomu ponadpodstawowego.
Punktacja zadań: 0 lub 1 punkt
Za każdą prawidłową odpowiedź uczeń otrzymuje 1 punkt. Za złą odpowiedź lub jej brak
uczeń otrzymuje 0 punktów.
Proponuje się następujące normy wymagań – uczeń otrzyma następujące
oceny szkolne:
−
dopuszczający – za rozwiązanie co najmniej 10 zadań z poziomu podstawowego,
−
dostateczny – za rozwiązanie co najmniej 15 zadań z poziomu podstawowego,
−
dobry – za rozwiązanie 22 zadań, w tym co najmniej 2 z poziomu ponadpodstawowego,
−
bardzo dobry – za rozwiązanie 27 zadań, w tym co najmniej 4 z poziomu
ponadpodstawowego.
Klucz odpowiedzi: 1. c, 2. a, 3. b, 4. c, 5. c, 6. d, 7. c, 8. c, 9. b, 10. d, 11. c, 12. c,
13. c, 14. c, 15. c, 16. a, 17. d, 18. a, 19. d, 20. d, 21. c, 22. a,
23. b, 24. d, 25. b, 26. d, 27. b, 28. a, 29. b, 30. d.
Plan testu
Nr
zad.
Cel operacyjny
(mierzone osiągnięcia ucznia)
Kategoria
celu
Poziom
wymagań
Poprawna
odpowiedź
1. Rozróżnić surowce energetyczne
B
P
c
2. Wskazać metody oczyszczania ropy naftowej
A
P
a
3.
Rozróżnić produkty uzyskiwane w wyniku
rozdziału destylacyjnego ropy
B
P
b
4.
Scharakteryzować właściwości składników paliw
sillnikowych
C
P
c
5. Scharakteryzować właściwości benzyn
C
P
c
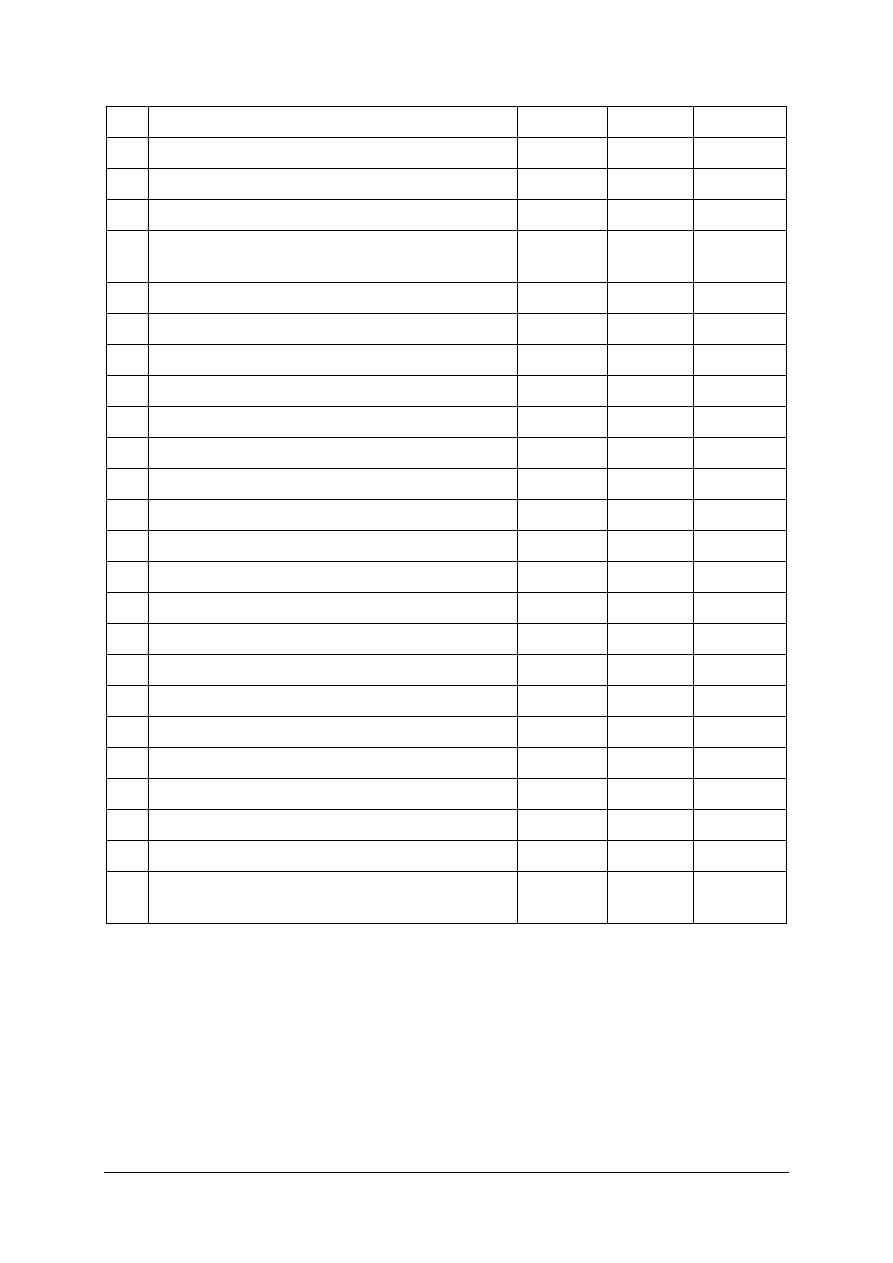
„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
28
6. Rozróżnić metody przerobu węgla
B
P
d
7. Wskazać produkty procesu
B
P
c
8. Objaśnić toksyczność substancji
B
P
c
9. Zidentyfikować surowiec podstawowy
A
P
b
10.
Posłużyć się uproszczonym schematem
technologicznym
C
PP
d
11. Rozróżnić proces technologiczny
B
P
c
12. Wskazać skład katalizatora
B
P
c
13. Opisać produkty procesu
B
P
c
14. Nazwać surowce podstawowe procesu
A
P
c
15. Rozpoznać proces technologiczny
C
P
c
16. Rozróżnić procesy technologiczne
B
P
a
17. Opisać surowce podstawowe procesu
C
P
d
18. Scharakteryzować budowę urządzeń
C
P
a
19. Rozpoznać stopień zagrożenia środowiska pracy
B
P
d
20. Wskazać katalizator procesu
B
P
d
21. Wskazać surowce podstawowe procesu
B
P
c
22. Rozpoznać substancje
C
PP
a
23. Wyznaczyć ilość surowca
C
PP
b
24. Rozróżnić procesy technologiczne
B
P
d
25. Objaśnić działanie stabilizatorów
B
P
b
26. Zdefiniować surowiec podstawowy
A
P
d
27. Rozróżnić produkty procesu
B
P
b
28. Zdefiniować surowiec podstawowy
B
P
a
29. Przeliczyć masę zanieczyszczeń
C
PP
b
30.
Posłużyć się uproszczonym schematem
technologicznym
C
PP
d

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
29
Przebieg testowania
Instrukcja dla nauczyciela
1.
Ustal z uczniami termin przeprowadzenia sprawdzianu z wyprzedzeniem co najmniej
jednotygodniowym.
1.
Omów cel stosowania pomiaru dydaktycznego.
2.
Zapoznaj uczniów z rodzajem zadań podanych w zestawie oraz z zasadami punktowania.
3.
Omów z uczniami sposób udzielania odpowiedzi (karta odpowiedzi).
4.
Zapewnij uczniom możliwość samodzielnej pracy.
5.
Rozdaj uczniom zestawy zadań testowych i karty odpowiedzi, podaj czas przeznaczony
na udzielanie odpowiedzi.
6.
Postaraj się stworzyć odpowiednią atmosferę podczas przeprowadzania pomiaru
dydaktycznego (rozładuj niepokój, zachęć do sprawdzenia swoich możliwości).
7.
Kilka minut przed zakończeniem sprawdzianu przypomnij uczniom o zbliżającym się
czasie zakończenia udzielania odpowiedzi.
8.
Zbierz karty odpowiedzi oraz zestawy zadań testowych.
9.
Sprawdź wyniki i wpisz do arkusza zbiorczego.
10.
Przeprowadź analizę uzyskanych wyników sprawdzianu i wybierz te zadania, które
sprawiły uczniom największe trudności.
11.
Ustal przyczyny trudności uczniów w opanowaniu wiadomości i umiejętności.
12.
Opracuj wnioski do dalszego postępowania, mającego na celu uniknięcie niepowodzeń
dydaktycznych – niskie wyniki przeprowadzonego sprawdzianu.
Instrukcja dla ucznia
1.
Przeczytaj uważnie instrukcję.
2.
Podpisz imieniem i nazwiskiem kartę odpowiedzi.
3.
Zapoznaj się z zestawem zadań testowych.
4.
Test zawiera 30 zadań wielokrotnego wyboru o różnym stopniu trudności. W każdym
zadaniu tylko jedna odpowiedź jest prawidłowa.
5.
Udzielaj odpowiedzi tylko na załączonej karcie odpowiedzi, stawiając w odpowiedniej
rubryce znak X. W przypadku pomyłki należy błędną odpowiedź zaznaczyć kółkiem,
a następnie ponownie zakreślić odpowiedź prawidłową.
6.
Pracuj samodzielnie, bo tylko wtedy będziesz miał satysfakcję z wykonanego zadania.
7.
Kiedy udzielenie odpowiedzi będzie Ci sprawiało trudność, wtedy odłóż jego rozwiązanie
na później i wróć do niego, gdy zostanie Ci czas wolny.
8.
W czasie pracy możesz korzystać z kalkulatora do wykonywania niezbędnych obliczeń
oraz układu okresowego pierwiastków.
9.
Na rozwiązanie testu masz 60 minut.
Powodzenia!
Materiały dla ucznia:
−
instrukcja,
−
zestaw zadań testowych,
−
karta odpowiedzi.

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
30
ZESTAW ZADAŃ TESTOWYCH
1.
Do grupy surowców energetycznych nie należy
a)
ropa naftowa.
b)
gaz ziemny.
c)
węglan wapnia.
d)
węgiel kamienny.
2.
Usuwania wody z ropy naftowej nie prowadzi się metodą
a)
absorpcyjna.
b)
termiczną.
c)
chemiczną.
d)
elektryczną.
3.
W wyniku destylacji atmosferycznej ropy naftowej nie można uzyskać
a)
benzyny.
b)
asfaltów.
c)
nafty.
d)
oleju napędowego.
4.
Węglowodory aromatyczne dodaje się do benzyny w celu
a)
ochrony środowiska.
b)
wzrostu lotności mieszanki.
c)
podniesienia liczby oktanowej mieszanki.
d)
wywołania efektu stukowego spalania mieszanki.
5.
Większość współczesnych samochodów tankuje benzyny bezołowiowe. Jest to
spowodowane
a)
wyczerpywaniem się zapasów czteroetylku ołowiu.
b)
wysoką ceną ołowiu na rynkach światowych.
c)
wysoką szkodliwością związków ołowiu.
d)
wysoką biodegradowalnością związków ołowiu.
6.
Do typowych sposobów przerobu węgla nie zalicza się procesu
a)
koksowania.
b)
zgazowania.
c)
upłynniania
d)
azotowania.
7.
Gęsta, czarna ciecz uzyskiwana w procesie koksowania węgla to
a)
woda amoniakalna.
b)
koks.
c)
smoła węglowa.
d)
mazut.
„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
31
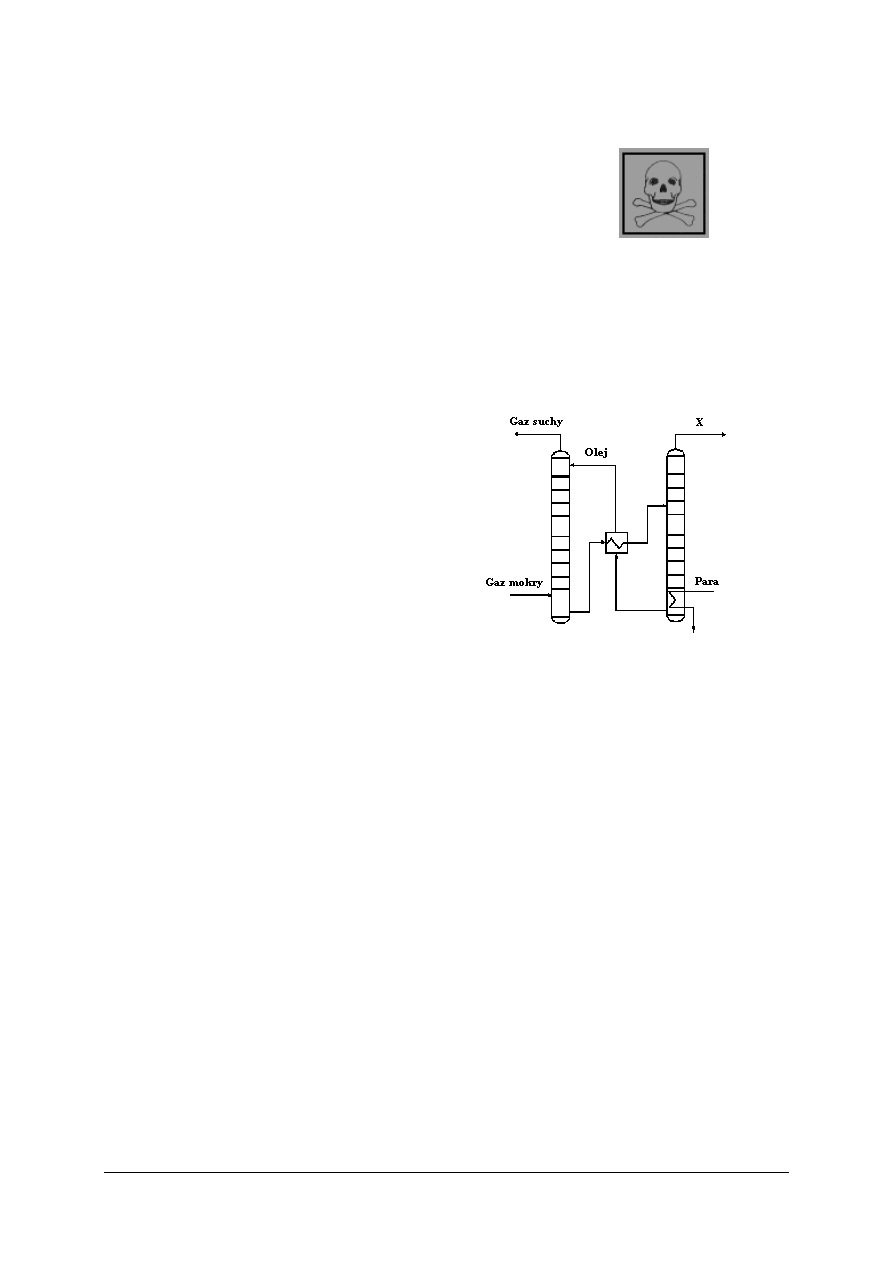
8.
Jednym ze znaków ostrzegawczych jest znak przedstawiony poniżej. Informuje on, że
benzen należy do substancji
a)
wybuchowych.
b)
wysoce łatwopalnych.
c)
bardzo toksycznych.
d)
niebezpiecznych dla środowiska.
9.
Gaz ziemny nie jest wykorzystywany technologicznie jako surowiec
a)
energetyczny.
b)
do produkcji naftalenu.
c)
do produkcji acetylenu.
d)
do produkcji gazu syntezowego.
10.
W schemat odgazolinowania gazu ziemnego metodą absorpcyjną oznaczona literą X
główny produkt procesu. Jest nim
a)
gazol.
b)
gazolina stabilizowana.
c)
gaz suchy.
d)
gazolina do stabilizacji.
11.
Przedstawiony poniżej zapis reakcji zachodzącej w procesie krakingu
C
6
H
14
= C
3
H
6
+ C
3
H
8
opisuje
a)
izomeryzację węglowodorów.
b)
aromatyzację węglowodorów.
c)
degradację węglowodorów.
d)
odwodnienie węglowodorów.
12.
Katalizatorem procesu reformingu jest najczęściej
a)
pięciotlenek wanadu.
b)
kwas siarkowy.
c)
platyna na nośniku tlenkowym.
d)
tlenek żelaza na nośniku tlenkowym.
13.
Proces reformingu nie jest ukierunkowany na otrzymywanie węglowodorów
a)
aromatycznych.
b)
alifatycznych rozgałęzionych.
c)
alifatycznych nierozgałęzionych.
d)
alifatyczno-aromatycznych.

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
32
14.
Nienasyconym kwasem tłuszczowym jest kwas
a)
stearynowy.
b)
palmitynowy.
c)
oleinowy.
d)
octowy.
15.
Przedstawiona reakcja
C
3
H
5
(OCOC
17
H
33
)
3
+ 3H
2
= C
3
H
5
(OCOC
17
H
35
)
3
opisuje proces produkcji
a)
mydła.
b)
parafiny.
c)
tłuszczów stałych.
d)
tłuszczów ciekłych.
16.
Przedstawiona reakcja
C
3
H
5
(OCOC
17
H
35
)
3
+ 3NaOH = C
3
H
5
(OH)
3
+ 3C
17
H
35
COONa
opisuje proces produkcji
a)
mydła.
b)
ś
rodków zapachowych.
c)
parafiny.
d)
tłuszczów stałych.
17.
Procesu nitrowania nie można przeprowadzić stosując
a)
stężony kwas azotowy.
b)
mieszaninę nitrującą.
c)
mieszaninę azotan(V) sodu z kwasem siarkowym.
d)
rozcieńczony kwas azotowy.
18.
Nitratory powinny być wyposażone w
a)
mieszadła, wewnętrzne chłodnice, zewnętrzny płaszcz i termometry.
b)
dmuchawy, wewnętrzne chłodnice, zewnętrzny płaszcz i termometry.
c)
sprężarki, wewnętrzne chłodnice, zewnętrzny płaszcz i termometry.
d)
dmuchawy, wewnętrzne chłodnice, zewnętrzny płaszcz i manometry.
19.
W czasie sulfonowania węglowodorów aromatycznych istnieje poważne zagrożenie
występowania
a)
oparzeń termicznych.
b)
oparzeń chemicznych.
c)
zatruć tlenkami azotu.
d)
oparzeń termicznych i chemicznych.
20.
W procesie otrzymywania octanu etylu stosowany jest stężony kwas siarkowy jako
a)
katalizator.
b)
substancja związująca nadmiar powstającej wody.
c)
główny substrat.
d)
katalizator i substancja związująca nadmiar powstającej wody.
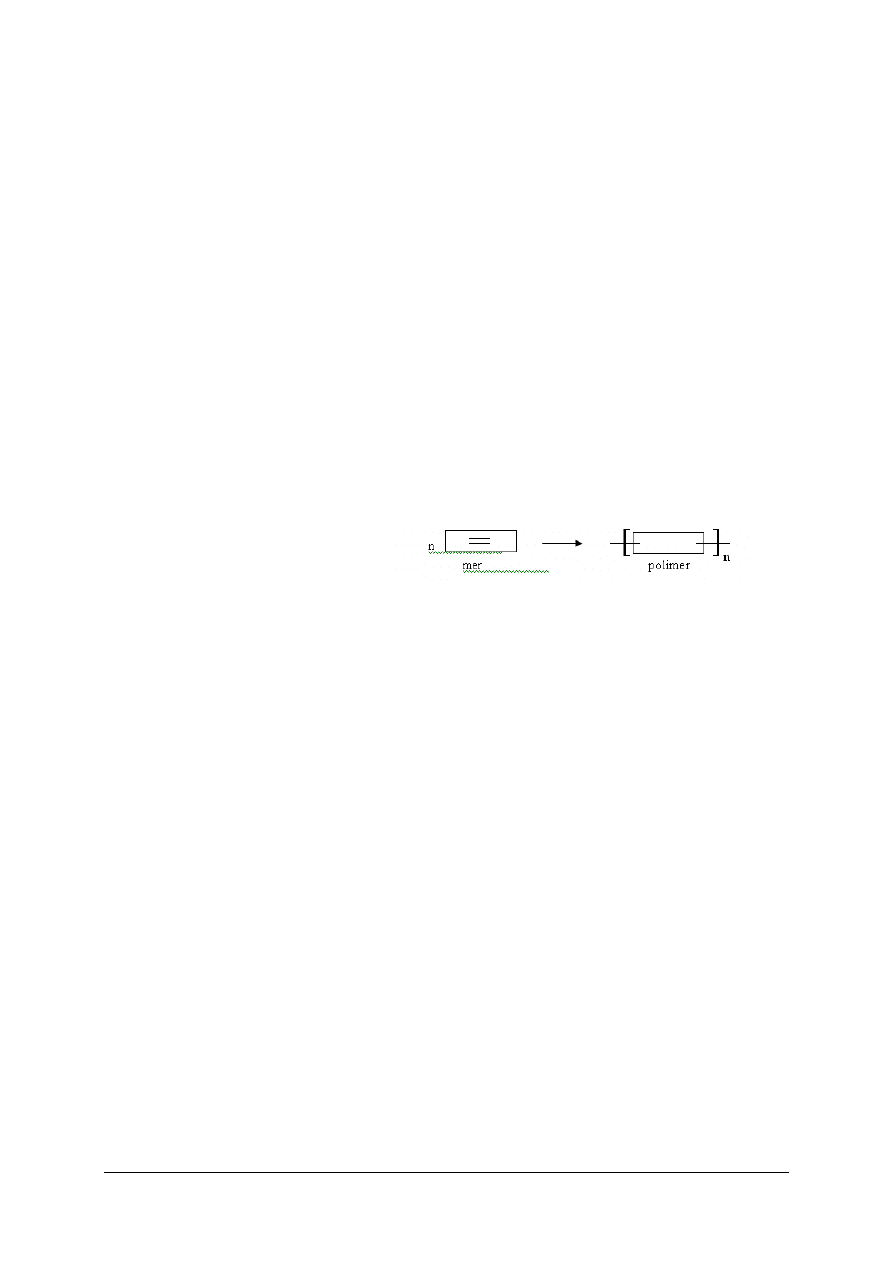
„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
33
21.
Do najczęściej stosowanych w przemyśle środków chlorujących należą
a)
chlorowodór i kwas solny.
b)
chlorowodór i siarkowodór.
c)
chlorowodór i chlor gazowy.
d)
chloran(V) potasu i kwas solny.
22.
Wzór CH
2
=CHCl przedstawia
a)
chlorek winylu.
b)
chlorek propylu.
c)
chloroetan.
d)
chloropropan.
23.
Reakcja monochlorowania 2 moli benzenu wymaga zastosowania
a)
22,4 dm
3
gazowego chloru.
b)
44,8 dm
3
gazowego chloru.
c)
2,24 dm
3
gazowego chloru.
d)
4,,48 dm
3
gazowego chloru.
24.
Przedstawiony schemat reakcyjny opisuje reakcję
a)
polikondensacji.
b)
poliaddacji.
c)
depolimeryzacji.
d)
polimeryzacji.
25.
Substancje, które wprowadzone do tworzywa zwiększają jego odporność na określone
czynniki, takie jak temperatura, oddziaływanie promieni ultrafioletowych to
a)
wypełniacze.
b)
stabilizatory.
c)
pigmenty.
d)
antystatyki.
26.
Z substancji o wzorze CH
2
=CH
2
produkowany jest
a)
polipropylen.
b)
polistyren.
c)
kauczuk.
d)
polietylen.
27.
Produktami reakcji zgazowania węgla kamiennego przegrzaną parą wodną są
a)
dwutlenek węgla i wodór.
b)
tlenek węgla i wodór.
c)
dwutlenek węgla i woda.
d)
tlenek węgla i woda.
28.
Do produkcji acetylenu wykorzystuje się głównie
a)
metan, etan i karbid.
b)
etan, propan i karbid.
c)
węglik wapnia, węglik glinu i metan.
d)
węgiel, wodór i wodę.
„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
34
29.
Masa wody zawarta w 2 tonach ropy naftowej zawierającej 0,1 % wody wynosi
a)
0,2 kg.
b)
2 kg.
c)
0,02 kg.
d)
20 kg.
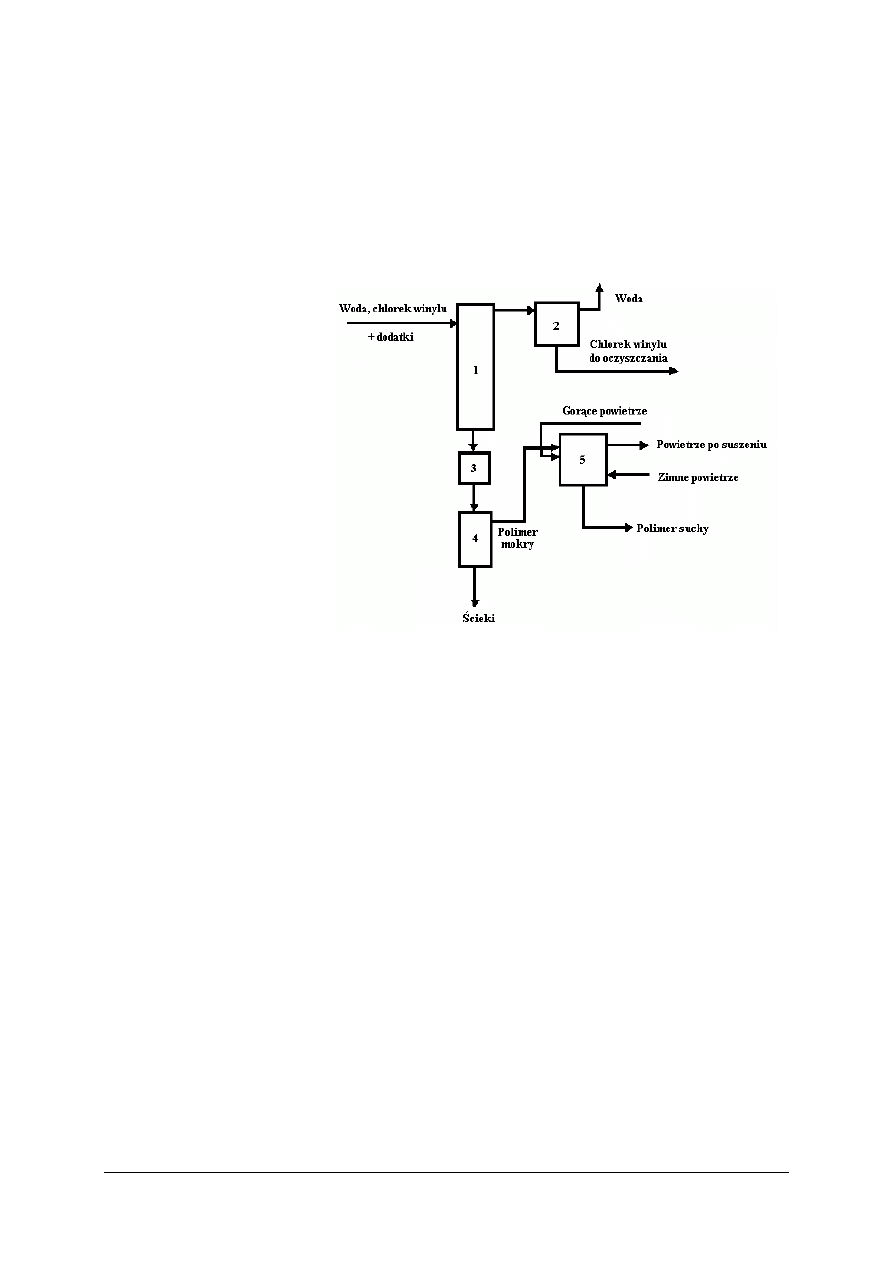
30.
Na przedstawionym uproszczonym schemacie technologicznym proces suszenia produktu
odbywa się w elemencie opisanym cyfrą
a)
1.
b)
2.
c)
4.
d)
5.
„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
35
KARTA ODPOWIEDZI
Imię i nazwisko................................................................................................................
Wytwarzanie podstawowych półproduktów i produktów organicznych
Zakreśl poprawną odpowiedź.
Nr
zadania
Odpowiedź
Punkty
1
a
b
c
d
2
a
b
c
d
3
a
b
c
d
4
a
b
c
d
5
a
b
c
d
6
a
b
c
d
7
a
b
c
d
8
a
b
c
d
9
a
b
c
d
10
a
b
c
d
11
a
b
c
d
12
a
b
c
d
13
a
b
c
d
14
a
b
c
d
15
a
b
c
d
16
a
b
c
d
17
a
b
c
d
18
a
b
c
d
19
a
b
c
d
20
a
b
c
d
21
a
b
c
d
22
a
b
c
d
23
a
b
c
d
24
a
b
c
d
25
a
b
c
d
26
a
b
c
d
27
a
b
c
d
28
a
b
c
d
29
a
b
c
d
30
a
b
c
d
Razem:

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
36
TEST 2
Test typu próba pracy do jednostki modułowej „Wytwarzanie
podstawowych półproduktów i produktów organicznych”
Proponowany test sumujący jest przeznaczony do przeprowadzenia po zakończonym
procesie kształcenia w jednostce modułowej „Wytwarzanie podstawowych półproduktów
i produktów organicznych”. Test ma charakter próby pracy i pozwala na ocenę umiejętności
uczniów w zakresie:
−
posługiwania się instrukcją,
−
organizacji stanowiska pracy laboratoryjnej,
−
posługiwania się sprzętem laboratoryjnym,
−
przestrzegania parametrów procesu,
−
przestrzegania zasad bhp i ppoż.
Test ma charakter sprawdzający, tzn. ukierunkowany jest na porównanie wyników
z założonymi w programie celami kształcenia.
Instrukcja dla nauczyciela
1.
Czas trwania testu 120 minut.
2.
Należy przygotować indywidualne stanowisko pracy dla każdego ucznia.
3.
Zapewnić dostęp do literatury potrzebnej do wykonania zadania.
4.
Omówić z uczniami przebieg testu praktycznego.
5.
Podczas testu nauczyciel pełni rolę obserwatora.
Uczeń może maksymalnie otrzymać 11 punktów.
Punktacja dla testu
−
test uczeń zaliczy jeśli uzyska 5 punktów,
−
ocena dostateczna 6–7 punktów,
−
ocena dobra 8–9 punktów,
−
ocena bardzo dobra 10–11 punktów.
Instrukcja dla ucznia
1.
Przeczytaj uważnie instrukcję wykonania zadania.
2.
Zanim przystąpisz do wykonania zadania, zaplanuj pracę. Pomoże Ci w tym KARTA
PRACY.
3.
Odpowiedzi wpisuj w wyznaczonych miejscach KARTY.
4.
Pracuj samodzielnie.
5.
Po zakończeniu zadania oddaj nauczycielowi KARTĘ PRACY.
6.
Powodzenia.
Na wykonanie zadania masz 90 minut.
Powodzenia!

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
37
Treść zadania
W wielu gałęziach przemysłu i w życiu codziennym stosuje się tworzywa sztuczne.
Podstawą tworzywa sztucznego jest polimer. Jedną z metod otrzymywania polimeru jest
polimeryzacja. Twoje zadanie polega na przeprowadzeniu procesu polimeryzacji emulsyjnej
styrenu oraz uzyskanie polistyrenu w warunkach laboratoryjnych.
Instrukcja wykonania zadania
Aby wykonać zadanie powinieneś:
1)
wnikliwie przeczytać instrukcję wykonania zadania,
2)
wykonać czynności laboratoryjne opisane w instrukcji otrzymywania polistyrenu metodą
emulsyjną,
3)
przestrzegać przepisy bhp i ppoż. w czasie wykonywania czynności laboratoryjnych,
4)
przestrzegać ład i porządek na stanowisku pracy,
5)
uporządkować stanowisko pracy po jej zakończeniu.
Wyposażenie stanowiska pracy:
Odczynniki:
–
styren,
–
kwas oleinowy,
–
wodorotlenek sodu,
–
nadsiarczan potasu K
2
S
2
O
8,
–
nasycony roztwór ałunu glinowo-potasowego: AlK(SO
4
)
2
·12H
2
O.
Sprzęt laboratoryjny:
–
kolba okrągłodenna (pojemność 200–250 cm
3
),
–
zlewka (pojemność 400 cm
3
),
–
chłodnica powietrzna pionowa,
–
elektryczny płaszcz grzewczy,
–
zestaw do sączenia (filtracji),
–
suszarka.
Instrukcja otrzymywania polistyrenu metodą emulsyjną
1.
Wlej do kolby 100 cm
3
wody destylowanej i 4,0 cm
3
kwasu oleinowego, mieszaninę
należy dobrze wymieszać.
2.
Do powstałej emulsji dodaj około 0,9 g stałego wodorotlenku sodu.
3.
Zawartość kolby dobrze wymieszaj, aż do utworzenia się trwałej piany.
4.
Ciągle mieszając dodaj do mieszaniny w kolbie 50 cm
3
styrenu i 1,3 g nadsiarczanu
potasu.
5.
Nałóż na kolbę pionową chłodnicę powietrzną i rozpocznij ogrzewanie kolby.
6.
Ogrzewaj emulsję przez około 12 minut, co pewien czas mieszając (wstrząsając)
zawartość kolby. Przygotuj w międzyczasie zlewkę z 200 cm
3
nasyconego roztworu ałunu
glinowo-potasowego.
7.
Po zakończeniu ogrzewania przelej emulsję z kolby do zlewki z roztworem ałunu.
8.
Stały produkt reakcji przefiltruj i wysusz.

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
38
Karta pracy
Nazwisko i imię ucznia
Data
Uzyskana liczba
punktów
Lp.
Elementy zadania
Odpowiedź (krótki opis)
1.
Wyposażenie stanowiska pracy
2.
Przygotowanie mieszaniny
reakcyjnej
3.
Ogrzewanie mieszaniny
reakcyjnej
4.
Odfiltrowanie produktu
5.
Suszenie produktu

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
39
Karta obserwacji
Lp.
Czynność
Maksymalna
liczba
punktów
Uzyskana
liczba
punktów
1.
Wyposażenie stanowiska pracy
1
Dobór sprzętu
1
Kolejność wykonywanych
czynności laboratoryjnych
1
2.
Przygotowanie mieszaniny
reakcyjnej
Przestrzeganie zasad bhp
i ppoż.
1
Dobór sprzętu
1
3.
Ogrzewanie mieszaniny
reakcyjnej
Przestrzeganie zasad bhp
i ppoż.
1
Dobór sprzętu
1
4.
Odfiltrowanie produktu
Ład i porządek na
stanowisku pracy
1
Dobór sprzętu
1
5.
Suszenie produktu
Ład i porządek na
stanowisku pracy
1
6.
Uporządkowanie stanowiska pracy po jej zakończeniu
1

„
Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
40
7.
LITERATURA
1.
Klepaczko-Filipiak B., Jakubiak Z., Wulkiewicz U.: Produkcja chemiczna. Podręcznik
dla uczniów liceum technicznego o profilu chemicznym. WSiP,
2.
Kwiatkowski A.: Technologia chemiczna ogólna i nieorganiczna. Wydawnictwo
Politechniki Gdańskiej, Gdańsk 1982
3.
Molenda J.: Chemia w przemyśle. WSiP, Warszawa 1996
4.
Molenda J.: Chemia techniczna. WNT, Warszawa 1985
5.
Molenda J.: Technologia chemiczna. WSiP, Warszawa 1996
6.
Wielopolski A.: Technologia chemiczna organiczna. PWN, Warszawa 1959
Strony internetowe
7.
www.retsat1.com.pl/michauer/chemia/O_tech_org.pdf
Wyszukiwarka
Podobne podstrony:
operator urzadzen przemyslu chemicznego 815[01] z2 03 u
operator urzadzen przemyslu chemicznego 815[01] z2 01 u
operator urzadzen przemyslu chemicznego 815[01] z1 03 n
operator urzadzen przemyslu chemicznego 815[01] z2 01 n
operator urzadzen przemyslu chemicznego 815[01] o1 03 u
operator urzadzen przemyslu chemicznego 815[01] o2 03 n
operator urzadzen przemyslu chemicznego 815[01] z2 02 u
operator urzadzen przemyslu chemicznego 815[01] o1 03 n
operator urzadzen przemyslu chemicznego 815[01] z1 03 u
operator urzadzen przemyslu chemicznego 815[01] o2 03 u
operator urzadzen przemyslu chemicznego 815[01] z2 01 u
operator urzadzen przemyslu chemicznego 815[01] z1 03 n
operator urzadzen przemyslu chemicznego 815[01] z1 04 n
operator urzadzen przemyslu chemicznego 815[01] z1 02 u
operator urzadzen przemyslu chemicznego 815[01] o2 01 n
operator urzadzen przemyslu spozywczego 827[01] z2 03 n
operator urzadzen przemyslu chemicznego 815[01] o2 02 n
więcej podobnych podstron