
1
ŻELOWANIE – Ogólna Technologia Żywności II rok WNoŻiŻ
Hydrokoloidy
Substancje zagęszczające i żelujące zaliczane są do hydrokoloidów - biopolimerów o dużej
masie cząsteczkowej (100 000 – 1 000 000 D), rozpuszczalnej w wodzie lub tworzące w niej
zawiesinę. Zwiększają lepkość roztworów lub tworzą żele, często wykazują również właściwości
emulgujące i stabilizujące. Stosuje się je również do zapobiegania retrogradacji, stabilizacji emulsji,
lepszego związania wody, ukształtowania odpowiedniej tekstury produktu.
Pod względem budowy chemicznej hydrokoloidy dzielą się na polisacharydowe i białkowe, a
dodatkowymi cechami różnicującymi są:
rodzaj łańcucha (prosty lub rozgałęziony)
typ reaktywnej grupy bocznej (np. hydroksylowa, siarczanowa, karboksylowa,
aminowa)
powinowactwo elektryczne (np. polisacharydy anionowe, obojętne)
Podstawy tworzenia się żeli
Żelowanie jest to proces przejścia zolu lub roztworu wielkocząsteczkowego w żel, czyli
układ koloidowy który utracił swą płynność wskutek wzajemnego oddziaływania między
cząsteczkami zolu.
Strukturę żelu zależnie od rodzaju polimeru tworzą wiązania hydrofobowe i wodorowe oraz
wiązania jonowe i kowalencyjne. Proces żelowania może zostać zainicjowany pod wpływem
czynników fizycznych takich jak zmiany temperatury lub chemicznych.
Proces tworzenia roztworu lub dyspersji o wysokiej lepkości przez hydrokoloidy polega na
przyłączaniu się cząstek wody do polimeru za pomocą wiązań wodorowych. Proces ten przebiega w
środowisku wodnym i powoduje zwiększenie efektywnej wielkości cząsteczek, ograniczając ich
naturalne tendencję do zwijania się w ścisłe, zbite kształty. Wynikiem procesu żelowania jest
utworzenie roztworu lub dyspersji o wysokiej lepkości.
Cząsteczki mogą się łączyć ze sobą w następujący sposób:
a) liniowo jedna z drugą na części swojej długości za pomocą wiązań poprzecznych i w ten
sposób tworzyć mocne żele
b) znacznie rozgałęzione cząsteczki mogą łączyć się ze sobą jedynie w paru punktach tworząc
żele o innej charakterystyce.

2
Żelowanie hydrokoloidów zachodzi na drodze:
1. asocjacji makrocząsteczek
2. tworzenia się wiązań chemicznych (wodorowych, elektrostatycznych, kowalencyjnych)
między makrocząsteczkami lub cząsteczkami koloidów
3. indukcji termicznej (najczęściej) lub chemicznej oraz obecności jonów metali np.
wapnia, potasu, magnezu.
1. Formowanie żelu hydrokoloidów białkowych (żelatyna)
Żelowanie przebiega na ogół dwustopniowo. Najpierw dysocjują struktury czwartorzędowe
i rozfałdowują się łańcuchy polipeptydowe wskutek denaturacji lub częściowej hydrolizy
polimerów. Zdenaturowane cząsteczki w łańcuchach polipeptydowych oddziałując między sobą
wiązaniami wodorowymi, tworzą trójwymiarową strukturę. Oziębienie układu zazwyczaj ją
stabilizuje. Jeśli szybkość tworzenia struktury jest mniejsza niż szybkość denaturacji, to powstaje
uporządkowana sieć przezroczystego, odwracalnego żelu.
Żelatyna tworzy żel już w 0,5-1,0% schłodzonym wodnym roztworze zgodnie z formułą:
ŻEL ZOL
Proces jest odwracalny – po ogrzaniu żel przechodzi w zol.
Lepkość żelu wzrasta wykładniczo ze wzrostem stężenia roztworu oraz ze spadkiem temperatury.
Do wytworzenia galaretki żelatyna nie wymaga obecności cukru.
2. Formowanie żeli hydrokoloidów polisacharydowych
Formowanie żeli pektynowych
Szybkość żelowania preparatów pektynowych zależy głównie od stopnia estryfikacji pektyn
(stopień estryfikacji jest określony jako stosunek liczby zestryfikowanch jednostek kwasu
galakturonowego do łącznej liczby jednostek kwasu galakturonowego w cząsteczce). Stopień
estryfikacji stanowi podstawę klasyfikacji pektyn na wysoko i niskometylowane.
1) Pektyny wysokometylowane HM są to rozpuszczalne w wodzie estry alkoholu metylowego i
kwasu poligalakturonowego o stopniu zestryfikowania grup karboksylowych powyżej 50%, co
odpowiada zawartości grup metoksylowych (CH
3
O-) 8-12%.
Optymalną zdolność żelowania pektyny wysokometylowanej (HM) uzyskuje się w następujących
warunkach: stężenie cukru 65%, pH 3,5 i stężenie pektyny 0.3-2%, w zależności od zdolności
żelowania preparatu pektynowego.
40C
30C
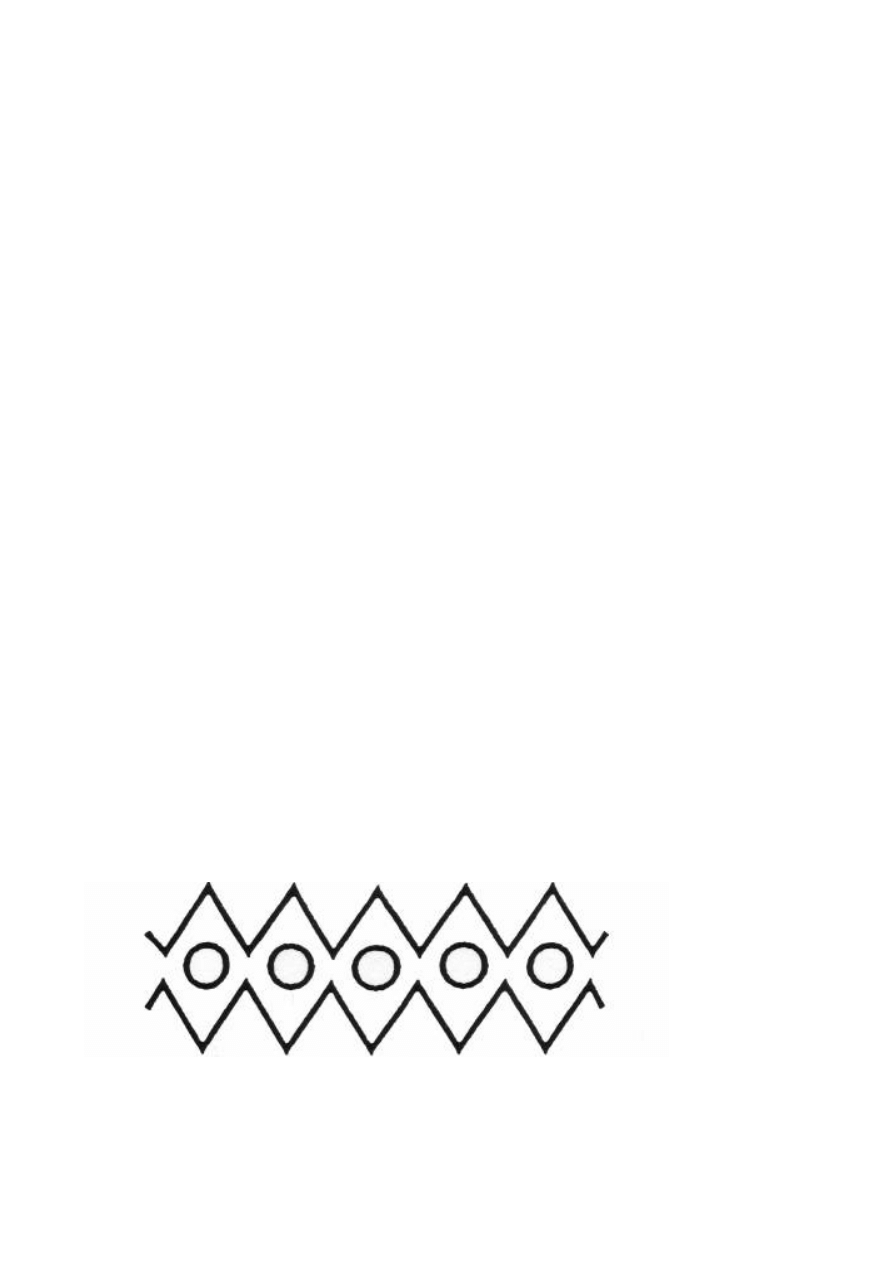
3
Pektyna rozpuszczona w wodzie lub roztworze cukru tworzy układ koloidalny, w którym cząsteczki
związków pektynowych są zdysocjonowane i tworzą ujemny ładunek elektryczny, a to powoduje że
odpychają się wzajemnie. Obniżenie pH przez dodatek kwasu powoduje cofnięcie dysocjacji grup
karboksylowych pektyn, a tym samym ich neutralizację czyli obniżenie ładunku elektrycznego i
utworzenia się siatki przestrzennej. Dodatek cukru powoduje odciągnięcie cząsteczek wody od
cząsteczek pektyny i skupienie ich wokół cząsteczek cukru, co ułatwia tworzenie się wiązań
wodorowych między grupami hydroksylowymi (-OH) łańcuchów pektynowych.
Cząsteczki pektyn ulegają w roztworze ruchom drgającym i ruchom Browna, a energia kinetyczna
tych cząsteczek wzrasta w miarę wzrostu temperatury podgrzewania roztworu. Obniżając
temperaturę uzyskuje się zmniejszenie wartości energii kinetycznej cząsteczek pektyn, a przez to
wiązania tworzące siatkę przestrzenną żelu są trwalsze.
Temperatura żelowania zwiększa się wraz ze wzrostem stopnia estryfikacji, z obniżeniem pH
środowiska i wzrostem zawartości ekstraktu
.
Stosując odpowiednio wysoko zestryfikowaną pektynę można np. wydłużyć czas żelowania
rozlewanych dżemów, tak aby nie następowało ich żelowanie już w naczyniu napełniającym.
2) Pektyny nikskometylowane (LM) są to rozpuszczalne w wodzie estry alkoholu metylowego i
kwasu poligalakturonowego o stopniu zestryfikowania grup karboksylowych poniżej 50%, gdzie
zawartość grup metoksylowych CH
3
O- wynosi 7%.
Pektyny niskometylowane zdolne są do tworzenia żeli niskocukrowych (stężenie cukru 30-40%) w
obecności jonów Ca
2+
. W cząsteczkach pektyn LM istnieją mocno związane obszary, utworzone
przez jednostki kwasu galakturonowego położone naprzeciwko siebie w linii zygzakowatej. Układ
taki związany zostaje jonami Ca
2+
, które wchodzą w połączenia z grupami karboksylowymi i
hydroksylowymi łańcucha pektynowego. Taki model żelu pektyn LM określony jest jako egg- box
czyli „pudełko na jaja” (ryc. 1).
Ryc. 1. Model żelu pektyny LM egg-box. O – jony Ca
2+

4
Niezbędne stężenie jonów wapnia powinno wynosić 0,01-0,1%, pH 3-6 a stężenie pektyny
1,5-3%. Temperatura żelowania jest tym wyższa im niższy stopień estryfikacji, niższe pH i większa
zawartość ekstraktu. W przeciwieństwie do pektyny HM żel pektyny LM może być roztopiany
przez podgrzewanie. Żele te są podatne na synerezę.
Formowanie żelu skrobi
Ziarna skrobi są nierozpuszczalne w zimnej wodzie, podczas podgrzewania wodnej
zawiesiny skrobi natywnej następuje wzrost jej lepkości. Siły wiążące pomiędzy poszczególnymi
łańcuchami skrobi ulegają osłabieniu i do ziarna skrobi wnika woda, ziarna te pęcznieją i
powiększają się, a powyżej pewnej temperatury, innej dla każdego gatunku skrobi, otoczka ziaren
pęka, wydobywa się z nich amyloza, której liniowe proste lub spiralnie skręcone łańcuchy za
pośrednictwem wiązań wodorowych, tworzą trójwymiarową sieć unieruchamiającą znaczne ilości
wody. Struktura tych ziaren ulega wówczas nieodwracalnemu zniszczeniu powodując jednocześnie
wzrost lepkości roztworu. Właściwości żelujące skrobi są zależne głównie od frakcji amylozy.
Temperaturę odpowiadającą tym przemianom nazywa się temperaturą kleikowania. Gdy taki
roztwór odstawi się na pewien czas, przy dużej koncentracji skrobi tworzy się trójwymiarowa
usieciowana konstrukcja żelu.
Żele amylozy wykazują tendencję do retrogradacji, czyli nieodwracalnej przemiany skrobi
rozpuszczalnej lub zdyspergowanej w formę nierozpuszczalną – mikrokrystaliczną, co powoduje
wytrącanie się osadów lub zmianę konformacji produktów skrobiowych.
Żel skrobi modyfikowanej uzyskuje się w wyniku obróbki chemicznej, fizycznej lub
enzymatycznej. Te metody modyfikacji skrobi mają na celu polepszenie określonych właściwości
skrobi lub nadanie nowych specyficznych dla danego preparatu właściwości, np. dodatek
acetylowanych adypinianów dwuskrobiowych (E 1422) do jogurtów w ilości od 0.6 do 1.0%
wpływa na ich stabilizację powodując, że jogurty są gęste, kremowe o niezmienionym smaku.
Otrzymywanie skrobi modyfikowanych przez utlenianie może odbywać się za pomocą różnego
rodzaju czynników chemicznych: podchlorynów, wody utlenionej i nadtlenków, nadmanganianów,
chloranów, itp. W łańcuchach skrobi powstają grupy aldehydowe, karboksylowe, karbonylowe.
Najstarszym a jednocześnie najpowszechniej stosowanym sposobem jest utlenianie za pomocą
podchlorynu sodu (5,5%NaOCl) z niewielkim dodatkiem NaOH (pH 9-10).
5
Formowanie żeli karagenów
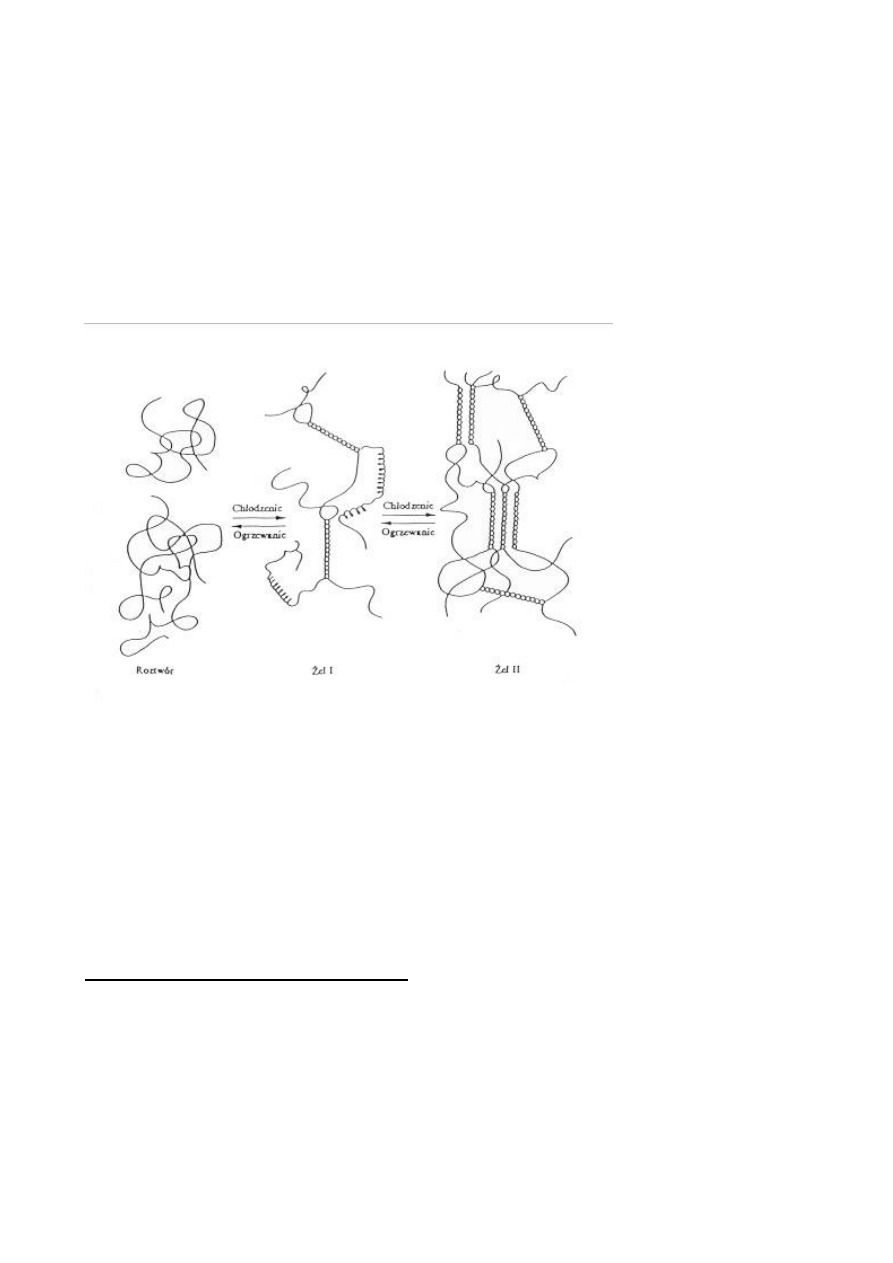
Mechanizm formowania żelu związany jest ze strukturą konformacyjną karagenu, który
tworzy podwójne spirale (ryc. 2). Przy zbliżonej sekwencji łańcuchów moc żeli karagenowych jest
tym większa im bardziej jednorodna jest sekwencja łańcucha, ponieważ możliwe jest wówczas
utworzenie podwójnej spirali o większej długości, dzięki czemu wzajemne dopasowanie spirali jest
lepsze. Podczas schładzania zolu powstaje trójwymiarowa struktura sieciowa.
Ryc. 2. Schemat procesu żelowania karagenu
Duży wpływ na zdolność żelowania karagenów oraz jakość żeli ma obecność jonów metali:
potasu, wapnia i amonu: kappa karagen tworzy najmocniejsze i najbardziej elastyczne żele w
obecności K
+
, a jota karagen w obecności Ca
2+
. Ze wzrostem stężenia KCl rośnie sztywność i siła
żelu.
Galaretki karagenowe żelują w temperaturze 30˚C, a rozpływają się w temperaturze 45˚C.
Czynniki wpływające na proces żelowania
1. Stężenie
Szybkość formowania żeli zwiększa się wraz ze wzrostem stężenia roztworu, w wyniku
zwiększonej liczby zderzeń cząsteczek. W przypadku gdy cząstki wykazują nitkowatą formę,
żelowanie może zachodzić przy bardzo niskim ich stężeniu.

6
2. Temperatura
Szybkość żelowania maleje wraz ze wzrostem temperatury wskutek wzrostu energii kinetycznej
cząsteczek roztworu i związanej z tym większej trudności ich uporządkowania. Temperatura
żelowania jest niższa niż temperatura przejścia żelu w zol. Im niższe stężenie, tym niższa
temperatura żelowania.
3. Budowa cząsteczek
Cząsteczki nitkowe lub blaszkowe tworzą żele o wiele łatwiej niż cząsteczki kuliste. Proste
łańcuchy amylozy o wiele łatwiej żelują niż rozgałęzione łańcuchy amylopektyny. Cząsteczki o
małym stopniu spolimeryzowania nie posiadają zdolności żelowania np. pektyny o masie
cząsteczkowej 50 000, dopiero cząsteczki o masie powyżej 100 000 (do 350 000) są zdolne do
żelowania. Żelatyna o masie cząsteczkowej 10 00- 15 000 również nie tworzy żelu.
4. Obecność związków odciągających wodę
W łańcuchach pektynowych grupy karboksylowe –COOH i hydroksylowe –OH są otoczone
osłonkami wodnymi. Dodatek cukru przy otrzymaniu żelu pektynowego niszczy te osłony czyli
dehydratyzuje grupy –OH, –COOH w cząsteczkach kwasu galakturonowego, które w ten sposób
mogą wytworzyć silne wiązania pomiędzy cząsteczkami pektyny.
Zjawiska związane z żelowaniem
1. Retrogradacja
Jest to zjawisko charakterystyczne dla żeli skrobiowych. Polega ono na wytworzeniu pomiędzy
sąsiednimi cząsteczkami amylozy mostków wodorowych i powstaniu struktury krystalicznej z
jednoczesnym wydzieleniem wody. Wskutek przybliżenia się łańcuchów skrobi następuje
wypchnięcie wody na zewnątrz. Retrogradacji sprzyja duża zawartość amylozy. Zjawisko to nie
występuje w wysokich temperaturach (55-70C), a jego tempo jest bardzo powolne w niskich
temperaturach (poniżej –20C). Retrogradacja jest odpowiedzialna m. in. za czerstwienie pieczywa,
rozwarstwienie sosów i zup zagęszczonych skrobią, mąką.
2. Synereza
Jest to samoczynne zmniejszenie się ilości żelu wskutek powstawania dodatkowych wiązań
poprzecznych, powodujących zmniejszenie się miejsca dla wody i jej wypchnięcie na zewnątrz.
Przykładem może być starzenie się zsiadłego mleka i oddzielenie serwatki.

7
3. Tiksotropia
Jest to odwracalny izotermiczny proces przemiany żelu w zol pod wpływem bodźców
mechanicznych (np. wytrząsanie, mieszanie). Czynności te powodują, że cząstki koloidowe w żelu
ulegają odwracalnej solwatacji, której siła jest mniejsza od siły wiążącej z powrotem skoagulowane
cząstki, co powoduje, że na nowo tworzy się żel.
Charakterystyka hydrokoloidów żelujących
Żelatyna E 441
Jest to produkt cieplnej degradacji kolagenu (białka z grupy skleroprotein), głównego składnika
tkanki łącznej skóry i kości zwierząt uzyskanego w procesie hydrolizy alkalicznej lub kwaśnej, a
następnie ekstrahowanego gorącą wodą. Żelatyna zawiera znaczne ilości proliny, hydroksyproliny,
glicyny, alaniny i kwasu glutaminowego i 15 innych aminokwasów.
A.D.I.: nie dotyczy
(ADI Accetable Daily Intake – dopuszczalne dzienne spożycie)
Właściwości: substancja żelująca, zagęstnik, stabilizator
Zastosowanie: do produkcji galaret mięsnych i rybnych, dodawana jest do wyrobów
garmażeryjnych i konserw mięsnych w ilościach 4-10%, do wyrobów cukierniczych trwałych,
kremów owocowych, deserów, pianek i galaretek, stabilizacji lodów, jako środek klarujący soki,
wina.
Dodatek żelatyny w ilości 0.2% do 0.6% korzystnie wpływa na lepkość i cechy organoleptryczne
jogurtu oraz zapobiega synerezie.
Pektyny E 440
Związki pektyn są obecne we wszystkich tkankach roślin, bulwach łodygach, słomie i owocach,
gdzie występują w ścianach komórkowych, blaszkach środkowych, i przestrzeniach
międzykomórkowych roślin. Są odpowiedzialne za strukturalne właściwości roślin. Pektyny są
heteropolisacharydami, których główny szkielet stanowi łańcuch nierozgałęziony, zbudowany z
cząsteczek kwasu galakturonowego, częściowo zestryfikowanego alkoholem metylowym,
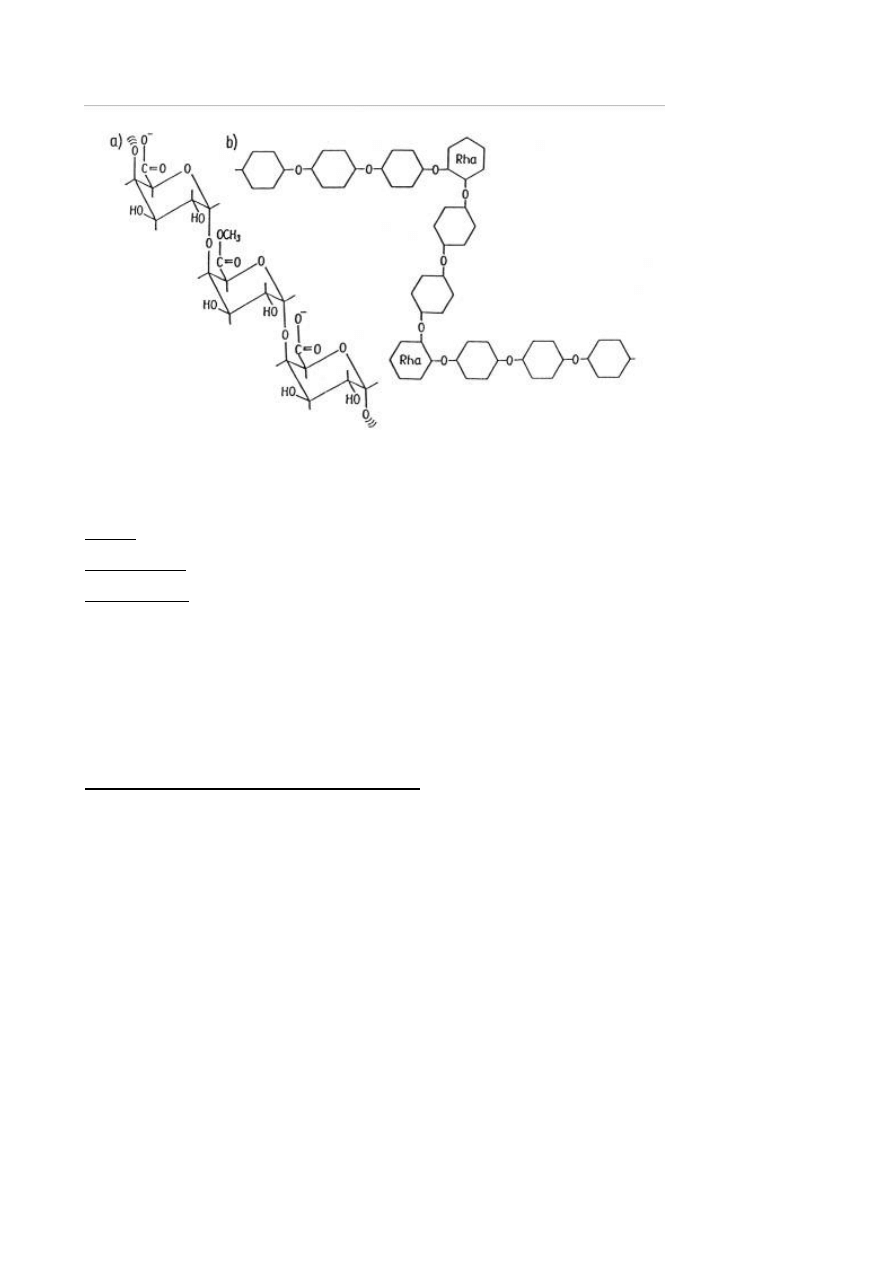
połączonych wiązaniami glikozydowmi (ryc. 3a). W skład pektyn wchodzą również cukry tworzące
łańcuchy boczne, są to głównie ksyloza, galaktoza i arabinoza. Na dziesięć cząsteczek kwasu
galakturonowego przypada jedna cząsteczka L-ramnozy, połączonej z kwasem galakturonowym
wiązaniem α-(1-2), co powoduje skręcenie łańcucha (ryc. 3b).
8
Ryc. 3. Schemat struktury chemicznej łańcucha pektyny
A.D.I.: nie określono
Właściwości: substancja żelująca, stabilizująca
Zastosowanie: pektyny HM stosowane są w produkcji: dżemów, galaretek owocowych, nadzień
cukierniczych owocowych, napojów bezalkoholowych; pektyny LM w produkcji: dżemów
niskosłodzonych, nadzień cukierniczych owocowych, półproduktów owocowych do napojów
mlecznych, keczupu, jako składniki wsadów owocowych do produkcji jogurtów, w przemyśle
piekarskim, cukierniczym, koncentratów.
Skrobia modyfikowana tzw. żelująca E1404
Skrobia to materiał zapasowy roślin. Gromadzi się w nasionach i korzeniach: w ziarnach zbóż,
ziemniakach, nasionach roślin strączkowych, warzywach i niektórych owocach. Jest
polisacharydem zbudowanym z jednostek d-glukozy. Cząsteczki glukozy w skrobi połączone są
wiązaniem glikozydowym. W zależności od sposobu powiązania cząsteczek d-glukozy powstaje
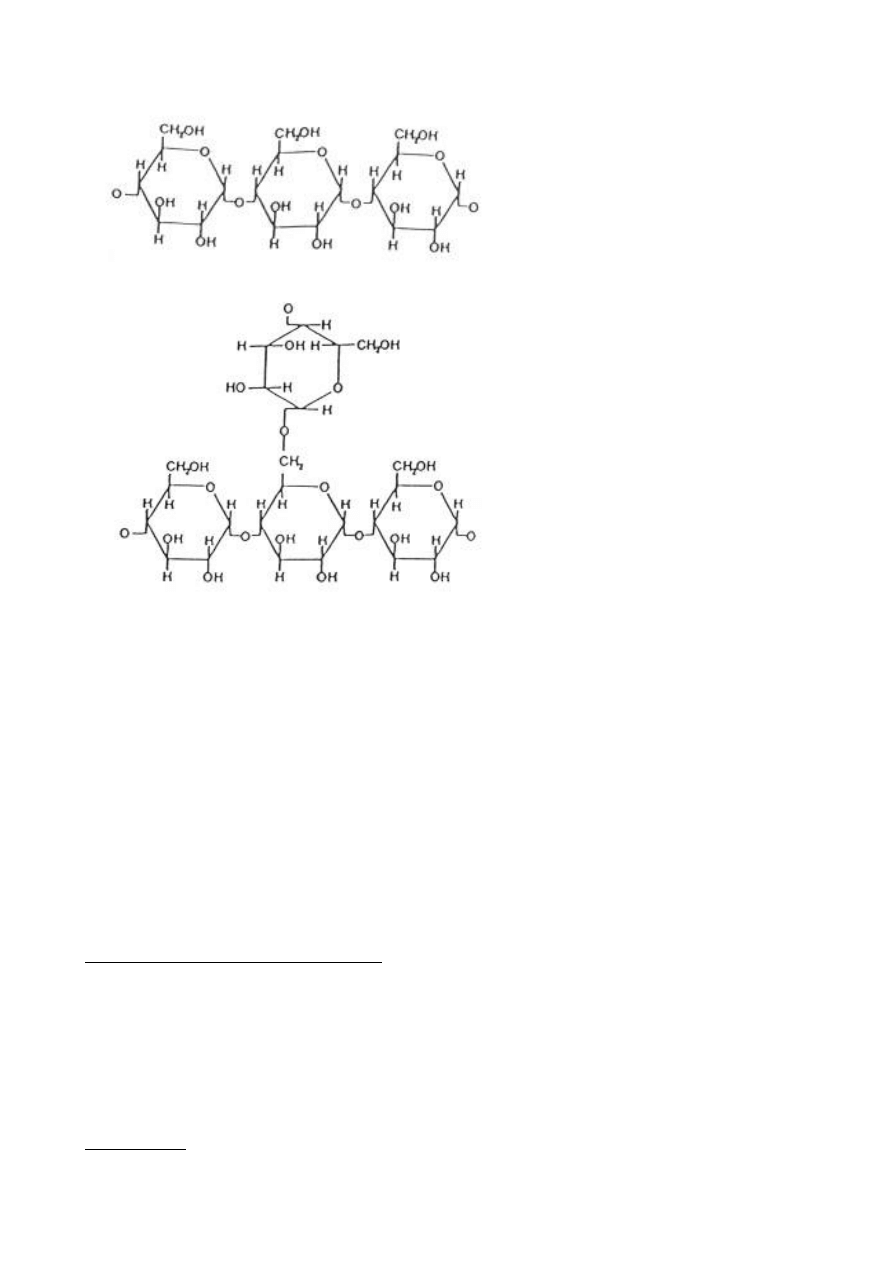
amyloza lub amylopektyna, które są podstawowymi składnikami skrobi (ryc.4).
9
Ryc.4. Schemat struktury chemicznej amylozy i amylopektyny
Skrobia łatwo ulega depolimeryzacji pod wpływem czynników fizycznych i chemicznych.
Jednostki glukozy w cząsteczce skrobi zawierają trzy grupy hydroksylowe, które łatwo wchodzą w
reakcje, tworząc estry lub estry skrobiowe. Ponadto wiązania glikozydowe łatwo ulegają
rozerwaniu pod wpływem kwasów, podchlorynu sodowego, enzymów, co także powoduje
depolimeryzację i spadek lepkości skrobi.
Wśród skrobi modyfikowanych stosowanych w żywności wyróżnia się grupy:
- skrobie modyfikowane enzymatycznie
- skrobie modyfikowane za pomocą hydrolizy kwasowej
- skrobie modyfikowane przez utlenianie i hydrolizę podchlorynem sodu
Niektóre modyfikacje skrobi i ich efekty:
Usieciowani: decyduje o teksturze produktu
Stabilizacja: podwyższa trwałość magazynowanych produktów końcowych
Dekstrynowanie: podwyższa rozpuszczalność skrobi, wyklucza zdolność do pęcznienia
Hydroliza kwasowa: podwyższa rozpuszczalność skrobi, obniża zdolność zagęszczania
Utlenianie: zwiększenie przejrzystości, obniżona zdolność zagęszczania
Właściwości: substancja zagęszczająca, żelująca, stabilizująca.
odcinek amylozy
odcinek amylopektyny
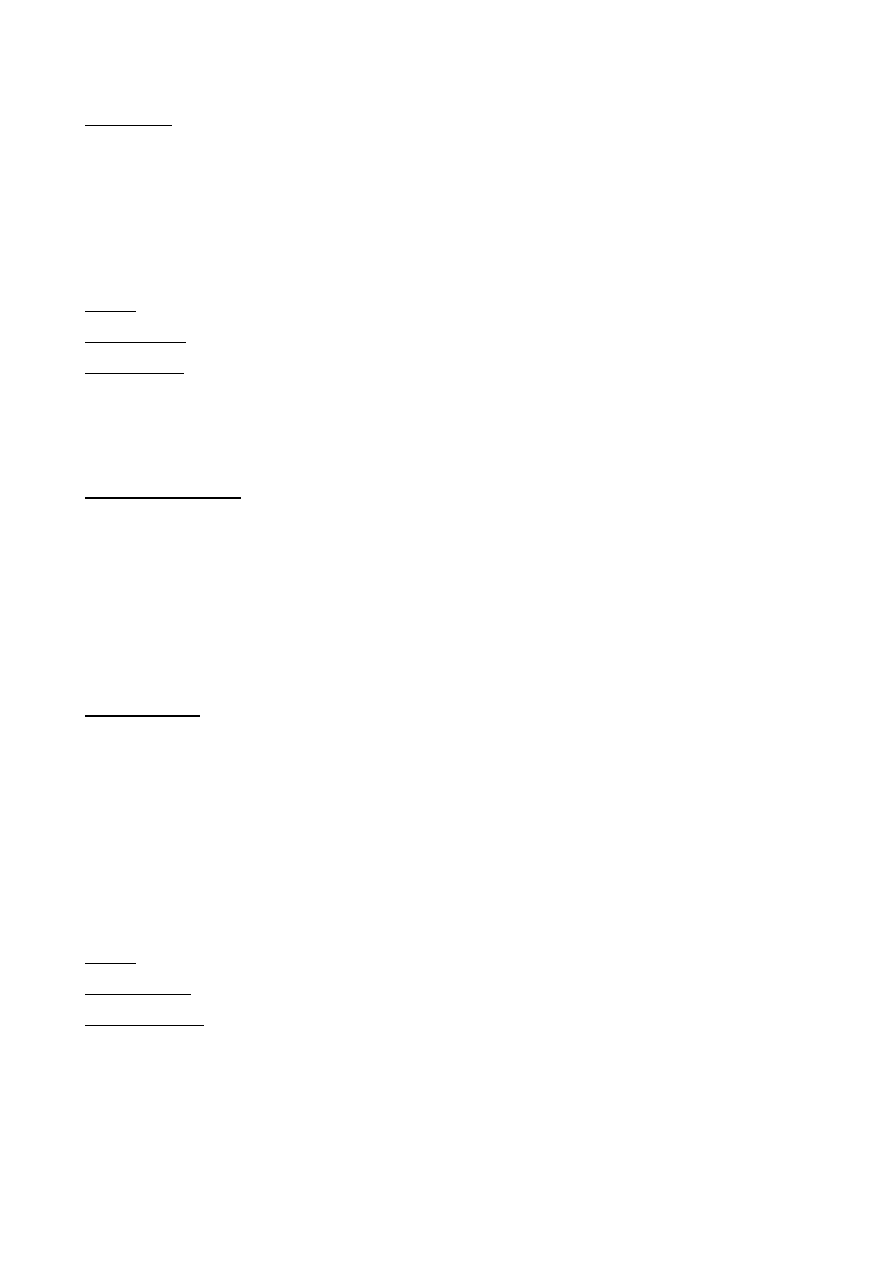
10
Agar E 406
Jest to ekstrakt z czerwonych alg morskich rosnących u wybrzeży Cejlonu, Japonii i Korei
stanowiący mieszaninę polisacharydów o m.cz. 120 000. Agar nie rozpuszcza się w zimnej wodzie,
natomiast jest dobrze rozpuszczalny w wodzie wrzącej (najlepiej przy pH 8-9). Po ostudzeniu do
temperatury 36-40ºC tworzy zwarte, klarowne i odwracalne termicznie żele. Dodatek cukru
zwiększa odporność żelu na hydrolizę.
A.D.I.: nie określono
Właściwości: zagęstnik, substancja żelująca, stabilizator
Zastosowanie: do wyrobuzżelowanych produktów owocowych, klarowania win, soków, octu,
lodów, przetworów mięsnych i rybnych o jędrnej galarecie, do produkcji wyrobów cukierniczych
trwałych, koncentratów, deserów w proszku, margaryny o obniżonej kaloryczności, twarogów
terminizowanych.
Alginiany E 401-405
Otrzymuje się je z wodorostów morskich z rodziny Phaeophyceae (algi brązowe) jako mieszaninę
soli sodowej i magnezowej kwasu alginowego o m. cz. 32 000 - 50 000. Sól sodowa kwasu
alginowego (alginian sodowy) jest rozpuszczalna w wodzie, dając roztwory o dużej lepkości.
Wprowadzenie do takiego roztworu soli wapnia powoduje wzrost lepkości aż do utworzenia żelu.
Alginiany są rozpuszczalne w wodnych roztworach przy pH zbliżonym do obojętnego. Żele
alginowe charakteryzują się dużą stabilnością w wysokiej temperaturze.
Karagen E 407
Jest to mieszanina hydrokoloidów otrzymywana z czerwonych glonów morskich Rodophyceae
biorących swoją nazwę od okręgu w Irlandii – Carragheen oraz alg bałtyckich (Furcellearia
fastigate). Pod względem chemicznym karagen jest estrem kwasu siarkowego kompleksu D i L-
galaktozy oraz 3,6- anhydro-D-glalaktozy. Wyróżnia się trzy główne typy karagenów: kappa, jota,
lambda z których pierwsze dwa tworzą żele. W obecności jonów potasu karageny są stosowane
jako czynnik żelujący przy produkcji deserów i dżemów o małej zawartości cukru.
Dodatek cukru zwiększa też odporność żelu na hydrolizę.
A.D.I.: nie określono
Właściwości: substancja żelująca, stabilizująca
Zastosowanie; do wyrobu przetworów owocowych typu konfitur, galaretek owocowych
niskosłodzonych, w przemyśle mleczarskim do wyrobu jogurtów smakowych i terminizowanych,
serów topionych, twarogów terminizowanych, w przemyśle piekarskim, cukierniczym,
koncentratów, mięsnym, rybnym.

11
ŻELOWANIE
WYKONANIE ĆWICZENIA
Celem ćwiczenia jest zapoznanie studentów z właściwościami żelującymi wybranych
hydrokoloidów oraz wpływem dodatków i innych czynników technologicznych na zmiany tych
właściwości.
1. Z przygotowanych hydrokoloidów: pektyny wysoko i niskometylowanej, agaru, żelatyny i
karagenu wykonać żele wg zamieszczonego przepisu.
2. Określić warunki w jakich dany hydrokoloid tworzy zwarte żele. W przypadku braku
żelowania podać przyczyny nie utworzenia się struktury żelu.
3. Zbadać odwracalność termiczną i mechaniczną otrzymanych żeli.
4. Podać charakterystykę hydrokoloidów, których żele zostały wykonane: budowę
pochodzenie i zastosowanie w przemyśle spożywczym.
W
YKONANIE ŻELU PEKTYNY WYSOKOMETYLOWANEJ
(HM)
1 wariant
Odważyć 3g preparatu pektynowego i wymieszać z ok. 25 g mielonego cukru, po czym przenieść
do wytarowanego wraz z łyżeczką porcelanową garnka zawierającego 160 cm
3
wody destylowanej.
Mieszać łyżeczką przez około 2 minuty, a następnie ogrzać do wrzenia, ciągle mieszając. Dodać
pozostałą część cukru (155 g) w dwóch porcjach, za każdym razem doprowadzając do wrzenia.
Łączny czas ogrzewania 5-8 minut. Masę zolu ustalić na poziomie 300 g netto (ogrzewając lub
dodając wodę), usunąć pianę, a po osiągnięciu przez zol temperatury 95
°C dodać 2,7 g kwasu
cytrynowego, wymieszać i napełnić zlewki.
2 wariant
Odważyć 3g preparatu pektynowego i wymieszać z około 25 g mielonego cukru, po czym przenieść
do wytarowanego wraz z łyżeczką porcelanową garnka zawierającego 160 cm
3
wody destylowanej.
Mieszać łyżeczką przez około 2 minuty, a następnie ogrzać do wrzenia, ciągle mieszając. Dodać
pozostałą część cukru (50 g) w dwóch porcjach, za każdym razem doprowadzając do wrzenia.
Łączny czas ogrzewania 5-8 minut. Masę zolu ustalić na poziomie 225 g netto (ogrzewając lub
dodając wodę), usunąć pianę i napełnić zlewki.
W
YKONANIE ŻELU PEKTYNY NISKOMETYLOWANEJ
(LM)
1 wariant
Odważyć 3 g preparatu pektynowego z dokładnością do 0,01 g i wymieszać z 20 g zmielonego
cukru. W rondlu wytarowanym wraz z łyżeczką do mieszania, przygotować mieszaninę 212,5 cm
3
wody destylowanej z dodatkiem 2,5 cm
3
roztworu kwasu cytrynowego oraz 5 cm
3
cytrynianu sodu.
Przenieść do rondla mieszaninę pektyny z cukrem i mieszać do rozpuszczenia. Mieszaninę
ogrzewać, doprowadzić do wrzenia, dodać 70 g cukru, dalej gotować mieszając, aż do
rozpuszczenia. Następnie dodać 12,5 cm
3
roztworu chlorku wapniowego, kroplę po kropli przy
ciągłym mieszaniu. Kontynuować mieszanie do uzyskania masy netto 300 g. Zdjąć garnek z ognia i
pozostawić na 1 minutę, po czym napełnić preparatem trzy zlewki.

12
2 wariant
Odważyć 3 g preparatu pektynowego z dokładnością do 0,01 g i wymieszać z 20 g zmielonego
cukru. W rondlu wytarowanym wraz z łyżeczką do mieszania, przygotować mieszaninę 212,5 cm
3
wody destylowanej z dodatkiem 2,5 cm
3
roztworu kwasu cytrynowego oraz 5 cm
3
cytrynianu sodu.
Przenieść do rondla mieszaninę pektyny z cukrem i mieszać do rozpuszczenia. Mieszaninę
ogrzewać, doprowadzić do wrzenia, dodać 40 g cukru, dalej gotować mieszając, aż do
rozpuszczenia. Kontynuować mieszanie do uzyskania masy netto 300 g. Zdjąć garnek z ognia i
pozostawić na 1 minutę, po czym napełnić preparatem dwie zlewki.
W
YKONANIE
Ż
ELU ŻELATYNOWEGO
Odważyć 7,5 g badanej żelatyny i wsypać do zlewki o pojemności 250-300 cm
3
. Do zlewki z
żelatyną wlać 105 cm
3
wody destylowanej o temperaturze pokojowej, przykryć i odstawić na 20
minut do napęcznienia, po czym wstawić do łaźni wodnej o temperaturze 60
°C i mieszać do
rozpuszczenia żelatyny (około 15 min). Klarowny roztwór rozlać do zlewek, wstępnie schłodzić w
temperaturze pokojowej, a następnie wstawić do lodówki.
W
YKONANIE
Ż
ELU AGAROWEGO
Odważyć 1,5 g agaru i umieścić w zlewce o pojemności 150 cm, dodać 65 cm
3
wody destylowanej i
gotować do całkowitego rozpuszczenia agaru. Następnie dodać 80 g cukru i ogrzewać do
całkowitego rozpuszczenia. Otrzymany roztwór schłodzić do temperatury 60
°C, dodać 1 g kwasu
cytrynowego i dokładnie wymieszać. Roztwór powinien zawierać 38% wody, a całkowita masa
próbki powinna wynosić 140 g. Jeżeli jest mniej to uzupełnić wodą do uzyskania tej masy. Roztwór
przenieść na płytki Petriego i pozostawić w celu zakrzepnięcia.
W
YKONANIE
Ż
ELU KARAGENOWEGO
1 wariant
Odważony 1 g karagenu zalać 95 cm
3
wody destylowanej z dodatkiem 5 cm
3
roztworu chlorku
potasowego. Odczekać 10 minut, po czym zlewkę wstawić do łaźni wodnej i mieszać od czasu do
czasu do całkowitego rozpuszczenia karagenu. Natychmiast schłodzić w zimnej wodzie.
2 wariant
Odważony 1 g karagenu zalać 100 cm
3
wody destylowanej. Odczekać 10 minut, po czym zlewkę
wstawić do łaźni wodnej i mieszać od czasu do czasu do całkowitego rozpuszczenia karagenu.
Natychmiast schłodzić w zimnej wodzie.
BADANIE ODWRACALNOŚCI TERMICZNEJ ŻELI
Próbki żelu ogrzać w łaźni wodnej w temperaturze 70
°C (w przypadku agaru ogrzewanie prowadzić
w temperaturze 95
°C) i utrzymując tę temperaturę przez ok. 5 min. obserwować zachowanie się
żeli, po czym schłodzić je do temperatury około 10
°C. Opisać wyniki obserwacji.
BADANIE ODWRACALNOŚCI MECHANICZNEJ ŻELI
Zniszczyć strukturę żelu przez mechaniczne wytrząsanie lub miksowanie, po czym obserwować
próbkę pozostawioną w temperaturze ok. 10
°C. Opisać wynik obserwacji.
Wyszukiwarka
Podobne podstrony:
OTZ wykłady, Materiały studia, OTŻ, OTŻ
OTŻ Wykłady
OTŻ- WYKŁAD 2, OTŻ, OTZ WYKŁAD
OTZ 7, Wykład VI
OTŻ 3!!!!!!, Materiały studia, OTŻ, wykłady
otż wykłady, WNoZ, OTŻ
OTŻ- WYKŁAD, OTZ WYKŁAD
OTZ wyklady
otż wykłady2, WNoZ, OTŻ
OTZ Wyklady
OTŻ 2 wykłady
OTŻ 2!!!!!!, Materiały studia, OTŻ, wykłady
Ogólna technologia żywnosci Wykład I, studia, Maja, Studia, II rok, IV semestr, OTŻ, Wykłady
więcej podobnych podstron