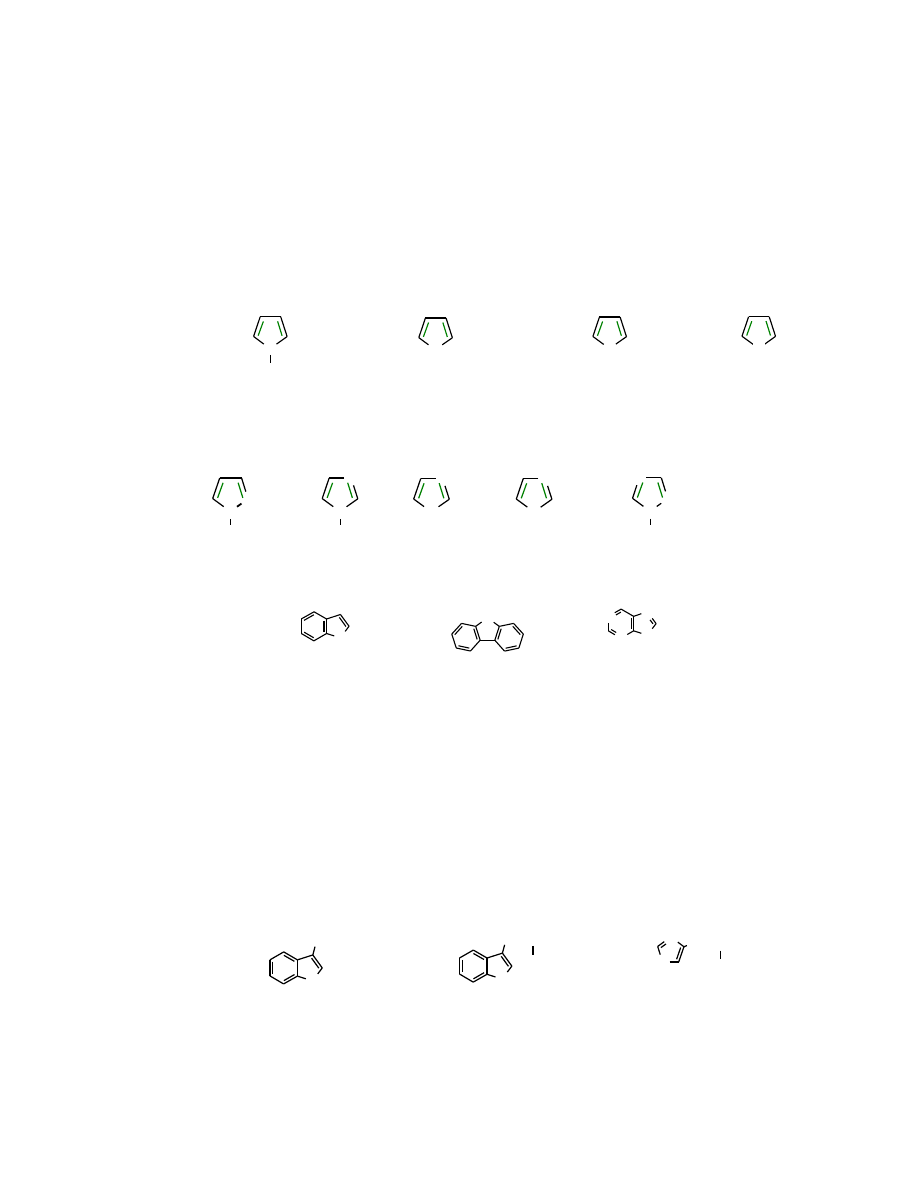
1
26. H E T E R O C Y K L I C Z N E Z W I Ą Z K I A R O M A T Y C Z N E
Aleksander Kołodziejczyk
2009 wrzesień
Cykliczne związki organiczne zawierające w pierścieniu heteroatomy, czyli atomy inne niż atom
węgla (jeden lub więcej, najczęściej N, O lub S) oraz odpowiednią liczbę podwójnych wiązań,
tak żeby spełnić regułę Hückla (ewentualnie razem z wolną parą heteroatomu) wykazują
właściwości aromatyczne.
Należą do nich heterocykle pięciocio- lub sześcioczłonowe
26.1 Pięcioczłonowe heterocykle aromatyczne
Przykłady pięcioczłonowych heterocykli aromatycznych.
N
O
S
H
..
..
..
C
-
..
..
pirol
furan
tiofen
anion cyklo-
pentadienowy
azacyklopentadien
(
)
oksacyklopentadien
(
)
tiacyklopentadien
(
)
..
Warto zwrócić uwagę, że podobną, spełniającą regułę Hückla strukturę elektronową ma anion
cyklopentadienowy. Oczywiście wszystkie przedstawione pierścienie są płaskie.
Heterocykle aromatyczne mogą zawierać więcej heteroatomów.
N
N
O
N
S
N
H
N
N
H
N
N
N
H
..
..
..
..
..
..
..
oksazol
tiazol
imidazol
pirazol
triazol
(1,3,5-triazol)
Znane są też heterocykle pięcioczłonowe skondensowane z innymi pierścieniami homo- lub
heterocyklicznymi.
N
H
N
H
N
N
N
H
N
indol
puryna
karbazol
26.1.1 Występowanie
Pięcioczłonowe, heterocykliczne pierścienie znajdują się w wielu związkach naturalnych.
Przykładem mogą być aminokwasy –
tryptofan
i
histydyna
, aminy biogenne, np.
tryptamina
,
histamina
czy
skatol
, alkaloidy, np. alkaloidy sporyszu (pochodne
kwasu lizerginowego
), LSD-
25 (syntetyczna pochodna
kwasu lizerginowego
),
johimbina
,
strychnina
(zawierają układ
indolowy), alkaloidy purynowe (
kofeina
i analogi), aminy wchodzące w skład kwasów
nukleinowych, np.
guanina
, związki zawierające
hem
, np.
hemoglobina
,
chlorofil
,
tiamina
(witamina B
1
) i wiele innych.
Kwas indolilo-3-octowy
jest hormonem ułatwiającym wzrost
korzeni roślin. Stymuluje on ukorzenienie już przy stężeniu 10
-12
g; po przekroczeniu stężenia
optymalnego staje się inhibitorem wzrostu korzeni. W handlu jest dostępny preparat zawierający
kwas indolilo-3-octowy
, stosowany przy przesadzaniu roślin w celu ułatwiania ich ukorzeniania.
Kwasy i aminokwasy:
N
H
N CH
2
CHCOOH
NH
2
N
H
CH
2
CHCOOH
NH
2
N
H
CH
2
COOH
tryptofan
histydyna
kwas indolilo-3-octowy
aminy biogenne:

2
N
H
CH
2
CH
2
NH
2
N
H
N CH
2
CH
2
NH
2
N
H
CH
3
N
H
CH
2
N(CH
3
)
2
N
H
CH
2
CH
2
NH
2
O
H
tryptamina
histamina
skatol
gramina
serotonina
Histamina
powstaje z
histydyny
w trakcie
dekarboksylacji
białek. Należy do hormonów
tkankowych, pojawia się w skórze, płucach i komórkach tucznych. Jest składnikiem wielu
toksyn, np. pszczół, os, niektórych toksycznych ryb. Wywołuje reakcje alergiczne oraz obniża
ciśnienie krwi. Tego rodzaju objawy wymagają podania leków antyhistaminowych.
Skatol
występuje w kale; tworzy się z
tryptofanu
z procesach gnilnych. Ma niezwykle
nieprzyjemny zapach. Jego zapach w roztworze wodnym wyczuwalny jest przy stężeniu 10 ppb.
Znajduje się także w aromacie niektórych serów.
Tryptamina
także należy do produktów degradacji biologicznej
tryptofanu
, powstaje również ze
strychniny
pod wpływem silnych zasad. Jest szeroko rozpowszechniona w przyrodzie.
Znaleziono ją w grzybach, w wyższych roślinach i u zwierząt. Znajduje się w owocach jadalnych,
np. ananasach, pomarańczach, śliwkach i pomidorach.
Gramina
należy do alkaloidów grupy indoliloalkiloamin. Została wyodrębniona ze zbóż (z
jęczmienia). Powstaje w wyniku biodegradacji
tryptofanu
. Jest toksyczna.
Serotonina
jest aminą biogenną często występującą zarówno w roślinach, jak i u zwierząt.
Znajduje się w owocach jadalnych, np. bananach, ananasach, pokrzywach, a także w groźnych
toksynach. U saków, w tym u ludzi pełni rolę
neuroprzekaźnika
działającego w ośrodkowym
układzie nerwowym i układzie pokarmowym, występuje też w trombocytach.
Pewne czynności związane z odczuwaniem przyjemności, np. jedzenie czekolady wywołują
zwiększone wydzielanie
serotoniny
.
Serotonina
bierze aktywny udział w procesie zasypiania - u
zwierząt doświadczalnych blokowanie jej syntezy wywoływało bezsenność. Wpływa na popęd
seksualny, zachowania impulsywne i apetyt. Niektóre narkotyki, w tym opioidy, meskalina i
LSD przyspieszają syntezę i uwalnianie
serotoniny
w mózgu lub zastępują ją w roli
neuroprzekaźnika.
alkaloidy sporyszu LSD-25 i strychnina
N
N
H
COOH
CH
3
N
N
H
CO
CH
3
NH CH CH
2
OH
CH
3
N
N
H
CON(Et)
2
CH
3
N
N
O
O
H
H
H
H
H
H
kwas
lizerginowy
ergometryna
H
LSD-25
strychnina
alkaloidy purynowe
N
N
N
N
N
N
N
N
OH
OH
O
H
N
N
N
N
O
O
O
N
N
N
N
O
O
O
CH
3
C
H
3
CH
3
H
H
H
puryna
H
H
H
H
kwas moczowy
kofeina
3
hem chlorofil i tiamina
N
N
N
N
N
N
N
N
COOH
COOH
..
..
..
..
N
N
N
N
O
OC
CO
O
C
20
H
39
O
N S
N
N
NH
3
OH
H
H
tetrapirol
Fe
hem
Mg
CH
3
+
-
Cl
chlorofil a
tiamina
Zadanie: wskaż i nazwij heterocykliczne ugrupowania w związkach naturalnych prezentowanych powyżej
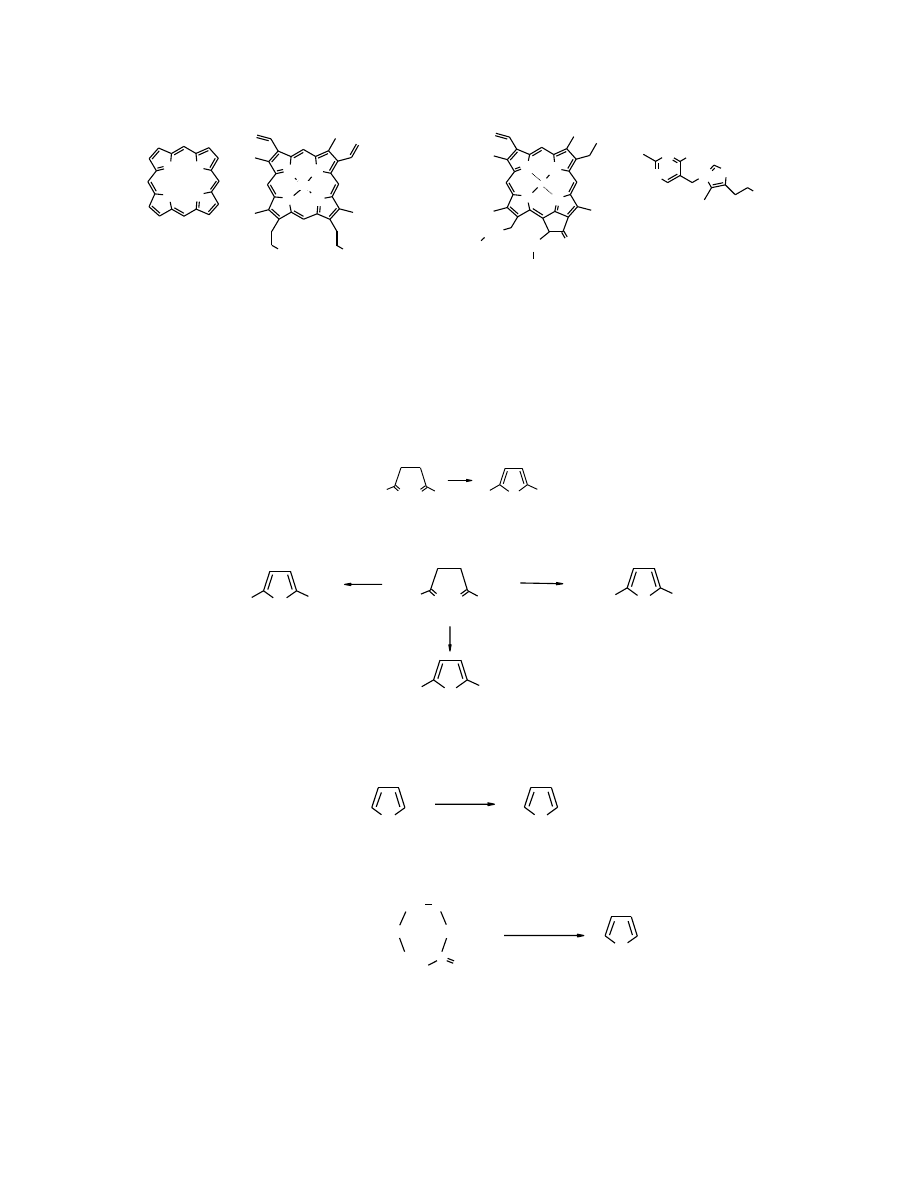
26.1.2 Otrzymywanie
Ogólna metoda otrzymywania pięcioczłonowych heterocykli zarówno
pirolu
,
furanu
,
tiofenu
, jak
i ich analogów polega na ogrzewaniu związków 1,4-dikarbonylowych z odpowiednimi
reagentami.
Furan
i jego homologi powstają w wyniku ich odwodnienia, np. za pomocą P
2
O
5
. Do
otrzymania pierścienia pirolowego potrzebny jest amoniak lub jego sole, a
tiofen
i analogi
zawierające w pierścieniu atom S tworzą się w obecności siarczków fosforu, np. pentasiarczku
fosforu – P
4
S
10
.
R
R
z
O
R
R
O
Z
związki
1.4-dikarbonylowe
związki
heterocykliczne
Z
acetonyloacetonu
(
heksa-2,5-dionu
) można w ten sposób otrzymać 2,5-dimetylowe pochodne
pięcioczłonowych heterocykli.
O
CH
3
C
H
3
O
CH
3
C
H
3
O
N
H
CH
3
C
H
3
S
CH
3
C
H
3
acetonyloaceton
P
2
O
5
(NH
4
)
2
CO
3
100
o
C
P
4
S
10
2,4-dimetylofuran
2,4-dimetylopirol
2,4-dimetylotiofen
Pirol
i
tiofen
występują w smole węglowej i z niej są wyodrębniane.
Pirol
powstaje w trakcie
pirolizy
produktów naturalnych zawierających białka. Można go też otrzymać z
furanu
w
reakcji z amoniakiem w temp. 400
o
C, wobec katalizatora, jakim jest tlenek glinu.
O
N
H
NH
3
.
aq
Al
2
O
3
, 400
o
C
furan
pirol
Polecaną metodą otrzymywania
pirolu
jest
piroliza
galaktaronianu amonu
(soli amonowej
kwasu
galaktarowego
, zwanego inaczej
kwasem śluzowym
).
N
H
CH(OH)
CH
(OH)HC
CH(OH)
O
O
pirol
(OH)
C
- 2 CO
2
, - NH
3
, - HOH
(37%)
+
-
galaktaronian amonu
NH
4
OO C
NH
4
N-metylowane pochodne pirolu powstają w podobnej jak wyżej reakcji z
soli metyloamoniowej
kwasu arowego
.
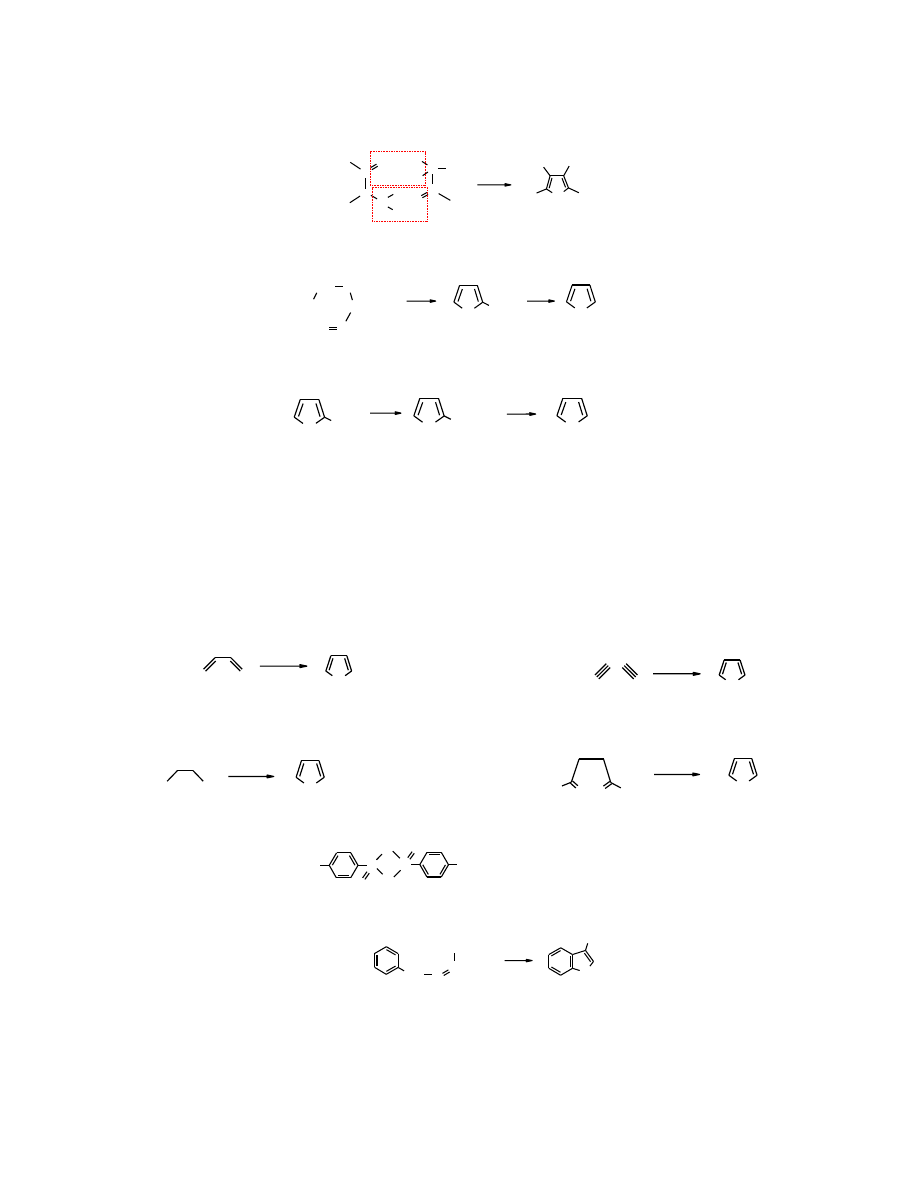
4
C-Alkilowe pochodne pirolu tworzą się w reakcji kondensacji
-aminoketonów (aldehydów) ze
związkami karbonylowymi.
O
N
H
H
H
H
O
H
N
H
C
C
H
C
C
- 2 HOH
homologi
pirolu
aminoketon
keton
Furan
powstaje w reakcji
dekarbonylowania
(
eliminacji
CO)
furfuralu
.
Furfural
natomiast jest
produktem
pirolizy
pentoz.
O
CHOH
CH
HOC
CHOH
O
O
CHO
furan
HO
CH
,
kat.
- CO
H
2
- HOH
+
H,
furfural
pentoza
Z
furfuralu
można otrzymać
kwas furano-2-karboksylowy
, z niego w reakcji
dekarboksylacji
tworzy się
furan
.
O
O
CHO
O
COOH
furan
,
kat.
- CO
2
[O]
furfural kwas furano-2-karboksylowy
Tiofen
występuje w smole węglowej, we frakcji benzenowej, przez co utrudnia otrzymanie
czystego
benzenu
– trudno rozdzielić te dwa związki z uwagi ich na zbliżone temperatury
wrzenia. Oczyszczenie
benzenu
poprzez usunięcie
tiofenu
wymaga metod opartych na reakcjach
chemicznych. Podczas
sulfonowania
w łagodnych warunkach tej mieszaniny powstaje jedynie
kwas tiofenosulfonowy
, który łatwo usuwa się poprzez wymycie wodą.
Tiofen
jest głównym produktem reakcji
1,3-butadienu
z siarką w wysokiej temperaturze. Do
otrzymywania
tiofenu
można również wykorzystać
etyn
.
S
S
S, 600
o
C
1,3-butadien
tiofen
- H
2
S
S, 300
o
C
tiofen
+
etyn
Przemysłowa metoda otrzymywania
tiofenu
polega ogrzewaniu
n-butanu
z siarką. Także z
kwasu
bursztynowego
powstaje
tiofen
.
S
S
O
OH
O
H
O
S,
n-butan
tiofen
560
o
C
- 2 H
2
S
P
4
S
10
kwas
bursztynowy
tiofen
W laboratorium zamiast siarki można stosować pentasiarczek fosforu lub odczynnik Lawessona.
P
OMe
S
S
P
OMe
S
S
odczynnik Lawessona
Skatol
otrzymuje się syntetycznie z
fenylohydrazonu propanalu
.
NH N
CH
CH
2
CH
3
N
H
CH
3
- NH
3
skatol
fenylohydrazon
propanalu
26.1.3 Właściwości fizyczne i fizjologiczne
Pirol
,
furan
i
tiofen
są bezbarwnymi, hydrofobowymi (trudno rozpuszczalnymi w wodzie)
cieczami, o temperaturach wrzenia odpowiednio: 130, 31 i 84
o
C. Temperatura wrzenia
furanu
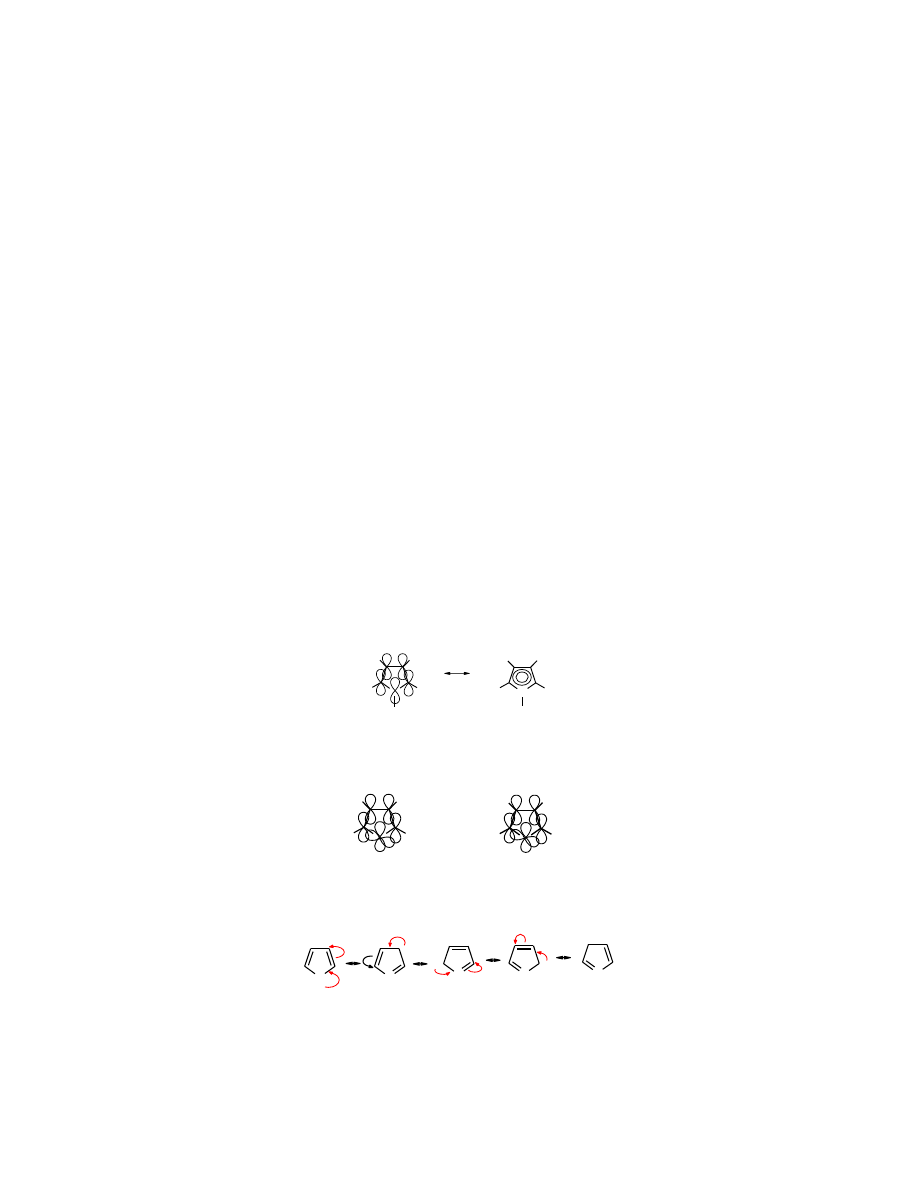
5
jest zbliżona do tw. wrzenia
eteru dietylowego
(34,5
o
C). Wysoka tw.
pirolu
jest rezultatem jego
zdolności, podobnie jak i innych amin 1
o
i 2
o
, do tworzenia wiązań wodorowych; wrze wyżej niż
dietyloamina
(56
o
C). Natomiast wyższa tw.
tiofenu
w porównaniu z
furanem
wynika z jego
wyższej masy cząsteczkowej (tw.
sulfidu dietylowego
wynosi 92
o
C).
Wszystkie trzy omawiane związki i ich homologi mieszają się z większością popularnych
rozpuszczalników organicznych.
Pirol
na świetle i przy dostępie powietrza szybko ciemnie. Jest bardzo słabą zasadą, pod
wpływem mocnych kwasów polimeryzuje.
Zapach
tiofenu
jest słaby, mało charakterystyczny. Zapach
furanu
jest również słaby, przypomina
chloroform
. Charakterystyczny zapach ma
pirol
.
Skatol
należy do związków o bardzo
nieprzyjemnym zapachu, jest głównym składnikiem zapachowym kału.
26.1.4 Właściwości chemiczne
Pięcioczłonowe heterocykle nie wykazują charakterystycznych właściwości sprzężonych dienów
pomimo tego, iż zawierają dwa sprzężone podwójne wiązania – nie ulegają
addycji
, nie
polimeryzują
i nie reagują z dienofilami. W środowisku mocnych kwasów
pirol
jednak szybko
polimeryzuje
, jakby pod ich wpływem tracił jakąś osłonę zabezpieczającą go przed tą reakcją.
Te nadzwyczajne właściwości heterocykli wynikają z ich charakteru aromatycznego. Pierścienie
hetrocykli są płaskie, a dwa sprzężone wiązania
razem z wolną parą elektronową na
heteroatomie tworzą sekstet elektronowy; spełniają one zatem reguły aromatyczności Hückla.
Energia aromatyzacji
pirolu
wynosi 92 kJ/mol (22 kcal/mol).
Wolna para elektronowa na heteroatomie, tak jak i elektrony na atomach węgla sp
2
zajmują
orbitale p, prostopadłe do płaszczyzny pierścienia. Elektrony walencyjne heteroatomu i atomów
węgla przyjmują hybrydyzację sp
2
.
N
H
H
H
H
H
N
H
H
H
H
H
.
.
.
.
..
Rys. 26.1 Aromatyczne sprzężenie elektronów
i wolnej pary elektronowej w
pirolu
Podobnie jest w
furanie
i
tiofenie
. Druga wolna para elektronów nie przeszkadza w sprzężeniu.
O
H
H
H
H
S
H
H
H
H
. .
.
.
..
. .
.
.
:
:
furan
tiofen
Rys. 26.2 Aromatyczne sprzężenie elektronów
oraz wolnej pary elektronowej w
furanie
i
tiofenie
Wzory mezomeryczne, wynikające ze sprzężenia elektronów
i wolnej pary elektronów
przypominają wzory mezomeryczne
benzenu
; nie są one jednak równocenne.
z
z
z
z
z
..
..
+
-
..
+
-
..
+
-
..
+
-
Furan
ma słabsze właściwości aromatyczne w porównaniu z
pirolem
i
tiofenem
, z uwagi na
silniejsze właściwości elektroujemne atomu tlenu, który w większym stopniu wyciąga elektrony
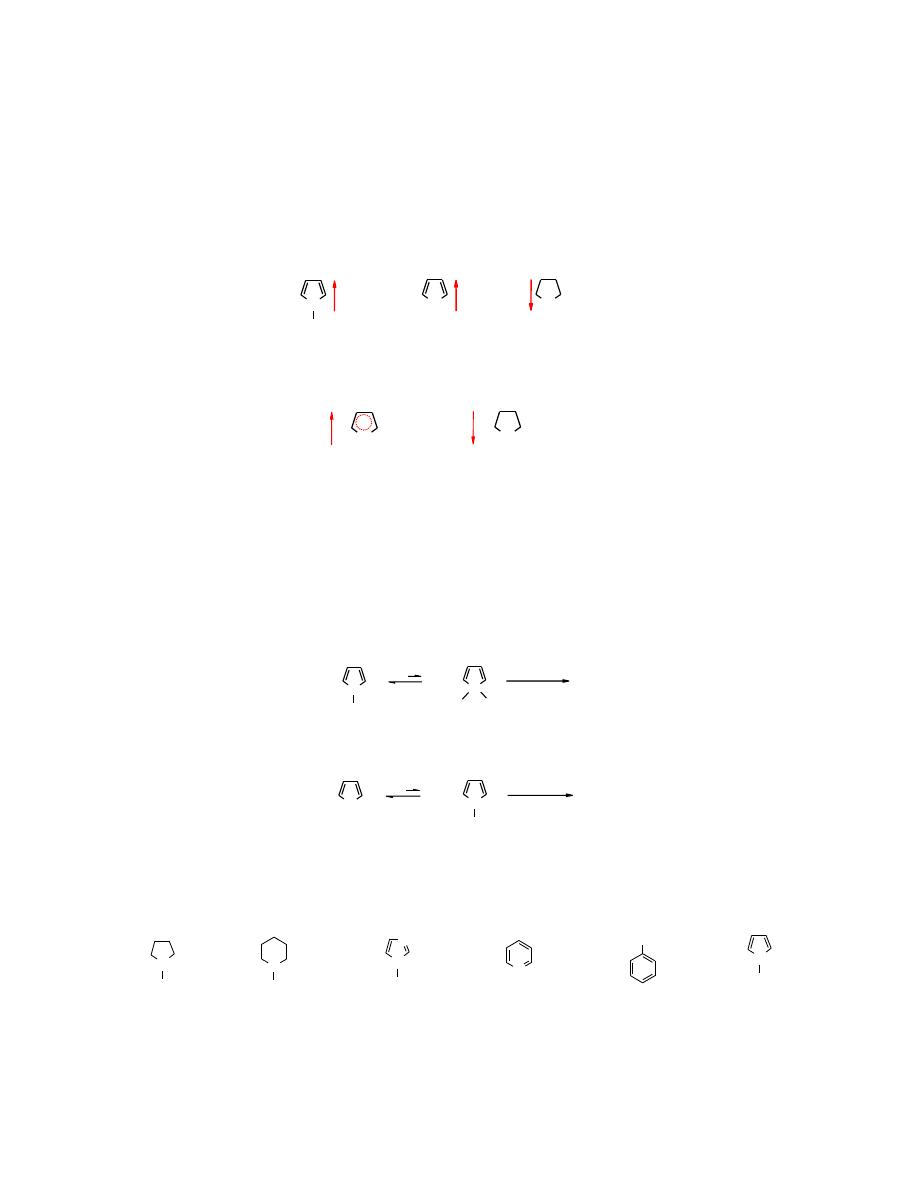
6
z pierścienia niż atomy N czy S. Te różnice przejawiają się chociażby w reakcjach
cykloaddycji
(Dielsa-Adlera),
furan
stosunkowo łatwo jej ulega, podczas gdy
pirol
i
tiofen
bardzo trudno.
Z powyższej przedstawionych wzorów mezomerycznych wynika, że cząsteczki heterocykli, w
przeciwieństwie do cząsteczki
benzenu
, powinny wykazywać moment dipolowy, ponieważ w
pozycjach
i
zgromadzony jest ładunek ujemny, a na heteroatomie dodatni. Faktycznie, np.
pirol
czy
furan
wykazują moment dipolowy o wartościach odpowiednio 1,6 i 0,7D, skierowany
zgodnie z oczekiwaniem, tzn. z dodatnim biegunem na atomie tlenu.
O
O
N
H
..
..
= 1,6D
furan
..
..
tetrahydrofuran
..
piran
0,7D
1,7D
Warto zwrócić uwagę, że
tetrahydrofuran
, uwodorniony analog
furanu
, ma biegun ujemny
zlokalizowany na atomie tlenu, jako że atom tlenu jest w tej cząsteczce najbardziej
elektroujemny, a żadne efekty nie zakłócają rozmieszczenia elektronów.
O
O
..
furan
..
..
tetrahydrofuran
+
+
+
-
-
-
-
-
26.1.5 Właściwości kwasowo-zasadowe
26.1.5.1 Zasadowość
Pirol
z uwagi na obecność wolnej pary elektronową na atomie azotu powinien, jak wszystkie
aminy, wykazywać właściwości zasadowe, tzn. przyłączać protony. Elektrony te jednak są
zaangażowane w utworzenie aromatycznego sekstetu i nie przejawiają powinowactwa do
protonów. Przyłączenie przez nie protonu wiąże się z utratą energii rezonansu,
która dla układów
aromatycznych jest rzędu wartości energii wiązania kowalencyjnego. Pod wpływem silnych
kwasów
pirol
ulega jednak protonowaniu, a tracąc przy tym aromatyczność odzyskuje
właściwości sprzężonego dienu i szybko polimeryzuje.
N
H
N
H
H
..
polimeryzacja
polimer
+
H
+
pirol
Z silnymi kwasami etery też tworzą sole (oksoniowe), dlatego
furan
w środowisku silnie
kwaśnym również
polimeryzuje
.
O
O
H
..
polimeryzacja
polimer
+
H
+
furan
..
..
Zasadowość heterocykli
bardzo zależy od budowy cząsteczki. Poniżej podano wartości pK
a
kationów kilku najbardziej znanych heterocykli. Z podanych danych wynika, że najmniej
zasadowy jest
pirol
.
Wartości stałych pK
a
kationów
N
N
N
N
N
NH
2
N
H
H
H
H
..
..
..
..
..
sp
3
sp
3
sp
3
sp
2
sp
2
sp
2
..
..
11,27
11,2
6,95
5,25
4,63
0,4
pirolidyniowego piperydyniowego imidazolidyniowego pirydyniowego aniliniowego piroliowego
26.1.5.2 Kwasowość
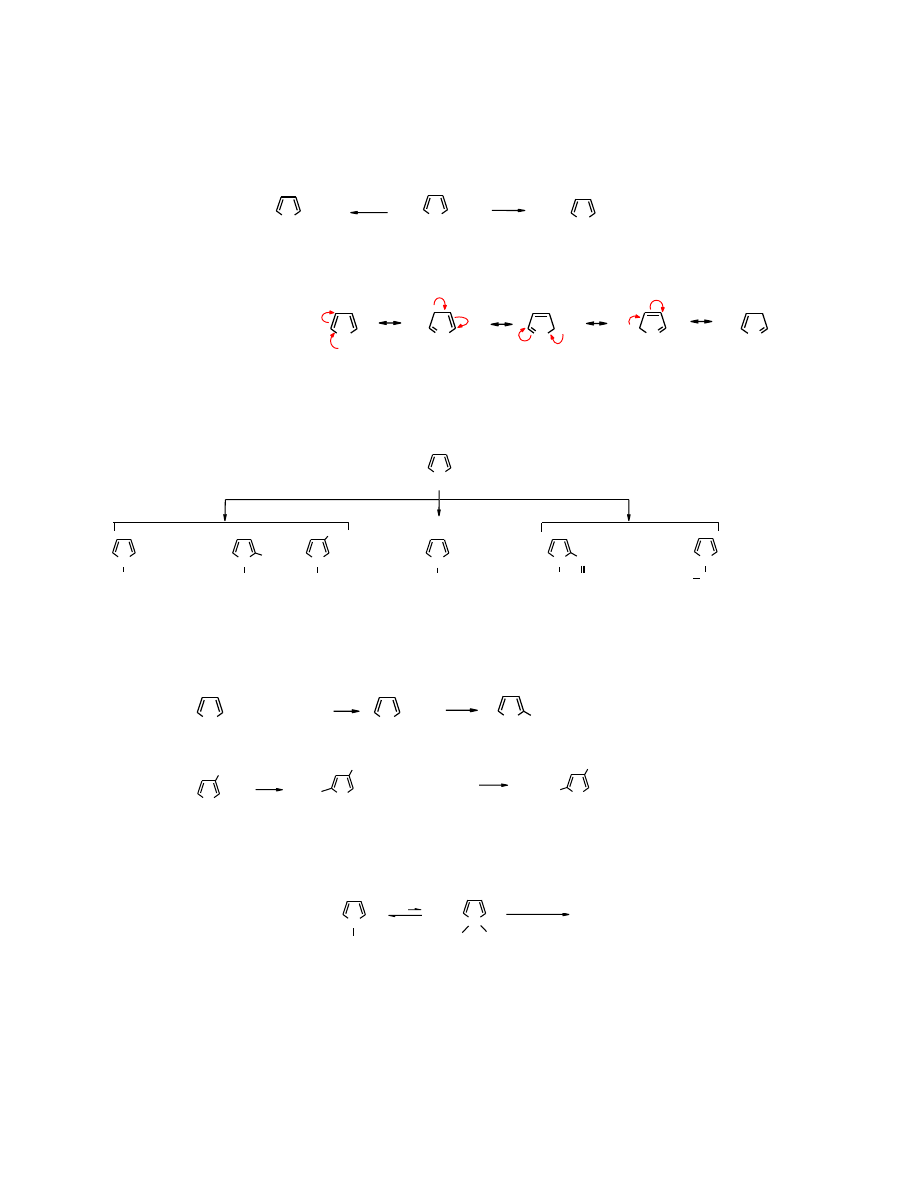
7
Atom wodoru związany z atomem azotu
pirolu
jest znacznie bardziej kwaśny niż w amoniaku,
czy aminach. pK
a
Pirolu
wynosi 17,5; dla porównania pK
a
amoniaku dochodzi do 36, a
pirolidyny
27.
Pirol
tworzy sole z wodorotlenkami metali alkalicznych, a ze związkami
Grignarda reaguje, tak jak kwasy czy związki o właściwościach kwasowych.
N
H
N
N
..
..
KOH
CH
3
MgBr
..
-
K
+
HOH
..
..
-
MgBr
+
+ CH
4
pirol
metan
pK
a
= 17,5
+
Jak wynika ze struktur mezomerycznych anion powstały z
pirolu
jest
nukleofilem
ambidentnym
.
N
N
N
N
N
struktury mezomeryczne
anionu
..
..
-
..
..
-
..
..
-
.. ..
-
..
..
-
pirolu
Ambidentny
charakter anionu
pirolu
przejawia się w tym, że ulega on zarówno N, jak i C
alkilowaniu
. Kierunek reakcji zależy głównie od właściwości odczynnika alkilującego, a także
od rodzaju rozpuszczalnika oraz towarzyszącego kationu.
Acylowanie
anionu
pirolu
prowadzi
do pochodnej zawierającej resztę acylową w pozycji 1 i 2.
N
N
H
Me
N
Me
N
H
C-CH
3
O
N
C=O
C
H
3
N
Me
N
H
Me
..
..
-
MgBr
+
TosOMe
MeI
AcCl
..
..
..
N-metylopirol
2-metylopirol
3-metylopirol
2-acetylopirol
N-metylopirol
+
+
..
N-acetylopirol
..
..
+
Silne zasady (BuLi, PhNa itp.) są w stanie oderwać protony z pierścienia N-alkilopirolu,
furanu
i
tiofenu
. Oderwaniu (deprotonacji) w pierwszej kolejności ulega proton w pozycji 2, a następnie
4. Deprotonowane heterocykle (aniony) wchodzą w typowe reakcje, np.
acylowania
czy
alkilowania
.
O
O
O COOH
furan
..
..
+ PhNa
..
..
: Na
+
-
- C
6
H
6
1. CO
2
2. H
+
..
..
fenylosód
kwas furano-2-karboksylowy
S
CH
3
S
CH
3
Li
S
CH
3
HOOC
3-metylotiofen
..
..
BuLi
..
..
..
..
1.
CO
2
2.
H
+
3-metylotiofenylo-5-lit
kwas 3-metylotiofeno-5-karboksylowy
26.1.5.3 Polimeryzacja
Pod wpływem silnych kwasów
pirol
i
furan
tracą właściwości aromatyczne i szybko
polimeryzują
, czyli ulegają reakcji charakterystycznej dla sprzężonych dienów.
N
H
N
H
H
..
polimeryzacja
polimer
+
H
+
pirol
Mechanizm polimeryzacji
Protonowany
pirol
staje się elektrofilem i reaguje z drugą cząsteczką
pirolu
wg typowego
mechanizmu reakcji S
E
.
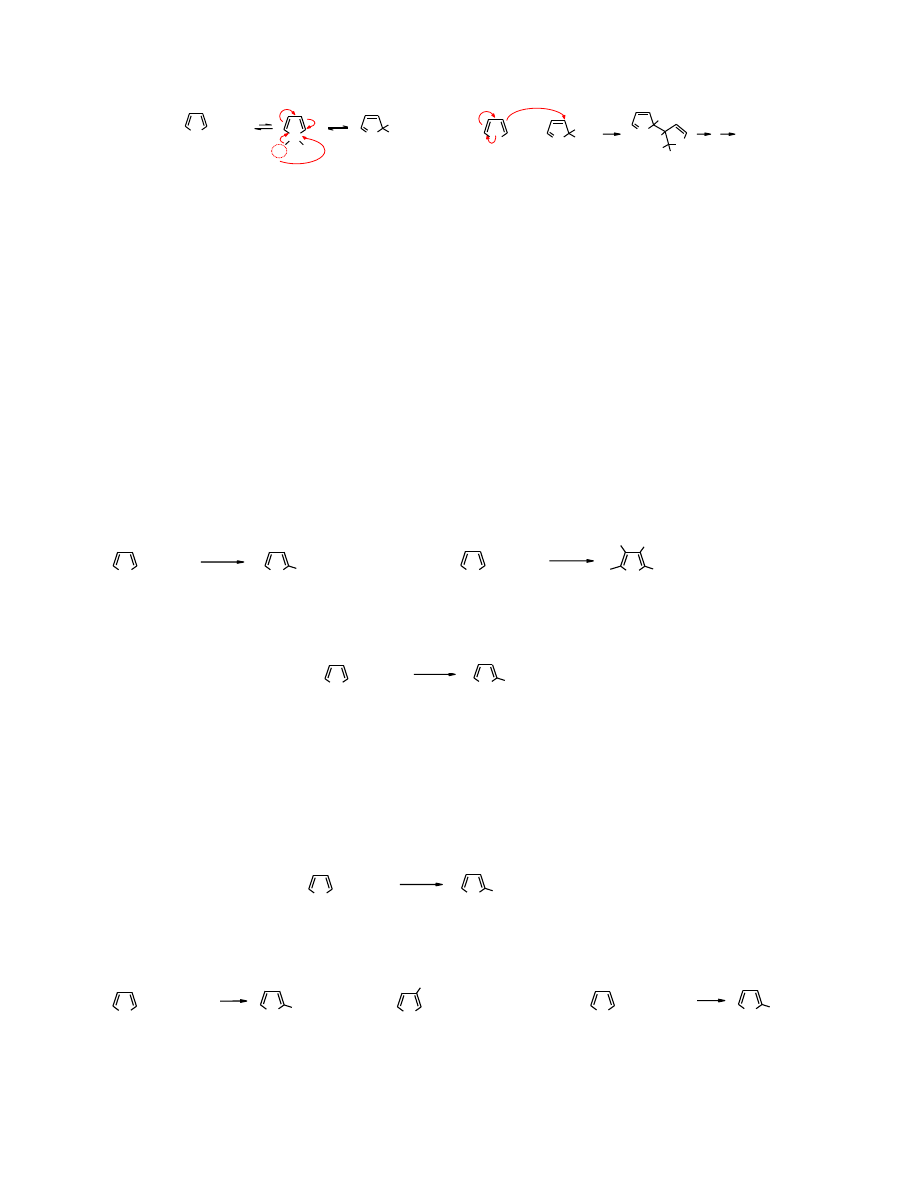
8
N
H
N
H
H
N
H
H
N
H
N
H
H
N
H
N
H
H
H H
..
+ H
+
+
+
H
..
+
+
H
+
H
tautomeria
Zadanie: przedstaw mechanizm
polimeryzacji
furanu
.
26.1.5.4 Substytucja elektrofilowa S
E
Właściwości aromatyczne heterocykli pięcioczłonowych przejawiają się w ich podatności na
substytucję elektrofilową
.
Pirol
,
furan
i
tiofen
ulegają reakcją S
E
znacznie łatwiej niż
benzen
.
Obecność heteroatomu w pierścieniu aktywuje te związki w reakcjach S
E
podobnie jak
przyłączona do pierścienia benzenowego grupa aminowa czy fenolowa.
Halogenowanie
,
nitrowanie
,
sulfonowanie
czy
acylowanie
heterocykli pięcioczłonowych prowadzi się w niskich
temperaturach, głównie dlatego żeby zapewnić selektywność reakcji (ograniczyć podstawienie
kolejnych atomów wodoru). Monopodstawienie następuje w pozycji 2, pod warunkiem, że nie
jest ona zajęta. Reaktywność heterocykli pięcioczłonowych zmienia się wg następującego
szeregu:
tiofen
>
pirol
>
furan
. Mechanizm reakcji S
E
tych związków jest bardziej
skomplikowany niż prosta
addycja/eliminacja
, jak to ma miejsce w reakcjach arenów
homocyklicznych.
26.1.5.4.1 Halogenowanie
Halogenowanie
, podobnie jak w przypadku
aniliny
i
fenolu
nie wymaga stosowania katalizatora
i w pewnych warunkach następuje wyczerpujące
bromowanie
.
N
N
Br
Br
Br
Br
O
O
Br
+ 4 Br
2
etanol
0
o
C
+ 4 HBr
furan
+ Br
2
dioksan
0
o
C, - HBr
2-bromofuran
(90%)
pirol
2,3,4,5-tetrabromopirol
26.1.5.4.2 Sulfonowanie
Najdogodniejszym czynnikiem sulfonującym jest tritlenek siarki. Kwas siarkowy powoduje
polimeryzację
pirolu
i
furanu
.
O
O
SO
3
H
+ SO
3
pirydyna
0
o
C
furan
kwas furano-2-
-karboksylowy
Tiofen
znacznie łatwiej ulega
sulfonowaniu
niż
benzen
, dlatego oczyszczanie
benzenu
zawierającego
tiofen
polega na działaniu na taką mieszaninę kwasem siarkowym w temperaturze
pokojowej. W tych warunkach jedynie
tiofen
zostaje przekształcony w kwas sulfonowy (
tiofeno-
2-sulfonowy
), który jest łatwo oddzielany od
benzenu
poprzez przemycie wodą.
26.1.5.4.3 Nitrowanie
W mieszaninie nitrującej zamiast kwasu siarkowego stosuje się
bezwodnik octowy
, którego
głównym zadaniem jest wiązanie wydzielającej się wody.
N
H
N
H
NO
2
+ HNO
3
Ac
2
O
0
o
C
pirol
2-nitropirol
(83%)
Można również do tego celu wykorzystać
octan nitrozylu
. Nitrowanie
tiofenu
octanem nitrozylu
daje jeden izomer.
N
H
N
H
NO
2
N
H
NO
2
S
S
NO
2
+ AcO
-
NO
2
+
-10
o
C
pirol
(61%)
(13%)
+
0
o
C
tiofen
2-nitrotiofen
2-nitropirol
3-nitropirol
octan nitrozylu
+ AcO
-
NO
2
+
26.1.5.4.4 Acylowanie
9
Acylowanie
heterocykli pięcioczłonowych prowadzi się typowymi odczynnikami acylującymi, a
więc chlorkami kwasowymi i bezwodnikami, można jednak stosować inne niż chlorek glinu
katalizatory.
O
O
O
CH
3
S
S
O
Ac
2
O
BF
3
furan
2-acetylofuran
C
PhCOCl
SnCl
4
tiofen
2-benzoilotiofen
C
26.1.5.4.5 Sprzęganie
Sole diazoniowe łatwo
sprzęgają
się z pięcioczłonowymi heterocyklami. Podstawienie grupą
azową następuje w najbardziej reaktywnym miejscu, czyli w pozycji 2.
N
H
N
H
N N
N N
SnCl
4
pirol
2-(fenyloazo)pirol
+ -
Cl
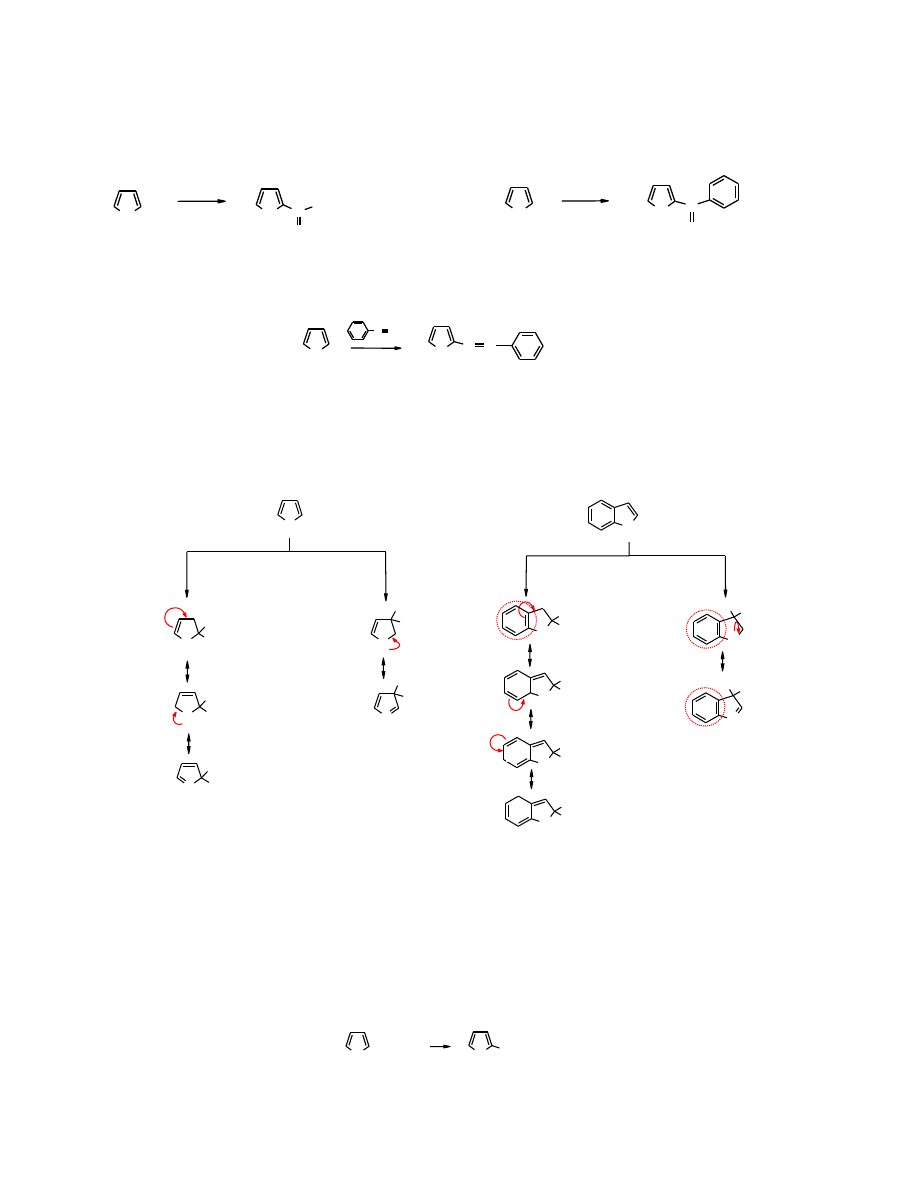
Analiza stanów granicznych adduktu po przyłączeniu elektrofila do pięcioczłonowego związku z
jednym heteroatomem wyjaśnia, dlaczego do substytucji dochodzi w pozycji 2. Dla adduktu w
pozycji 3 można napisać tylko 2 wzory mezomeryczne, przy czym drugi jest niekorzystny
energetycznie, ponieważ ładunek dodatni jest zlokalizowany na heteroatomie, czyli bardziej
elektroujemnym atomie niż atom węgla.
z
z
Y
H
z
Y
H
z
Y
H
z
Y
H
z
Y
H
N
N
Y
H
N
H
Y
N
H
Y
N
Y
H
N
Y
H
N
Y
H
Z: O; S lub NH
atak na
pozycję 2
atak na
pozycję 3
..
Y +
+
+
+
+
+
..
..
..
atak na
pozycję 2
atak na
pozycję 3
Y +
+
.. H
.. H
..
H
+
H
+
+
.. H
+
.. H
+
.. H
indol
W
indolu
, analogu
pirolu
substytucja S
E
dokonuje się w pozycji 3 pierścienia heterocyklicznego,
ponieważ addukt w tej pozycji zapewnia pełny sekstet eletronów
w pierścieniu benzenowym.
26.1.6 Barwniki pirolowe
26.1.6.1 Barwniki dipirylometenowe
Reakcja
metanalu
z
pirolem
(podobnie jak z
fenolem
) prowadzi do produktów kondensacji.
Kondensaty liniowe są wykorzystywane jako barwniki, tzw.
pirometany
(inaczej
barwniki
dipirylometenowe
); mają one zabarwienie żółte lub pomarańczowe. W środowisku zasadowym
reakcja
pirolu
i jego pochodnych z
metanalem
zatrzymuje się na etapie alkoholi 1
o
.
N
H
N
H
CH
2
OH
+ CH
2
O
-
OH
pirol
2-hydroksy-
metylopirol
10
N
H
CH
2
C
H
3
CH
3
N
H
CH
3
N
H
CH
C
H
3
CH
3
N
CH
3
[O]
CH
3
CH
3
Natomiast w środowisku kwaśnym powstały alkohol 1
o
reaguje z drugą cząsteczką
pirolu
lub
jego homologiem tworząc odpowiedni dipirylometan.
N
H
CH
2
OH
C
H
3
CH
3
N
H
CH
3
C
H
3
N
H
CH
2
C
H
3
CH
3
N
H
CH
3
H
+
+
CH
3
2,5-dimetylopirol
2-hydroksymetylo-
3,5-dimetylopirol
2,5,2',5'-dimetylopirolo
tetrametylopirylometan
Dipirylometany łatwo ulegają odwodornieniu do dipirylometenów. Siłą napędową reakcji
odwodornienia
jest rozszerzanie układu sprzężenia.
2,5,2’,5’-tetrametylopirylomet
an
2,5,2’,5’-tetrametylopirylomet
en
Inny kolor końcówek nazw pokazuje różnice w budowie tych związków.
Dipirylometeny są silnymi zasadami; z kwasami dają łatwo krystalizujące sole. Kationy tych soli
są stabilizowane mezomerycznie.
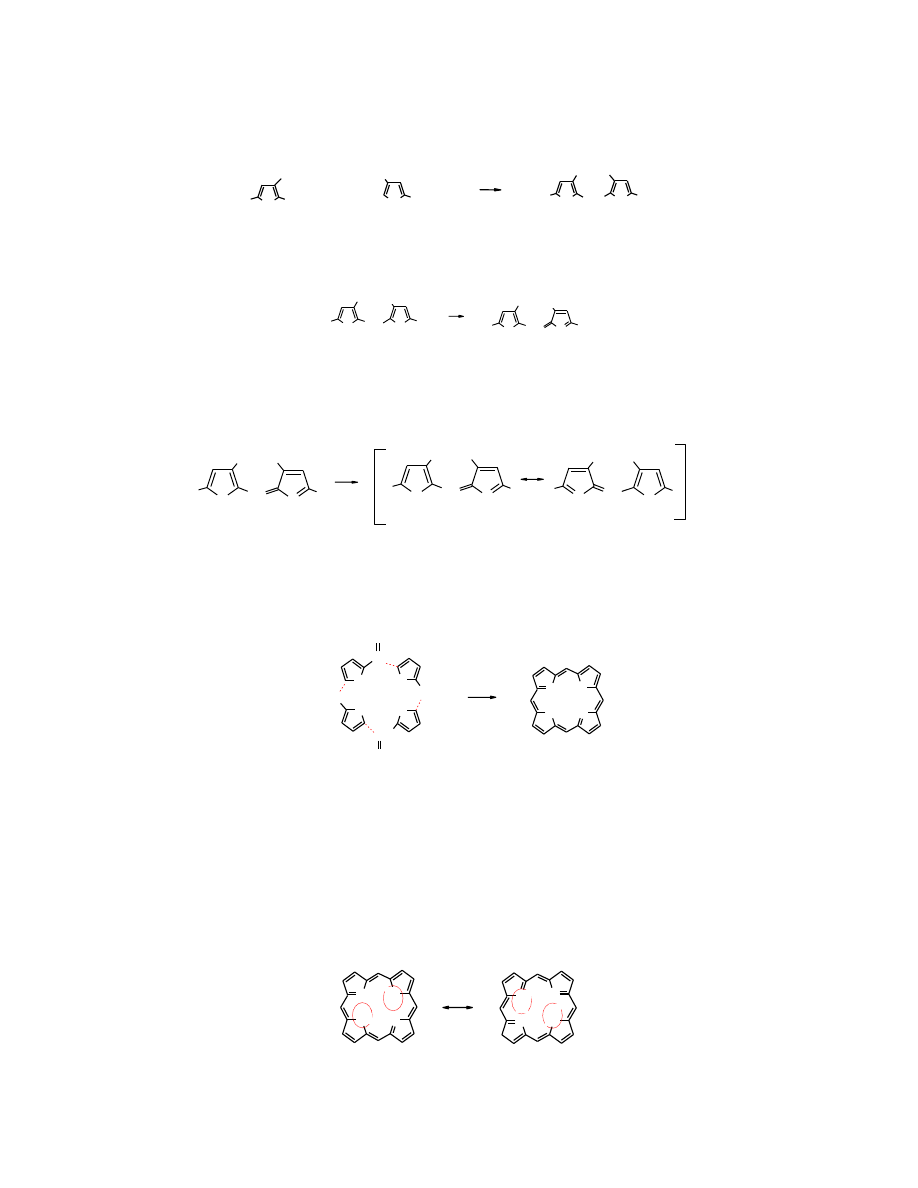
26.1.6.2 Barwniki porfirynowe
Pirol
i jego pochodne tworzą makrocykliczne pierścienie składające się z czterech reszt
pirolowych. Noszą one nazwę
porfiryn
. Najprostszą
porfirynę
można otrzymać w wyniku
kondensacji
pirolo-2-karboaldehydu
.
Przestrzenna budowa rosnącego oligomeru sprzyja
zamykaniu się w pierścień tetrameru.
N
CH
N
H CHO
N
CH
N
H
OHC
O
O
N
N
H
N
H
N
- 4 HOH
porfiryna
H
H
+
pirolo-2-
-karboaldehyd
:
:
:
:
Porfiryna
jest związkiem krystalicznym, który nie topnieje, lecz rozkłada się w temperaturze
360
o
C. Ma zabarwienie ciemnoczerwone. Jest cząsteczką płaską, a jej 11 wiązań podwójnych
C=C lub C=N i 4 wolne pary elektronów atomów azotu tworzą nieprzerwaną sieć układu
sprzężonego, składającą się w sumie z 30 elektronów. Liczba ta spełnia regułę aromatyczności
Hückla (n = 7). Sprzężenie elektronów w
porfirynie
daje energię rezonansu równą 250 kcal.
Cztery pierścienie pirolowe są równocenne
, a atomy wodoru przy atomach azotu zajmują
miejsce nieokreślone. Można napisać szereg struktur mezomerycznych, przy czym dwie są
najważniejsze, wykazują one równocenność pierścieni pirolowych i nieokreśloną pozycję
atomów wodoru.
N
N
H
N
H
N
N
N
N
N
: :
:
:
: :
:
:
H
H
N
H
R
CH
R
N
R
R
N
R
CH
R
N
R
R
N
R
CH
R
N
H
R
R
HBr
H
+
H
H
..
..
..
+
H
Br
-
bromek dipirylometeniowy
dipirylometen
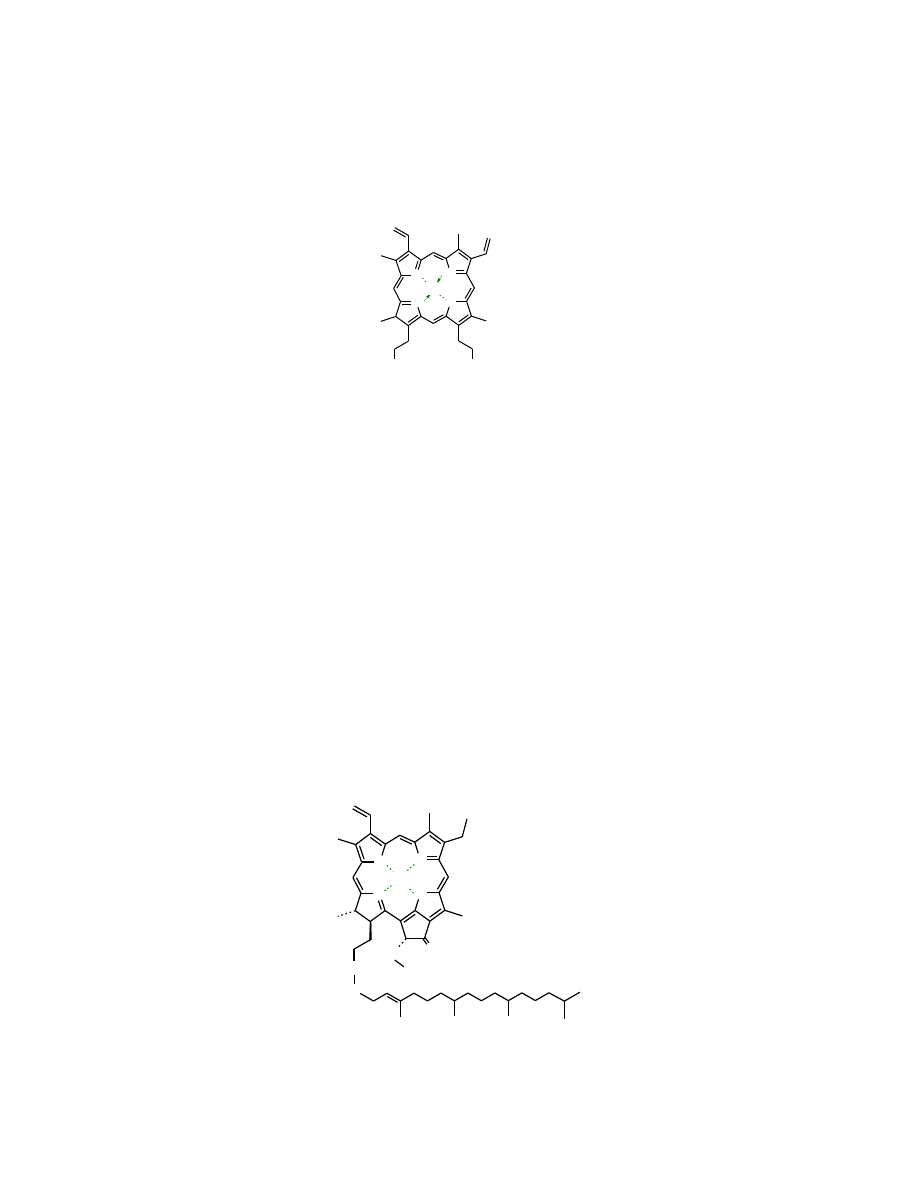
11
Układ porfiryny znajduje się w wielu związkach biologicznie czynnych, takich jak hemoglobina
(w części zwanej hemem), chlorofil, witaminia B
12
i inne.
Hemoglobina
jest białkiem złożonym. W jej skład wchodzą cztery elementy zbudowane jedynie z
aminokwasów, zwane globulinami (fragmenty białkowe) i
hem
– pochodna
porfiryny
zawierająca dodatkowo podstawniki i grupy funkcyjne oraz skoordynowany kation Fe
+2
.
N
N
N
N
COOH
COOH
:
Fe
:
hem
Cztery atomy azotu
hemu
są równocenne. Rola
hemoglobiny
polega na przenoszeniu tlenu z
płuc, gdzie jego stężenie jest wysokie do komórek, gdzie jego stężenie jest niższe. Tlen z
hemoglobiny
przekazywany jest do
mioglobiny
, która stanowi magazyn tlenu w komórkach i w
miarę potrzeby przekazuje go do reakcji utleniania.
Hemoglobina
w drodze powrotnej odbiera z
komórek CO
2
i w płucach wymienia go na tlen. Żelazo w trakcie tych procesów nie zmienia
stopnia utlenienia; tlen i CO
2
łączy się koordynacyjnie z atomem żelazem
hemu
.
Hemoglobina
zawierająca cząsteczkę tlenu nazywa się
hemoglobiną utlenowaną
lub
oksyhemoglobiną
(
nie
utlenioną
).
Hem
można wyizolować; tworzy on brunatne, krystaliczne igły; łatwo ulega utlenieniu. Produkt
utlenienia jonu żelaza w
hemoglobinie
do Fe
+3
nosi nazwę
met
hemoglobiny
lub
ferri
hemoglobiny
, w odróżnieniu od
hemoglobiny
zawierającej Fe
+2
, nazywanej również
ferro
hemoglobiną
.
Methemoglobina
jest nieczynna w procesie przenoszenia tlenu.
Hem
w zależności od otaczających go białek może pełnić różne funkcje, oprócz przenoszenia
tlenu i ditlenku węgla (w
hemoglobinie
), magazynowaniu tlenu (w
mioglobinie
), jest także
przenośnikiem elektronów (w
cytrochromie c
), bierze też udział w rozkładzie nadtlenku wodoru
(w
katalazie
).
W
chlorofilu
znajduje się
magnezoporfiryna
, która bierze udział w procesach
fotosyntezy
(jest
fotoakceptorem).
O
N
N
N
N
C=O
O
O=C
Mg
chlorofil a
OCH
3
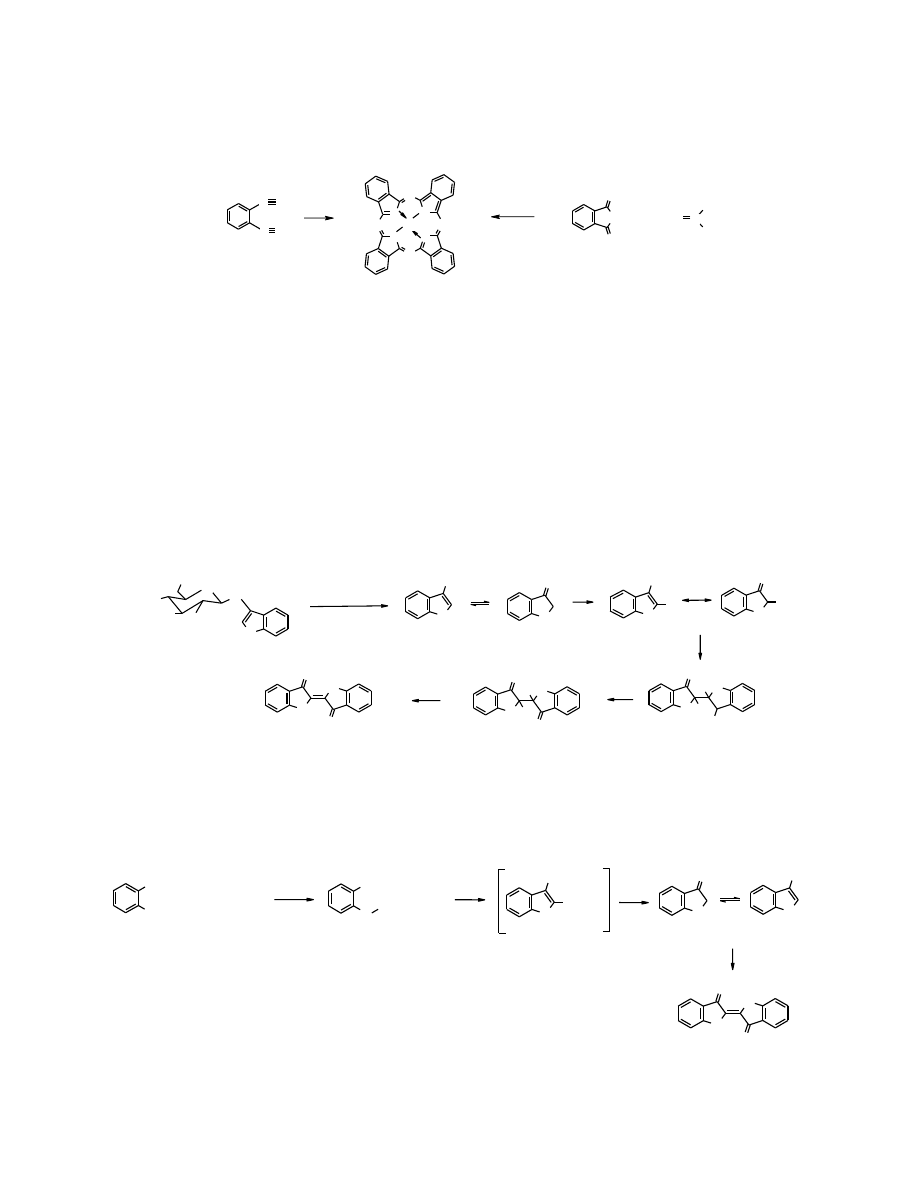
12
Syntetyczne analogi porfiryn znalazły zastosowanie jako barwniki. Należą do nich ftalocyjaniny.
Niebieski barwnik z tej grupy powstaje w reakcji ogrzewania
dinitrylu kwasy ftalowego
z solami
miedzi. Można je otrzymać także z
bezwodnika ftalowego
pod wpływem mocznika.
N
N
N
N
N
N
N
N
N
N
O
O
O
O
NH
2
NH
2
C
C
4
Cu
2
Cl
2
lub Cu
Cu
Cu
2
Cl
2
H
3
BO
3
+ 8
C
dinitryl kwasu ftalowego
ftalocyjanina
bezwodnik ftalowy
mocznik
Ftalocyjaniny są stosowane jako pigmenty do wyrobu farb poligraficznych, olejnych, do
barwienia
kauczuku
i tworzyw syntetycznych.
26.1.6.3 Indygo
Do najstarszych naturalnych barwników
należy
indygo
(
indygotyna
). Było stosowane w
starożytnym Egipcie i w dawnych Indiach. Do Europy zaczęto je sprowadzać w XVI wieku.
Wydobywa się je z roślin gatunku Indigofera. Od XIX w.
indygo
stało się popularnym
barwnikiem, ponieważ opracowano syntetyczne metody jego otrzymywania. Służy między
innymi do barwienia niebieskich dżinsów.
W stanie naturalnym
indygo
występuje w postaci glukozydu –
3-glukozyloindolu
, zwanego
indykanem
, który pod wpływem enzymów jest rozkładany (
hydrolizuje
) do
indoksylu
. Tlen z
powietrza
utlenia
indoksyl
do rodnika, a ten z kolei
dimeryzuje
i tworzy się bezbarwne
leukoindygo
, z niego zaś w dalszym procesie
utleniania
powstaje barwne
indygo
.
O
O
H
O
H
OH
O
N
H
N
H
OH
N
H
O
N
H
O
H
N
H
O
H
N
H
O
H
N
H
O
H
H
N
H
O
N
H
O
H
H
N
H
O
N
H
O
indykan
hydroliza
enzymatyczna
lub kwaśna
O
2
.
.
rodnik
indoksyl
O
2
dimeryzacja
0,5 O
2
- HOH
odwodornienie
indygo
glukozyd indoksylu
OH
leukoindygo
indygotyna
(
)
(
)
Rys. 26.3 Przekształcanie surowca roślinnego w
indygo
Opracowano wiele metod syntezy
indygo
. W jednej z nich surowcem jest
kwas antranilowy
,
który w reakcji
N-alkilowania
solą
kwasu chlorooctowego
zostaje przekształcony w
o-
karboksyfenyloglicynę
.
Z kolei po jej
cyklizacji
i
dekarboksylacji
tworzy się
indoksyl
, który po
utlenieniu przechodzi
indygo
.
N
H
OH
N
H
O
N
H
O
N
H
O
NH
2
COOH
N
COOH
CH
2
COOH
N
H
OH
COOK
O
2
indoksyl
indygo
+ ClCH
2
COOH
1.
Na
2
CO
3
KOH
260
o
C
H
2.
H
+
- CO
2
o-karboksy-N-fenyloglicyna
kwas antranilowy
(39%)
(55%)
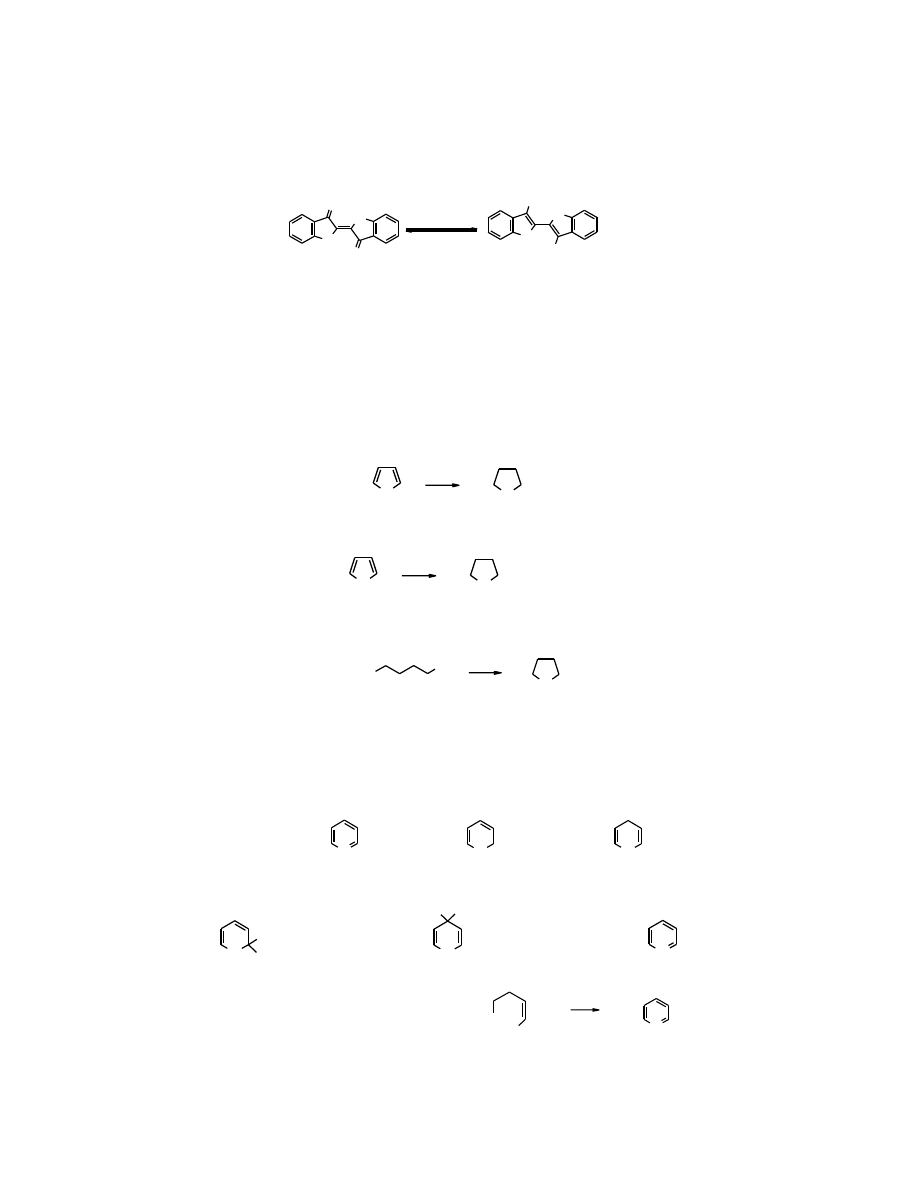
13
Barwienie
za pomocą
indygo
dokonuje się
technika kadziową
. Najpierw nierozpuszczalne w
wodzie
indygo
redukuje się za pomocą ditionianu sodu do rozpuszczalnej formy, która nosi
nazwę
leukoindygo
. Klarownym roztworem (
kadzią
) nasącza się tkaniny, które schnąc na
powietrzu zabarwiają się pod wpływem tlenu (
leukoindygo
zostaje
utlenione
do
indygo
)
.
N
H
O
N
H
O
N
H
O
N
H
O
indygo
-
-
leukoindygo
Na
2
S
2
O
4
[H]
powietrze [O]
Zanik barwy w
leukoindygo
jest spowodowany zmianą układu sprzężonych wiązań podwójnych.
26.1.7 Nasycone, pięcioczłonowe związki heterocykliczne
Pirol
redukowany wodorem na Ni traci aromatyczność i przekształca się w cykliczną aminę
alifatyczną –
pirolidynę
. Widoczna jest ogromna różnica w zasadowości obu związków.
Zarówno
pirolidyna
, jak i
piperydyna
znalazły zastosowanie w chemii organicznej jako zasady, a
przede wszystkim do otrzymywania enamin, które są wykorzystywane w syntezie pochodnych
związków karbonylowych.
N
H
N
H
H
2
/Ni
pirol
pirolidyna
pK
a
~ 14
pK
a
~ 3
Podobnie z
furanu
powstaje
tetrahydrofuran
(THF), popularny rozpuszczalnik eterowy.
O
O
H
2
/Ni
furan
tetrahydrofuran
Tetrahydrotiofen
najłatwiej otrzymać w reakcji
1,4-dibromobutanu
z siarczkiem sodu.
Tetrahydrotiofen
ma właściwości typowych sulfidów.
Br
Br
S
Na
2
S
tetrahydrotiofen
1,4-dibromobutan
26.2
Sześcioczłonowe heterocykle aromatyczne
Do głównych przedstawicieli tej grupy związków należy
pirydyna
(
azabenzen
). Jej analogi
tlenowe –
pirany
– są nietrwałe; nie mają właściwości aromatycznych, szybko polimeryzują.
Trwałe są dihydro- i tetrahydropirany.
N
O
O
pirydyna
-piran
-piran
..
..
..
..
..
2H-piran
(
)
4H-piran
(
)
Znane są dialkilowe pochodne piranów i
kation piryliowy
, który ma właściwości aromatyczne.
O
R
R
O
R
R
O
..
..
..
..
..
+
X
-
dialkilowe pochodne
- i
-piranu
kation
piryliowy
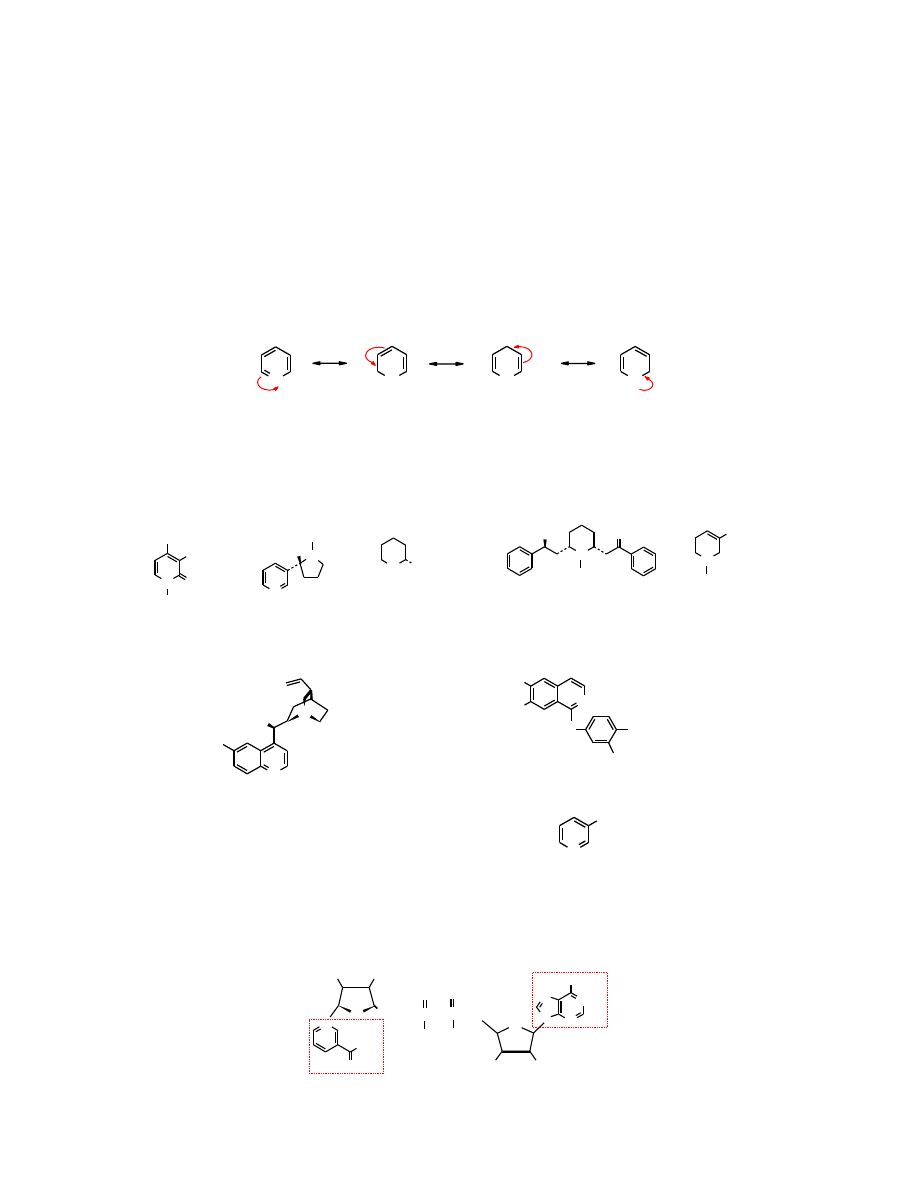
Sole kationu pirylowego
powstają w wyniku
odwodnienia
odpowiednich
1,5-dialdehydów lub 1,5-diketonów.
O
CHO
O
H
..
+
Cl
-
POCl
3
- 2 HOH
aldehyd glutakonowy
chlorek piryliowy
(penta-2,4-dien-1,5-dial)
14
26.2.1 Budowa cząsteczki pirydyny
Kształt cząsteczki
pirydyny
różni się nieco od kształtu cząsteczki
benzenu
, który odpowiada
regularnemu sześciokątowi. W
pirydynie
wiązania C-N (0,134 nm) są krótsze niż C-C (0,14 nm).
Ta różnica wynika z większej elektroujemności atomu azotu w porównaniu do atomu węgla i
wpływa na rozkład gęstości elektronów; jest większa wokół atomu N. W
pirydynie
podobnie jak
w
benzenie
wszystkie atomy tworzące pierścień mają hybrydyzację sp
2
, przy czym wolna para
elektronów atomu azotu obsadzająca orbital sp
2
może być akceptorem protonu, a przez to
pirydyna
wykazuje właściwości zasadowe. Cząsteczka
pirydyny
jest polarna, jej moment
dipolowy wynosi 2,2 D, podczas gdy benzenu
= 0. Na atomie azotu skupiony jest cząstkowy
ładunek ujemny, a na atomach węgla C2, C4 i C6 cząstkowy ładunek dodatni. Do takiego
wniosku można dojść porównując wynikające z mezomerii
formy kanoniczne
pirydyny
.
N
N
N
N
+
-
+
-
+
-
26.2.2 Występowanie
Pirydyna
znajduje się w smole pogazowej, natomiast wiele jej analogów i pochodnych występuje
w naturze. Pierścień pirydynowy wchodzi skład wielu alkaloidów, np.
rycyniny
(w nasionach
olejodajnej rośliny – rącznika) czy
nikotyny
. Uwodorniony pierścień odnajdujemy w
koniinie
,
lobelinie
(w stroiczce rozdętej) czy w alkaloidach palmy areki (np.
arekaidyna
).
N
O
CH
3
CN
N
N
H
CH
3
N
H
CH
2
CH
2
CH
3
N
OH
O
CH
3
N
COOH
CH
3
OCH
3
rycynina
(-)-(S)-nikotyna
(+)-(S)-koniina
lobelina
arekaidyna
Pierścień pirydynowy znajduje się w
chinolinie
i
izochinolinie
. Pochodnymi tych związków są
między innymi, takie alkaloidy, jak
chinina
i
papaweryna
.
N
N
O
H
N
CH
3
O
CH
3
O
CH
3
O
chinina
papaweryna
H
2
C
OCH
3
OCH
3
Kwas nikotynowy
i jego
amid
(pochodne
pirydyny
)
należą do grupy witaminy B.
Kwas ten otrzymał nazwę
nikotynowy
, ponieważ po raz
pierwszy został otrzymany w wyniku utlenienia
nikotyny
.
Nikotynamid
wchodzi w skład
dinukleotydu nikotynoamidoadeninowego
(NAD
+
), koenzymu
ATP. NAD
+
jest ważnym biochemicznym utleniaczem. W trakcie
redukcji
przekształca się w
zredukowany dinukleotyd nikotynoamidoadeninowy
(NADH).
N
O
CH
2
-O-P-O-P-O-CH
2
NH
2
O
OH
O
H
O
O
O
O
O
O
H
OH
N
N
N
N
NH
2
+
-
-
nikotynamid
adenina
N
COOH
kwas nikotynowy
15
26.2.3 Otrzymywanie pirydyny
Głównym, a właściwie jedynym źródłem
pirydyny
jest smoła pogazowa, w której jej zawartość
dochodzi do 0,1%. Wyodrębnia się ją za pomocą destylacji. Znajduje się we frakcji zwanej
olejem lekkim, w której towarzyszą jej homologi: trzy metylopirydyny – zwane pikolinami,
dimetylopirydyny, tzw. lutydyny i kolidyny, czyli trimetylopirydyny.
Zadanie: narysuj wzory i nazwij homologi
pirydyny
.
Nie ma prostej syntezy
pirydyny
.
3-Pikolina
powstaje w reakcji
akroleiny
z amoniakiem w temperaturze 350
o
C,
w obecności katalizatorów.
26.2.4 Właściwości fizyczne pirydyny
Pirydyna jest cieczą wrzącą w temperaturze 115
o
C, topnieje w -41
o
C. Miesza się całkowicie z
wodą. Ma nieprzyjemny zapach, trochę przypominający tytoń.
26.2.5 Właściwości chemiczne pirydyny
Pirydyna
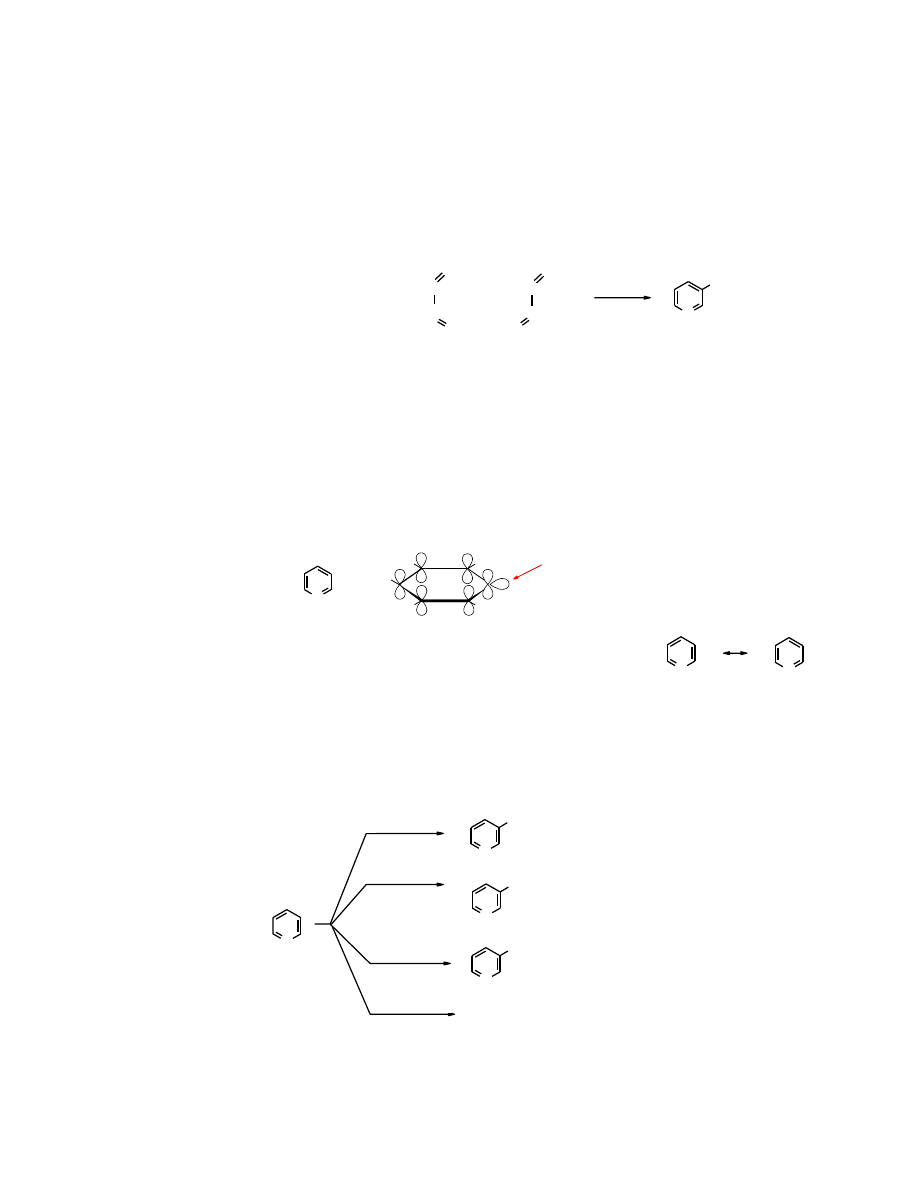
ma właściwości związków aromatycznych. Aromatyczność
pirydyny
wynika z
planarnej budowy jej cząsteczki i sprzężenia 6 elektronów
Pięć atomów węgla i atom azotu w
pierścieniu
pirydyny
mają hybrydyzację sp
2
. Wolna para elektronów atomu azotu znajduje się na
orbitalu sp
2
, a więc inaczej niż w
pirolu
i nie bierze udziału w sprzężeniu.
N
H
H
N
H
H
H
.
.
.
.
.
.
:
wolna para
na orbitalu sp
2
pirydyna
Kąty pomiędzy wiązaniami C-C i C-N wynoszą po 120
o
, wiązania
tworzące pierścień są jednakowej długości – 1,39 Å.
Pirydynę
można
przedstawić za pomocą wzorów mezomerycznych.
26.2.5.1
Reakcje substytucji elektrofilowej, S
E
Pirydyna
jest znacznie mniej aktywna w reakcjach
substytucji elektrofilowej
, nie tylko w
porównaniu z aromatycznymi heterocyklami pięcioczłonowymi, ale również w porównaniu z
benzenem
. Reakcje S
E
pirydyny
wymagają drastycznych warunków (wysokiej temperatury). W
reakcjach Friedel-Craftsa
pirydyna
jest nieaktywna.
N
N
Br
N
SO
3
H
N
NO
2
Br
2
300
o
C
+ HBr
SO
3
, HgSO
4
H
2
SO
4
,220
o
C
HNO
3
NaNO
3
, 370
o
C
RX lub RCOX
AlCl
3
brak reakcji
+ HOH
3-bromopirydyna
30%
kwas
3-pirydynosulfonowy
70%
3-nitropirydyna
5%
pirydyna
N
N
CH
CH
CH
2
O
CH
CH
CH
2
O
N
CH
3
NH
3
+
350
o
C, kat.
- 2 HOH
3-pikolina
akroleina
16
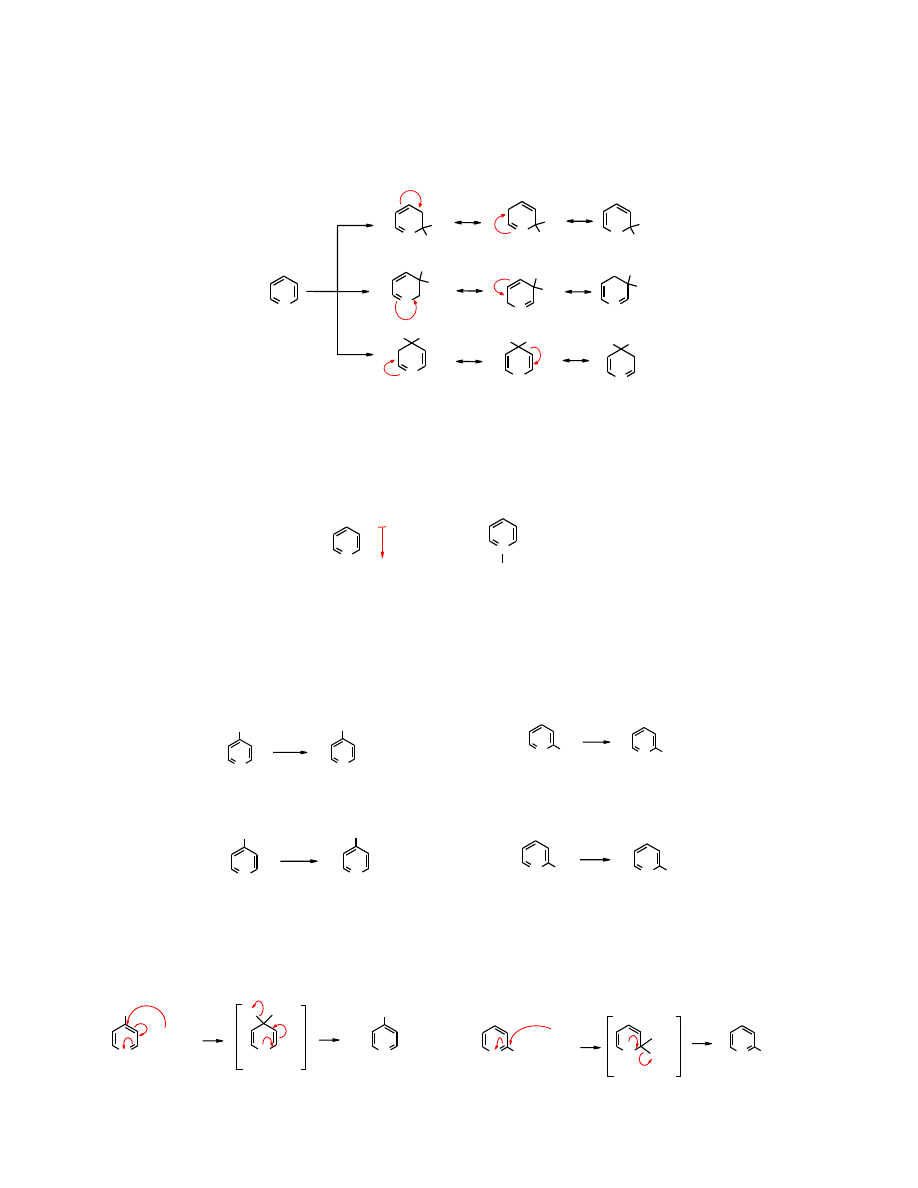
Substytucja elektrofilowa
w
pirydynie
zachodzi w pozycji 3, ponieważ pozycja 2 i 4 jest
dezaktywowana. We wzorach mezomerycznych po ataku odczynnika elektrofilowego na pozycję
2 i 4 obserwuje się ładunek dodatni na atomie azotu, co jest niekorzystne, z uwagi na to, że atom
azotu jest bardziej elektroujemny od atomu węgla.
N
N
Y
H
N
Y
H
N
H
Y
N
Y
H
N
H
Y
N
Y
H
N
Y
H
N
Y
H
N
H
Y
Y
+
2
3
4
+
+
..
..
..
..
+
..
+
+
..
+
+
..
..
+
+
..
Obniżona reaktywność
pirydyny
spowodowana jest wyciąganiem elektronów z pierścienia i
skupienie się ładunku ujemnego na atomie azotu, co dezaktywuje pierścień na atak nukleofilowy.
Stosunkowo do najmniejszej utraty elektronów dochodzi w położeniu 3 oraz 5 i w tych miejscach
dochodzi do
substytucji
. Duża wartość momentu dipolowego, z ujemnym biegunem na atomie
azotu, świadczy o przesunięciu elektronów w stronę atomu azotu.
N
N
H
= 2,26D
-
+
+
+
+
+
..
+
pirydyna
protonowana
Ponadto reakcje S
E
biegną często w środowisku kwaśnym, co powoduje
protonowanie
atomu
azotu i utworzenie ładunku dodatniego, a więc jeszcze silniejszą dezaktywację.
26.2.5.2
Reakcje substytucji nukleofilowej
Częściowy ładunek dodatni w cząsteczce
pirydyny
w położeniach 2, 4 i 6 czyni te miejsca
podatne na atak silnych nukleofili. Odpowiednie pochodne pirydyny ułatwiają reakcję z
nukleofilami.
N
Cl
N
OC
2
H
5
N
Br
N
NH
2
Na
+
OEt
-
EtOH
4-chloropirydyna
4-etoksypirydyna
(75%)
NaNH
2
NH3
2-bromopirydyna
2-aminopirydyna
(67%)
W podwyższonej temperaturze nawet sam amoniak jest zdolny wymieć atom halogenu.
N
Cl
N
NH
2
N
Cl
N
NH
2
NH
3
180
o
C
4-chloropirydyna
4-aminopirydyna
NH
3
2-chloropirydyna
2-aminopirydyna
180
o
C
Mechanizm reakcji
Powyższe reakcje biegną wg typowego mechanizmu
aromatycznej substytucji nukleofilowej
–
addycja-eliminacja. Obecność atomu azotu w pierścieniu
pirydyny
aktywuje położenie 2 na atak
nukleofilowy. Po
addycji
nukleofila następuje
eliminacja
halogenu.
N
Cl
N
Cl
N
NH
2
N
Cl
N
Cl
NH
2
N
NH
2
+ NH
2
: ..
..
-
..
-
..
..
- Cl
-
NH
2
+ NH
2
: ..
..
-
..
-
..
..
- Cl
-
4-chloropirydyna
4-aminopirydyna
2-chloropirydyna
2-aminopirydyna
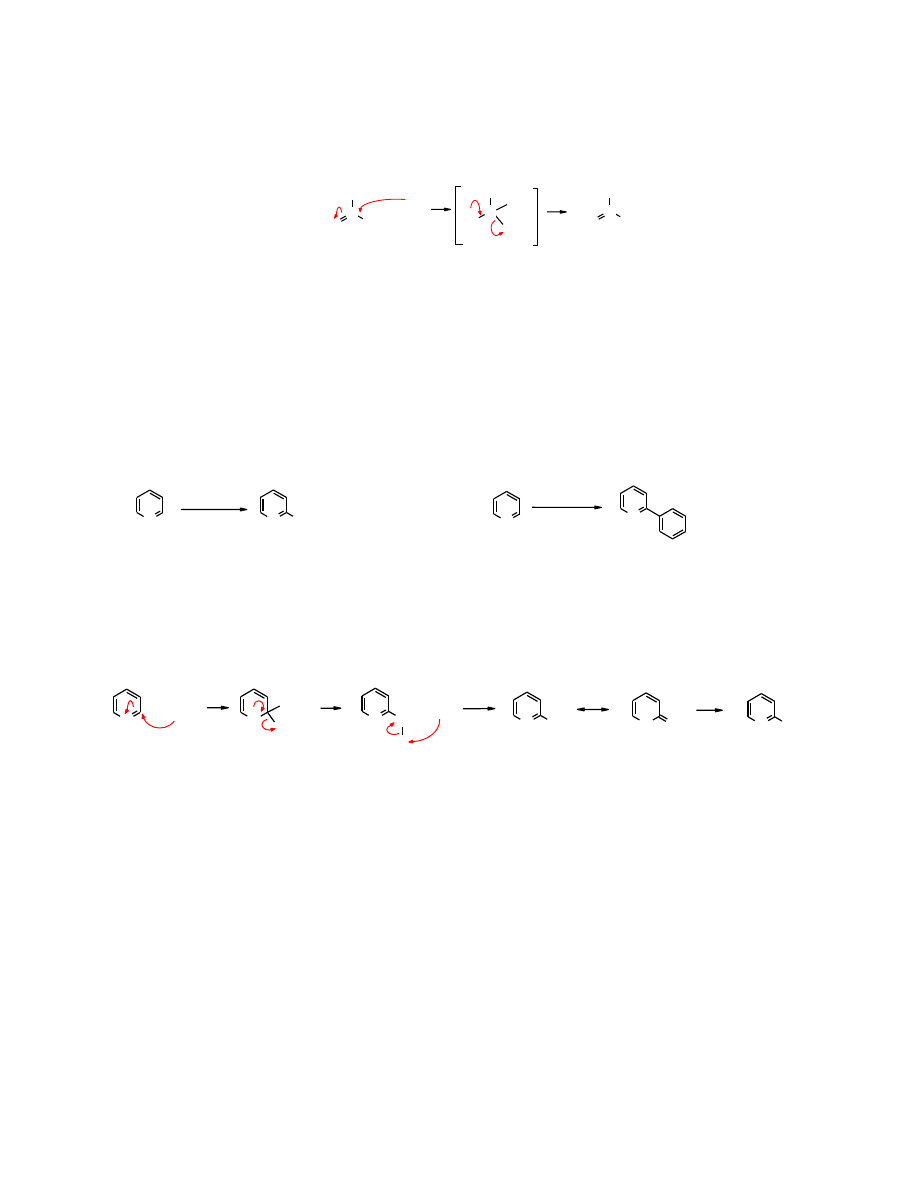
17
Warto zwrócić uwagę na to, że powyższy mechanizm przypomina mechanizm reakcji
substytucji
w grupie karbonylowej pochodnych kwasów karboksylowych, np.
amonolizę
chlorków kwasowych do amidów.
R
Cl
O
R
Cl
O
NH
2
R
NH
2
O
C
+ NH
2
:
..
..
-
..
..
- Cl
-
C
:
:
-
C
..
:
chlorek kwasowy
amid
Oczywiście chlorki kwasowe są znacznie aktywniejsze niż
chloropirydyny
i ulegają
amonolizie
amoniakiem lub aminami już w obniżonej temperaturze; nie trzeba stosować drastycznych
warunków ani tak silnych nukleofili jak amidki.
Substytucji nukleofilowej
nie ulegają pochodne
pirydyny
zawierające grupę odchodząca w
położeniu 3.
26.2.5.3
Reakcja Cziczibabina
Pod wpływem silnych nukleofili dochodzi do podstawienia atomu wodoru w niepodstawionej
pirydynie
, a powstaje głównie
2-aminopirydyna
, ponieważ pozycja 2- jest najbardziej
uprzywilejowana na atak nukleofila.
N
N
NH
2
N
N
..
1.
NaNH
2
/140
o
C
2.
HOH
+ H
2
pirydyna
2-aminopirydyna
..
1.
PhLi/100
o
C
pirydyna
2-fenylopirydyna
2. HOH
+ H
2
Mechanizm reakcji
Reakcja polega na
addycji
nukleofila w pozycji 2
pirydyny
, odszczepienie jonu wodorkowego,
utworzenie cząsteczki H
2
z protonem oderwanym z grupy aminowej i przekształcenie adduktu w
stabilizowany mezomerycznie anion aminopirydyniowy. Pod wpływem wody z anionu powstaje
2-aminopirydyna
. Reakcja jest wolniejsza niż z halogenopochodnymi pirydyny, ponieważ anion
wodorkowy jest znacznie trudniej odchodząca grupą niż anion halogenkowy.
N
N
NH
2
H
N
NH
H
N
NH
N
NH
N
NH
2
2-aminopirydyna
..
- H
2
..
+ NH
2
:..
-
..
..
..
..
+ H
-
:
..
..
..
-
..
..
.
.
-
-
..
pirydyna
HOH
Aminopirydyny występują głównie w formie aminowej, a nie iminowej.
Zadanie: przedstaw schemat tautomeryzacji
2-aminopirydyny
z formy aminowej do iminowej.
26.2.5.4 Reakcja 2-pikoliny z aldehydami
Atomy
-wodoru w alkilopirydynach mają właściwości kwasowe i pod wpływem zasad ulegają
odszczepieniu. Powstały w ten sposób karboanion reaguje ze związkami karbonylowymi jako
donor elektronów. Produkty addycji – hydroksypochodne – łatwo tracą cząsteczkę wody tworząc
nowe wiązanie C=C, sprzężone z aromatycznymi elektronami
.
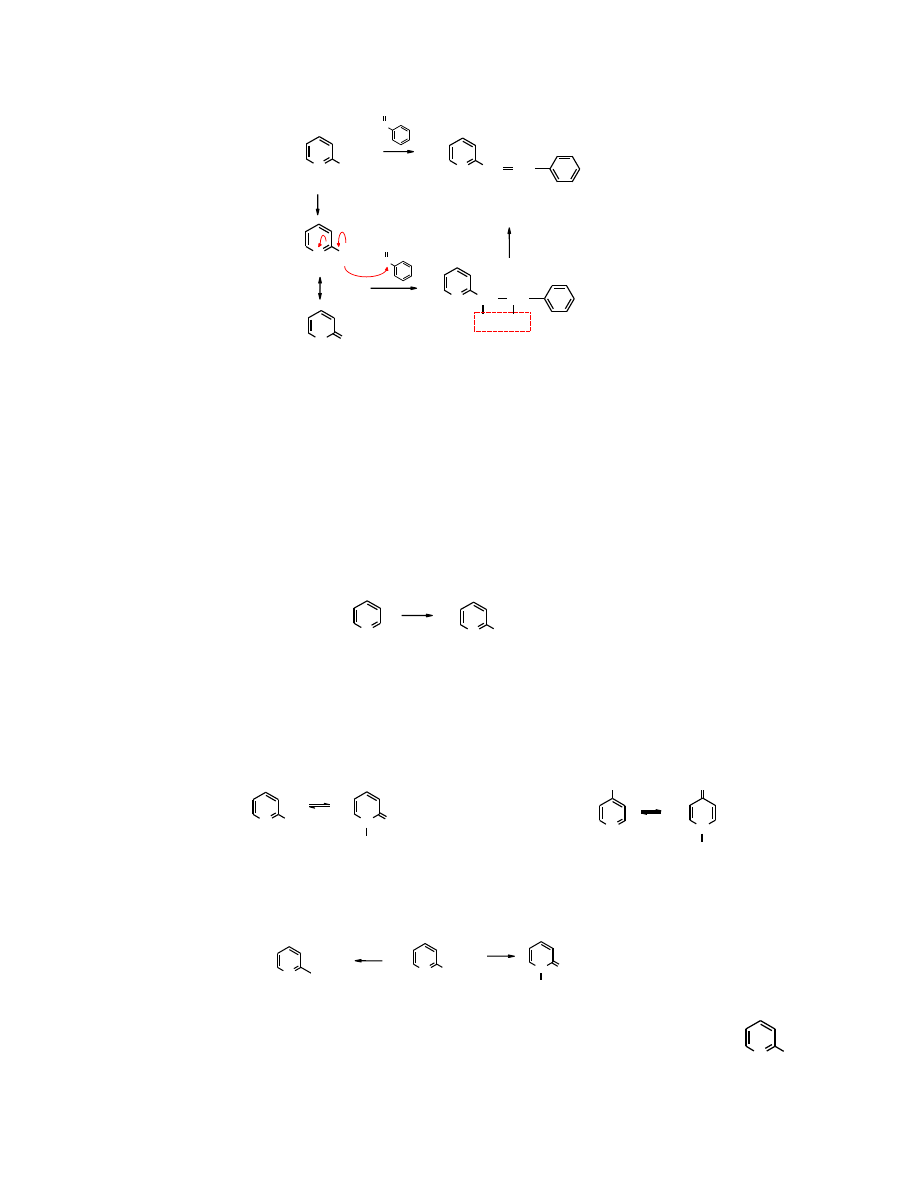
18
N
CH
3
HC
O
N
CH CH
N
CH
2
N
CH
2
HC
O
N
CH CH
H
OH
NaOH
..
..
..
-
OH
..
-
..
..
-
..
- HOH
2-pikolina
1-fenylo-2-(2-pirydylo)eten
1-fenylo-1-hydroksy-2(2-pirydylo)etan
26.2.5.5
Hydroksypirydyny
Znane są trzy hydroksypirydyny –
2-hydroksypirydyna
,
3-hydroksypirydyna
i
4-
hydroksypirydyna
. Izomery 2- i 3- można otrzymać podobnie jak
fenol
poprzez
diazowanie
aminopirydyn i
reakcję
zagotowania
lub w wyniku
stapiania
kwasów pirydynosulfonowych z
wodorotlenkiem sodu.
Zadanie: napisz schematy reakcji otrzymywania hydroksypirydyn za pomocą
reakcji zagotowania
i
reakcji
stapiania
.
Hydroksypirydyny powstają również w wyniku bezpośredniego
hydroksylowania
pirydyny
wodorotlenkiem sodu w podwyższonej temperaturze. Jest to reakcja zbliżona do reakcji
Cziczibabina.
N
N
OH
NaOH
..
pirydyna
..
2-hydroksypirydyna
Synteza izomeru 3 jest bardziej skomplikowana.
Wszystkie hydroksypirydyny mają właściwości zbliżone do
fenolu
. Łatwiej ulegają reakcjom
substytucji elektrofilowej niż sama
pirydyna
.
2-
i
4-Hydroksypirydyny
są w równowadze
tautomerycznej
z odpowiednimi
pirydonami.
Odmiany pirydonowe
przeważają w
rozpuszczalnikach protonowych i w takiej formie krystalizują.
N
O
N
OH
H
N
O
N
OH
H
pirydyn-2-on
.
.
2-hydroksypirydyna
(pirydyn-2-ol)
(pirydyn-4-ol)
pirydyn-4-on
.
.
4-hydroksypirydyna
Z
hydroksypirydyn
można otrzymać pochodne obu tautomerów.
Diazometan
przekształca
2-
hydroksypirydynę
w
2-metoksypirydynę
, a
alkilowanie
jodkiem metylu
prowadzi do
N-
metylopiryd-2-onu
.
N
OH
N
N
O
CH
3
CH
2
N
2
OCH
3
2-metoksypirydyna
2-hydroksypirydyna
N-metylo-
pirydyn-2-on
CH
3
I
Znane są również tiolowe pochodne
pirydyny
. One także
występują w stanie równowagi z formą tautomeryczną.
N
SH
..
2-merkaptopirydyna
(pirydyno-2-tiol)
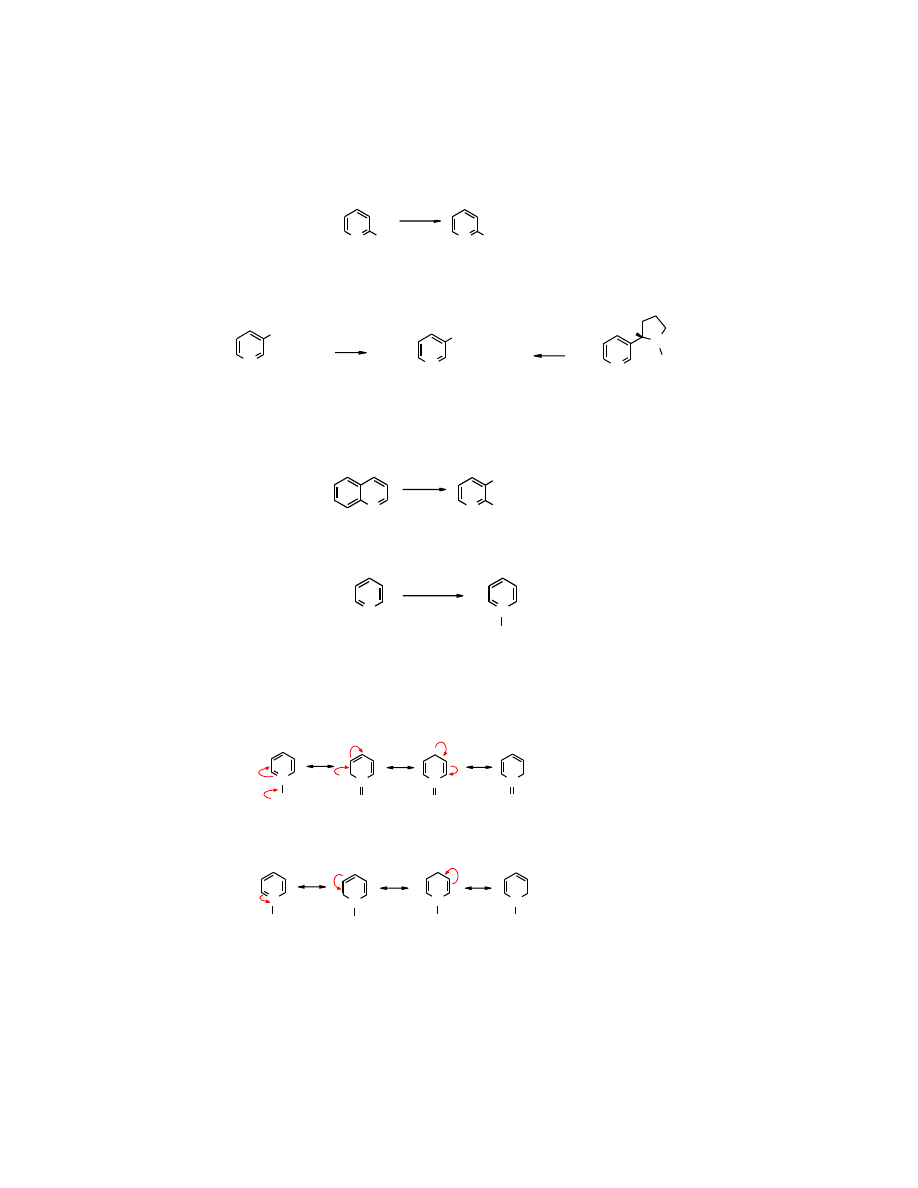
19
Zadanie: narysuj wzór tiolowej pochodnej
pirydyny
i przedstaw przemianę jej tautomeryczną.
26.2.5.6 Utlenianie pirydyny i jej pochodnych
Pirydyna
jest odporna na działanie wielu utleniaczy. Podobnie jak w arenach homocyklicznych
łatwo daje się
utlenić
jej łańcuch boczny.
N
CH
3
N
COOH
KMnO
4
2-pikolona
kwas 2-pikolinowy
Kwas 3-pikolinowy
znany jest pod nazwą
kwasu nikotynowego
, ponieważ powstaje w wyniku
utlenienia
nie tylko
3-pikoliny
, ale i
nikotyny
, z której zresztą został otrzymany po raz pierwszy.
N
CH
3
N
COOH
N
N
CH
3
H
KMnO
4
KMnO
4
3-pikolina kwas nikotynowy
(
kwas 3-pikolinowy
)
nikotyna
Pirydyna
jest bardziej odporna na
utlenienie
niż
benzen
, dlatego z chinoliny pod wpływem
nadmanganianu potasu powstaje
kwas chinolinowy
– zostaje zachowany pierścień
heterocykliczny.
N
N
COOH
COOH
KMnO
4
chinolina
kwas chinolinowy
Pirydyna
utleniana
za pomocą nadkwasów zostaje przekształcona w
1-tlenek pirydyny
(
N-tlenek
pirydyny
).
N
N
O
CH
3
COOOH
-
+
- CH
3
COOH
pirydyna
1-tlenek pirydyny
1-Tlenek pirydyny
zachowuje właściwości aromatyczne, z tym że rozkład ładunków w
pierścieniu jest inny niż w
pirydynie
. Z poniżej przedstawionych wzorów mezomerycznych
wynika, że reakcje
substytucji elektrofilowej
w
1-tlenku pirydyny
powinny zachodzić w
pozycjach 2 i 4 (inaczej niż w
pirydynie
).
N
O
N
O
N
O
N
O
-
+
-
+
: :
..
..
-
+
..
: :
: :
-
+
..
: :
1-tlenek pirydyny
Z innych wzorów mezomerycznych wynika, że
1-tlenek pirydyny
powinien być aktywniejszy niż
pirydyna
w reakcjach
substytucji nukleofilowej
.
N
O
N
O
N
O
N
O
1-tlenek pirydyny
-
+
-
+
: :
..
..
: :
..
+
..
: :
..
+
..
: :
..
-
-
Poprzez
utlenienie
pirydyny
do jej N-tlenku można zsyntezować wiele pochodnych
niemożliwych do otrzymania bezpośrednio z
pirydyny
. Powrót z
tlenku pirydyny
(lub tlenku jej
pochodnych) do
pirydyny
(jej pochodnych) dokonuje się w reakcji z PCl
3
.
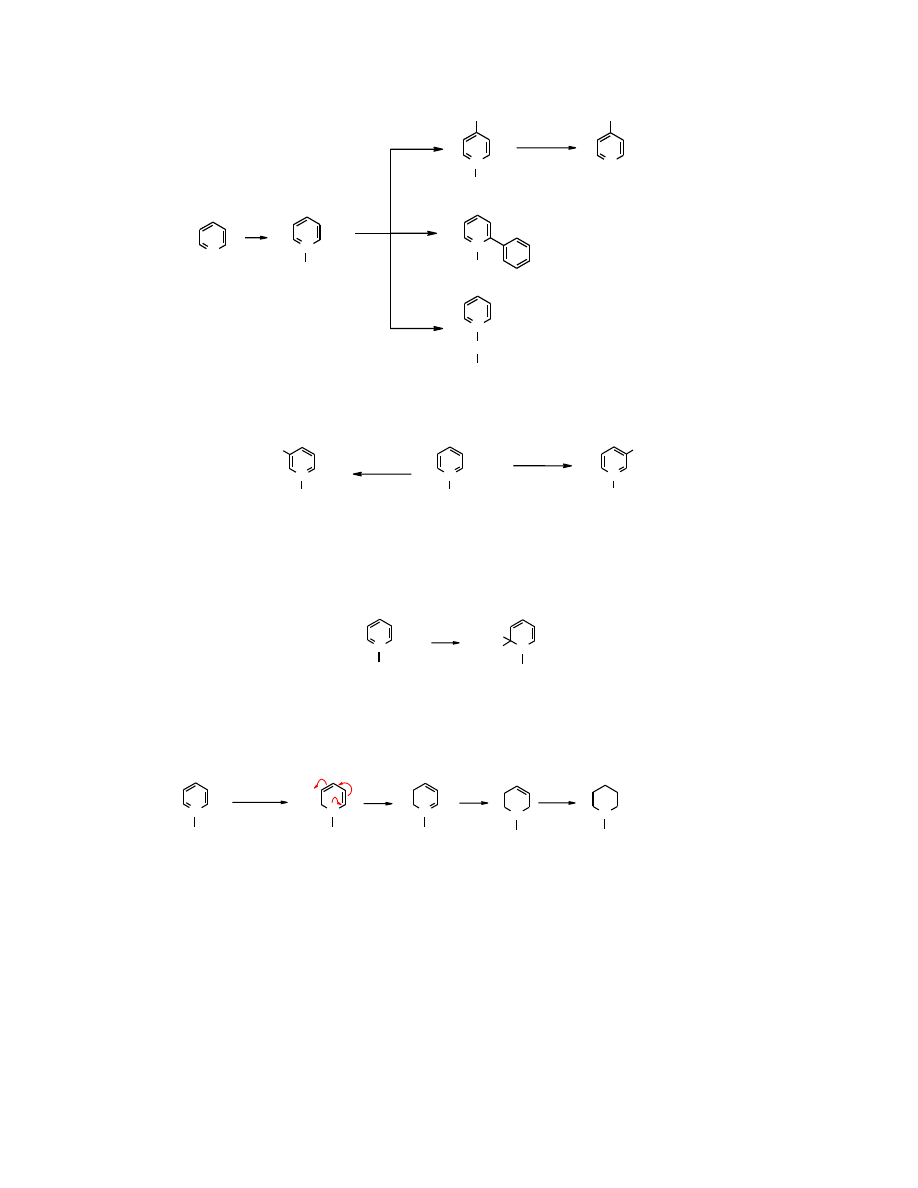
20
N
N
O
N
NO
2
O
O
N
O
CH
3
N
N
NO
2
: :
..
+
-
[O]
HNO
3
/
H
2
SO
4
100
o
C
PhMgBr
CH
3
I
: :
..
+
-
: :
..
+
-
: :
+
-
I
PCl
3
1-tlenek
4-nitropirydyny
pirydyna
1-tlenek pirydyny
1-tlenek 2-fenylopirydyny
jodek 1-metoksypirydyniowy
4-nitropirydyna
Natomiast
sulfonowanie
za pomocą oleum i
bromowanie
bromem w oleum prowadzi do
pochodnych w położeniu 3.
N
O
N
HO
3
S
O
N
Br
O
+
-
+
-
+
-
oleum/HgSO
4
240
o
C
70
o
C
Br
2
/oleum
1-tlenek pirydyny
1-tlenek 3-bromopirydyny
1-tlenek kwasu
pirydyno-3-sulfonowego
26.2.5.7 Sole pirydyniowe
W wyniku
alkilowania
pirydyny
tworzą się sole pirydyniowe, które stosunkowo łatwo ulegają
redukcji
reduktorami przenoszącymi aniony wodorkowe (wodorkami) do pochodnych 1,2-
dihydropirydyny.
N
R
N
R
H
H
+
X
-
LiAlH
4
- HX
..
N-alkilo-1,2-dihydropirydyna
kationN-alkilopirydyniowy
Redukcja soli pirydyniowych za pomocą LiAlH
4
w rozpuszczalnikach aprotycznych prowadzi
wyłącznie do pochodnych 1,2-dihydro-, natomiast użycie mniej aktywnego reduktora, jakim jest
NaBH
4
, ale w
etanolu
(w rozpuszczalniku protycznym) daje możliwość uzyskania 1,2,5,6-
tetrahydropochodnych.
N
R
N
R
N
R
N
R
N
R
..
kation
N-alkilo-
pirydyniowy
+
X
-
NaBH
4
EtOH/HOH
+
HOH
- HO
-
NaBH
4
H
2
, Pd/C
N-alkilo-
piperydyna
(N-alkilo-1,2,5,6-
tetrahydropirydyna)
Reakcja
redukcji
kationu N-alkilopirydyniowego do
N-alkilo-1,2-dihydropirydyny
i odwrotna –
utleniania
do związku wyjściowego – są wykorzystywane w procesach biochemicznych. Bierze
w nich udział koenzym zwany
dinukleotydem nikotynoamidoadeninowym
(NAD
+
) i jego
zredukowana forma –
zredukowany dinukleotyd nikotynoamidoadeninowy
(NADH). NAD
+
utlenia
alkohole do aldehydów lub ketonów, a także uczestniczy w „spalaniu” (w metabolizmie)
kwasów tłuszczowych.
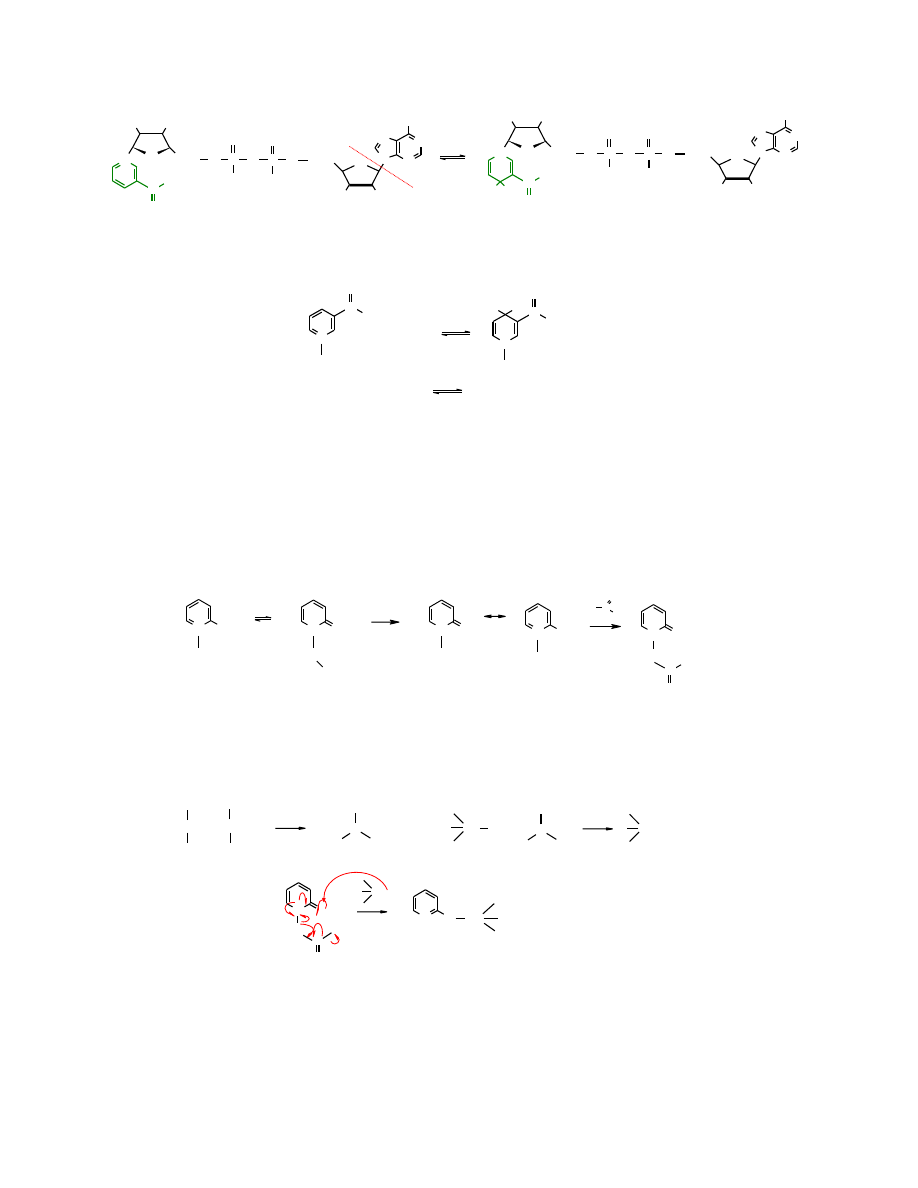
21
N
O
OH
O
H
CH
2
H H
O P O P O
O
O
H
OH
CH
2
N
N
N
N
NH
2
O
NH
2
O
O
O
O
N
O
OH
O
H
CH
2
O P O P O
O
O
H
OH
CH
2
N
N
N
N
NH
2
O
NH
2
O
O
O
O
[H]
[O]
C
-
-
dihydronikotynoamid
zredukowany dinukleotyd nikotynoamidoadeniny (NADH)
H
+
+
C
+
-
-
nikotynoamid
dinukleotyd nikotynoamidoadeniny (NAD
+
)
reszta adeniny
Zmiany zachodzą na reszcie
amidu kwasu nikotynowego
.
N
R
O
NH
2
N
H
H
R
O
NH
2
..
+
C
+ 2 H
+
C
+ H
NAD
+
+ 2 H
NADH + H
+
Dinukleotyd nikotynoamidoadeninowy
(NAD
+
) jest głównym akceptorem elektronów
(utleniaczem) w procesach
utleniania
substratów oddechowych.
Na podobnej zasadzie, co NAD
+
działa regent nazwany
estrem Bartona
.
Sir Derek H. R. Barton (ur. w 1918 r. w Gravelsend, Anglia); doktorat i habilitacja w Londynie; prof. w Birkbeck
College, Harvard, Glasgow, Imperial College, Institut de Chimie des Substances Naturelles, Texas A&M,; Nagroda
Nobla (1969).
Estrem Bartona nazywany jest
O-acetylo-1-tlenek 2-pirydynotiolu
.
N
SH
O
N
S
O
H
N
S
O
N
S
O
O
Cl
N
S
O
O
R
+
-
: :
..
-
: :
..
..
..
..
:
NaH
+
-
: :
..
..
..
:
: :
..:
..
-
R C
: :
..:
C
ester Bartona
1-tlenek pirydyno-2-tiolu
Ester Bartona służy między innymi do otrzymywania pochodnych cynoorganicznych.
Trialkilocyna pod wpływem czynników rodnikotwórczych zostaje przekształcona w rodnik,
który z kolei ulega addycji do estru Bartona. Stabilizacja adduktu następuje poprzez eliminację
rodnika acyliowego i jego rozkład na CO
2
i rodnik alkilowy.
CH
3
CN
CH
3
CN
CN
C
H
3
CH
3
H
CN
C
H
3
CH
3
N
S
O
O
R
..
N
S Sn
CH
3
-C-N=N-C-CH
3
80
o
C
C
2
.
+ N
2
Sn
+
C
.
Sn
.
+ (CH
3
)
2
CHCN
C
:
:
..
Sn
.
..
+ CO
2
+ R
.
..
..
..
26.2.5.8 Redukcja pirydyny
Pirydynę
, podobnie jak
benzen
najlepiej
redukuje
się wodorem wobec katalizatora niklowego,
można również użyć platyny, jako katalizatora. Produktem
redukcji
pirydyny
jest
piperydyna
(
azacykloheksan
).
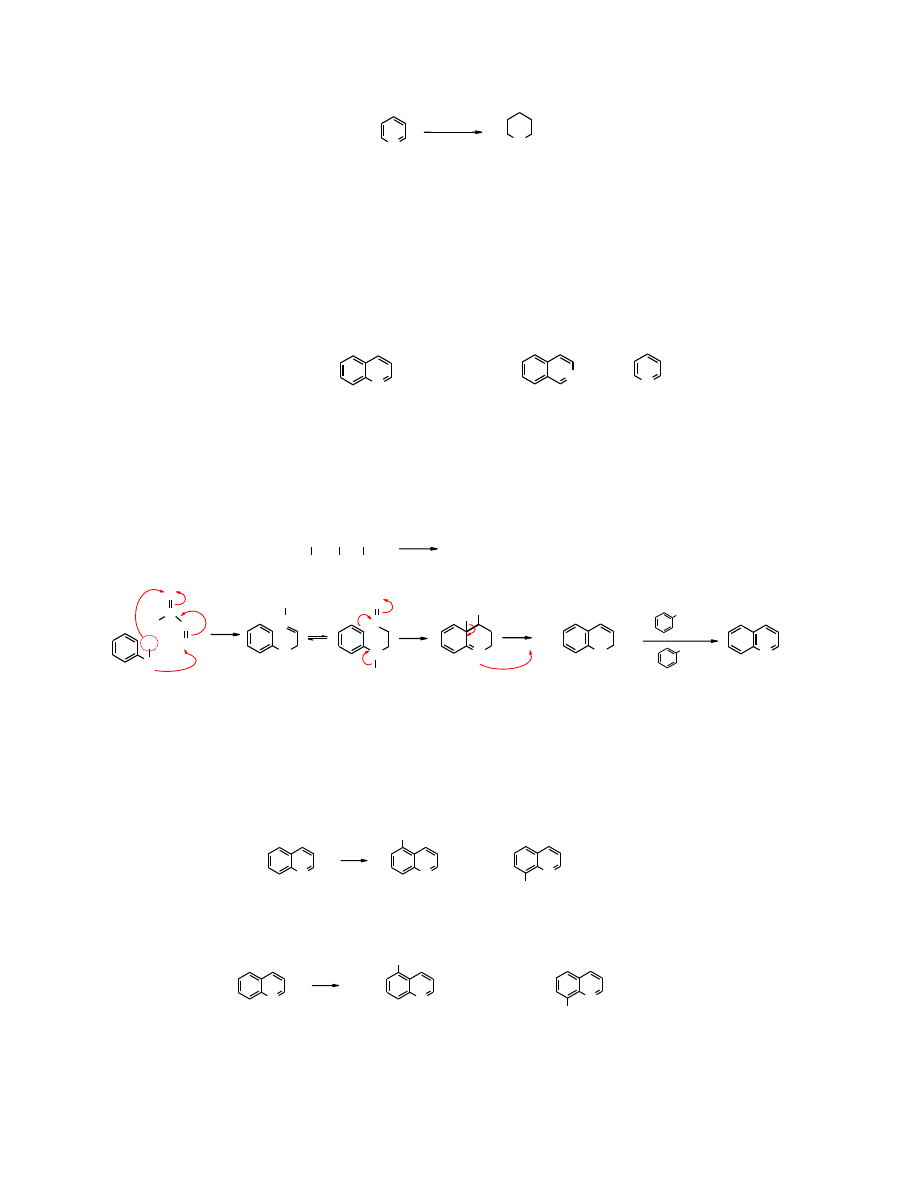
22
N
N
H
H
2
/Pt, H
+
3 at, 25
o
C
pirydyna
piperydyna
Zastosowanie tańszego katalizatora niklowego wymaga podniesienie temperatury reakcji do
200
o
C.
26.2.3 Chinolina
Chinolina
jest żółtawym, trudno rozpuszczalny w wodzie syropem, wrzącym w temperaturze
238
o
C. Pod wpływem światła i powietrza brunatnieje. Z silnymi kwasami tworzy sole; jest
słabszą zasadą niż
anilina
.
Izochinolina
, izomer konstytucyjny
chinoliny
różni się od niej
miejscem położenia atomu azotu;
chinolina
jest
benzo[b]pirydyną
, a
izochinolina
benzo[c]pirydyną
.
N
N
N
chinolina
izochinolina
benzo[b]pirydyna
benzo[c]pirydyna
(
)
(
)
[a]
[b]
[c]
26.2.3.1 Otrzymywanie
Chinolinę
otrzymuje się za pomocą syntezy Skraupa. Powstaje ona w reakcji Michaela
aniliny
z
akroleiną
.
Akroleina
tworzy się in situ z
glicerolu
pod wpływem kwasu siarkowego i
podwyższonej temperatury. Produkt addycji
akroleiny
do
aniliny
ulega
cyklizacji
, a potem
dehydratacji
do
1,2-dihydrochinoliny
, którą
nitrobenzen
utlenia
(reakcja
odwodornienia
) do
chinoliny
. Mogą być stosowane inne utleniacze, np. kwas azotowy.
OH OH OH
CH
2
-CH-CH
2
H
2
SO
4
CH
2
=CH-CHO +
2
HOH
glicerol
akroleina
NH
CH
CH
2
O
H
N
H
OH
N
OH
H
N
H
NO
2
NH
2
N
H
N
O
H
+
C
H
+
CH
..
- HOH
anilina
akroleina
4-hydroksy-1,2,3,4-
tetrahydrochinolina
-
- HOH
chinolina
(88%)
CH
1,2-dihydrochinolina
+ H
+
,
..
Zadanie: napisz stechiometrycznie równanie przekształcenia
1,2-dihydrochinoliny
w
chinolinę
26.2.3.2 Substytucja elektrofilowa chinoliny
Pierścień benzenowy jest bardziej podatny na reakcje S
E
niż pirydynowy, dlatego też do
podstawienia atomów wodoru elektrofilami w
chinolinie
dochodzi w części homocyklicznej.
Chinolina
w reakcjach S
E
jest mniej aktywna niż
benzen
.
N
N
Br
N
Br
chinolina
Br
2
H
2
SO
4
+
5-bromochinolina
8-bromochinolina
Oba izomery bromochinoliny powstają prawie w jednakowych ilościach, natomiast
5-
nitrochinolina
powstaje ze znacznie większą wydajnością niż izomer 8.
N
N
NO
2
N
NO
2
chinolina
HNO
3
H
2
SO
4
+
5-nitrochinolina
8-nitrochinolina
10 : 1

23
W środowisku mniej kwaśnym, np. w reakcji
chinoliny
z
azotanem (V) acetylu
powstaje głównie
3-nitrochinolina
. Być może w środowisku mniej kwaśnym w reakcji S
E
bierze udział
chinolina
nieprotonowana, a w bardziej kwaśnych kation chinoliniowy, który dezaktywuje pierścień
zawierający atom azotu i do nitrowania dochodzi głównie w pierścieniu homocyklicznym, wobec
czego tworzy się 5- i 8-pochodna.
N
N
NO
2
N
NO
2
N
NO
2
HNO
3
/Ac
2
O
20
o
C
dym. HNO
3
H
2
SO
4
stęż.
3-nitrochinolina
5-nitrochinolina
8-nitrochinolina
(35%)
(43%)
+
Halogenki alkilowe i acylowe
alkilują
bądź
acylują
chinolinowy atom azotu. N-alkilowe
pochodne
chinoliny
są trwałe, podczas gdy N-acylowe są bardzo reaktywne, ulegają np.
hydrolizie
już pod wpływem wilgoci z powietrza.
Zadanie: napisz schemat reakcji otrzymywania
N-etylochinoliny
Wyszukiwarka
Podobne podstrony:
26 Heterocykliczne zwiazki aromatyczne
ZWIAZKI AROMATYCZNE
Zwiazki aromatyczne 09
Cw 5 Zwiazki aromatyczne
związki aromatycznych, Naukowe PL, Biotechnologia, Enzymologia, Genetyka
Substytucja elektrofilowa w związkach aromatycznych(1), ++pomoc w nauce rózne przedmioty++
Cw 5-Zwiazki aromatyczne
08 Zwiazki aromatyczne materialy dodatkowe
ZWIAZKI AROMATYCZNE 2009pop., Chemia Organiczna
Główne szlaki biodegradacji związków aromatycznych, Naukowe PL, Biotechnologia, Enzymologia, Genetyk
ZWIAZKI AROMATYCZNE
ZWIĄZKI AROMATYCZNE
Związki heterocykliczne, Chemia
Enzymatyczna redukcja aromatycznych związków nitrowych
zwiazki heterocykliczne
więcej podobnych podstron