11. Wyznaczanie ciepła parowania i ciepła topnienia
Cel:
Poznanie procesów topnienia i wrzenia jako przykładu przemian fazowych.
Poznanie zasady sporządzania bilansu cieplnego.
Wyznaczenie ciepła parowania wody przy użyciu kalorymetru.
Wyznaczenie ciepła topnienia lodu przy użyciu kalorymetru.
Pytania i zagadnienia kontrolne:
Trzy podstawowe stany skupienia i przejścia fazowe między nimi.
Definicja ciepła właściwego, ciepła parowania i ciepła topnienia.
Zasada sporządzania bilansu cieplnego.
Wyznaczenie ciepła parowania wody – ułożyć bilans cieplny i wyprowadzić wzór na
ciepło parowania.
Wyznaczenie ciepła topnienia lodu – ułożyć bilans cieplny i wyprowadzić wzór na
ciepło topnienia.
Opis ćwiczenia:
Podstawowym przyrządem wykorzystywanym do pomiaru ciepła właściwego, ciepła
parowani i ciepła topnienia jest kalorymetr. Izoluje on termicznie badany układu od wpływu
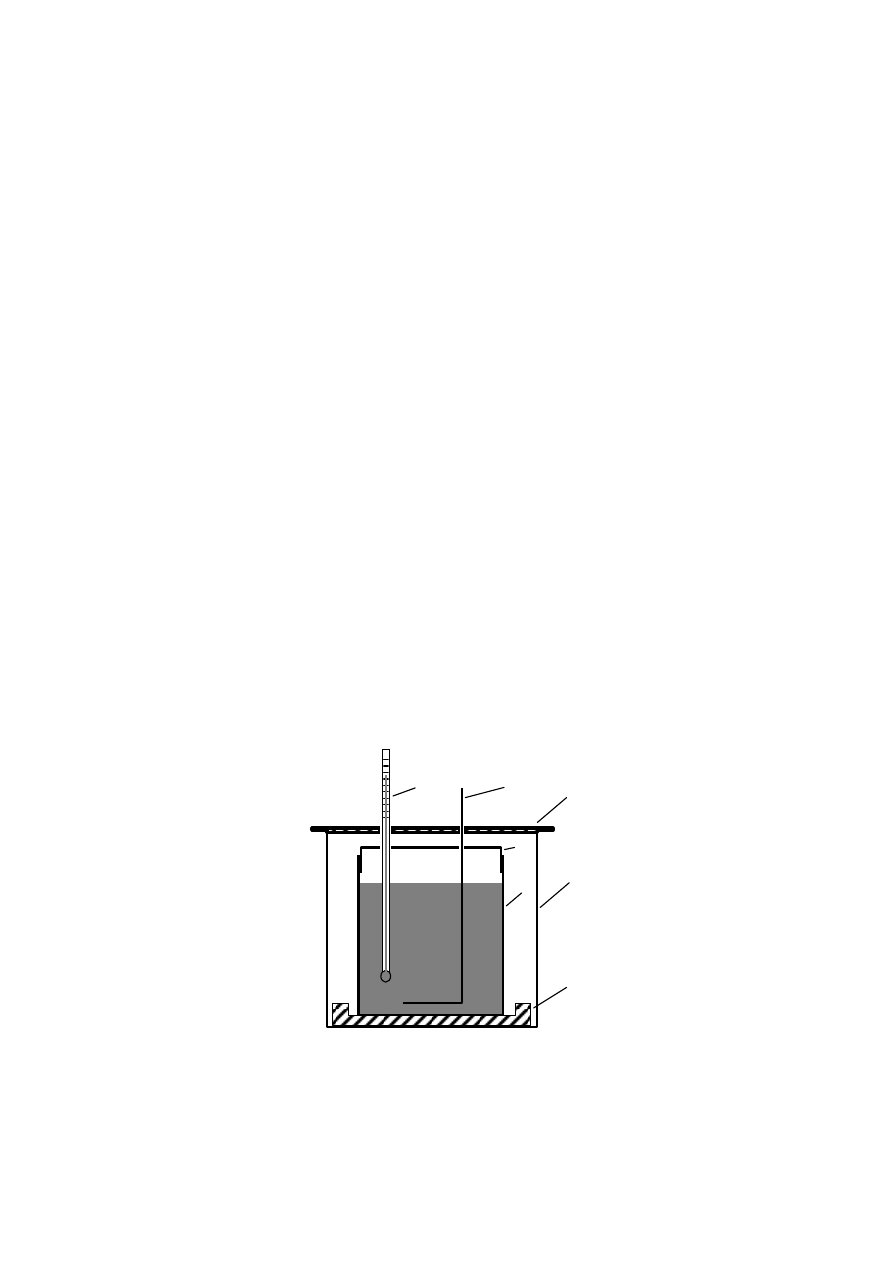
otoczenia. Najprostszy kalorymetr
składa się z dwóch naczyń aluminiowych: większego i
mniejszego. Na dnie naczynia większego - zewnętrznego
1
spoczywa drewniany krzyżak
2
,
na którym ustawione jest mniejsze naczynie wewnętrzne
3
– właściwy kalorymetr.
Kalorymetr ma aluminiową pokrywę
4
z otworami na termometr
5
i mieszadełko
6
.
Zewnętrzne naczynie przykryte jest płytką ebonitową
7
.
Rys. 11.1. Schemat kalorymetru wodnego
Wyznaczenie ciepła topnienia lodu
7
1
3
2
6
5
4
Wlewamy do kalorymetru o masie
k
m wodę o temperaturze około
C
40
. Ważymy
kalorymetr wraz z wodą i wyznaczamy masę wody
k
w
k
w
m
m
m
. Po zmierzeniu
początkowej temperatury
4
T kalorymetru i wody, wrzucamy lód o temperaturze
1
T . Na
skutek różnicy temperatur lód pobiera ciepło od wody i kalorymetru. Początkowo lód
ogrzewa się do temperatury
C
0
, topi się zamieniając w wodę o temperaturze
C
0
, która
następnie podgrzewa się do temperatury końcowej
3
T . Po całkowitym stopieniu się lodu
ważymy kalorymetr wraz z wodą i rozpuszczonym lodem w celu wyznaczenia masy lodu
w
k
l
w
k
l
m
m
m
. Równanie bilansu cieplnego dla tego przypadku ma postać:
5
4
3
2
1
Q
Q
Q
Q
Q
(11.1)
gdzie:
-
1
2
1
T
T
c
m
Q
l
l
– ciepło pobrane przez lód o masie
l
m na ogrzanie się od
temperatury początkowej
1
T do temperatury topnienia
C
0
2
T
,
-
L
m
Q
l
2
– ciepło pobrane przez lód o masie
l
m na stopienie się w
temperaturze
C
0
2
T
,
-
2
3
3
T
T
c
m
Q
w
l
– ciepło pobrane przez wodę powstałą z lodu o masie
l
m na
ogrzanie się od temperatury topnienia
C
0
2
T
do temperatury
końcowej
3
T ,
-
3
4
4
T
T
c
m
Q
w
w
– ciepło oddane przez wodę znajdującą się w kalorymetrze
podczas ochładzania się od temperatury początkowej
4
T do
temperatury końcowej
3
T ,
-
3
4
5
T
T
c
m
Q
k
k
– ciepło oddane przez kalorymetr podczas ochładzania się od
temperatury początkowej
4
T do temperatury końcowej
3
T .
W powyższych równaniach
l
c ,
w
c i
k
c oznaczają ciepło właściwe lodu, wody i kalorymetru
(aluminium),natomiast L jest poszukiwanym ciepłem topnienia lodu.
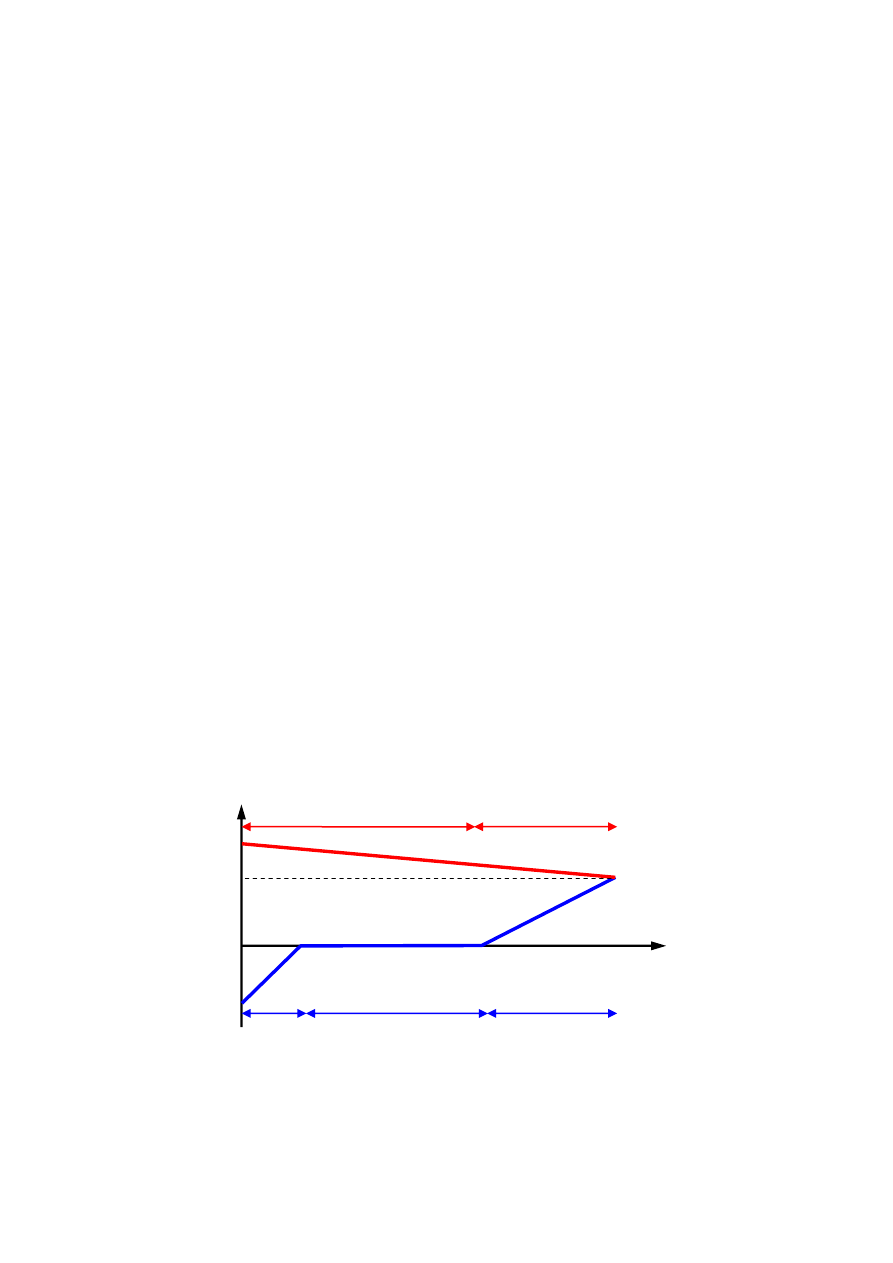
Rys. 11.2. Wykres bilansu cieplnego dla ciepła topnienia
Korzystając z równania bilansu cieplnego (11.1) możemy wyznaczyć ciepło topnienia lodu:
3
T
1
T
2
T
4
T
1
Q
2
Q
5
Q
3
Q
4
Q
Q
T
.
2
3
1
2
3
4
2
1
5
4
2
T
T
c
T
T
c
m
T
T
c
m
c
m
m
Q
Q
Q
Q
m
Q
L
w
l
l
k
k
w
w
l
l
(11.2)
Wyznaczenie ciepła parowania wody
Do naczynia nalewamy wodę do zaznaczonego poziomu i wyznaczamy łączną masę
naczynia z wodą. Umieszczamy w wodzie grzałkę i podłączamy ją do zasilania. Gdy woda
zacznie wrzeć włączamy stoper i dokonujemy pomiaru napięcia U oraz natężenie I prądu
przepływającego przez grzałkę. Po określonym czasie t wyłączamy zasilanie i wyjmujemy
grzałkę z naczynia. Ponownie ważymy naczynie z gorącą wodą, w celu wyznaczenia masy
wody
p
m która w trakcie procesu wrzenia zamieniła się w parę wodną. Należy pamiętać, że
nie cała energia cieplna grzałki zużywana jest na wyparowanie wody – część tej energii
zostaje oddana otoczeniu przez ścianki naczynia. Równanie bilansu cieplnego dla tego
przypadku ma postać:
g
o
w
Q
Q
Q
(11.3)
gdzie:
-
R
m
Q
p
w
– ciepło pobrane przez wodę o masie
p
m na przejście w stan gazowy
( R jest ciepłem parowania wody),
-
o
Q
– ciepło pobrane przez otoczenie w wyniku strat cieplnych na ściankach
naczynia,
-
UIt
Q
g
– ciepło oddane przez grzałkę.
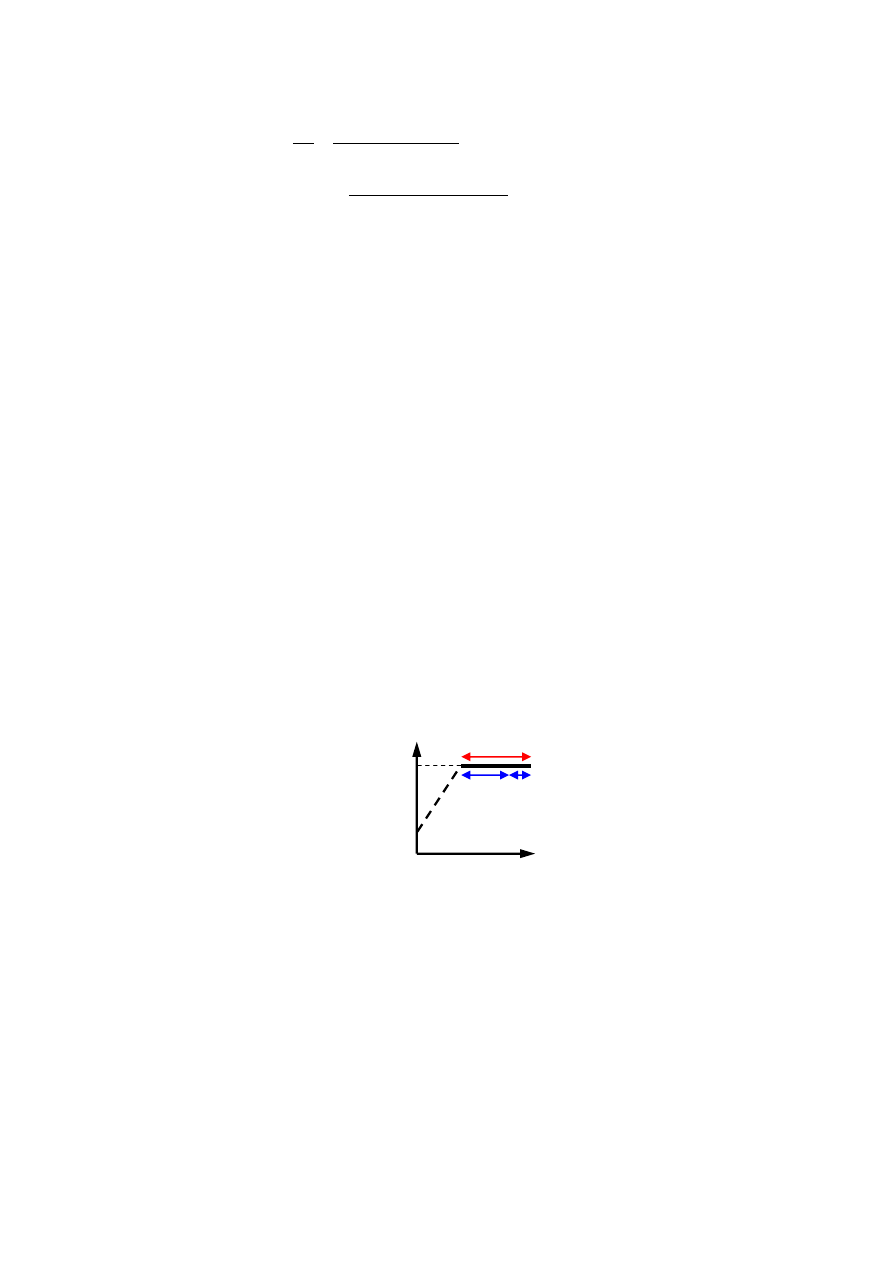
Rys. 11.3. Wykres bilansu cieplnego dla ciepła parowania
Aby wyznaczyć nieznaną wartość ciepła
o
Q wykonujemy ponownie doświadczenie,
ogrzewając wodę grzałką o mniejszej mocy przez taki sam czas
t . W obu przypadkach ciepło
o
Q będzie miało taką samą wartość ponieważ czas gotowania się wody i różnica temperatur
między naczyniem i otoczeniem są takie same. Ulegnie natomiast zmianie ciepło
w
Q (w obu
doświadczeniach wyparuje inna ilość wody) oraz ciepło
g
Q (zmienia się prąd płynący przez
grzałkę). Równanie bilansu cieplnego (11.3) dla pierwszego i drugiego pomiaru przyjmie
postać:
C
100
T
T
Q
w
Q
g
Q
o
Q

t
I
U
Q
R
m
o
p
1
1
1
,
t
I
U
Q
R
m
o
p
2
2
2
.
(11.4)
Przekształcając powyższy układ równań otrzymujemy wzór na ciepło parowania wody
2
1
2
2
1
1
p
p
m
m
t
I
U
I
U
R
(11.5)
oraz ciepło oddane przez naczynie do otoczenia
R
m
m
t
I
U
I
U
Q
p
p
o
2
1
2
2
1
1
2
1
.
(11.6)
W ćwiczeniu wyznaczmy dodatkowo wydajność obu grzałek w procesie wrzenia
UIt
R
m
p
.
(11.7)
Literatura:
1. Ćwiczenia laboratoryjne z fizyki. Cz. 1, praca zbiorowa pod red. J. Kirkiewicza, WSM,
Szczecin, 2001.
2. Szydłowski H., Pracownia fizyczna, PWN, Warszawa (dostępne wydania).
3. Ćwiczenia laboratoryjne z fizyki w politechnice, praca zbiorowa pod red. T. Rewaja,
PWN, Warszawa (dostępne wydania).
4. Ćwiczenia laboratoryjne z fizyki, praca zbiorowa pod red. T. Rewaja, Wydawnictwo
Politechniki Szczecińskiej, Szczecin (dostępne wydania).
5. Dryński T., Ćwiczenia laboratoryjne z fizyki, PWN, Warszawa (dostępne wydania).
6. Resnick R., Halliday D., Walker J., Podstawy fizyki T.2, PWN, Warszawa (dostępne
wydania).
7. Bobrowski C., Fizyka: krótki kurs, WNT, Warszawa (dostępne wydania).
8. Orear J., Fizyka T.1, WNT, Warszawa (dostępne wydania).
Wyszukiwarka
Podobne podstrony:
Ciepło topnienia i parowania - Sprawozdanie, Akademia Morska, I semestr, FIZYKA, Fizyka - Laboratori
Mech- Wyznaczanie ciepła topnienia lodu(1), Sprawozdania - Fizyka
Wyznaczanie ciepła topnienia lodu, Emilia Wieteska
spraw, 24, Wyznaczanie ciepla topnienia lodu
Mech- Wyznaczanie ciepła topnienia lodu, Sprawozdania - Fizyka
wyznaczanie ciepła topnienia lodu
fizyka, Ciepło topnienia lodu 2 (inne spr.), Temat ćwiczenia nr 32:Wyznaczanie ciepła topnienia lodu
Wyznaczanie ciepła topnienia lodu ćw nr 11, PWSZ Krosno budownictwo, Fizyka
WYZNACZANIE CIEPLA TOPNIENIA LODU, Sprawozdania
C1- Wyznaczanie ciepła topnienia lodu przy pomocy kalorymetru. sprawozdanie, Sprawozdania
Wyznaczanie ciepła topnienia lodu przy pomocy kalorymetru, Studia, Pracownie, I pracownia
Wyznaczanie ciepła topnienia lodu, topnienie lodu
C1 - Wyznaczanie ciepła topnienia lodu metoda kalorymetryczn, Sprawozdania
wyznaczanie ciepła topnienia lodu, Sprawozdania
wyznaczanie ciepla topnienia lodu, Budownictwo PG, Semestr 2, Fizyka, Laborki Fizyka, Laborki - chom
Wyznaczanie ciepła topnienia lodu, Sprawozdania - Fizyka
Wzyanczanie ciepła topnienia lodu przy pomocy kalorymetru, Studia, Pracownie, I pracownia, 27 Wyznac
więcej podobnych podstron