
ROZDZIELCZA CZASOWO DETEKCJA FOSFORESCENCJI
TLENU SINGLETOWEGO
Cel ćwiczenia:
a) Detekcja tlenu singletowego poprzez pomiar charakterystycznej fosforescencji przy
1268 nm.
b) Wyznaczenie stałej szybkości wygaszania tlenu singletowego przez
α-tokoferol
i
β-karoten.
c) Pomiar wydajności kwantowej generacji tlenu singletowego przez porfirynę.
Wprowadzenie
W
stanie
podstawowym
cząsteczka tlenu ma dwa elektrony na dwóch orbitalach
antywiążących л a ich spiny są równoległe.
Całkowity spin S cząsteczki tlenu wynosi zatem ½ + ½ = 1, a liczba poziomów energetycznych
(multipletowość) w zewnętrznym polu magnetycznym wynosi 2S + 1 = 3. Oznacza to, że tlen
w stanie podstawowym jest trypletem
3
O
2
(
3
Σ
g
-
). Większość związków organicznych, z którymi
tlen mógłby reagować w komórkach to związki w stanie singletowym: wszystkie elektrony ich
cząsteczek mają spiny sparowane i wypadkowy spin każdej cząsteczki tych związków równy jest
zeru. Aby cząsteczka tlenu w stanie trypletowym utleniła inną cząsteczkę i uległa
dwuelektronowej redukcji, musiałaby przyjąć od utlenianej cząsteczki dwa elektrony. Zgodnie
z prawami mechaniki kwantowej, oba te elektrony musiałyby mieć równoległe spiny,
antyrównoległe w stosunku do spinów dwóch niesparowanych elektronów na antywiążących
orbitalach л
x
* i л
y
*. Innymi słowy, wymaga to, by utleniana cząsteczka była również w stanie
trypletowym, bądź też by nastąpiło odwrócenie spinu jednego z elektronów takiej cząsteczki (co
jest procesem silnie wzbronionym). Dlatego też możliwości reakcji cząsteczki tlenu są
ograniczone; W reakcjach z wieloma cząsteczkami, które mogą ulegać utlenieniu, tlen jest
znacznie mniej reaktywny niż by to wynikało z termodynamiki tych procesów. Tlen
cząsteczkowy staje się o wiele bardziej reaktywny po wzbudzeniu elektronowym do stanu
singletowego (
1
∆
g
,
3
Σ
g
+
). Podwyższenie reaktywności tlenu w stanie singletowym wynika
zarówno ze zniesienia zakazu spinowego w reakcjach z cząsteczkami w stanie singletowym, jak
i z nadmiaru energii, którą cząsteczka tlenu singletowego, jako elektronowo wzbudzona posiada.
Poziomy energetyczne tlenu w stanie singletowym wynoszą 92,4 kJ/mol i 159,6 kJ/mol
odpowiednio dla
1
∆
g
i
3
Σ
g
+
powyżej stanu podstawowego.

W układach biologicznych tlen singletowy (
1
O
2
) może być produkowany w wyniku
reakcji kwasu podchlorawego z nadtlenkiem wodoru lub w reakcjach fotouczulanych
(fotosensybilizowanych). W przypadku reakcji fotosensybilizowanych tlen singletowy
generowany jest w procesie transferu energii ze stanu trypletowego wzbudzonej cząsteczki
fotouczulacza (
3
S) na tlen cząsteczkowy w stanie podstawowym (
3
O
2
):
S + h
ν →
1
S
→
3
S
3
S +
3
O
2
→ S +
1
O
2
W układach skondensowanych czas życia cząsteczki tlenu w stanie
1
∆
g
jest około 10
4
razy
dłuższy niż w stanie
3
Σ
g
+
. Dlatego w typowych reakcjach chemicznych z udziałem tlenu
singletowego znaczenie będzie miał przede wszystkim stan
1
∆
g
i do cząsteczki tlenu w tym
właśnie stanie odnosi się nazwa „tlen singletowy” (
1
O
2
). Tak długi czas życia we wzbudzonym
stanie singletowym (10
-6
- 10
-1
s w zależności od rozpuszczalnika) wynika z reguł wyboru dla
przejść elektronowych według których przejście
1
∆
g
→
3
Σ
g
-
jest silnie wzbronione nie tylko ze
względu na to, że jest to przejście międzysystemowe pomiędzy stanami o różnej multipletowości
(przejście singlet
→ tryplet) ale również ze względu na reguły wyboru dotyczące parzystości
i symetrii.
Dezaktywacja tlenu singletowego do stanu podstawowego zachodzi na drodze
promienistej
− fosforescencji oraz bezpromienistej − przejścia międzysystemowego
z wydzieleniem ciepła.
Fosforescencja
1
O
2
→
3
O
2
+ h
ν
k
R
[
1
O
2
]
Dezaktywacja bezpromienista
1
O
2
→
3
O
2
+ ciepło
k
NR
[
1
O
2
]
Naturalny czas życia
τ
∆
0
związany jest ze stałymi szybkości tych obu procesów:
τ
∆
0
= (k
R
+ k
NR
)
-1
Fosforescencja tlenu singletowego charakteryzuje się maksimami przy 1270 nm (przejście
na najniższy poziom oscylacyjny (0,0)) i 1580 nm (przejście na pierwszy wzbudzony poziom
oscylacyjny (0,1)). W większości rozpuszczalników dominują przejścia bezpromieniste a k
R
silnie zależy od rodzaju rozpuszczalnika a w szczególności od jego polarności. Woda należy do
rozpuszczalników, w których k
R
jest najniższe i tylko jedna cząsteczka
1
O
2
na milion ulega
dezaktywacji na drodze fosforescencji. Szybkość dezaktywacji na drodze bezpromienistej
również zależy od rodzaju rozpuszczalnika. W obecności ciężkich atomów wzrasta

prawdopodobieństwo przejścia interkombinacyjnego do stanu podstawowego. Najdłuższe czasy
życia
1
O
2
obserwuje się w rozpuszczalnikach zawierających atomy chlorowców, natomiast wraz
ze wzrostem liczby atomów wodoru w cząsteczkach rozpuszczalnika
τ
∆
0
ulega skróceniu.
Najkrótsze wartości
τ
∆
0
przyjmuje w roztworach zawierających grupy hydroksylowe. I tak,
w wodzie
τ
∆
0
przyjmuje najniższą wartość,
τ
∆
0
= 3,3
µs podczas gdy podstawienie atomów
wodoru deuterem powoduje wydłużenie tego czasu życia do około 60
µs, a w przypadku
rozpuszczalnika pozbawionego atomów wodoru czas życia
1
O
2
jest o kilka rzędów wielkości
większy, np. dla C
2
F
3
Cl
τ
∆
0
= 0,1 s.
Wydajność kwantowa generacji tlenu singletowego
Φ
1O2
w reakcjach fotouczulanych
zależy od wydajności kwantowej przejścia interkombinacyjnego fotosensybilizatora
Φ
isc
≡
Φ
T
oraz od efektywności transferu energii z cząsteczki fotosensybilizatora w stanie trypletowym na
cząsteczki tlenu w stanie podstawowym f
T
Σ
.
Φ
1O2
= f
T
Σ
Φ
isc
f
T
Σ
określa jaka część stanów trypletowych fotouczulacza ulega dezaktywacji na drodze transferu
energii wzbudzenia na cząsteczki tlenu i może być wyrażona jako stosunek szybkości tego
procesu k
T
Σ
[O
2
] do sumy szybkości wszystkich procesów prowadzących do dezaktywacji:
gdzie
τ
T
i
τ
T
0
oznaczają czasy życia stanu trypletowego odpowiednio w obecności i pod
nieobecność tlenu. Widać zatem, że
Φ
1O2
zależy nie tylko od własności samego fotouczulacza
(
Φ
isc
) ale również od lokalnego stężenia tlenu, naturalnego czasu życia trypletu oraz lepkości
ośrodka. Wydajność kwantowa generacji
1
O
2
osiąga górną granicę
Φ
1O2
=
Φ
isc
o ile w ośrodku
występuje wysokie stężenie tlenu, a stała szybkości k
T
Σ
przyjmuje odpowiednio duże wartości,
tak, żeby w czasie życia stanu trypletowego doszło do jego oddziaływania z tlenem. Jeśli czas
życia stanu trypletowego cząsteczki fotosensybilizatora
τ
T
0
jest krótki i znajduje się on w ośrodku
lepkim lub przy małej dostępności tlenu, wówczas generacja tlenu singletowego jest procesem
mało wydajnym.
W przypadku fotosensybilizatorów o wystarczająco długim czasie życia w stanie
singletowym (> 1 ns), tlen cząsteczkowy może wygaszać również stan singletowy na trzy
sposoby:
1) Dezaktywacja indukowana tlenem:
1
S +
3
O
2
→ S +
3
O
2
;
2) Indukowane tlenem przejście interkombinacyjne:
1
S +
3
O
2
→
3
S +
3
O
2
;
3) Transfer
energii:
1
S +
3
O
2
→
3
S +
1
O
2
.
f
k
O
k
k
k
O
k
O
k
O
k
O
T
T
P
isc
T
T T
T T
T T
T
Σ
Σ
Σ
Σ
Σ
Σ
=
+
+
=
=
+
[
]
[
]
[
]
[
]
[
]
3
2
3
2
3
2
0
3
2
0
3
2
1
τ
τ
τ

O ile dezaktywacja indukowana tlenem zazwyczaj nie ma większego znaczenia,
oddziaływanie tlenu ze wzbudzonymi stanami singletowymi sensybilizatora prowadzi do
zwiększenia
Φ
1O2
poprzez: 1) zwiększenie prawdopodobieństwa przejścia interkombinacyjnego
(a zatem zwiększa się populacja cząsteczek fotosensybilizatora w stanie trypletowym), 2) transfer
energii (jeśli tylko przerwa energetyczna pomiędzy wzbudzonym stanem singletowym
i trypletowym cząsteczki fotosensybilizatora jest większa niż 94,6 kJ/mol, czyli niż energia
wzbudzenia tlenu w stanie
1
∆
g
). W wyniku transferu energii generowany jest tlen singletowy oraz
stan trypletowy fotosensybilizatora, który może przekazać swoja energię wzbudzenia na następną
cząsteczkę tlenu, a zatem pochłonięcie pojedynczego fotonu może spowodować generację
dwóch cząsteczek
1
O
2
. Gdy w układzie zachodzi wygaszanie stanów singletowych przez tlen,
wówczas
Φ
1O2
zależy w sposób złożony od stężenia tlenu i może osiągać graniczną wartość
równą 2. Analogicznie jak w przypadku wygaszania stanów trypletowych fotouczulacza można
wprowadzić parametr f
S
Σ
. Ze względu na znacznie krótsze czasy życia stanów singletowych niż
trypletowych, w większości przypadków f
S
Σ
jest znacznie mniejsze niż 1.
Opis metody i jej wybranych zastosowań
Rozdzielcza czasowo detekcja fosforescencji tlenu singletowego w podczerwieni
stosowana jest w celu monitorowania fotosensybilizowanej generacji
1
O
2
oraz jego zaniku.
Ideowy schemat układu do monitorowania fosforescencji próbki po impulsie lasera
przedstawiony jest na Rys. 1. Próbka zawierająca fotouczulacz oraz tlen w znanym stężeniu
znajduje się w kuwecie fluorescencyjnej. Detektor germanowy ustawiony jest pod kątem 90
°
w
stosunku do wiązki wzbudzającego promieniowania laserowego. Pomiędzy próbką
a powierzchnią czynną detektora znajdują się odpowiednie filtry mające za zadanie
zminimalizować rozproszone promieniowanie lasera lub fluorescencję próbki. I tak, filtr
krzemowy absorbuje promieniowanie poniżej 1100 nm, natomiast filtr interferencyjny
przepuszcza wąski zakres spektralny promieniowania z maksimum transmisji przy 1270 nm.
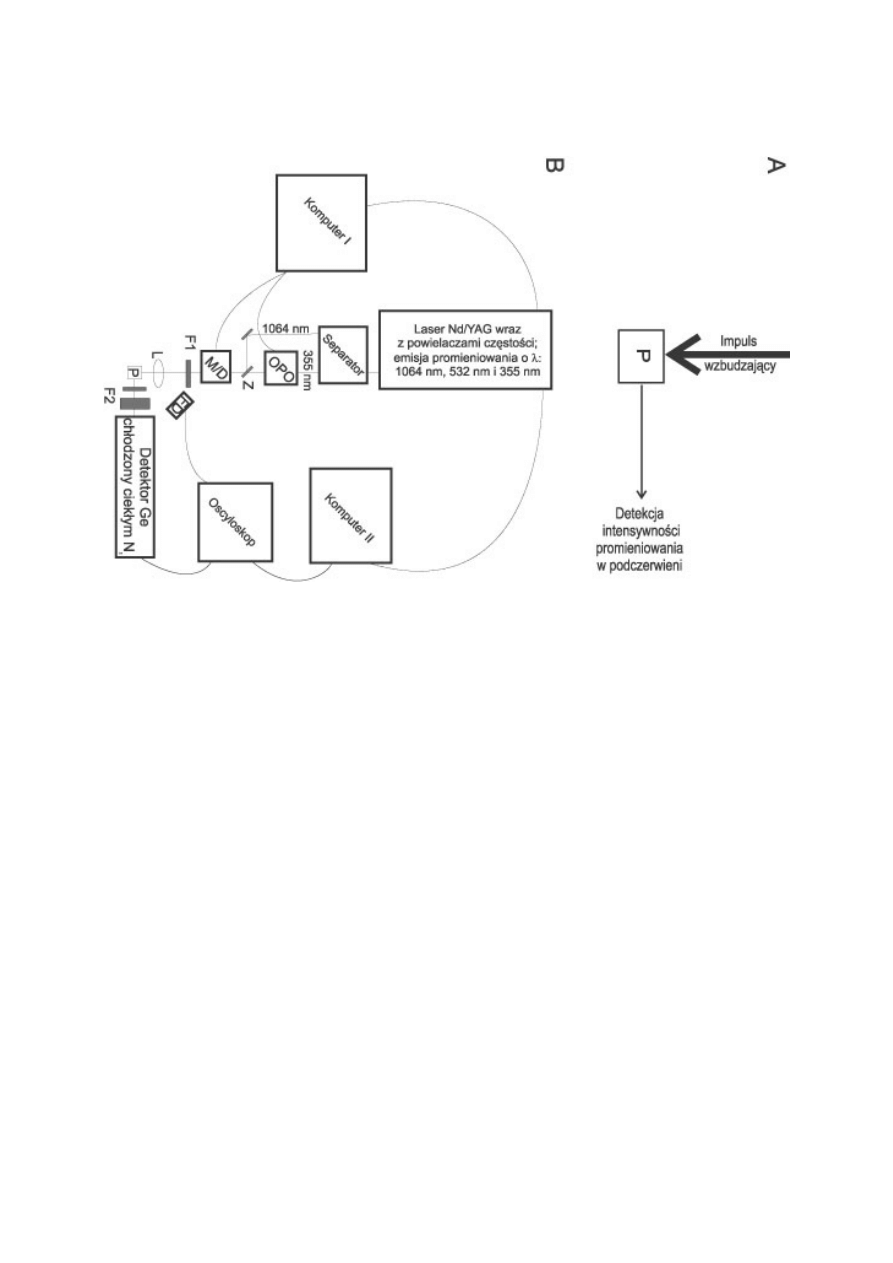
Rys. 1. Schemat ideowy (A) oraz uproszczony schemat układu pomiarowego (B) do rozdzielczej czasowo detekcji
charakterystycznej fosforescencji
1
O
2
przy 1270 nm. P – kuweta fluorescencyjna z próbką; OPO – optyczny
oscylator parametryczny; ; Z- zwierciadła dichroiczne; M/D – mieszacz/podwajacz częstości; FD – fotodioda; F1 –
filtr szary do regulacji energii promieniowania i/lub filtr pochłaniający promieniowanie o niepożądanej długości fali;
L – soczewki formujące wiązkę lasera; F2 – filtr krzemowy obcinający promieniowanie o
λ< 1100 nm oraz filtr
interferencyjny z maksimum transmisji przy 1270 nm.
Czas życia tlenu singletowego
τ
w danym rozpuszczalniku można wyznaczyć z analizy
kinetyki zaniku intensywności fosforescencji w czasie. W tym celu do danych doświadczalnych
dopasowuje się krzywą eksponencjalną:
I(t) = I
0
exp(-kt)
gdzie I
0
jest początkową intensywnością fosforescencji ekstrapolowaną do czasu zakończenia
błysku lasera, natomiast k =
τ
-1
jest stałą szybkości zaniku intensywności fosforescencji.
W warunkach gdy w próbce znajduje się dodatkowo substrat Q, reagujący z
1
O
2
na drodze
reakcji chemicznej lub wygaszania fizycznego, wówczas pomiar obserwowanej szybkości zaniku
fosforescencji (k) w zależności od stężenia substratu pozwala na wyznaczenie
stałej szybkości
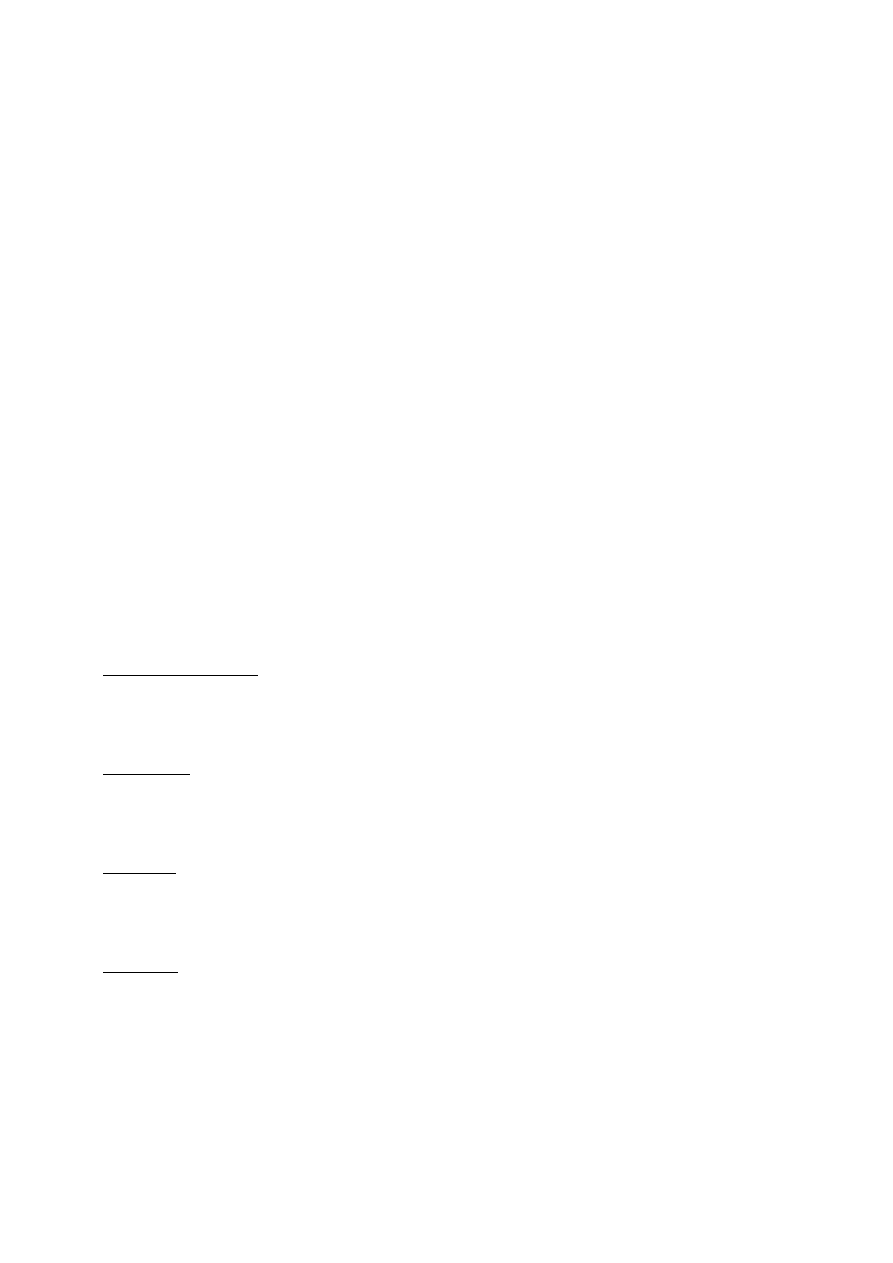
gaszenia k
Q
będącej sumą stałych szybkości wszystkich oddziaływań substratu z
1
O
2
natury
zarówno chemicznej jak i fizycznej:
k([Q]) =
τ
-1
+ k
Q
[Q]
Wydajność kwantową generacji tlenu singletowego
Φ
1O2
przez badany związek można
wyznaczyć metodą porównawczą przy pomocy detekcji fosforescencji
1
O
2
. W tym celu stosuje
się standard - fotosensybilizator o znanej
Φ
1O2
w stężeniu odpowiadającym identycznej
absorbancji przy długości fali impulsu wzbudzającego jak próbka ze związkiem o nieznanej
Φ
1O2
. W ten sposób zapewnia się warunki, w których liczba fotonów pochłoniętych przez
obydwie próbki będzie identyczna. Aby wyznaczyć
Φ
1O2
przeprowadza się pomiar początkowych
intensywności fosforescencji I
0
dla obu próbek przy różnych energiach impulsu wzbudzającego.
Jest to konieczne gdyż w przypadku gdy generowane jest odpowiednio duże stężenie stanów
trypletowych w próbce będą one ulegać dezaktywacji w wyniku oddziaływania tryplet-tryplet, a
co za tym idzie ich czas życia będzie krótszy i mniejsze prawdopodobieństwo transferu energii na
cząsteczkę tlenu. Co więcej, przy większych energiach impulsów może dochodzić do procesów
dwufotonowych. Do obliczeń bierze się pod uwagę jedynie te początkowe intensywności
fosforescencji I
0
, które w sposób liniowy rosną wraz ze wzrostem energii lasera. Stosunek
nachyleń obu prostych jest równy stosunkowi wydajności kwantowych obu próbek.
Wykonanie ćwiczenia
1.
Pomiar stałej szybkości wygaszania tlenu singletowego przez
β
-karoten i
α
-tokoferol
Odczynniki:
Roztwory wyjściowe tetra-fenylo-porfiryny,
α-tokoferolu (c
TOC
= 5
×10
-3
M) i
β-karotenu (c
CAR
=
5
×10
-5
M) w benzenie.
Materiały:
Kwarcowe kuwety spektrofotometryczne i fluorescencyjne
Pipety i końcówki
Aparatura:
Spektrofotometr diodowy
Układ do detekcji rozdzielczej-czasowo fosforescencji przy 1270 nm
a) Zmierz widma absorpcji roztworów porfiryny,
α-tokoferolu i β-karotenu w benzenie.
b) Wybierz długość fali promieniowania wzbudzającego tak aby absorbancja porfiryny przy tej
długości fali mieściła się w zakresie 0,05-0,20, natomiast wkład absorpcji wygaszaczy był
możliwie najmniejszy.
Długośc fali promieniowania wzbudzającego:
λ
ex
= ......... nm
Absorbancja porfiryny przy
λ
ex
w 1 cm kuwecie:
A = ............
Początkowa objętość
próbki:
V
0
= ..............
µl
c) Zmierz kinetykę powstawania i zaniku luminescencji emitowanej przez próbkę po impulsie
lasera. Dopasuj do punktów pomiarowych zaniku intensywności emisji I w czasie t krzywą
eksponencjalną:
I(t) = I
0
exp(-kt)
d) Dodaj do próbki
α-tokoferol (np. 1% objętości V
0
) i powtórz krok c).
e) Powtarzaj pomiary zwiększając za każdym razem stężenie
α-tokoferolu dopóki nie
zaobserwujesz wyraźnego skrócenia czasu życia fosforescencji
1
O
2
.
f) Powtórz kroki c-e stosując jako wygaszacz
β-karoten.
Szybkość zaniku fosforescencji
k (s
-1
)
∆
V
Q
(
µl)
V
Q
(
µl)
Q
≡ α-tokoferol
Q
≡ β-karoten
∆
V
Q
– dodana objętość roztworu wygaszacza do próbki
V
Q
– całkowita objętość roztworu wygaszacza w próbce

g) Wyznacz stężenie wygaszaczy w poszczególnych próbkach:
h) Narysuj wykresy przedstawiające zależność stałej szybkości zaniku
1
O
2
k od stężenia
wygaszaczy
[Q]. Do punktów pomiarowych dopasuj prostą i wyznacz nieznane paramtery:
τ
-
naturalny czas życia tlenu singletowego w benzenie; k
Q
- stałą szybkości oddziaływania tlenu
singletowego z wygaszaczem Q.
k ([Q])=
τ
-1
+ k
Q
[Q]
2. Wyznaczanie wydajności kwantowej generacji tlenu singletowego metodą pośrednią.
Odczynniki:
Roztwory wyjściowe tetra-fenylo-porfiryny (TPP) stosowanej jako standard oraz wybranej
pochodnej porfiryny (PORF) o nieznanej
Φ
1O2
.
Materiały:
Kwarcowe kuwety fluorescencyjne
Pipety i końcówki
Zestaw filtrów szarych wraz z widmami transmisji i danymi liczbowymi
Aparatura:
Spektrofotometr diodowy
Układ do detekcji rozdzielczej-czasowo fosforescencji przy 1270 nm
a) Zmierz widma absorpcji próbek TPP oraz PORF. Dobierz długość fali promieniowania
wzbudzającego
λ
ex
w ten sposób by absorbancja przy
λ
ex
była jednakowa dla obu próbek i
mieściła się w zakresie 0,05 - 0,10 (jeśli to konieczne rozcieńcz próbki).
Długość fali promieniowania wzbudzającego:
λ
ex
= .......... nm
Absorbancja przy
λ
ex
w 1 cm kuwecie:
A = ............
b) Wybierz zestaw 6-10 filtrów pozwalający zmieniać natężenie promieniowania
wzbudzającego w zakresie od kilku do 90% dla wybranej
λ
ex
.
c) Zbierz kinetyki zaniku fosforescencji emitowanej przez próbki po impulsie lasera przy
różnych energiach impulsu wzbudzajacego dla obu próbek.
d) Dla wszystkich zmierzonych kinetyk dopasuj do punktów pomiarowych zaniku
intensywności emisji I w czasie t krzywą eksponencjalną:
[ ]
Q
c V
V
V
Q Q
Q
=
+
0
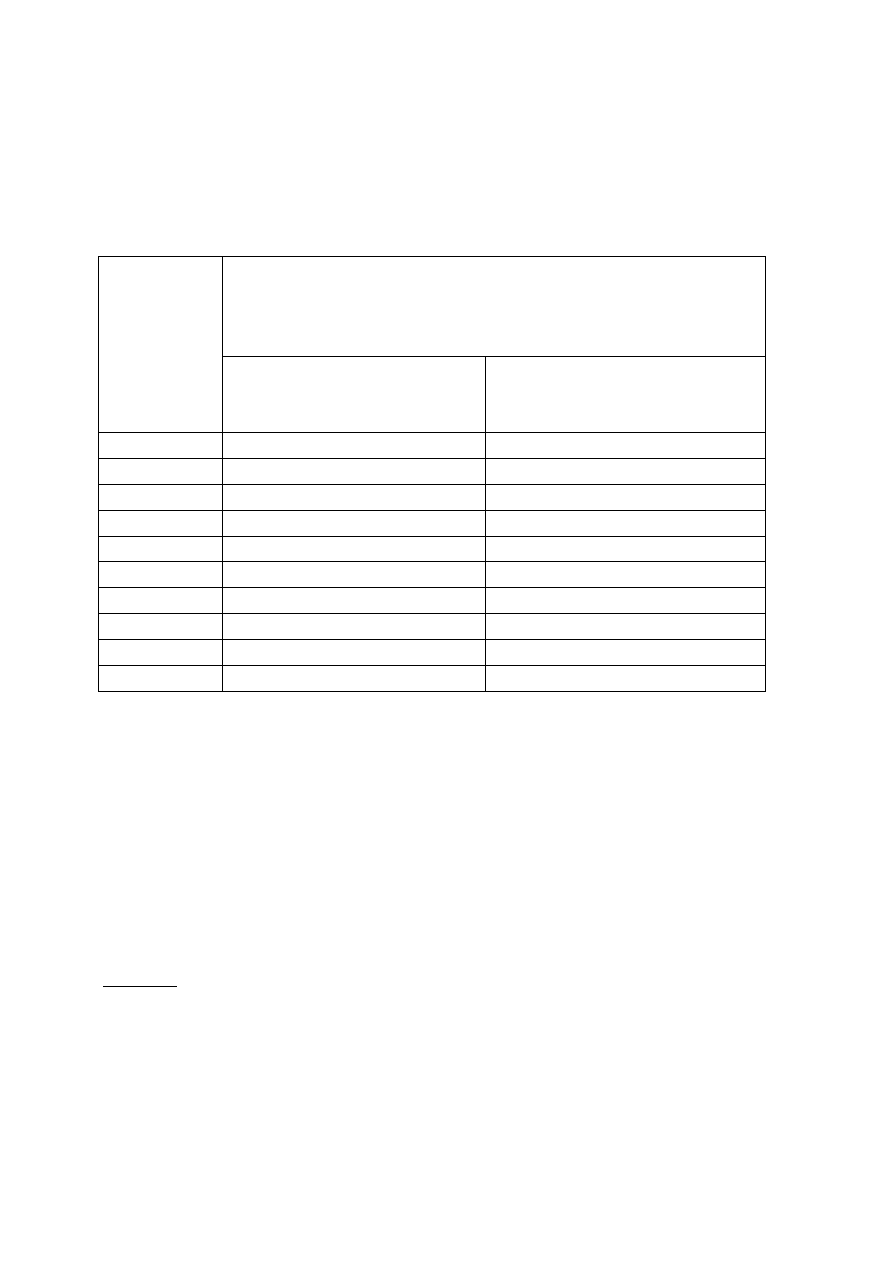
I(t) = I
0
exp(-kt)
i wyznacz początkową wartość intensywności fosforescencji I
0
ekstrapolując krzywą
eksponencjalną do czasu zakończenia błysku lasera. Wyniki wpisz do tabelki.
Początkowa intensywność fosforescencji I
0
(V)
Energia
lasera
(%)
TPP
PORF
e) Narysuj wykres zależności I
0
od energii impulsu wzbudzającego E(%) dla TPP i PORF. W
obszarze liniowego wzrostu I
0
(E) dopasuj do puntków doświadczalnych proste i wyznacz
współczynniki ich nachylenia a
TPP
i a
PORF
. Oblicz wydajność kwantową generacji tlenu
singletowego przez PORF korzystając ze związku:
Φ
PORF
=
Φ
TPP
×
a
PORF
/a
TPP
gdzie
Φ
TPP
= 0,63 w benzenie w równowadze z powietrzem (Bonnett et al., Photochem.
Photobiol. 48: 271-276, 1988).
Literatura:
Paszyc, S.: "Podstawy fotochemii", PWN, Warszawa, 1992.
Sarna, T.: Udział tlenu singletowego i wolnych rodników w reakcjach fotouczulanych
i zjawiskach fotodynamicznych. Zagadnienia Biofizyki Współczesnej 14(1): 5-30, 1989.
Bartosz, G.: "Druga twarz tlenu" PWN, Warszawa, 1995.
Wyszukiwarka
Podobne podstrony:
24 piątek
24(45)RUP
ostre białaczki 24 11 2008 (kurs)
ZPSBN T 24 ON poprawiony
24 NIEDZIELA ZWYKŁA A
Wykład 24
4 wykład0 24 10 2007
Atrybucje 23 24
od 24 do 32
24 G23 H19 QUALITY ASSURANCE OF BLOOD COMPONENTS popr
4 JM02 JS05 24 29 złamania
24 gold & 20's
mspo 24 2
24 Wykonywanie prac z zakresu obróbki ręcznej
2015 08 20 08 19 24 01
więcej podobnych podstron