
1
PODSTAWY ROBOTYKI
JW 14.3.1
Roboty medyczne
Zastosowanie robotyki w
medycynie

2
Wypunktowanie głównych podtematów
1. Wprowadzenie do tematu
Krótkie omówienie założeń medycyny
Przedstawienie definicji robota
Pogrupowanie dziedzin medycyny, w których może być stosowana
robotyka
2. Operacje chirurgiczne
Omówienie przebiegu operacji chirurgicznych
Wyjaśnienie pojęcia zabiegu małoinwazyjnego
Wprowadzenie robotów chirurgicznych
Operacja serca
Przedstawienie systemu chirurgicznego DaVinci, a także RobIn Heart
Operacje na odległość
System nawigacji HipNav
3. Robot symulujący żucie
Badania nad mechanizmem żucia
Przedstawienie robota-szczęki
4. Nanotechnologie (Nanoroboty)
Krótkie wprowadzenie do tematu
„Inteligentny” lek
Przedstawienie przykładowej budowy nanorobota i jego podsystemów

3
1. Wprowadzenie do tematu
1.1. Czym jest medycyna
To nauka o zdrowiu i chorobie człowieka, umiejętność (sztuka) zapobiegania chorobom
i leczenia chorych. Medycyna zajmuje się rozpoznawaniem chorób, a następnie leczeniem ich
poprzez różnego rodzaju zabiegi i operacje. Medycyna szuka coraz to nowych narzędzi oraz
technik operacji i leczenia pacjentów.
1.2. Definicja robota
Urządzenie techniczne przeznaczone do realizacji niektórych czynności
manipulacyjnych i lokomocyjnych człowieka, określonych na poziomie energetycznym,
informacyjnym i inteligencji maszyn (autonomii działania w pewnym środowisku). Roboty
projektuje się z myślą współpracy i pomocy człowiekowi w wielu dziedzinach życia.
1.3. Robotyka w medycynie
¾ Roboty operacyjne (operacje i zabiegi przy pomocy robotów)
¾ nanotechnologie (nanoroboty)
¾ roboty symulacyjne
¾ protezy
¾ sztuczne narządy
¾ robopersonel medyczny
2. Operacje chirurgiczne
Operacje chirurgiczne kojarzą się z rozcinaniem ciała, łamaniem żeber, bliznami i
bólem. W czasie zabiegu chirurg wycina chorobowo zmienione tkanki, usuwa nieprawidłowe
elementy, a potem zespala to, co zostało po drodze rozcięte lub rozerwane. Na szczęście co
roku wzrasta liczba zabiegów wykonywanych tzw. techniką mało inwazyjną (laparoskopia).
Chodzi o to, żeby nie niszczyć tkanek sąsiednich poprzez szukanie wygodnego „dojścia”.
Takie operacje wymagają wykonania tylko trzech-czterech niewielkich (ok. 1 cm) otworów w
skórze. Nacięcia w czasie zabiegu są zabezpieczone przez specjalne tulejki, przez które do
wnętrza ciała pacjenta wprowadzane są narzędzia chirurgiczne i kamery.
Jednakże technika laparoskopowa mało inwazyjna nie jest zbytnio precyzyjna i jest
mało wygodna dla chirurga. Długie ramiona wzmacniają drgania dłoni operatora i likwidują
naturalne wrażenie dotyku. Do tego zamiast na pole operacyjne trzeba patrzeć na
umieszczony z boku monitor, na który kamera przekazuje obraz z wnętrza ciała. Wszystko po
to, by pacjenta mniej bolało, by mógł szybciej wrócić do domu i by tylko niewielkie blizny
przypominały o małym „remoncie”, który przeszedł w szpitalu. Wprowadzenie robota między
dłoń chirurga a końcówkę narzędzia znacznie zwiększa dokładność i sprawność.
2.1. Operacje przy współpracy z robotem
Jeżeli wyposażymy robota w „inteligentny” program, usunie on drżenie ludzkiej dłoni
czy przeskaluje ruch tak, że kilkucentymetrowe przesunięcie ręki człowieka spowoduje ruch
końcówki narzędzia o kilka milimetrów. Każdy ruch chirurga jest analizowany przez
komputer, który odpowiednio filtruje sygnał sterujący. Założenie specjalnych okularów lub
korzystanie z konsoli stereowizyjnej umożliwia trójwymiarowy widok pola operacyjnego

4
2.2. Operacja serca
Operacja serca rozpoczyna się od otwarcia klatki piersiowej. Chirurdzy rozcinają
mostek, odciągają żebra, a następnie przecinają mięśnie, aż do odsłonięcia serca. Dopiero
wtedy zaczyna się prawdziwa operacja (po tylu cięciach). W przypadku takich operacji jak
usunięcie pęcherzyka żółciowego, operacje ginekologiczne oraz operacje w obszarze klatki
piersiowej, chirurdzy coraz częściej zamiast wszystko rozcinać wprowadzają do wnętrza ciała
miniaturowe instrumenty, przez niewielkie nacięcia.
Jednak w przypadku mikrochirurgii otwory te okazują się zbyt małe. Chyba, że te
otwory mogą posłużyć do wprowadzania bardzo stabilnej, cienkiej jak ołówek końcówki
robotycznej, którą manipuluje doświadczony kardiochirurg.
Różne firmy współzawodniczą o status dostawcy minimalnie inwazyjnych urządzeń
robotycznych oraz technik przeznaczonych do chirurgii serca. W jednym z takich systemów
(system Da Vinci) przez małe nacięcia (3 okienka w ciele pacjenta) w klatce piersiowej
pacjenta chirurdzy wprowadzają trzy zdalnie sterowane metalowe sondy wielkości palca –
niewielkie narzędzia chirurgiczne, źródło światła i kamerę światłowodową.
2.3. System chirurgiczny Da Vinci
Siedzący za konsolą sterowniczą chirurg ma przed sobą trójwymiarowy obraz pola
operacyjnego. Posługując się specjalnym joystickiem, chirurg porusza ramieniem robota,
które steruje miniaturowymi narzędziami chirurgicznymi. Narzędzia te zmontowane są na
„palcu” robota, który dzięki elastycznemu mechanicznemu nadgarstkowi potrafi wykonywać
niezwykle precyzyjne ruchy – jest to umiejętność ważna przy operacji wszczepiania by-
passów, wymagającej przecięcia i zszycia delikatnych naczyń krwionośnych na powierzchni
serca.
2.4. Robotyczne narzędzia chirurgiczne
Lekarze wprowadzają instrumenty robotyczne przez małe „okienka” w ciele pacjenta. Każdy
„robotyczny skalpel” ma opatentowany mechanizm EndoWrist, który pozwala mu się
poruszać z precyzją i zręcznością ludzkiej ręki, a nawet dokładniej ponieważ drżenie ludzkiej
ręki jest eliminowane przez specjalne filtry.
Rys.1

5
System Da Vinci ma 6 stopni swobody ruchu końcówki przyrządu(robota), co pozwala
na naturalne przekazywanie ruchów rąk na narzędzie chirurgiczne. Tradycyjne przyrządy
endoskopowe posiadają tylko 4 stopnie swobody.
Pierwsza zdalnie sterowana operacja wszczepienia bypassów (na pracującym sercu)
odbyła się w USA w sierpniu 1999 roku. W systemie tym można również symulować
operacje chirurgiczne, co na pewno znacznie ułatwi szkolenie chirurgów. Wadą systemu jest
brak dotykowego sprzężenia zwrotnego. Naukowcy pracują nad uzupełnieniem zestawu
zmysłów robota o dotyk – dzięki temu operujący chirurg mógłby wyczuć różnicę pomiędzy
kością a tkanką mięśniową czy tłuszczową albo pulsujące naczynia krwionośne.
2.5. Ćwiczenia na zwłokach
Obrazy otrzymuje się z dwóch małych kamer umieszczonych w jednym z trzech małych
„okienek” wyciętych w zwłokach. Pozostałe okienka służą do wprowadzania robotycznych
narzędzi chirurgicznych.
Rys.2
2.6. Opis techniczny robota
Nazwa:
System chirurgiczny da Vinci
Pochodzenie nazwy:
Leonardo da Vinci (uczony – artysta)
Cel budowy:
Bardziej precyzyjne i mniej inwazyjne wykonywanie operacji chirurgicznych
Układ wizyjny:
stereowizja
Komputery:
własna konstrukcja oparta na czterech procesorach Shark
Status przedsięwzięcia:
zakończone
Cena systemu wynosi ok. 1 miliona Euro.
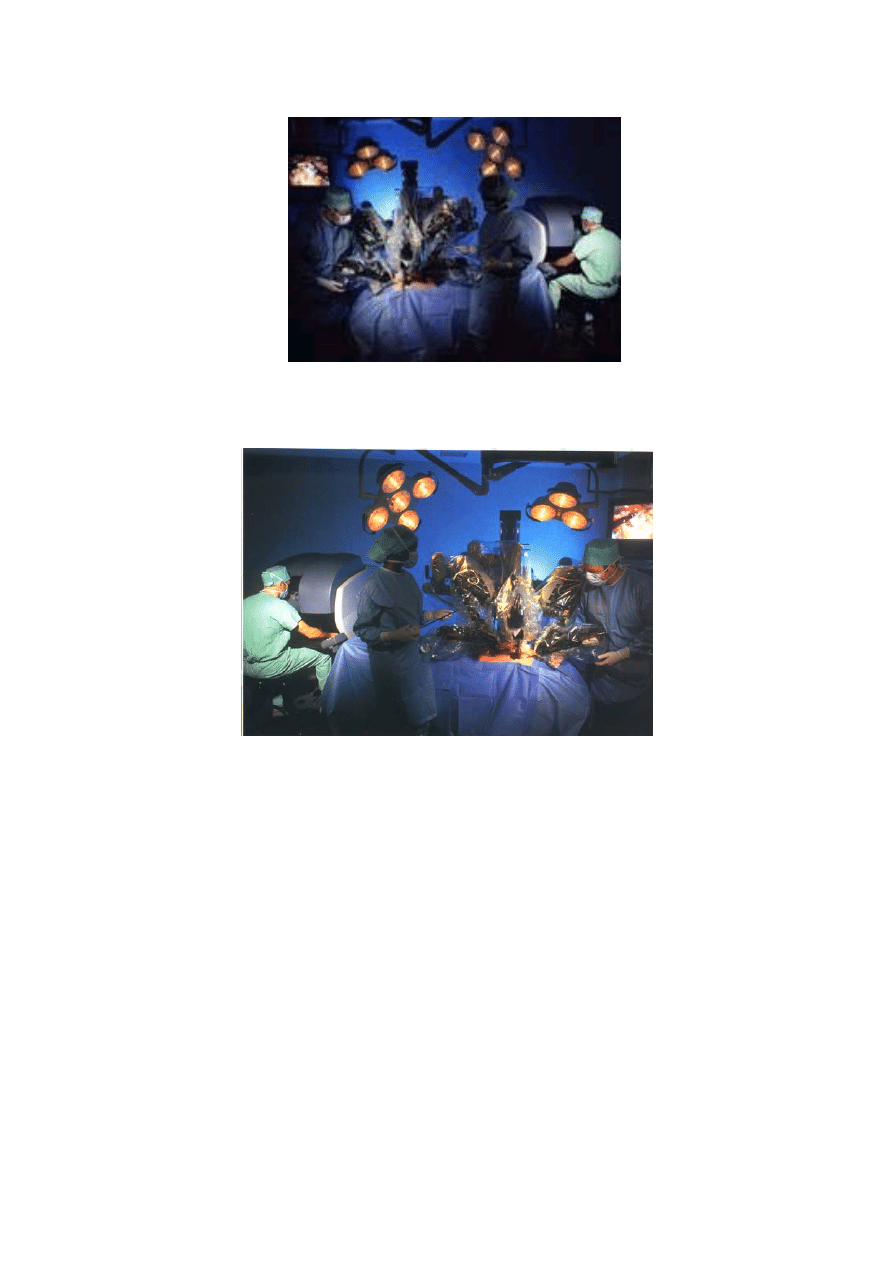
6
Rys. 3. Da Vinci w trakcie operacji wszczepiania bypassów;
operacja na bijącym sercu
Rys.4
2.7. Polski system chirurgiczny RobIn Heart
Na pomysł wykorzystania robotów w medycynie wpadli inżynierowie z NASA. Co by
się stało, gdyby podczas podróży na Marsa trzeba było operować członka załogi? Szybko i
bezbłędnie? Jedynym wyjściem jest robot, który precyzyjnie wykona polecenia chirurga
oddalonego o tysiące kilometrów.
W 1994 r. narodził się Ezop - metalowe ramię zaprojektowane na wzór ludzkiego. Ezop
spełnia funkcję asystenta chirurga. Jest niezwykle przydatny podczas operacji
małoinwazyjnych. Podtrzymuje endoskop, potrafi zapamiętać 23 komendy głosowe i obce są
mu ludzkie ułomności. Może stać przy stole operacyjnym godzinami i ramię mu nawet nie
drgnie. Dzięki Ezopowi chirurgom wystarczają coraz mniejsze cięcia – tylko takie, by
wprowadzić do wnętrza ciała pacjenta kamerę i narzędzia. W sumie Ezop uczestniczył w
ponad 60 tys. operacji małoinwazyjnych przeprowadzonych w 400 szpitalach na całym
świecie. Jeden z egzemplarzy pracuje w klinice w Ochojcu. W 1999 r. inżynierowie zrobili
krok dalej i skonstruowali Zeusa - robota nowej generacji. Dzięki niemu chirurg może

7
zoperować serce bez rozcinania klatki piersiowej. Teraz, w obecnych latach, naukowcy
skupiają się na doskonaleniu projektu RobIn Heart.
Ruchy chirurga przy pulpicie komputera są przekładane przez interfejs na precyzyjne
manipulacje końcówek robota w okolicy naczyń wieńcowych serca. RobIn Heart 1 ma
ramiona osadzone na niezależnej podstawie.
Rys. 5
Rys. 6

8
Tzw. port narzędzi (otwór w powłokach ciała) umiejscowiony jest między żebrami tak,
by umożliwić dostęp do ściany serca, gdzie będzie wykonany np. by-pass. Widoczny na
zdjęciu jest RobIn 2.
Rys.7
Rys. 7
Polski RobIn Heart jest jednym z niewielu projektów mogących konkurować z
amerykańskimi, a przy tym w pełni oryginalnym. Operując serce „przez dziurkę od klucza”,
można poruszać narzędziami robota tylko w niewielkiej przestrzeni uzyskanej dzięki
pompowaniu do klatki piersiowej dwutlenku węgla i wykorzystaniu narzędzi rozciągających.
Dlatego szczególną wagę przywiązuje się do ruchliwości końcówek. Końcówka ta ma 1 cm
długości i dwa przeguby, tzw. łokieć i nadgarstek, napędzane przez minisilniki i sterowane za
pośrednictwem linek schowanych w rurce o średnicy 8 mm. Ponieważ przy każdej operacji
trzeba używać wielu różnych końcówek opracowano nową końcówkę – wielofunkcyjną jak
scyzoryk.
W dalszym ciągu prowadzone są prace nad inteligentną bazą danych - tak, aby lekarz-
operator mógł w każdej chwili wykorzystać program doradczy systemu RobIn Heart. Podczas
operacji mógłby przywołać głosem na ekran dane z historii choroby pacjenta, obrazy
diagnostyczne. Marzeniem twórców RobIna jest uruchomienie - po pomyślnym przejściu
testów klinicznych - produkcji polskiego robota kardiochirurgicznego i wyposażenie weń
wszystkich dużych klinik operujących serce. RobIn Heart 3, łączący najlepsze rozwiązania
dotychczasowych prototypów, mógłby stanąć koło chirurga na salach operacyjnych już za
trzy lata. Pokrzyżować te plany może jedynie brak środków na dokończenie badań; i to
właśnie jest największy problem stojący dziś przed zespołem dr. Nawrata.
9
2.8. Inne roboty chirurgiczne
W przypadku operacji kręgosłupa dokładność liczy się w dziesiętych częściach
milimetra, a jeden fałszywy ruch może doprowadzić do uszkodzenia rdzenia kręgowego i
paraliżu pacjenta. Jednak leczenie chirurgiczne bywa jedynym wyjściem w przypadku
nowotworów rdzenia, wypadnięcia dysku czy uszkodzenia kręgu. Opracowany przez
niemieckich specjalistów z Instytutu Fraunhofera robot ma zapewnić większe bezpieczeństwo
i dokładność, umożliwiając na przykład wkręcanie z wielką dokładnością śrub, na których
opierają się pręty stabilizujące kręgosłup. Szczególnie obiecująco wygląda perspektywa
użycia robota w operacjach kręgosłupa szyjnego – niektórych zabiegów ze względu na ryzyko
nie da się przeprowadzić w sposób tradycyjny.
W chirurgii mózgu rzecz ma się podobnie: można stworzyć komputerowy model,
przećwiczyć na nim operację i tak zaprogramować robota, by ją przeprowadził jak najmniej
uszkadzając zdrową tkankę. Ale mózg jest miękki – miejscowy obrzęk czy krwawienie może
przemieścić poszczególne struktury, a wtedy nieostrożny manewr mógłby uszkodzić ważny
obszar lub rozerwać naczynie krwionośne. Aby temu zapobiec, w NASA opracowano
specjalną sondę Smart Probe, która wykorzystując dane dostarczane przez spektroskopię
optyczną, ultradźwięki i endoskop określa rodzaj napotkanej tkanki i podpowiada
najbezpieczniejszą strategię postępowania. Taki robot może znaleźć zastosowanie również w
operowaniu raka piersi czy prostaty.
2.9. Operacje na odległość
Prof. Jacques Marescaux i jego asystent dr M. Gagner usadowili się wygodnie przed
ekranem monitora w jednym z biurowców przy Avenue of the Americas na Manhattanie. Ich
68-letnia pacjentka leżała w tym czasie na stole operacyjnym w Strasburgu odległym o 6000
km. Przy stole stanął tym razem nie chirurg, lecz robot. Manipulując joystickami, które
sterowały robotem, prof. Marescaux w 45 minut usunął pacjentce woreczek żółciowy.
Operację asekurował zespół chirurgów gotowych w każdej chwili wkroczyć do akcji. Nie
było takiej potrzeby. Wszystko się udało, a po tygodniu pacjentka wróciła do zdrowia.
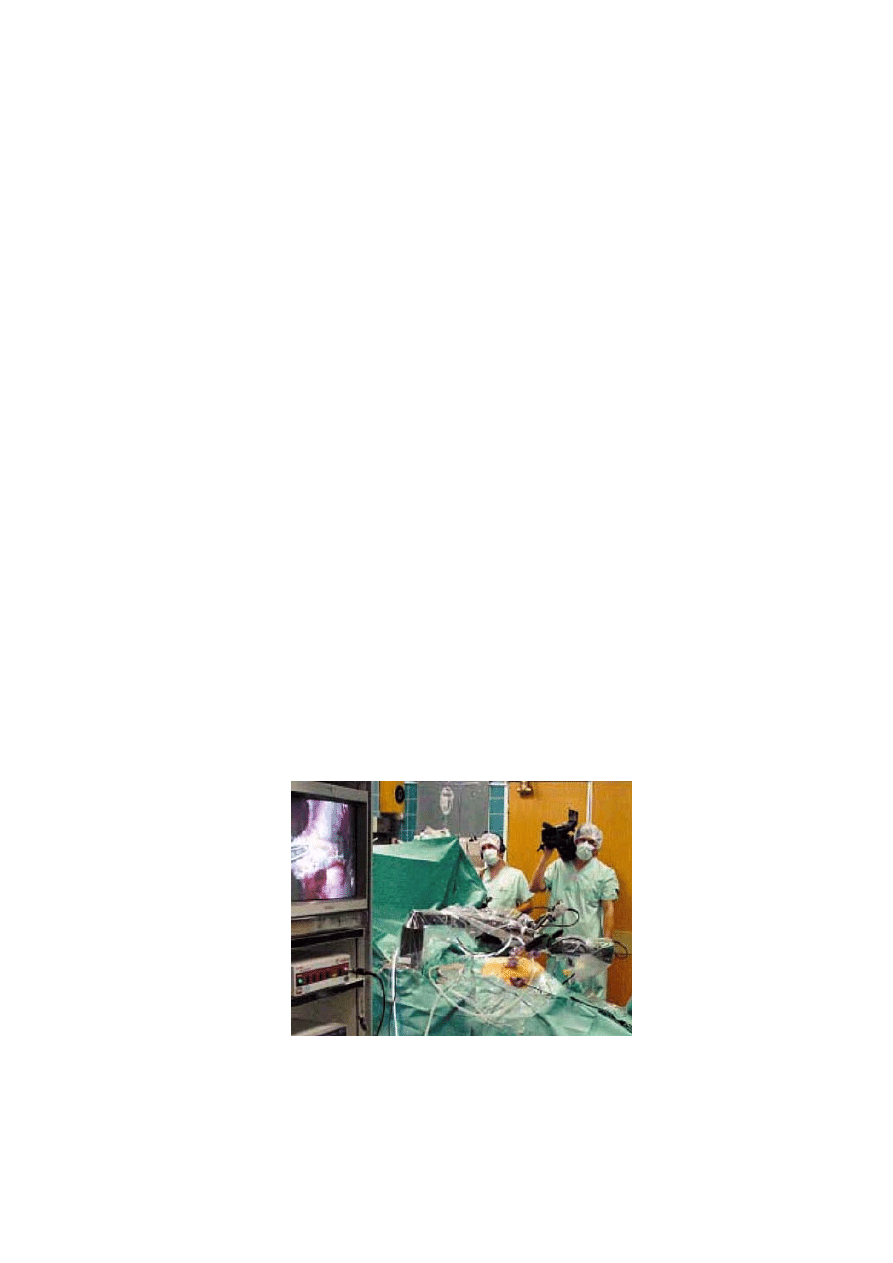
Rys. 8. Zdjęcie z operacji usuwania woreczka żółciowego
2.10. System nawigacyjny

10
Rys. 9
Na zdjęciu człowiek stojący w środku (DiGioia) wykorzystuje system HipNav przy
wymianie stawu biodrowego u 50-letniego mężczyzny z Pittsburga. HipNav jest
skomputeryzowanym układem nawigacji (zbudowanym przez Digioię). Właściwe ustawienie
stawu jest niezbędne w celu uniknięcia powikłań pooperacyjnych. DiGioia wykorzystuje do
wstawienia nowego stawu biodrowego wewnątrzoperacyjny system naprowadzania i prosty
inerfejs typu „wymierz i strzelaj”. Jeżeli kąt wstawienia stawu jest nieodpowiedni, komputer
wydaje dźwięk niczym Homer Simpson z kreskówki.
3. Robot symulujący żucie (Robot – szczęka)
Robot ten ma służyć badaniom nad mechanizmem żucia. W laboratorium profesora
Atsuo Takanishi na uniwersytecie Waseda są realizowane trzy projekty dotyczące robotów
dentystycznych. Oprócz robota czaszki symulującego żucie jest jeszcze robot otwierający i
zamykający usta oraz robot do pomiaru konsystencji żywności. Konstrukcję robota – czaszki
rozwija Hideaki Takanobu – adiunkt badawczy na Wydziale Mechaniczno-Energetycznym
Uniwersytetu Waseda i prof. Atsuo Takanishi.
Tradycyjne badania nad ludzkim mechanizmem żucia wykorzystywały model
teoretyczny, oparty na pomiarach ruchu szczęki człowieka. Robot czaszka nadaje się do
eksperymentów, ponieważ dzięki posiadaniu ludzkiej czaszki i podobnych do ludzkich mięśni
potrafi gryźć prawdziwe pożywienie. Model ilościowy opracowany za pomocą tego robota,
będzie miał wpływ na bardzo wiele zastosowań robotów oraz na konstrukcję różnych
urządzeń dentystyczno - medycznych.
Zwykłe maszyny są w stanie symulować stan gryzienia statycznego lub tylko położenie
szczęki. Nie potrafią symulować zjawisk całościowych, takich jak ruch mięśni, bodźce
czuciowe, czy też sygnały od centralnego układu nerwowego. Ze względu na to, że żucie
robota naśladuje działanie kości, mięśni i narządów czucia człowieka, jest on symulatorem
ludzkiego układu żucia.
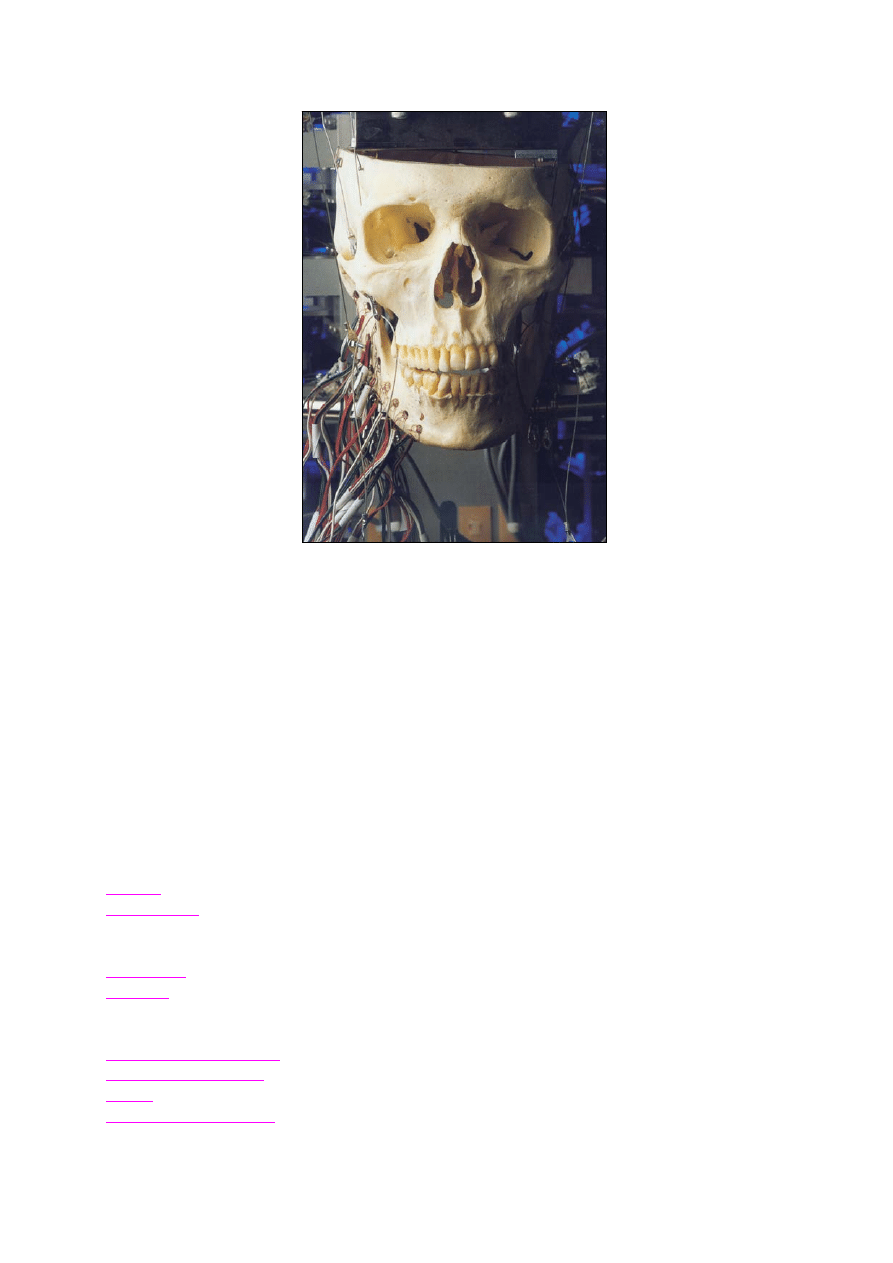
11
Rys. 10
3.1. Korzyści praktyczne ze stworzenia takiego robota
¾ Stworzenie robota o ludzkim kształcie, służącego jako „mechaniczny model człowieka”
(pełny model teoretyczny fizycznych naprężeń i sił działających w ludzkim ciele),
¾ Integracja robotów człekokształtnych – klasycznych modeli mechanicznych – z nowymi
metodologiami.
W Japonii bardzo wielu pacjentów, przeważnie młodych kobiet, cierpi na zaburzenie
stawu skroniowo – żuchwowego. Choroba ta wywołuje ból szczęki i zanik jej mięśni. Robot –
szczęka jest wyposażony w mechaniczne wędzidło, które wkładane do ust kobiety przywraca
jej zdolność żucia pokarmów.
3.2. Opis Techniczny
Nazwa:
Waseda – Okino Jaw No.1 (Szczęka Waseda – Okino nr 1)
Cel budowy:
Wyjaśnienie z robotycznego punktu widzenia działania układu żucia człowieka i
opracowanie podstawowych struktur mechaniki oraz sterowania dla celów badawczych i
edukacyjnych.
Wysokość:
51 cm
Sensory:
9 potencjometrów liniowych, 9 czujników naprężenia, 10 czujników
tensometrycznych (siła w stawie skroniowo-żuchwowym),
mikroczujnik nacisku (siła gryzienia)
Materiał konstrukcyjny:
duraluminium, czaszka ludzka
Zasilanie zewnętrzne:
napięcie przemienne 100 V
Koszt:
100 000 $
Status przedsięwzięcia:
w trakcie realizacji

12
4. Nanotechnologie (Nanoroboty)
Przedmiotem zainteresowania nanotechnologii są obiekty o rozmiarach rzędu
nanometrów. Nanotechnologię rozwinął w latach dziewięćdziesiątych XX wieku amerykański
naukowiec Eric Drexler. Nanotechnologii zawdzięczamy już m.in. coraz szybsze i mniejsze
procesory w komputerach, laserowe diody w czytnikach CD i płaskie ekrany komputerowe,
urządzenia wzmacniające sygnały w światłowodach i pozwalające tym samym przesyłać w
mgnieniu oka dane za pośrednictwem Internetu na drugi koniec świata oraz identyfikowanie
specyficznych oddziaływań białek na powierzchni komórek, pozwalające na projektowanie
nowych skuteczniejszych leków.
Naukowcy z Memorial Sloan-Kettering Center w Nowym Jorku skonstruowali
niewidoczny gołym okiem nanogenerator polujący na komórki rakowe. Jego najważniejsze
elementy, to przeciwciało rozpoznające komórki rakowe oraz atomy aktynu, nietrwałego
pierwiastka, który rozpadając się emituje promieniowanie. Po wstrzyknięciu nanogeneratora
do organizmu człowieka, tak długo krąży on w krwioobiegu aż natrafi na komórkę
nowotworową.
4.1. Inteligentny lek
Wyobraźmy sobie sztuczne maleńkie nanostruktury, które można byłoby wypełniać
cząsteczkami odpowiedniego medykamentu i kierować do chorych tkanek i narządów.
Wstrzyknięte do ciała pacjenta wraz z krwiobiegiem, dostawałyby się tylko do chorych
komórek. Tam ulegałyby rozpadowi, na przykład po nagrzaniu ich światłem podczerwonym,
a lek uwalniałby się o dokładnie wyznaczonej porze i - co jeszcze ważniejsze - w jednym
konkretnym miejscu. To zapewniałoby nie tylko największą skuteczność terapii, ale też
zmniejszyłoby niepożądane działania medykamentu, który nie miałby żadnej styczności ze
zdrowymi tkankami. Jeśli prowadzone eksperymenty się powiodą, to może już niedługo
będzie można uniknąć skutków ubocznych leczenia, na przykład, nowotworów. Zresztą w ten
sam sposób można by wprowadzać DNA do komórek, które chcemy poddać terapii genowej.
Kazushi Ishiyama z japońskiego Uniwersytetu Tohuku skonstruował maleńkie
urządzenia, które mogą się przemieszczać w naczyniach krwionośnych. Miałyby one
dostarczać leki do chorych tkanek bądź też nawet niszczyć guzy nowotworowe. Przy długości
ośmiu i średnicy jednego milimetra potrafią w czasie prób przewiercić dwucentymetrową
tkankę w 20 sekund. Nad podobnymi urządzeniami pracują amerykańska firma Renaissance
Technologies oraz niemiecki MicroTEC. Jeśli uda się rozwiązać problemy z miniaturyzacją,
zasilaniem i sterowaniem, być może do niewielkich operacji wystarczy wstrzyknąć w
odpowiednie miejsce robota. Jeszcze mniejsze „łodzie podwodne” opracowywane na
uniwersytecie w Utah mają być napędzane przez bakterie, na przykład Salmonella czy
Escherichia coli. Mogłyby dostarczać leki do tkanek nowotworowych.
Oto przykład podróży nanorobota w poszukiwaniu komórki nowotworowej.
Eksperyment wykonano wykorzystując zbiornik z krwią. Wyniki doświadczenia okazały się
zadowalające.

13
Rys.
11a Rys.
11b
Rys.
11c Rys.
11d
Rys.
11e Rys.
11f
Rys.
11g
Rys.
11h
4.2. Projektowanie i symulacja nanorobotów do naprawiania komórek (faza
projektowania). Wymagania stawiane nanorobotom medycznym
Muszą posiadać:
¾ bardzo dobry system nawigacji w celu prawidłowego funkcjonowania w krwioobiegu
¾ szeroki zakres sensorów do nawigacji i identyfikacji na poziomie molekularnym i
komórkowym
¾ mocny system transportu (musi dostarczać molekuły i atomy do pracujących
manipulatorów z magazynu)
¾ dobrą komunikację z innymi nanorobotami i z komputerem
¾ długie teleskopowe manipulatory do trzymania komórek i powierzchni.
Dodatkowo taki nanorobot musi być zbudowany z czystego diamentu (żeby nie wchodził w
reakcje chemiczne w organizmie), a przynajmniej powinien mieć diamentową powłokę.
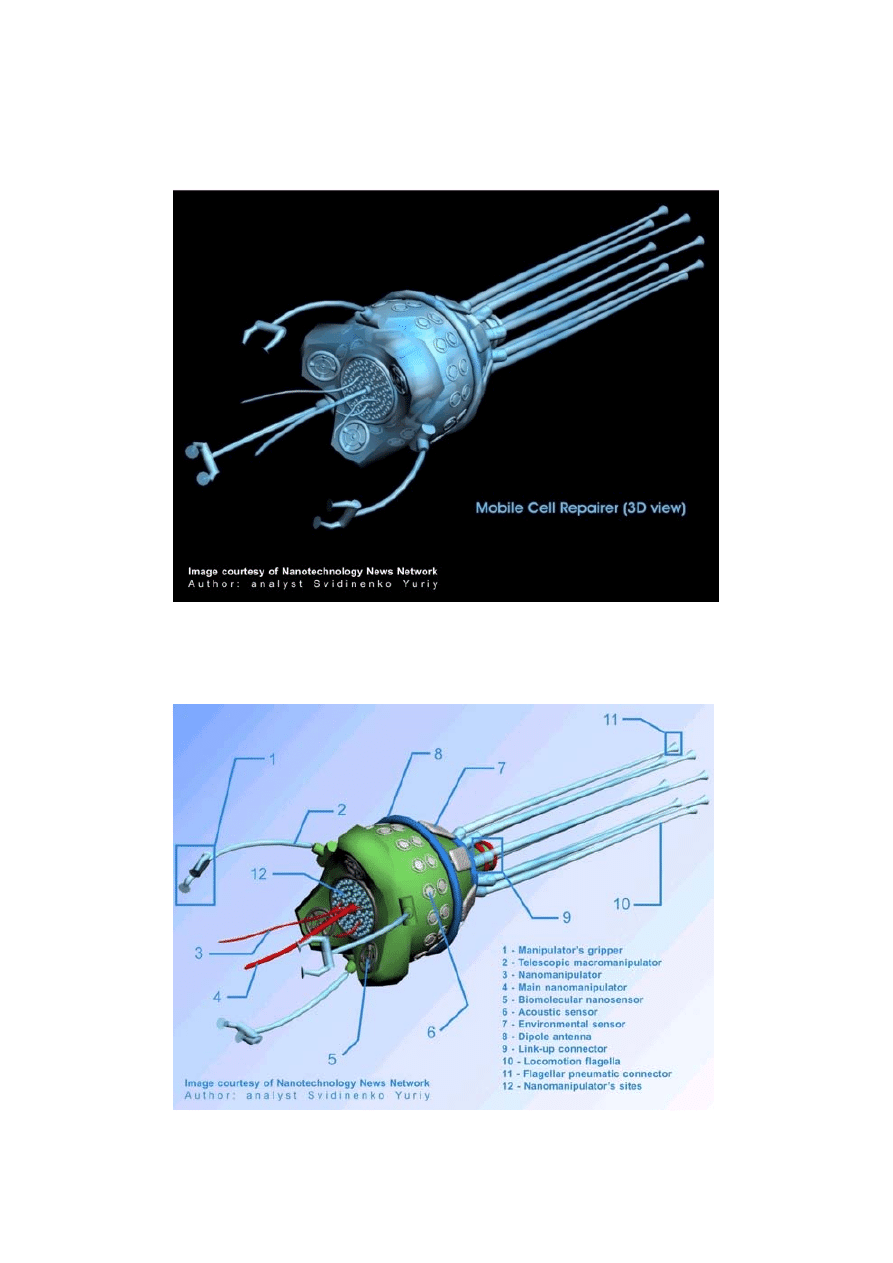
14
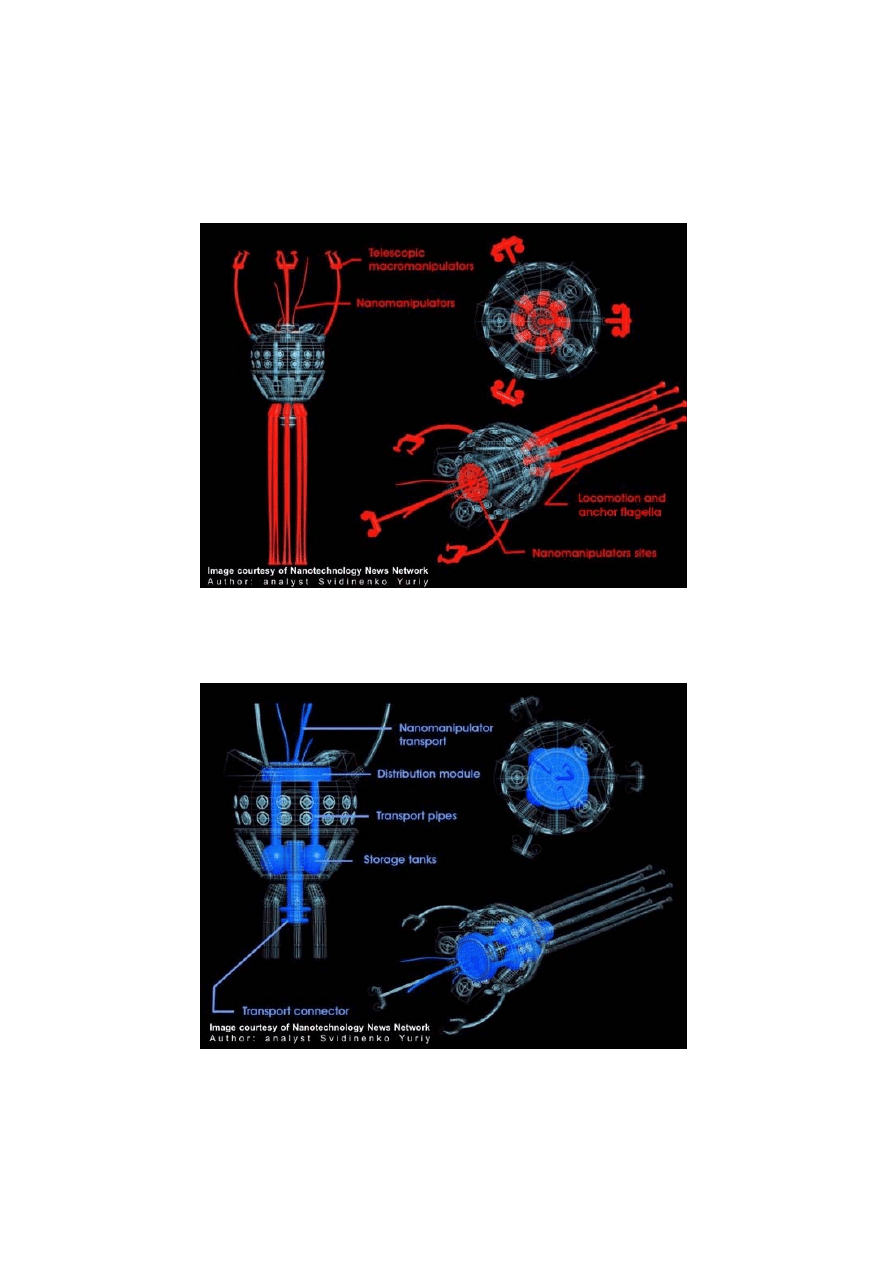
4.3. Przykładowa budowa nanorobota medycznego z pokrywą diamentową
Rys. 12
4.4. Opis nanorobota medycznego
Rys. 13
15
Każdy taki nanorobot medyczny miałby swoje podsystemy
Podsystem lokomocyjny
Rys. 14
Podsystem transportowy
Rys. 15
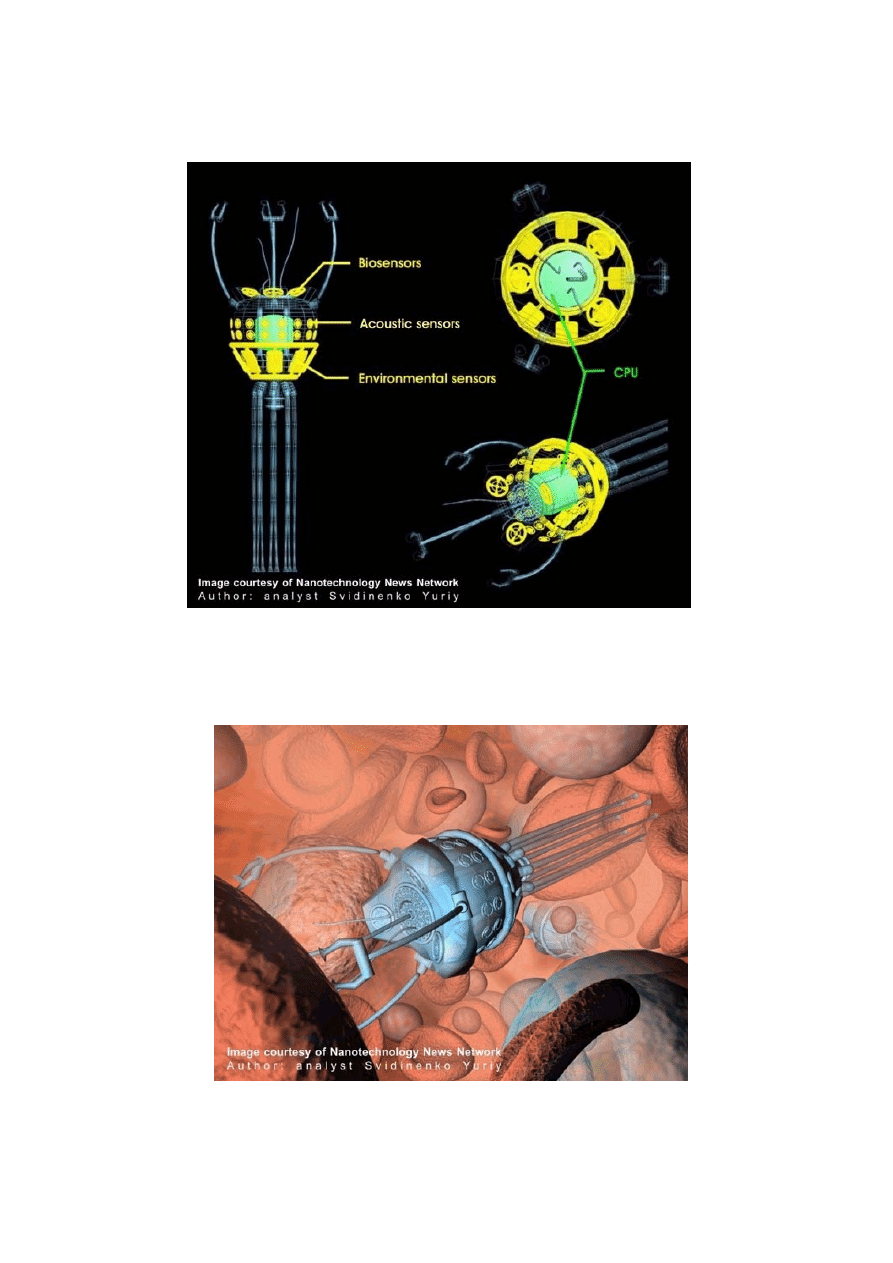
16
Podsystem czujników
Rys. 16
4.5. Nanoroboty podczas operacji naprawiania uszkodzonych komórek (dzięki symulacji
komputerowej)
Rys. 17
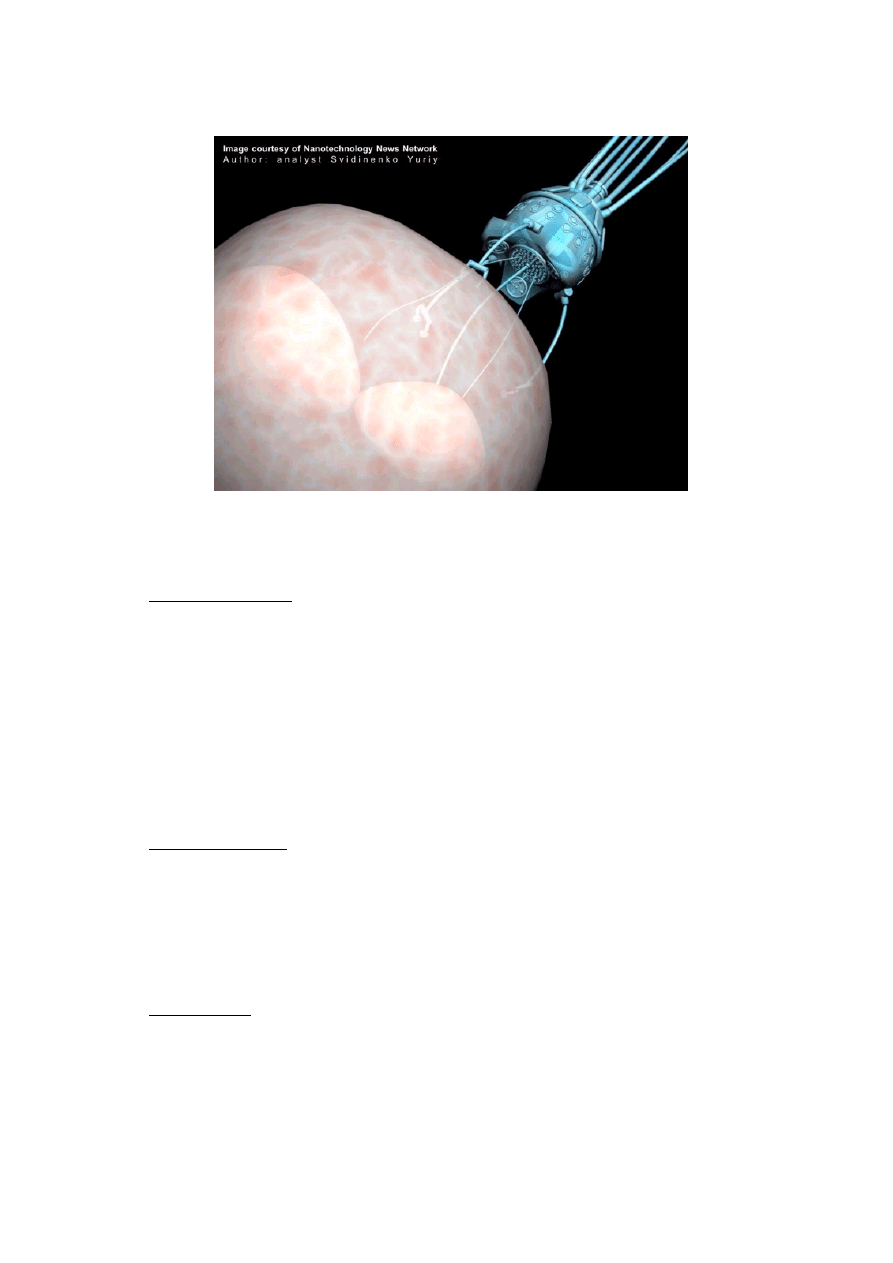
17
Rys. 18
4.6. „Bufor” czyli mechaniczny personel
Robot-pielęgniarka. W marcu 2004 r. przed kamerami BBC zaprezentowano robota,
który wkłuwał się do żyły swojego twórcy Alexa Zivanovica z Imperial College w Londynie.
To niełatwe nawet dla człowieka zadanie wykonywał posługując się dotykiem. Mięśnie są
twardsze, tkanka tłuszczowa miękka, zaś żyła podobna do nadmuchanego balonika. Robot
ukazuje zarys żyły na ekranie, sugerując najlepsze miejsce do wkłucia, decyzja jednak zależy
od operatora.
Pielęgnacja chorych to nie tylko zastrzyki i pobieranie krwi. Na przykład przenoszenie
chorych wymaga obok siły także dobrej orientacji przestrzennej. Poza tym pielęgniarka daje
choremu wsparcie emocjonalne – uśmiecha się, podtrzymuje na duchu. Japonia, której
społeczeństwo się starzeje, cierpi na ostry deficyt pielęgniarek. Dlatego całkiem serio myśli
się tam o robocie, który oprócz czynności pielęgnacyjnych potrafiłby zabawiać rozmową,
rozpoznawać mimikę chorego i uśmiechać się.
Robot-sprzątaczka. W brytyjskim szpitalu w Welwyn Garden City (Hertfordshire)
korytarze sprząta robot wielkości wózka z supermarketu. Porusza się z prędkością do 5
km/godz. i kosztuje 35 tys. funtów. Orientuje się dzięki czujnikom laserowym i
ultradźwiękowym. Jeśli ktoś stanie mu na drodze, grzecznie przeprasza: – Excuse me, I’m
cleaning. Wystarczy raz poprowadzić robota wyznaczoną trasą, by poznał zakres
obowiązków. Po pracy sam ładuje akumulatory i uzupełnia zapasy detergentów. Ludzie mogą
się skupić na trudniejszych zadaniach: toaletach i pokojach chorych. Zresztą opracowano już
robota do czyszczenia toalet.
Robot-goniec. Roboty HelpMate zastępują szpitalnych gońców, dając (w
amerykańskich warunkach) duże oszczędności na płacach. Niestrudzenie przenoszą leki,
próbki krwi czy tkanek. Sprawnie omijają przeszkody i potrafią korzystać z wind. Nie umieją
strajkować.
Bibliografia

18
‘Robo sapiens’ – Peter Menzel, Faith D’Aluisio
Wiedza i Życie 06.06.2004, Gazeta Wyborcza 29.11.2004
http://swiattechniki.pl/index.php/st/archiwum/2004_09/supertemat/polski_kardiobot
http://serwisy.gazeta.pl/nauka/1,34139,748528.html
http://www.swiattechniki.pl/index.php/st/galeria/wrzesie_3_2004/robin_heart
http://polityka.onet.pl/artykul.asp?DB=162&ITEM=1066102&MP=2
‘Robo sapiens’ – Peter Menzel, Faith D’Aluisio
http://radio.weblogs.com/0105910/2004/08/23.html
http://www.e-spaces.com/portfolio/trans/blood/
http://www.nanonewsnet.com/index.php?module=pagesetter&func=viewpub&tid=4&pid=2
Wyszukiwarka
Podobne podstrony:
PR ETI W 14 4 4
PR ETI W 14 6 1
PR ETI W 14 8 1
PR ETI W 14 5 1
PR ETI W 14 2 1
PR ETI W 14 11 1 id 382129 Nieznany
PR ETI W 14 12 1
PR ETI W 14 4 4
PR ETI W 14 6 1
PR ETI W 3 4 3 5
PR ETI W 2
PR ETI W 1 4
PR ETI W 1 3
PR ETI W 1 3
PR ETI W 21 1
PR ETI W 25 6
PR ETI W 22 1
serwis pr, ETI SUM, sem 1
więcej podobnych podstron