
255
AGNIESZKA JAGODA
*
, BARBARA DĄBROWSKA
**
, WITOLD ŻUKOWSKI
*
Kofeina jako wskaźnik antropogenicznego zanieczyszczenia środowiska
– metody oznaczania
Słowa kluczowe
kofeina – antropogeniczne zanieczyszczenie wody – metody analityczne
Streszczenie
Kofeina (1,3,7-trimetyloksantyna) występuje w kawie i herbacie, a także jest dodawana do napoi
energetyzujących, leków, a nawet do kosmetyków. Pomimo dobrego metabolizowania przez organizm ludzki
trafia do środowiska w coraz większych ilościach. Występowanie kofeiny w wodach powierzchniowych
i gruntowych daje możliwość wykorzystania tej substancji jako wskaźnika miejsc niekontrolowanego zrzutu
ścieków. Praca ma na celu przedstawienie metod analitycznych stosowanych do oznaczania zawartości
kofeiny w próbkach środowiskowych.
1. Wstęp
1,3,7-trimetyloksantyna (wg IUPAC: 1,3,7-trimetylo-1H-puryno-2,6(3H,7H)-dion), w zależności
od źródła pochodzenia, zwana jest: kofeiną, teiną, guaraniną lub mateiną [25]. Jest to substancja
o działaniu psychoaktywnym. Dzięki swym pobudzającym właściwościom zmniejsza uczucie
znużenia, zmęczenia i senności. W postaci naturalnej występuje w kawie i w herbacie, jest stosowna
przez ludzi na całym świecie. Dodaje się ją do popularnych napoi typu: Coca-Cola, Pepsi i napoi
energetyzujących (energy drink). Jest składnikiem leków, a obecnie coraz częściej jest
wykorzystywana jako dodatek do kosmetyków [25].
Oszacowanie ilości spożywanej kofeiny jest trudne. Według badań przeprowadzonych w latach
2002-2006 na zlecenie Holenderskiego Urzędu Statystycznego (Centraal Bureau voor de
Statistiek) największą ilość kawy wypijają Skandynawowie, przeciętnie 4,3 filiżanki dziennie.
Polacy spożywają jej stosunkowo mało - około jedną filiżankę dziennie [12, 13]. Zgodnie
z danymi GUS statystyczny Polak w 2008 roku spożył miesięcznie 0,19 kg kawy i 0,07 kg herbaty
[15]. 1,3,7-trimetyloksantyna jest uznawana za środek dopingowy, jej stężenie w moczu nie może
*
Wydział Inżynierii i Technologii Chemicznej, Politechnika Krakowska
e-mail: ajagoda@chemia.pk.edu.pl
**
Wydział Inżynierii Środowiska, Politechnika Krakowska
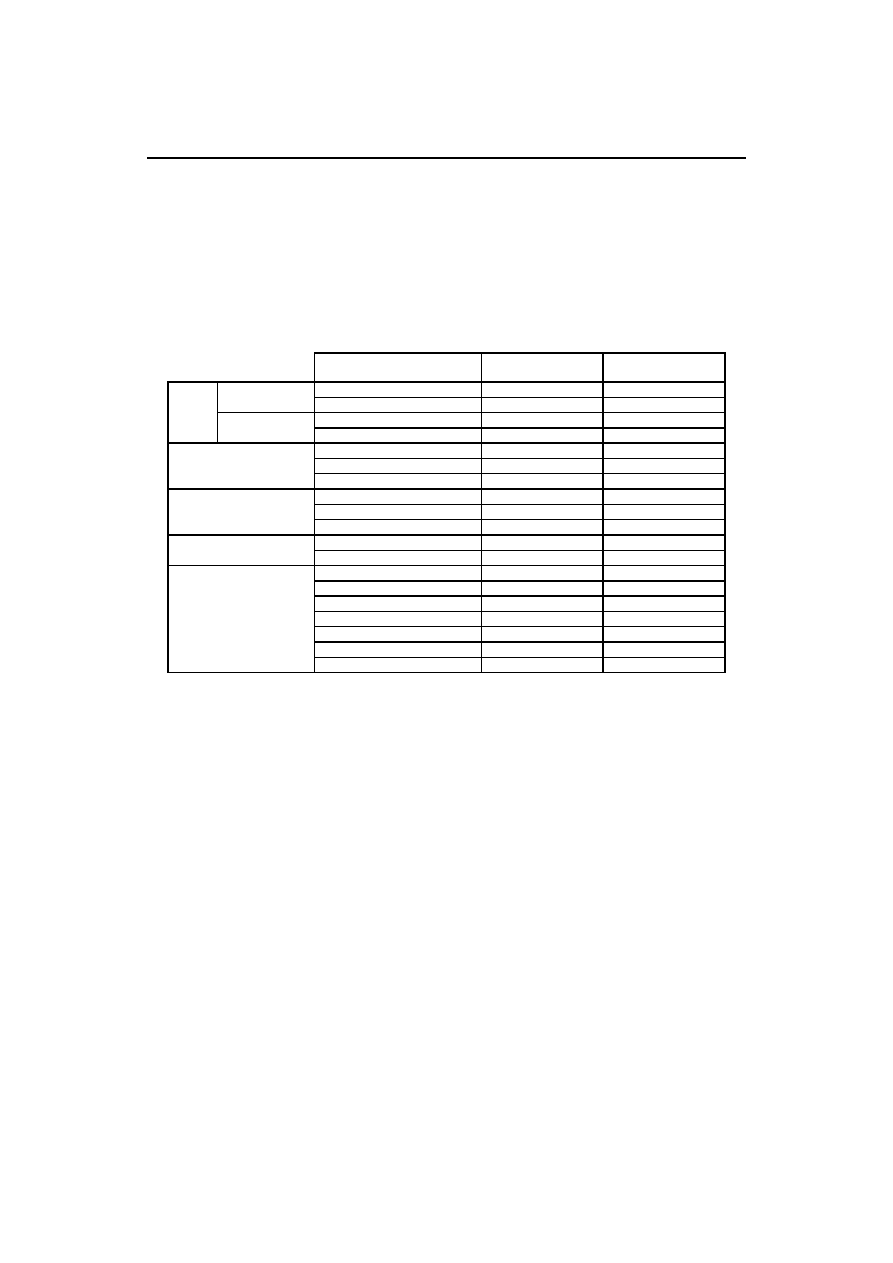
Jagoda A., Dąbrowska B., Żukowski W.: Kofeina jako wskaźnik antropogenicznego zanieczyszczenia …
256
przekraczać 12 mg/ml [11]. Kofeina w lekach jest nie tylko wykorzystywana jako środek
pobudzający, ale także jako środek wzmacniający działanie innych substancji leczniczych.
Potęguje działanie paracetamolu i dlatego jest składnikiem niektórych leków przeciwbólowych
i przeciwgrypowych (Tabela 1).
Tabela 1. Zawartość kofeiny w kawie, herbacie, napojach i lekach ([16], ulotki informacyjne)
Table 1. Concentration of caffeine in coffee, tea, beverages, energy drinks and medicines
([16], product notes)
Produkt
Wielkość porcji
Zawartość kofeiny
w porcji mg
Kawa
Mielona
Jacobs Krönung
2 łyż. w 160 ml
57,7
Tchibo Family
2 łyż. w 160 ml
99,2
Rozpuszczalna
Jacobs Krönung
2 łyż. w 160 ml
109,4
Tchibo Family
2 łyż. w 160 ml
136,6
Herbata
Czarna ekspresowa
Lipton
200 ml
48,4
Tetley
200 ml
40,0
Saga
200 ml
24,3
Napoje
Mountain Dew
100 ml
15
Coca-Cola
100 ml
12
Pepsi
100 ml
12
Energy drinks
Red Bull
100 ml
32
Tiger
100 ml
32
Leki
APAP Extra
1 tabletka
65
Coldrex MaxGrip
1 tabletka
25
Panadol Extra
1 tabletka
65
Saridon
1 tabletka
50
Aspirin Active
1 tabletka
50
CARDIAMID-COFFEIN
1 ml
100
Etopiryna
1 tabletka
50
Kofeina jest składnikiem wielu produktów spożywczych i farmaceutycznych [16]. Spożycie jej
na całym świecie jest tak duże, że można uznać, iż jest to jeden z najpowszechniej stosowanych far-
maceutyków. Substancja ta szybko się wchłania z przewodu pokarmowego i osiąga maksymalne
stężenie w osoczu już po 30-75 minutach od spożycia. Szybko przenika do tkanek i narządów. Meta-
bolizowana jest w wątrobie, na drodze demetylacji, w 80% do paraksantyny (1,7-dimetyloksantyna),
w 16% do teobrominy (3,7-dimetyloksantyna) i teofiliny (1,3-dimetyloksantyna). Jej okres półtrwa-
nia wynosi 4-5 godzin, a metabolity są wydalane z moczem. Od 0 do 3% kofeiny jest usuwane
z organizmu w postaci niezmienionej [21], chociaż istnieją dane literaturowe mówiące o 5-20% [10].
Pomimo faktu, że kofeina jest dobrze metabolizowana przez organizm ludzki, jej obecność
w wodach powierzchniowych jest znaczna, szczególnie w bliskiej obecności siedzib ludzkich. Do
podstawowych źródeł zanieczyszczeń należy: mycie naczyń wykorzystywanych w procesie
przygotowania napojów (kubki, części ekspresów do kawy), wyrzucanie fusów z kawy i herbaty,
wyrzucanie niezużytych leków do ścieków i na wysypiska. Wszystko to powoduje, że kofeina jest
dostarczana do wód w sposób ciągły i może być traktowana jako wskaźnik zanieczyszczenia wód
odpadami antropogenicznymi. Jej detekcja w próbach środowiskowych może służyć jako wskaźnik
miejsc niekontrolowanego zrzutu ścieków.
Powszechnie prowadzone są badania, których celem jest stworzenie skutecznych sposobów
oznaczania zawartości 1,3,7-trimetyloksantyny w próbkach wodnych. Jest to konieczne by możliwe
było opracowanie efektywnego monitoringu wód i wykrycie miejsc dopływów do środowiska
nieoczyszczonych ścieków.

V Krakowska Konferencja Młodych Uczonych, Kraków 2010
257
2. Charakterystyka metod analitycznych
Opracowanie skutecznych metod oznaczania zanieczyszczeń środowiska wodnego substan-
cjami farmaceutycznymi napotyka wiele przeszkód. Do najważniejszych utrudnień należy zaliczyć
niskie stężenia oznaczanych substancji oraz bardzo złożony, zmienny skład próbek. Problemem
jest duża oscylacja zarówno stężenia analizowanej substancji, jak i składu matrycy. Wiele zależy
od rodzaju cieku wodnego, od miejsca poboru próbki. Różnice w składzie mogą wystąpić nie tylko
między próbami pochodzącymi z rzek i ze ścieków, ale również z tej samej rzeki. Na skład
chemiczny badanej próbki wpływa także: teren przez jaki przepływa rzeka, rodzaj aglomeracji
(miejska, wiejska), typ i wielkość dopływów, itp.
Substancje lekowe zawierające np. kofeinę występują w próbkach środowiskowych w bardzo
małych stężeniach, co powoduje konieczność opracowania metod o bardzo niskich wartościach
granic detekcji (LOD, Limit of Detection) i oznaczalności (LOQ, Limit of Quantification).
Obecnie, dzięki rozwojowi nowoczesnej aparatury, staje się to możliwe do zrealizowania.
Powstają czułe i selektywne metody, wykorzystujące techniki łączone. Mają one jednak wady - są
zazwyczaj bardzo czaso- i pracochłonne oraz bardzo kosztowne.
W metodykach analiz zawartości kofeiny w próbkach wodnych wyróżnić można dwa główne
etapy. Pierwszy etap jest realizowany podczas procesu ekstrakcji, składa się na niego: izolacja,
wzbogacanie i oczyszczanie próbki. Z uwagi na fakt, że analizom poddawane są próbki
środowiskowe, pierwszy etap jest najczęściej poprzedzony filtracją na sączku szklanym. Pozwala
to usunąć cząstki, mogące przeszkadzać podczas procesu ekstrakcji. Drugi etap to rozdzielanie
analitów i analiza jakościowo-ilościowa. Realizuje się go przez chromatografię gazową lub
cieczową, sprzężoną ze spektrometrią mas [14].
Ekstrakcja odbywa się najczęściej poprzez ekstrakcję do fazy stałej (SPE, Solid-Phase
Extraction), aczkolwiek wykorzystuje się też ekstrakcję ciecz-ciecz (LLE, Liquid-Liquid
Extraction). Obie techniki należą do czasochłonnych, ale stosowanie SPE wymaga dużo
mniejszego zużycia rozpuszczalników. Podczas ekstrakcji do fazy stałej kofeiny z prób wodnych,
wykorzystywane
są
najczęściej
kolumienki
Oasis
HLB
(
wypełnienie
polimerowe
diwinylobenzeno-N-winylopirolidynowe) [2,4,5,8,9,19,20,22-24,27-29]
, chociaż stosowane są
także: C18 (
żel krzemionkowy modyfikowany łańcuchami oktadecylowymi
) [3,28] i HR-P
(kopolimer polistyren-diwinylobenzen) [17]. Jako eluenty są używane: aceton [3], dichlorometan
[22-24], metanol [19,20,22-24] i octan etylu [9,17] lub mieszaniny rozpuszczalników [5,19,22-
24,28,29]. Podczas LLE kofeiny jako ekstrahenty stosowano: chlorek metylenu [1], dichlorometan
[6,26], i n-pentan [6]. Ekstrahenty nie powinny być zanieczyszczone wodą, dlatego w celu
usunięcia wilgoci, będącej przeszkodą w analizach chromatograficznych stosuje się: suszenie
kolumienek pod próżnią, całkowite odparowanie rozpuszczalnika po ekstrakcji (w atmosferze gazu
obojętnego) i ponowne rozpuszczenie ekstraktu lub suszenie bezwodnym siarczanem sodu.
Chromatografia służy do rozdzielenia mieszaniny związków, w metodzie gazowej (GC, Gas
Chromatography) jako eluent zastosowano hel, a w wysoko ciśnieniowej chromatografii cieczowej
(HPLC, High Pressure Liquid Chromatography) wykorzystywano układy ze zmiennym (w trakcie
analizy) składem. W analizie zwartości kofeiny i paraksantyny na wlocie i wylocie z oczyszczalni
w Tajwanie, stosowno układ: roztwór wodny i metanolowy kwasu mrówkowego [19], a
w analizach cieków wodnych w Stanach Zjednoczonych Ameryki Północnej układ: acetonitryl
i bufor mrówczanowy (mrówczan amonu/kwas mrówkowy, 10 mM, pH 3,7) [2].
Następny etap to jonizacja analitów. W przypadku GC najpopularniejszą metodą jej
realizowania jest jonizacja strumieniem elektronów, a w chromatografii cieczowej jest to jonizacja
metodą elektrorozpylania (ESI, Electro Spray Ionization) oraz jonizacja chemiczna pod ciśnieniem
atmosferycznym (APCI, Atmospheric Pressure Chemical Ionization). Spektrometria mas
(MS, Mass Spektrometry) pozwala na identyfikację kofeiny w próbkach. Odbywa się poprzez
Jagoda A., Dąbrowska B., Żukowski W.: Kofeina jako wskaźnik antropogenicznego zanieczyszczenia …
258
oznaczenie stosunku masy do ładunku (m/z) powstających jonów. Wykorzystuje się do tego celu
analizatory mas: kwadrupolowe, pułapki jonowe (IT, Ion Trap), analizatory czasu przelotu (TOF,
Time-Of-Flight) [14].
3. Wyniki oznaczeń zawartości kofeiny w próbkach środowiskowych
W tabelach 2-4 przedstawiono dane literaturowe dotyczące zawartości kofeiny w różnego typu
próbkach środowiskowych, wraz z zaznaczeniem miejsca ich poboru i metod wykorzystanych do
przeprowadzania analiz. Zawartość kofeiny i paraksantyny została określona na wlotach i wylo-
tach z oczyszczalni ścieków, jak i wodach powierzchniowych i gruntowych.
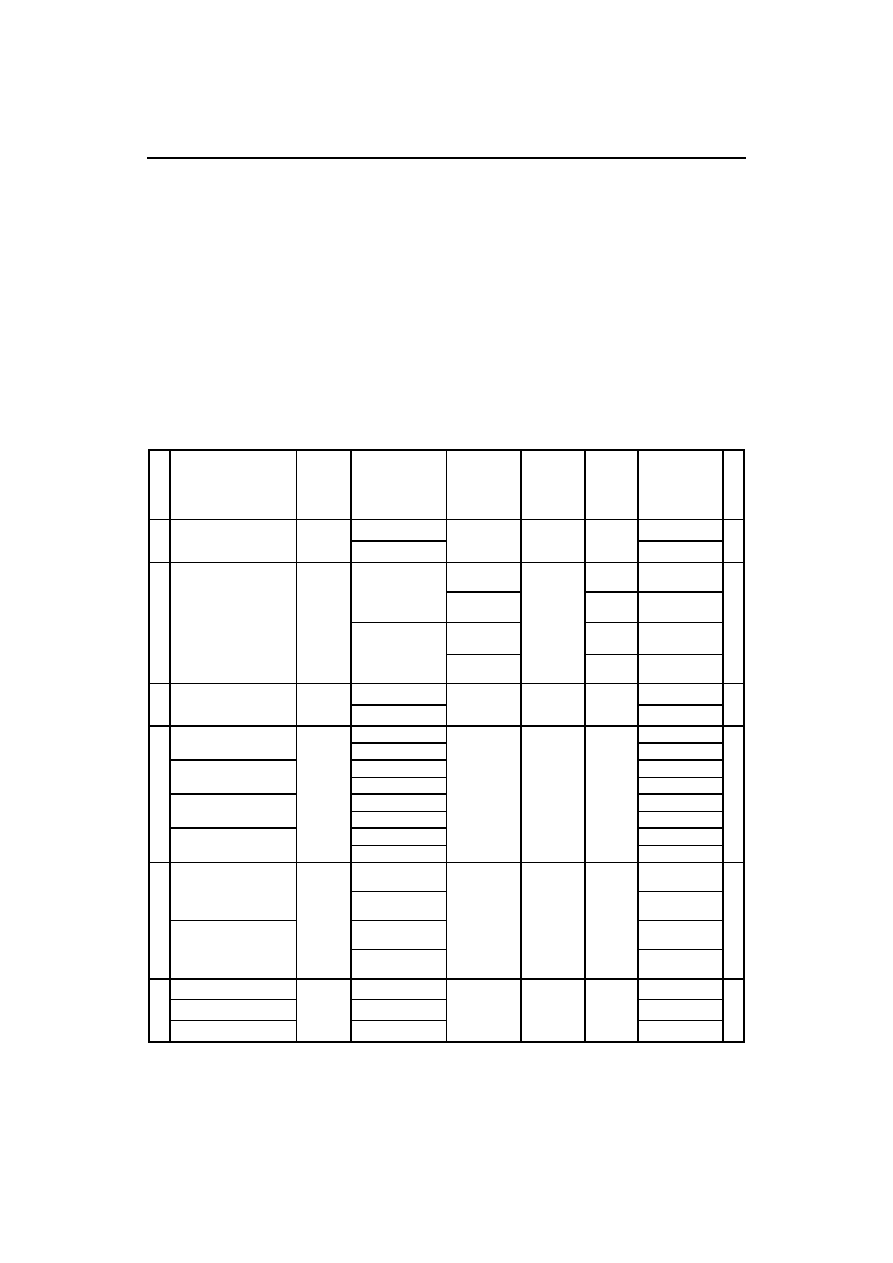
Tabela 2. Zawartość kofeiny i paraksantyny na wlotach i wylotach z oczyszczalni ścieków
Table 2. Concentration of caffeine and paraxanthine in influents and effluents of sewage treatment plants
K
ra
j
Oczyszczalnia ścieków
T
er
m
in
p
o
b
ra
n
ia
p
ró
b
ek
Miejsce pobrania
próbek
Analizowana
substancja
M
et
o
d
a
Granica
detekcji
µg/l
Zawartość
analizowanej
substancji
µg/l
Ź
ró
d
ło
U
S
A
Deer Island STP
V
1
9
9
8
dopływ
kofeina
L
L
E
G
C
-
M
S
20,0
[2
6
]
odpływ
6,7
H
is
zp
an
ia
Almeria (miejska,
oczyszcza ścieki
szpitalne)
V
II
2
0
0
3
-I
V
2
0
0
4
dopływ
paraksantyna
S
P
E
G
C
-M
S
0,014
48-111
79**
[9
]
kofeina
0,001
52-192
118**
odpływ
paraksantyna
0,014
0,60-50
18**
kofeina
0,001
1,4-44
12**
S
zw
ec
ja
Källby
X
2
0
0
2
dopływ
kofeina
S
P
E
G
C
M
S
3,69
[3
]
odpływ
0,22
T
aj
w
an
WWTP1
dopływ
kofeina
S
P
E
H
P
L
C
-E
S
I-
M
S
-
M
S
0,0005
2,59
[1
8
,1
9
]
odpływ
0,03
Dihua
dopływ
3,02
odpływ
0,46
WWTP3
dopływ
1,92
odpływ
0,08
Neihu
dopływ
1,26
odpływ
0,005
G
re
cj
a
Ioannina (miejska)
II
I
2
0
0
6
-I
II
2
0
0
7
dopływ
kofeina
S
P
E
G
C
-M
S
0,0145
0,0435*
17,1–113,2
74,9 **
[1
7
]
odpływ
1,9–13,9
7,9**
Ioannina (przyszpitalna)
dopływ
12,3–42,0
25,8**
odpływ
3,1–10,6
6,5**
F
ra
n
cj
a
Elbeuf
II
I-
X
I
2
0
0
2
odpływ
kofeina
S
P
E
G
C
-M
S
0,0023*
0,0350-0,2697
[2
8
]
Rouen
odpływ
0,0128-3,5274
Tancarville
odpływ
0,0023-0,9468
V Krakowska Konferencja Młodych Uczonych, Kraków 2010
259
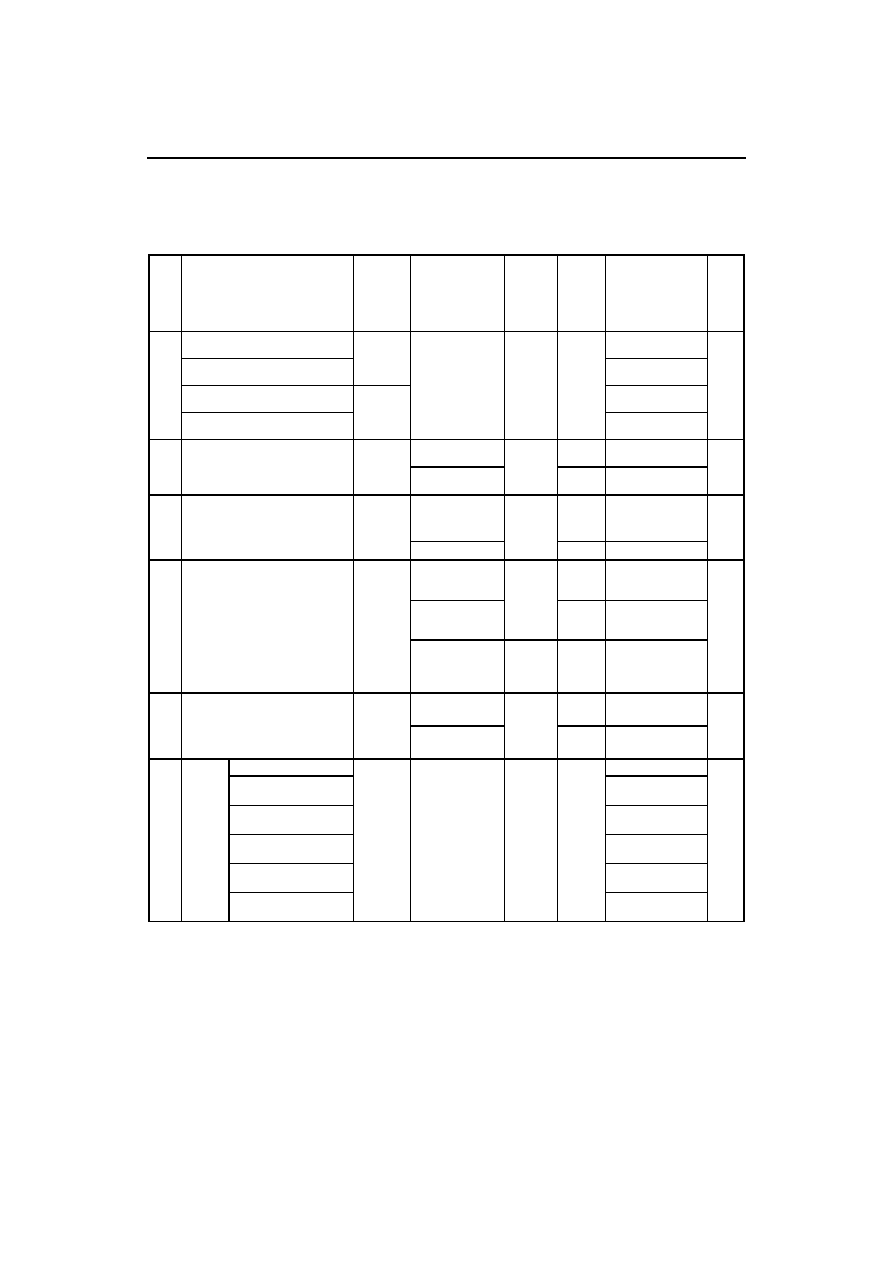
Tabela 3. Zawartość kofeiny i paraksantyny w wodach Ameryki Północnej
Table 3. Concentration of caffeine and paraxanthine in the waters of Northern America
K
ra
j
Miejsce pobrania próbek
T
er
m
in
p
o
b
ra
n
ia
p
ró
b
ek
Analizowana
substancja
M
et
o
d
a
RL
#
µg/l
Zawartość
analizowanej
substancji
µg/l
Ź
ró
d
ło
U
S
A
Przystań Boston
V
1
9
9
8
kofeina
L
L
E
G
C
-M
S
0,140-0,960
[2
6
]
Rzeka Karola
0,340-0,370
Przystań Boston
IV
1
9
9
9
0,160-1,600
Rzeka Karola
0,130-0,160
U
S
A
47 prób wody gruntowej
z 18 Stanów USA
2
0
0
0
paraksantyna
S
P
E
H
P
L
C
0,018
0,057*
[2
,5
]
kofeina
0,014
0,13*
U
S
A
Okolice wysypiska Himco
Dump, Elkhart, Indiana
2
0
0
0
,
2
0
0
2
paraksantyna
S
P
E
H
P
L
C
-
E
S
I-
M
S
0,018
<RL**
0,057**
[4
,5
]
kofeina
0,014
<RL**
U
S
A
Próbki wody po
zrealizowaniu procesu
uzdatniania.
X
I-
X
II
2
0
0
1
paraksantyna
S
P
E
H
P
L
C
-
E
S
I-
M
S
0,018
ND
[1
,5
,2
7
]
kofeina
0,014
0,119*
kofeina
L
L
E
G
C
-
M
S
0,5
ND
U
S
A
25 próbek wód gruntowych i 49
powierzchniowych z 25 Stanów
USA i Puerto Rico.
2
0
0
1
paraksantyna
S
P
E
H
P
L
C
-
E
S
I-
M
S
0,018
0,30*
[5
,8
]
kofeina
0,014
0,27*,***
K
an
ad
a
Z
ac
h
o
d
n
ie
w
y
b
rz
eż
e
w
y
sp
y
V
an
co
u
v
er
,
K
o
lu
m
b
ia
B
ry
ty
js
k
a
woda morska
kofeina
S
P
E
G
C
-I
T
-M
S
-M
S
0,0045-0,1490
[2
9
]
rzeka (nad wylotem
z oczyszczalni)
0,0021-0,0032
rzeka (pod wylotem
z oczyszczalni)
0,0072-0,0154
jezioro (duża
aktywność ludzka)
0,0061-0,0217
jezioro (średnia
aktywność ludzka)
0,0016-0,0104
jezioro (mała
aktywność ludzka)
ND-0,0065
#
- poziom raportowania (Reporting Level) - określona zawartość analitu, poniżej której wyniki nie są
brane pod uwagę, są oznaczane jako wartości poniżej wartości RL (bez podawania konkretnych wartości
stężeń), ND – nie wykryto, * - największa wartość stężenia, ** - przykładowe wyniki,*** - wyniki
zawartości kofeiny były poddane statystycznej obróbce ponieważ wykryto ją w ślepych próbach
Jagoda A., Dąbrowska B., Żukowski W.: Kofeina jako wskaźnik antropogenicznego zanieczyszczenia …
260
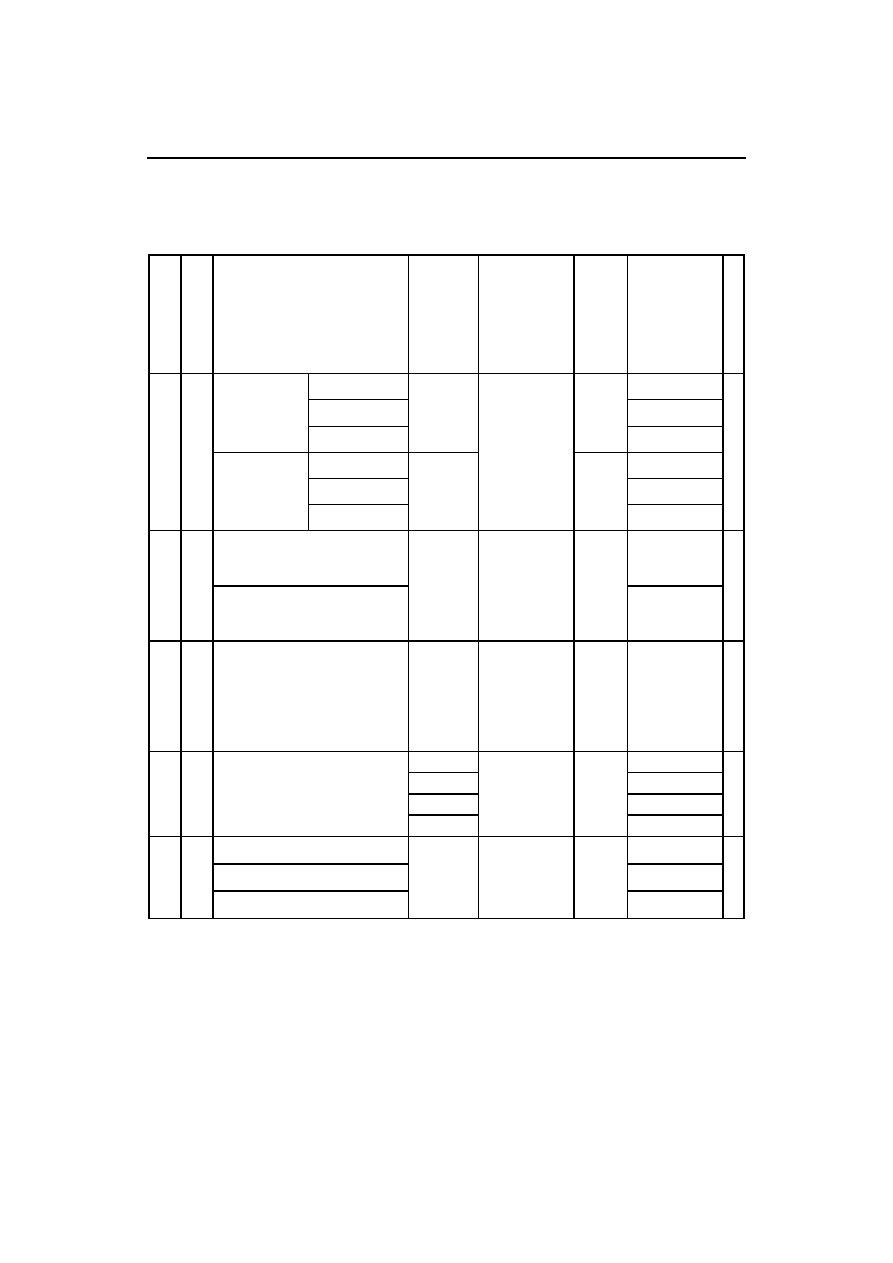
Tabela 4. Zawartość kofeiny w wybranych rzekach europejskich
Table 4. Concentration of caffeine in selected European rivers
K
ra
j
N
a
zw
a
r
ze
k
i
Miejsce pobrania próbek
Termin
pobrania
próbek
M
et
o
d
a
G
ra
n
ic
a
o
zn
a
cz
a
ln
o
śc
i
µ
g
/l
Zawartość
analizowanej
substancji
µg/l
Ź
ró
d
ło
Ru
m
u
n
ia
S
o
m
es
u
l
przed
modernizacją
oczyszczalni
ścieków
Cluj-Napoca
IV 2003
SPE GC-MS
0,03
2,772**
[2
2
,2
3
,2
4
]
Gherla
9,700**
Dej
0,428**
po
modernizacji
oczyszczalni
ścieków
Cluj-Napoca
IX 2006
0,01
0,228**
Gherla
0,333**
Dej
0,333**
1
0
k
ra
jó
w
D
u
n
aj
52 próbki
z rzeki Dunaj,
na całej jej długości
VIII-IX
2007
SPE HPLC-
ESI-MS-MS
0,001
#
1,467*
0,137**
[2
0
]
50 próbek z dopływów rzeki
Dunaj
6,798*
0,406**
S
zw
ec
ja
H
je
7 miejsc pobrania próbek
X 2002
SPE GC-MS
<0,005
0,43
0,07
0,38
0,11
0,01
0,01
[3
]
N
ie
m
cy
L
ip
p
e
19 miejsc pobrania próbek
VIII 1999
LLE GC-MS
0,01
<0,01-0,13
[6
,7
]
II 2000
<0,01-0,32
VIII 2000
<0,01-0,36
III 2001
<0,01-0,42
F
ra
n
cj
a
S
ek
w
an
a
Poses
III-XI
2002
SPE
GC-MS
0,0013
0,0102-0,1523
[2
8
]
Caudebec
0,0039-0,1869
Honfleur
0,0032-0,0436
#
- poziom raportowania (Reporting Level) - określona zawartość analitu, poniżej której wyniki nie są brane
pod uwagę, są oznaczane jako wartości poniżej wartości RL (bez podawania konkretnych wartości stężeń),
* - największa wartość stężenia, ** - uśredniona wartość stężenia

V Krakowska Konferencja Młodych Uczonych, Kraków 2010
261
4. Podsumowanie
Kofeina była wykrywana w próbkach pobranych na dopływach i odpływach z oczyszczalni
ścieków we wszystkich wymienionych oczyszczalniach (tabela 2), a najwyższe jej stężenie odnoto-
wano na wlocie do oczyszczani ścieków w Hiszpanii [9]. Dzięki danym przedstawiającym zwartość
1,3,7-trimetyloksantyny przed i po procesie oczyszczania ścieków (wyjątek stanowi Francja
z powodu braku danych) widać, że ładunek zanieczyszczeń dostarczany w poszczególnych przypad-
kach znacznie się różni. Wszystkie oczyszczalnie łączy natomiast brak pełnego usunięcia kofeiny
[3,9,17-19,26,28].
Zarówno wody Ameryki Północnej (tabela 3) i rzeki Europejskie (tabela 4) zawierają kofeinę
w stężeniach porównywalnych z tymi wykrywanymi na wylotach z oczyszczalni. Jest to powiązane
z faktem, iż wody po procesie oczyszczenia są odprowadzane do rzek, jezior i mórz. Niestety 1,3,7-
trimetyloksantyna jest wykrywana również w wodach gruntowych [2,5,8], co pozwala sądzić, że nie
ma już wód, które nie zostały antropogenicznie zanieczyszczone. Ważny jest jednak monitoring
i ciągła modernizacji oczyszczalni. Przypadek rzeki Somesul w Rumuni pokazuje jak dużą redukcję
stężenia daje modernizacja jednej tylko oczyszczalni [22,23,24]. Analiza danych dotyczących rzeki
Dunaj wskazuje na znaczenie dbania o czystość każdego dopływu rzeki, stężenie kofeiny w Dunaju
jest mniejsze niż w jego dopływach [20].
Opracowanie skutecznej metody analitycznej, w przypadku analiz środowiskowych jest trudnym
zadaniem, stąd w literaturze można znaleźć wiele opracowań podejmujących tę problematykę.
W metodach wykorzystywanych do oznaczania kofeiny w ściekach, stosowanych w laboratoriach,
można zauważyć powtarzające się trendy. Na etapie przygotowania próbki do analizy stosowana jest
ekstrakcja badanej substancji do fazy stałej. Co do kolumienek SPE, to z uwagi na ciągły rozwój
w tej dziedzinie i odkrycia coraz to bardziej selektywnych wypełnień, sprawa nie jest rozstrzygnięta,
chociaż najczęściej jest stosowana Oasis HLB. W metodach chromatograficznych decyzja
o stosowaniu chromatografii gazowej czy cieczowej zależy od dostępności aparatury, ale z przepro-
wadzonego przeglądu literaturowego wynika, że jedną z najczęściej stosowanych metod jest
wysokosprawna chromatografia cieczowa. Połączenie metod chromatograficznych ze spektrometrią
mas, umożliwia potwierdzenie identyfikacji kofeiny w próbach. Do opracowania szczegółów metod
analitycznych, polecanych do oznaczania kofeiny, zarówno w ściekach jak i w wodzie, konieczne są
dalsze badania nad tym zagadnieniem, umożliwiające opracowanie odpowiednich norm
postępowania. Istniejące Normy Polskie nie dotyczą tego typu oznaczeń.
Literatura
[1] Barber L.B., Brown G.K., Zaugg S.D.: Potential endocrine disrupting organic chemicals in treated
municipal wastewater and river water.
American Chemical Society, s. 97-123, 2000.
[2] Barnes K.K., Kolpin D.W., Furlong E.T., Zaugg S.D., Meyer M.T., Barber L.B.: A national
reconnaissance of pharmaceuticals and other organic wastewater contaminants in the United States –
I
. Groundwater, Science of the Total Environment, Vol. 402, s. 192-200, 2008.
[3] Bendz D., Paxéus N.A., Ginn T.R., Loge F.J.: Occurrence and fate of pharmaceutically active
compounds in the environment
, a case study: Höje River in Sweden, Journal of Hazardous Materials,
Vol. 122, s. 195-204, 2005.
[4] Buszka P.M., Yeskis D.J., Kolpin D.W., Furlong E.T., Zaugg S.D., Meyer M.T.: Waste-Indicator and
Pharmaceutical Compounds in Landfill-Leachate-Affected Ground Water near Elkhart
, Indiana, 2000–
2002
. Bull Environ Contam Toxicol, Vol. 82, s. 653-659, 2009.
[5] Cahill J.D., Furlong E.T., Burkhardt M.R., Kolpin D.W., Anderson L.G.: Determination of
pharmaceutical compounds in surface and ground-water samples by solid-phase extraction and high
performance liquid chromatography-electrospray ionization mass spectrometry
. J Chromatogr A 1041,
s. 171-180, 2004.

Jagoda A., Dąbrowska B., Żukowski W.: Kofeina jako wskaźnik antropogenicznego zanieczyszczenia …
262
[6] Dsikowitzky L., Schwarzbauer J., Littke R.: Distribution of polycyclic musks in water and particulate
matter of the Lippe River (Germany)
. Organic Geochemistry, Vol. 33, s.1747-1758, 2002.
[7] Dsikowitzky L., Schwarzbauer J., Littke R.: The anthropogenic contribution to the organic load of the
Lippe River (Germany). Part II: quantification of specific organic contaminants.
Chemosphere, Vol.
57, s. 1289-1300, 2004.
[8] Focazio M.J., Kolpin D.W., Barnes K.K., Furlong E.T., Meyer M.T., Zaugg S.D., Barber L.B.,
Thurman M.E.: A national reconnaissance for pharmaceuticals and other organic wastewater
contaminants in the United States - II) Untreated drinking water sources, Science of the Total
Environment 402, s. 201-216, 2008.
[9] Gómez M.J., Mart nez Bueno M.J., Lacorte S., Fernández-Alba A.R., Agüera A.: Pilot survey
monitoring pharmaceuticals and related compounds in a sewage treatment plant located on the
Mediterranean coast
. Chemosphere, Vol.66, s. 993-1002, 2007.
[10] http://leki-informacje.pl/jamnik/img/galeriaplikow/3/etopiryna_spc.pdf, (aktualizacja: 13.06.2010).
[11] http://medycynasportowa.pl/download/doping_code_e.pdf, (aktualizacja: 13.06.2010).
[12] http://www.cbs.nl/en-GB/menu/themas/inkomen-bestedingen/publicaties/artikelen/archief/2007/2007-
2344-wm.htm, (dostęp: 13.06.2010).
[13] http://www.filizankasmakow.pl/index.php?option=com_content&view=article&id=98%3Aspoycie-
kawy-przez-polakow-&catid=42%3Amarketing&Itemid=81, (dostęp: 13.06.2010).
[14] http://www.pg.gda.pl/chem/Dydaktyka/Analityczna/MISC/hyph-tech.pdf, dostęp: 13.06.2010.
[15] http://www.stat.gov.pl/cps/rde/xbcr/gus/PUBL_wz_budzety_gospodarstw_domowych_w_2008.pdf,
dostęp: 13.06.2010.
[16] Jarosz M., Wierzejska R., Mojska H., Świderska K., Siuba M.: Zawartość kofeiny w produktach
spożywczych.,
Bromat. Chem. Toksykol. – XLII. 3, s. 776-781, 2009.
[17] Kosma
a
C.I., Lambropoulou
b
D.A., Albanis
a
T.A.: Occurrence and removal of PPCPs in municipal
and hospital wastewaters in Greece.
Journal of Hazardous Materials, Vol.179, s. 804-817, 2010.
[18] Lin A.Y.-C., Yu T.-H., Lateef S.K.: Removal of pharmaceuticals in secondary wastewater treatment
processes in Taiwan.
Journal of Hazardous Materials, Vol. 167, s. 1163-1169, 2009.
[19] Lin A.Y.-C., Yu T.-H., Lin C.F.: Pharmaceutical contamination in residential, industrial, and agricul-
tural waste streams: Risk to aqueous environments in Taiwan.
Chemosphere, Vol.74, s. 131-141, 2008.
[20] Loos R., Locoro G., Contini S.: Occurrence of polar organic contaminants in the dissolved water
phase of the Danube River and its major tributaries using SPE-LC-MS2 analysis
. Water Research, Vol.
44, s. 2325-2335, 2010.
[21] Mandel H.G.: Update on caffeine consumption, disposition and action, Food and Chemical
Toxicology, Vol. 40, s. 1231-1234, 2002.
[22]
Moldovan Z., Chira R., Alder A.C.: Environmental exposure of pharmaceuticals and musk fragrances
in the Somes River before and after upgrading the municipal wastewater treatment plant Cluj-Napoca,
Romania.
Environ Sci Pollut Res, Vol. 16 (Suppl 1), s. 46-54, 2009.
[23]
Moldovan Z., Schmutzer G., Tusa F., Calin R., Alder A.C.: An overview of pharmaceuticals and
personal care products contamination along the river Somes watershed, Romania
. J Environ Monit,
Vol. 9, s. 986-993, 2007.
[24]
Moldovan Z.: Occurrences of pharmaceutical and personal care products as micropollutants in rivers
from Romania
. Chemosphere, Vol. 64, s. 1808-1817, 2006.
[25]
Molski M.: Chemia piękna. Wydawnictwo Naukowe PWN, 2009.
[26] Siegener R., Chen R.F.: Caffeine in Boston Harbor seawater. Marine Pollution Bulletin, Vol. 44, s.
383-387, 2002.
[27] Stackelber P.E., Furlongb E.T., Meyerc M.T., Zaugg S.D., Hendersond A.K., Reissmand D.B.:
Persistence of pharmaceutical compounds and other organic wastewater contaminants in a conventional
drinking-watertreatment plant
. Science of the Total Environment, Vol. 329, s. 99-113, 2004.
[28]
Togola A., Budzinski H.: Analytical development for analysis of pharmaceuticals in water samples by
SPE and GC–MS
. Anal Bioanal Chem, Vol. 388, s. 627-635, 2007.
[29]
Verenitch S.S., Mazumder A.: Development of a methodology utilizing gas chromatography ion-trap
tandem mass spectrometry for the determination of low levels of caffeine in surface marine and
freshwater samples
. Anal Bioanal Chem, Vol. 391, s. 2635-2646, 2008.

V Krakowska Konferencja Młodych Uczonych, Kraków 2010
263
AGNIESZKA JAGODA, BARBARA DĄBROWSKA, WITOLD ŻUKOWSKI
Caffeine as environmental anthropogenic contamination
– determination’s methods
Keywords
caffeine – anthropogenic water pollution – analytical methods
Abstract
Caffeine - 1,3,7-trimethylxanthine - is one of the ingredients in coffee, tea, energy drinks, drugs and even
in cosmetics. Although it is well metabolized by the human body, its environmental concentration increases.
Presence of caffeine in ground and surface waters gives the possibility to use it as the indicator of places
where the illegal sewage discharge takes place. An aim of the current paper is to present a limited number of
analytical methods for the determination of caffeine in the environmental samples.

Wyszukiwarka
Podobne podstrony:
Instrukcja Naturalne i Antropogenne zanieczyszczenia srodowiska II I OS, Matematyka UP WROC, Ćwiczen
Rodzaje zanieczyszczeń środowiska
02 Zanieczyszczenie środowiskaid 3460 ppt
WYROK - ZANIECZYSZCZANIE ŚRODOWISKA, OCHRONA ŚRODOWISKA
Cytogenetyczne i?kteryjne testy monitorowania skutków zanieczyszczenia środowiska
,Analiza chemicznych zanieczyszczeń środowiska , Zasada powstawania widma mas
zanieczyszczenia środowiska
Hałas zanieczyszczanie środowiska
4 źródła zanieczyszczeń środowiska
,Analiza chemicznych zanieczyszczeń środowiska , Chromatografia
Rodzina jako naturalne r, Przedszkole rodzina środowisko dziecka
Wykład I Antropologia jako nauka, ANTROPOLOGIA
,Analiza chemicznych zanieczyszczeń środowiska , specjacja
,Analiza chemicznych zanieczyszczeń środowiska , chemometria
Wpływ zanieczyszczeń środowiska na zdrowie człowieka, Studia, 1-stopień, inżynierka, Ochrona Środowi
Zanieczyszczenie środowiska naturalnego
gospodarka wykład III, Zanieczyszczenia środowiska jest to dziedzina ochrony środowiska, którą zaczę
Możliwości ograniczenia negatywnych skutków zanieczyszczenia środowiska metalami ciężkimi ppt
więcej podobnych podstron