W poszukiwaniu leku doskonałego...
Działania niepożądane: W trakcie leczenia mogą
wystąpić: pocenie się, nudności, wymioty, krwawienie z
przewodu pokarmowego, zaostrzenie (nawrót) choroby wrzodowej, zaburzenia krzepnięcia krwi, zwiększone
krwawienia miesiączkowe. Uważa się, że kwas acetylosalicylowy jako hapten może prowadzić
do reakcji
uczuleniowych typu dychawicy oskrzelowej. Rzadko powoduje reakcje uczuleniowe pod postacią
napadów
duszności, zmian skórnych, rumienia, pokrzywki. Większe dawki lub długotrwałe stosowanie może
prowadzić
do śródmiąższowego zapalenia nerek, przyspieszenia oddechu, niewydolności krążenia, zaburzeń
równowagi kwasowo-zasadowej (przejściowa zasadowica
a następnie kwasica), stanów zamroczenia,
pobudzenia, omamów, drgawek (zwłaszcza u dzieci). Wyjątkowo powoduje zaburzenia o.u.n. (ataksja,
zamroczenie, zaburzenia wzroku i słuchu). Opisano pojedyncze przypadki zaburzenia czynności nerek i
wątroby, hipoglikemii, ciężkich reakcji skórnych.
Nie stosować
w III trymestrze ciąży (może powodować
wady płodu i komplikacje w czasie porodu). W I i II trymestrze ciąży stosować
tylko po rozważeniu stosunku
ryzyka do oczekiwanych korzyści. Salicylany przenikają
w niewielkich ilościach do mleka matki. W
przypadku regularnego przyjmowania dużych dawek (300 mg/dobę) karmienie piersią
powinno być
wcześniej przerwane ze względu na zagrożenie dla dziecka.
Działania niepożądane: W trakcie leczenia mogą
wystąpić: pocenie się, nudności, wymioty,
krwawienie z
przewodu pokarmowego
, zaostrzenie (nawrót) choroby wrzodowej,
zaburzenia krzepnięcia krwi
, zwiększone
krwawienia miesiączkowe. Uważa się, że kwas acetylosalicylowy jako hapten może prowadzić
do reakcji
uczuleniowych typu dychawicy oskrzelowej. Rzadko powoduje reakcje uczuleniowe pod postacią
napadów
duszności, zmian skórnych, rumienia, pokrzywki. Większe dawki lub długotrwałe stosowanie może
prowadzić
do śródmiąższowego zapalenia nerek, przyspieszenia oddechu, niewydolności krążenia, zaburzeń
równowagi kwasowo-zasadowej (przejściowa zasadowica
a następnie kwasica), stanów zamroczenia,
pobudzenia, omamów, drgawek (zwłaszcza u dzieci). Wyjątkowo powoduje zaburzenia o.u.n. (ataksja,
zamroczenie, zaburzenia wzroku i słuchu). Opisano pojedyncze przypadki zaburzenia czynności nerek i
wątroby, hipoglikemii, ciężkich reakcji skórnych.
Nie stosować
w III trymestrze ciąży (może powodować
wady płodu i komplikacje w czasie porodu). W I i II trymestrze ciąży stosować
tylko po rozważeniu stosunku
ryzyka do oczekiwanych korzyści. Salicylany przenikają
w niewielkich ilościach do mleka matki. W
przypadku regularnego przyjmowania dużych dawek (300 mg/dobę) karmienie piersią
powinno być
wcześniej przerwane ze względu na zagrożenie dla dziecka.
Działania niepożądane: W trakcie leczenia mogą
wystąpić: pocenie się, nudności, wymioty,
krwawienie z
przewodu pokarmowego
, zaostrzenie (nawrót) choroby wrzodowej,
zaburzenia krzepnięcia krwi
, zwiększone
krwawienia miesiączkowe. Uważa się, że kwas acetylosalicylowy jako hapten może prowadzić
do reakcji
uczuleniowych typu dychawicy oskrzelowej. Rzadko powoduje
reakcje uczuleniowe pod postacią
napadów
duszności
, zmian skórnych, rumienia, pokrzywki. Większe dawki lub długotrwałe stosowanie może
prowadzić
do śródmiąższowego zapalenia nerek, przyspieszenia oddechu,
niewydolności krążenia
, zaburzeń
równowagi kwasowo-zasadowej (przejściowa zasadowica
a następnie kwasica), stanów zamroczenia,
pobudzenia, omamów, drgawek (zwłaszcza u dzieci). Wyjątkowo powoduje zaburzenia o.u.n. (ataksja,
zamroczenie, zaburzenia wzroku i słuchu). Opisano pojedyncze przypadki zaburzenia czynności nerek i
wątroby, hipoglikemii, ciężkich reakcji skórnych.
Nie stosować
w III trymestrze ciąży (może powodować
wady płodu i komplikacje w czasie porodu). W I i II trymestrze ciąży stosować
tylko po rozważeniu stosunku
ryzyka do oczekiwanych korzyści. Salicylany przenikają
w niewielkich ilościach do mleka matki. W
przypadku regularnego przyjmowania dużych dawek (300 mg/dobę) karmienie piersią
powinno być
wcześniej przerwane ze względu na zagrożenie dla dziecka.
Działania niepożądane: W trakcie leczenia mogą
wystąpić: pocenie się, nudności, wymioty,
krwawienie z
przewodu pokarmowego
, zaostrzenie (nawrót) choroby wrzodowej,
zaburzenia krzepnięcia krwi
, zwiększone
krwawienia miesiączkowe. Uważa się, że kwas acetylosalicylowy jako hapten może prowadzić
do reakcji
uczuleniowych typu dychawicy oskrzelowej. Rzadko powoduje
reakcje uczuleniowe pod postacią
napadów
duszności
, zmian skórnych, rumienia, pokrzywki. Większe dawki lub długotrwałe stosowanie może
prowadzić
do śródmiąższowego zapalenia nerek, przyspieszenia oddechu,
niewydolności krążenia
, zaburzeń
równowagi kwasowo-zasadowej (przejściowa zasadowica
a następnie kwasica),
stanów zamroczenia
,
pobudzenia, omamów
,
drgawek (zwłaszcza u dzieci).
Wyjątkowo powoduje zaburzenia o.u.n. (ataksja,
zamroczenie,
zaburzenia wzroku i słuchu
). Opisano pojedyncze przypadki zaburzenia czynności nerek i
wątroby, hipoglikemii, ciężkich reakcji skórnych.
Nie stosować
w III trymestrze ciąży (może powodować
wady płodu i komplikacje w czasie porodu). W I i II trymestrze ciąży stosować
tylko po rozważeniu stosunku
ryzyka do oczekiwanych korzyści. Salicylany przenikają
w niewielkich ilościach do mleka matki. W
przypadku regularnego przyjmowania dużych dawek (300 mg/dobę) karmienie piersią
powinno być
wcześniej przerwane ze względu na zagrożenie dla dziecka.
Działania niepożądane: W trakcie leczenia mogą
wystąpić: pocenie się, nudności, wymioty,
krwawienie z
przewodu pokarmowego
, zaostrzenie (nawrót) choroby wrzodowej,
zaburzenia krzepnięcia krwi
, zwiększone
krwawienia miesiączkowe. Uważa się, że
kwas acetylosalicylowy
jako hapten może prowadzić
do reakcji
uczuleniowych typu dychawicy oskrzelowej. Rzadko powoduje
reakcje uczuleniowe pod postacią
napadów
duszności
, zmian skórnych, rumienia, pokrzywki. Większe dawki lub długotrwałe stosowanie może
prowadzić
do śródmiąższowego zapalenia nerek, przyspieszenia oddechu,
niewydolności krążenia
, zaburzeń
równowagi kwasowo-zasadowej (przejściowa zasadowica
a następnie kwasica),
stanów zamroczenia
,
pobudzenia, omamów,
drgawek (zwłaszcza u dzieci).
Wyjątkowo powoduje zaburzenia o.u.n. (ataksja,
zamroczenie, zaburzenia wzroku i słuchu). Opisano pojedyncze przypadki zaburzenia czynności nerek i
wątroby, hipoglikemii, ciężkich reakcji skórnych.
Nie stosować
w III trymestrze ciąży (może powodować
wady płodu i komplikacje w czasie porodu).
W I i II trymestrze ciąży stosować
tylko po rozważeniu stosunku
ryzyka do oczekiwanych korzyści. Salicylany przenikają
w niewielkich ilościach do mleka matki.
W
przypadku regularnego przyjmowania dużych dawek (300 mg/dobę) karmienie piersią
powinno być
wcześniej przerwane ze względu na zagrożenie dla dziecka.

Działania niepożądane: W trakcie leczenia mogą
wystąpić: pocenie się, nudności, wymioty, krwawienie z
przewodu pokarmowego, zaostrzenie (nawrót) choroby wrzodowej, zaburzenia krzepnięcia krwi, zwiększone
krwawienia miesiączkowe. Uważa się, że kwas acetylosalicylowy jako hapten może prowadzić
do reakcji
uczuleniowych typu dychawicy oskrzelowej. Rzadko powoduje reakcje uczuleniowe pod postacią
napadów
duszności, zmian skórnych, rumienia, pokrzywki. Większe dawki lub długotrwałe stosowanie może
prowadzić
do śródmiąższowego zapalenia nerek, przyspieszenia oddechu, niewydolności krążenia, zaburzeń
równowagi kwasowo-zasadowej (przejściowa zasadowica
a następnie kwasica), stanów zamroczenia,
pobudzenia, omamów, drgawek (zwłaszcza u dzieci). Wyjątkowo powoduje zaburzenia o.u.n. (ataksja,
zamroczenie, zaburzenia wzroku i słuchu). Opisano pojedyncze przypadki zaburzenia czynności nerek i
wątroby, hipoglikemii, ciężkich reakcji skórnych.
Nie stosować
w III trymestrze ciąży (może powodować
wady płodu i komplikacje w czasie porodu). W I i II trymestrze ciąży stosować
tylko po rozważeniu stosunku
ryzyka do oczekiwanych korzyści. Salicylany przenikają
w niewielkich ilościach do mleka matki. W
przypadku regularnego przyjmowania dużych dawek (300 mg/dobę) karmienie piersią
powinno być
wcześniej przerwane ze względu na zagrożenie dla dziecka.

Działania niepożądane: ból
głowy,
senność,
uczucie dezorientacji,
możliwe obniżenie temperatury.
Uwagi: Po przyjęciu preparatu nie należy prowadzić
pojazdów i wykonywać
czynności wymagających
koncentracji.


Lipobay
(Baycol)
działanie: obniżenie poziomu cholesterolu
działanie niepożądane:
degeneracja mięśni, około 100 zgonów

Lipobay
(Baycol) -
ceriwastatyna
działanie: obniżenie poziomu cholesterolu
działanie niepożądane:
degeneracja mięśni, około 100 zgonów
VIOXX [rofekoksyb]
działanie: przeciwbólowe w chorobach
reumatycznych
działanie niepożądane:
wzrost ciśnienia krwi, zawały serca,
udary mózgu

“It is not the strongest of the species that survive,
nor the most intelligent, but the one most
responsive to change.”
Charles Darwin
Wizja działalności |
Adamed
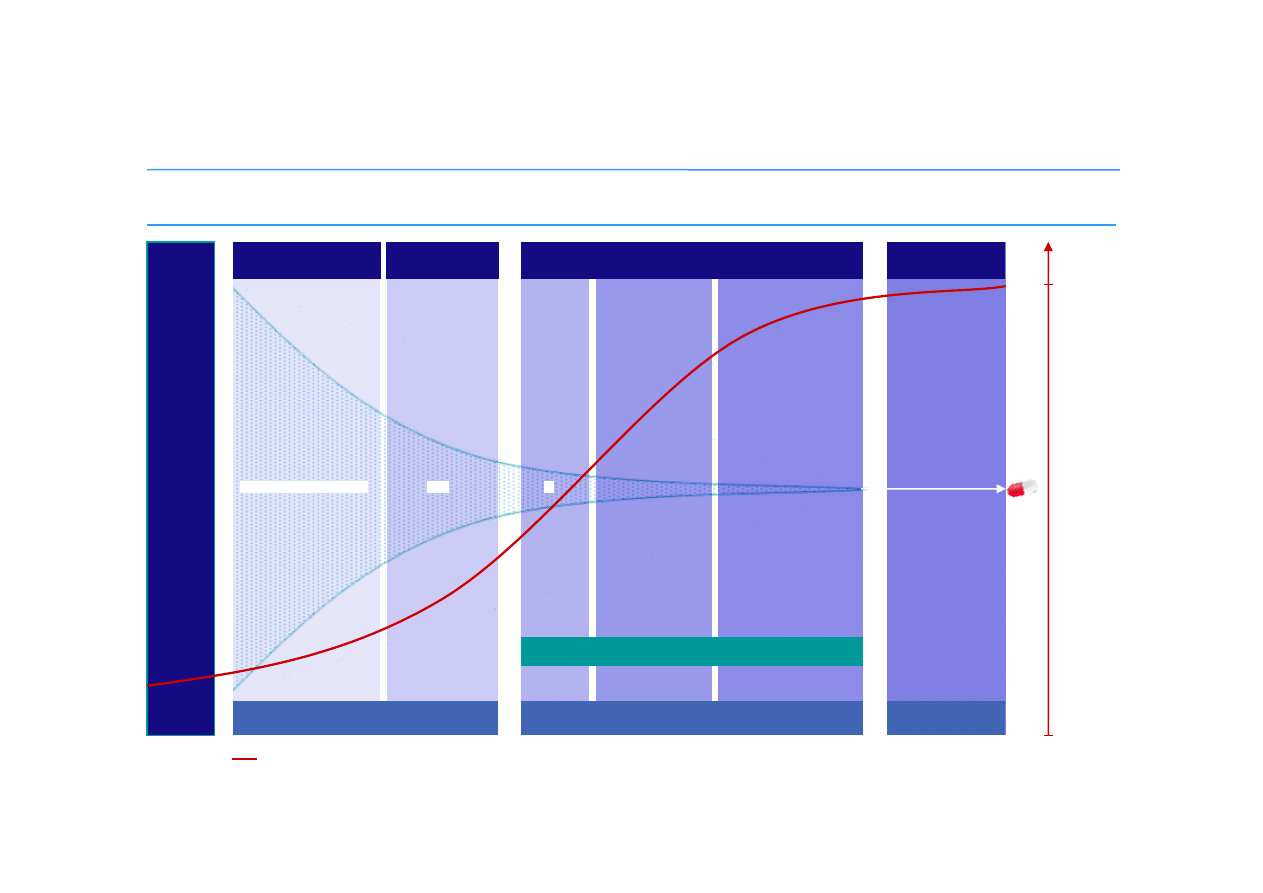
Opracowanie nowego leku i wprowadzenie go na rynek trwa około 20 lat
i pochłania 2 miliardy zł
BADANI
A
NA
UK
OWE
3-6 LAT
6-7 LAT
0,5-2 LATA
WYNALEZIENIE
LEKU
BADANIA KLINICZNE
REJESTRACJA
BADANIA
PREKLINICZNE
2 MLD ZŁ
0
NAKŁADY
INWESTYCYJNE
5 000 –
10 000 MOLEKUŁ
250
5
LICZBA OCHOTNIKÓW
FAZA I
FAZA II
FAZA III
20-100
100-500
1 000 –
5 000
SKUMULOWANE NAKŁADY INWESTYCYJNE
1 NOWY LEK
DOPUSZCZONY
NA RYNEK
PROCES R&D
NOWEGO LEKU ORYGINALNEGO
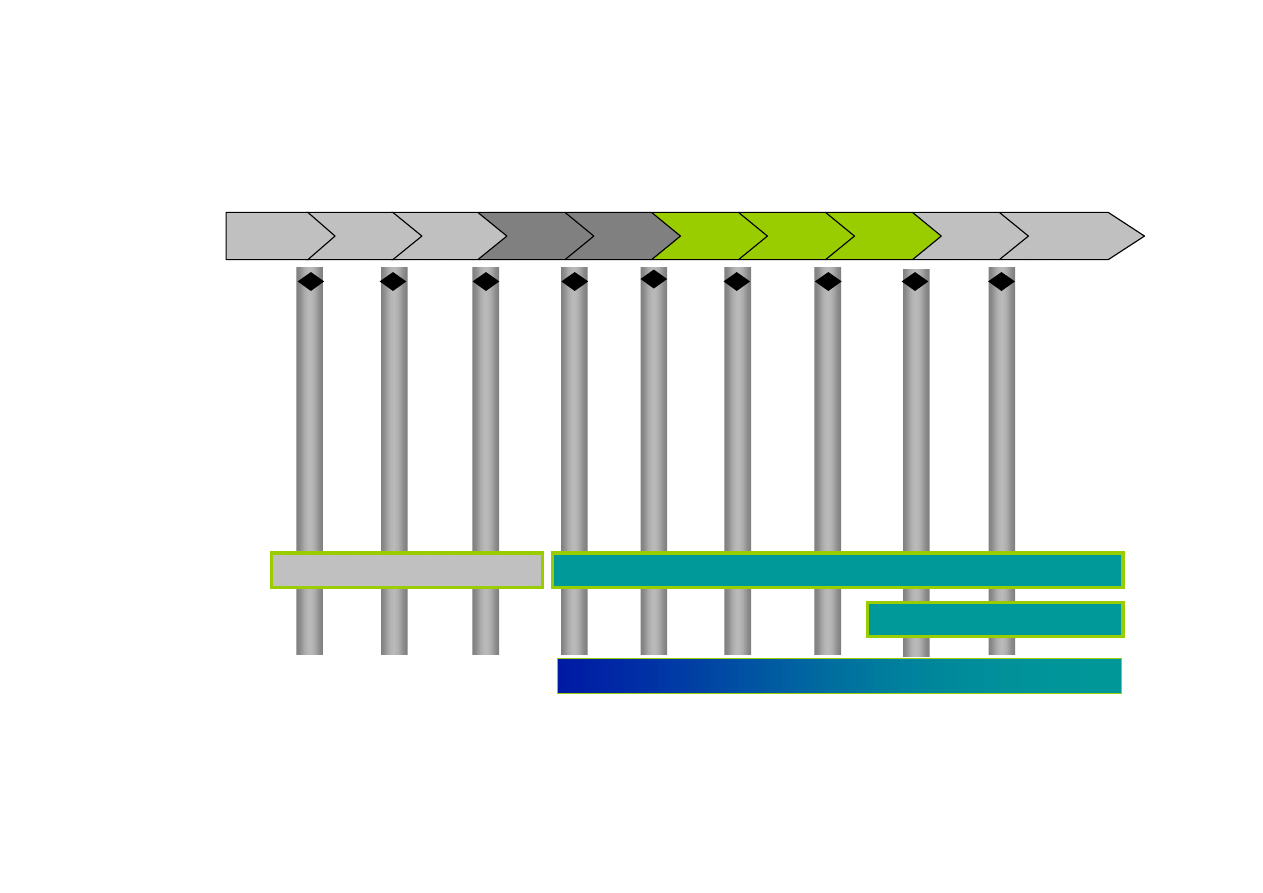
Early Target
Preclinical
Research
Clinical Research
Commercialization
Launch/
Post-Launch
Filing
Phase
3
Phase
2
Phase
1
Pre-
clinical
Lead
Opt
Hit-to-
lead
Screen
Discovery
Research Teams
Product Strategy Teams
Teams
Screen Team
Project Team
Research Project Team
Proof of Biol
ogical Activity
End of Phas
e 2
Commit To Fi
le
Commit To Launch
First in Human
Medical Affairs
Product St
ra
tegy
Team
Brand Teams
Increase in plasma glucose
and progression of disease
Glucose influx from GI tract
Impaired insulin action
(insulin desensitization)
Inadequate glucagon
suppression (α-cell dysfunction)
Acute β-cell dysfunction
(insulin undersupply)
Chronic β-cell decline
Gluconeogenesis
(Glucose generation)
α-Glucosidase
inhibitors
Metformin
TZDs
unmet need
Meglitinides
Sulfonylureas
unmet need
Unmet medical need
Unmet market
need
unmet need
Poor diagnosis rate
Niezaspokojone potrzeby medyczne
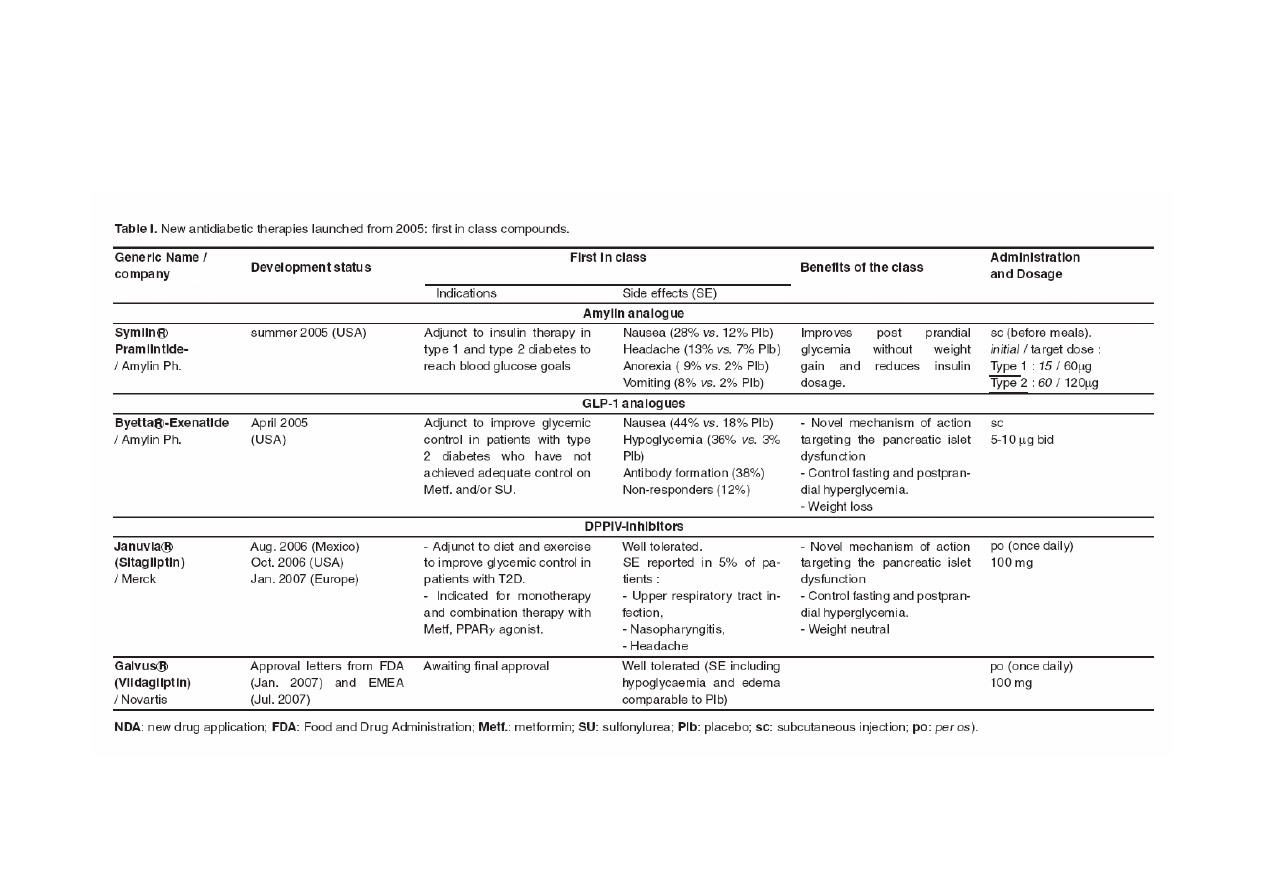
Combettes
M, Kargar
C. Newly
approved
and
promising
antidiabetic
agents.
Therapie. 2007 Jul-Aug;62(4):293-310.
Nowe obiecujące leki przeciwcukrzycowe
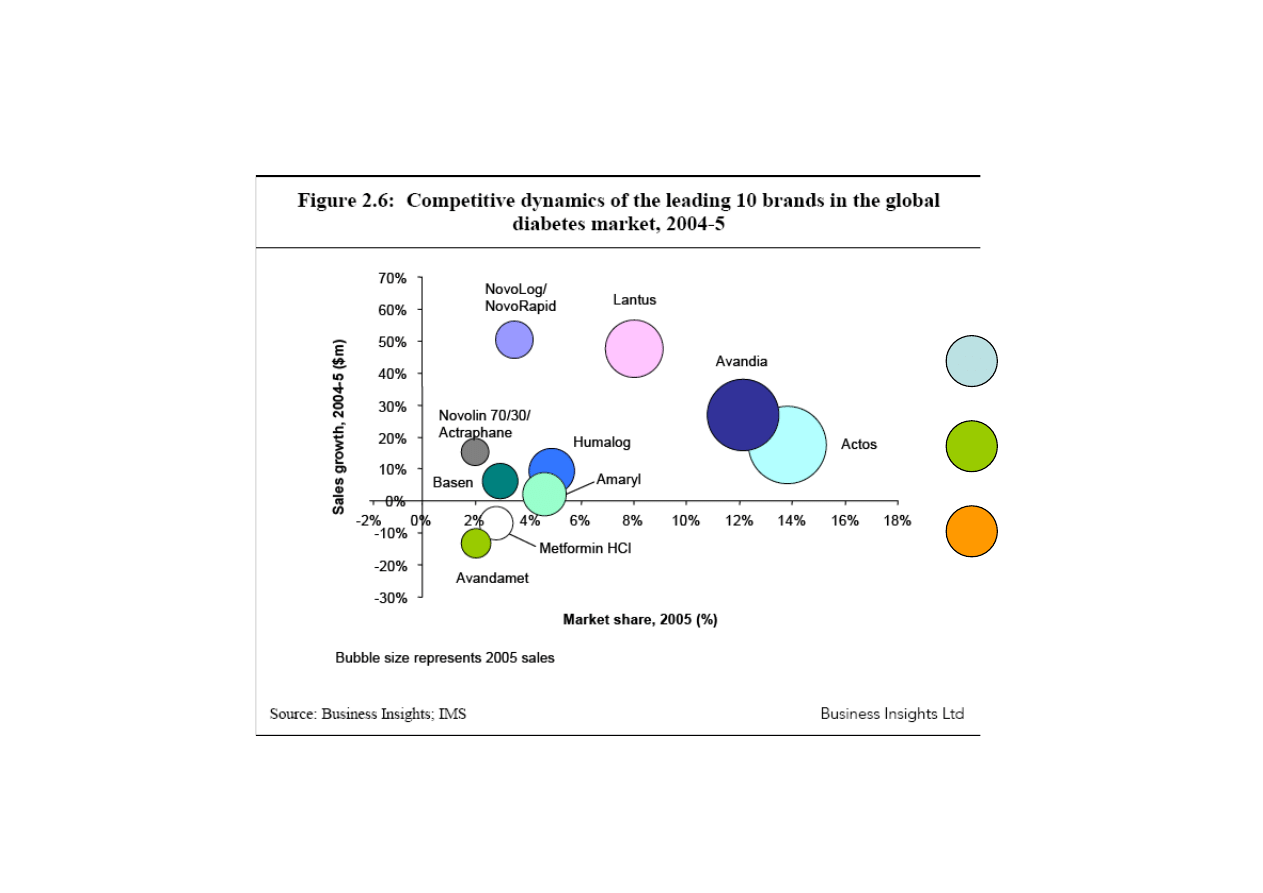
Januvia
(sitagliptyna)
Galvus
(vidagliptyna)
Byetta
(GLP-1)
2006/2008
59 R-1438
60 R-1440
61 Ro-0730699
62 solabegron (427353)
63 T-1095
64 TA-6666
65 TAK-654
66 TRX-4
67 rivoglitazone (Phase II/III)
68 Redona (denagliptin)
69 Byetta LAR
70 Diamyd
71 DiaPep277
72 liraglutide
73 saxagliptin
74 SYR-322
75 Galvus
76 Januvia
31 677954
32 anti-CD3 antibody
33 AVE-0010
34 AVE-0847
35 AVE-2268
36 AVR-118
37 BIM-51077
38 BLX-1002
39 CJC-1134-PC
40 CKD-501
41 CS-917
42 DIO-901
43 DIO-902
44 DRF-2593
45 E1-INT
46 GRC-8200
47 ISIS-113715
48 K-111
49 mecasermin (iPlex)
50 metaglidasen
51 MP-513
52 naveglitazar
53 netoglitazone
54 ONO-5129
55 PHX-1149
56 PLX-204
57 PSN-357
58 PSN-9301
1 189075
2 625019
3 716155
4 825964
5 AMG-221
6 APD-668
7 arimoclomol
8 AVE-5376
9 AVE-8134
10 AZD-6610
11 AZD-8677
12 BAY-73 7977
13 EMD-387008
14 EN-122004
15 KRP-104
16 MB-07803
17 MBX-2044
18 MK-0533
19 MK-0893
20 MK-0941
21 NN-0606
22 NN-9101
23 PSN-010
24 R-1439
25 SGLT-2 lead (BMS)
26 SSR-162369
27 SUN-E7001
28 TH-0318
29 TS-021
30 TS-033
Phase
II
Phase
III
Phase
I
Registration
75
76
1
2
3
4
5
8
7
9
10
6
12
11
13
14
15
16
18
19
17
20
21
22
23
24
25
26
27
28
29
30
59
44
50
31
32
33
34
35
37
39
40
36
42
41
43
45
46
49
48
47
54
51
55
56
60
63
62
65
52
58
57
61
64
67
66
68
53
38
73
74
72
70
71
69
Nowe obiecujące leki przeciwcukrzycowe
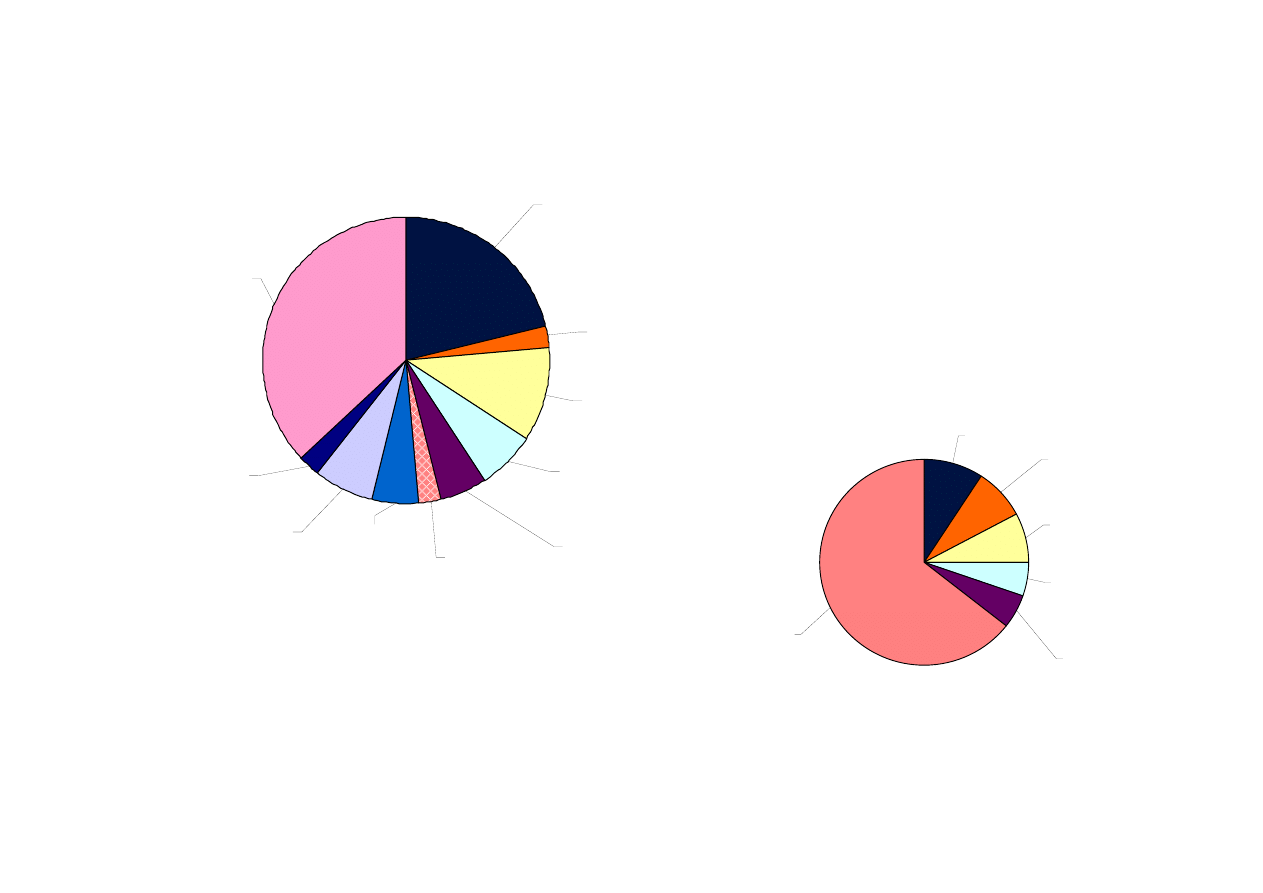
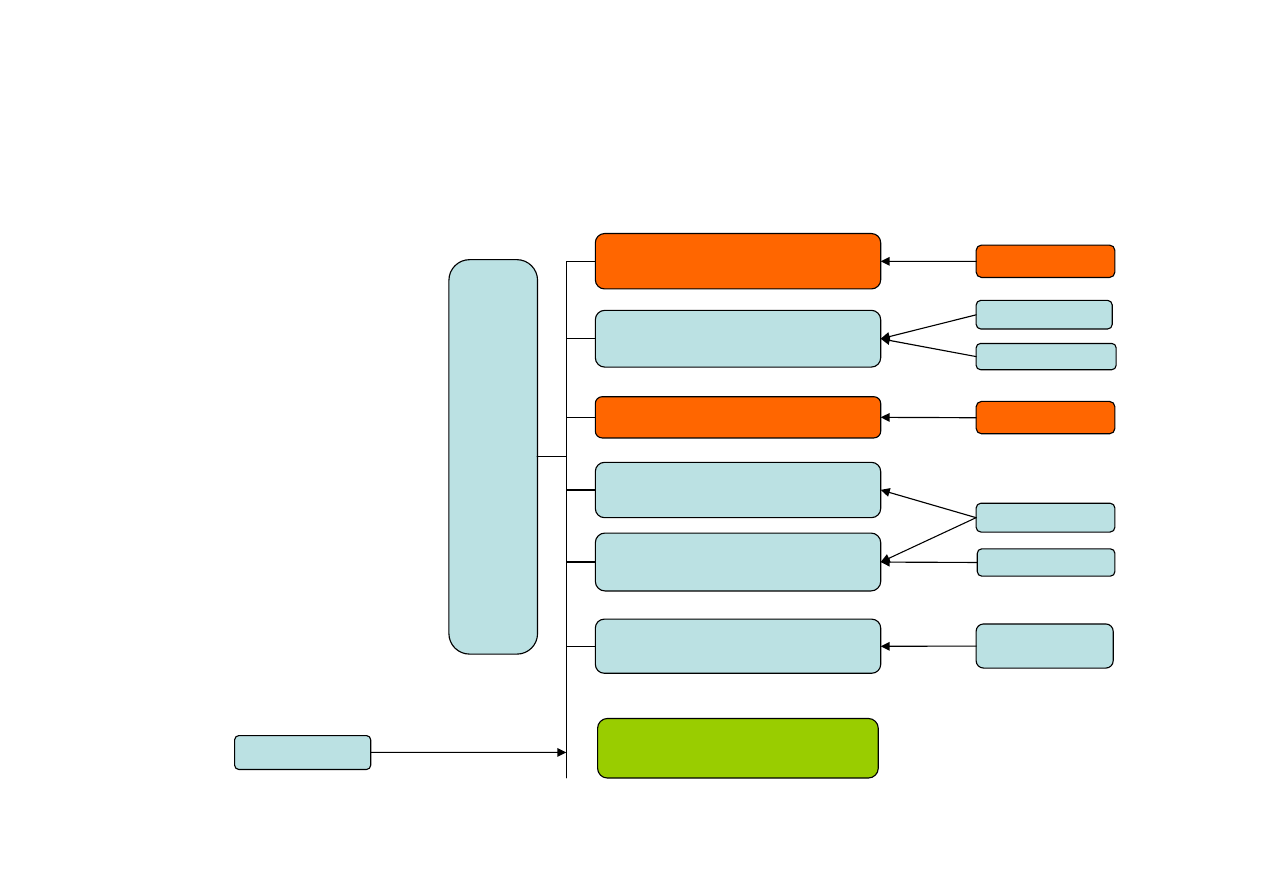
DPP-4 inhibitor:
16 agents
Fructose
biphosphatase
inhibitor: 2
agents (3%)
GLP-1 agonist:
8 agents
PPAR dual (α,γ)
modulator: 5
agents
PPAR pan (αγδ)
modulator: 4
agents
PPAR-α
modulator: 2
agents (3%)
PPAR-γ
modulator:
4 agents
SGLT-2 inhibitor:
5 agents
Vaccine: 2
agents (3%)
Others (including
"unspecified"
mechanisms):
28 agents
36%
20%
11%
7%
5%
7%
5%
Novo
Nordisk:
4 agents
Merck & Co:
4 agents
Roche AG:
6 agents
Sanofi-
Aventis:
6 agents
GSK:
7 agents
Residual
projects:
49 agents
5%
65%
5%
8%
8%
9%
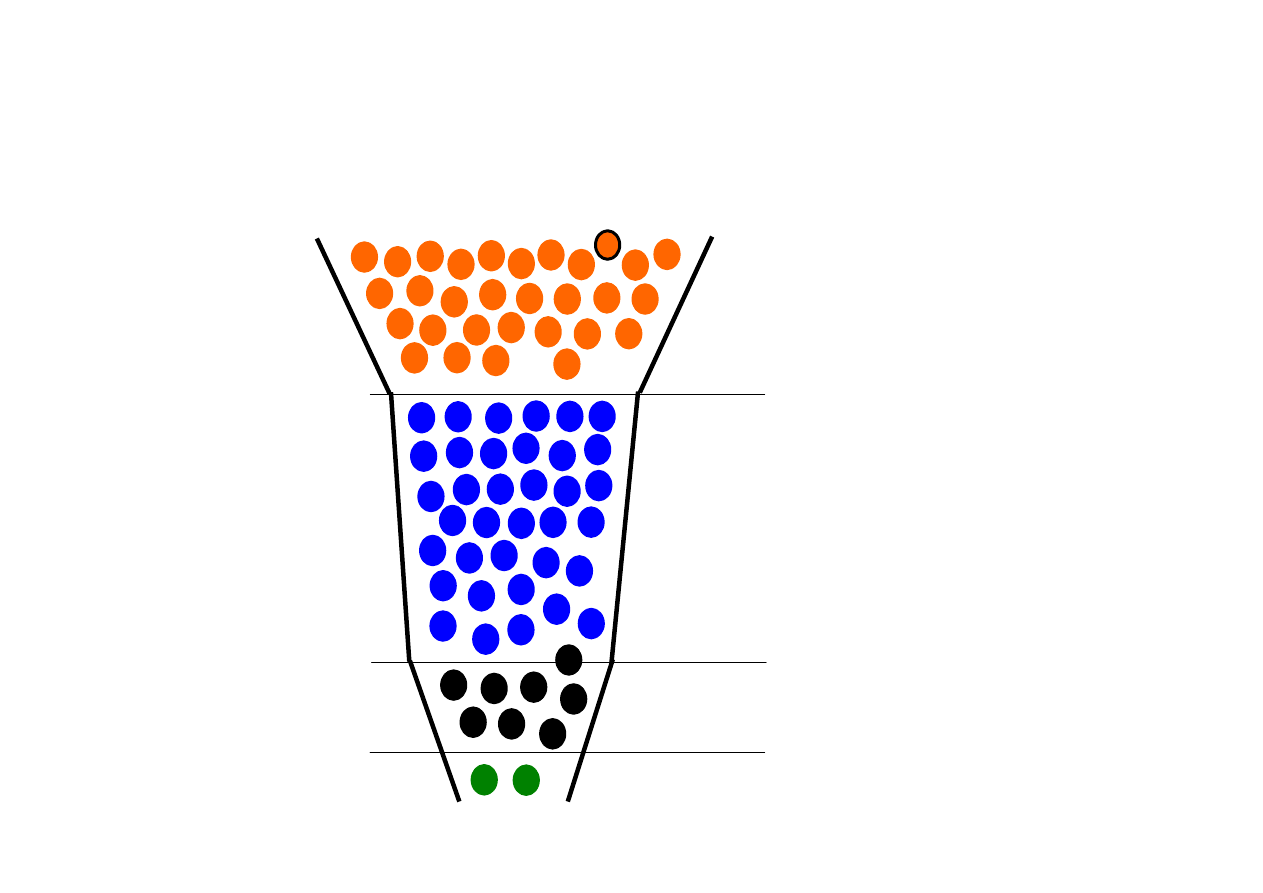
Nowe obiecujące leki przeciwcukrzycowe
Combettes
M, Kargar
C. Newly
approved
and
promising
antidiabetic
agents.
Therapie. 2007 Jul-Aug;62(4):293-310.
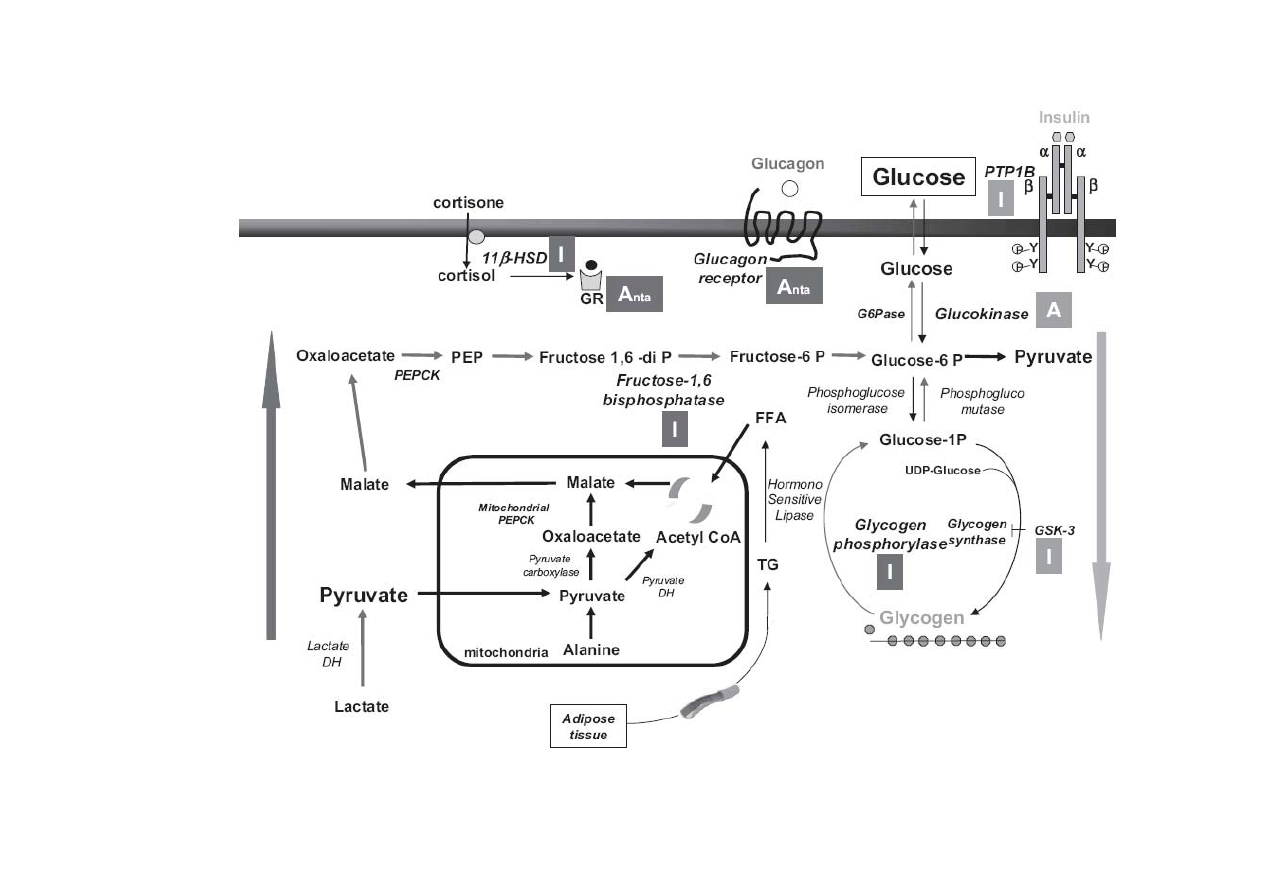
Nowe obiecujące leki przeciwcukrzycowe
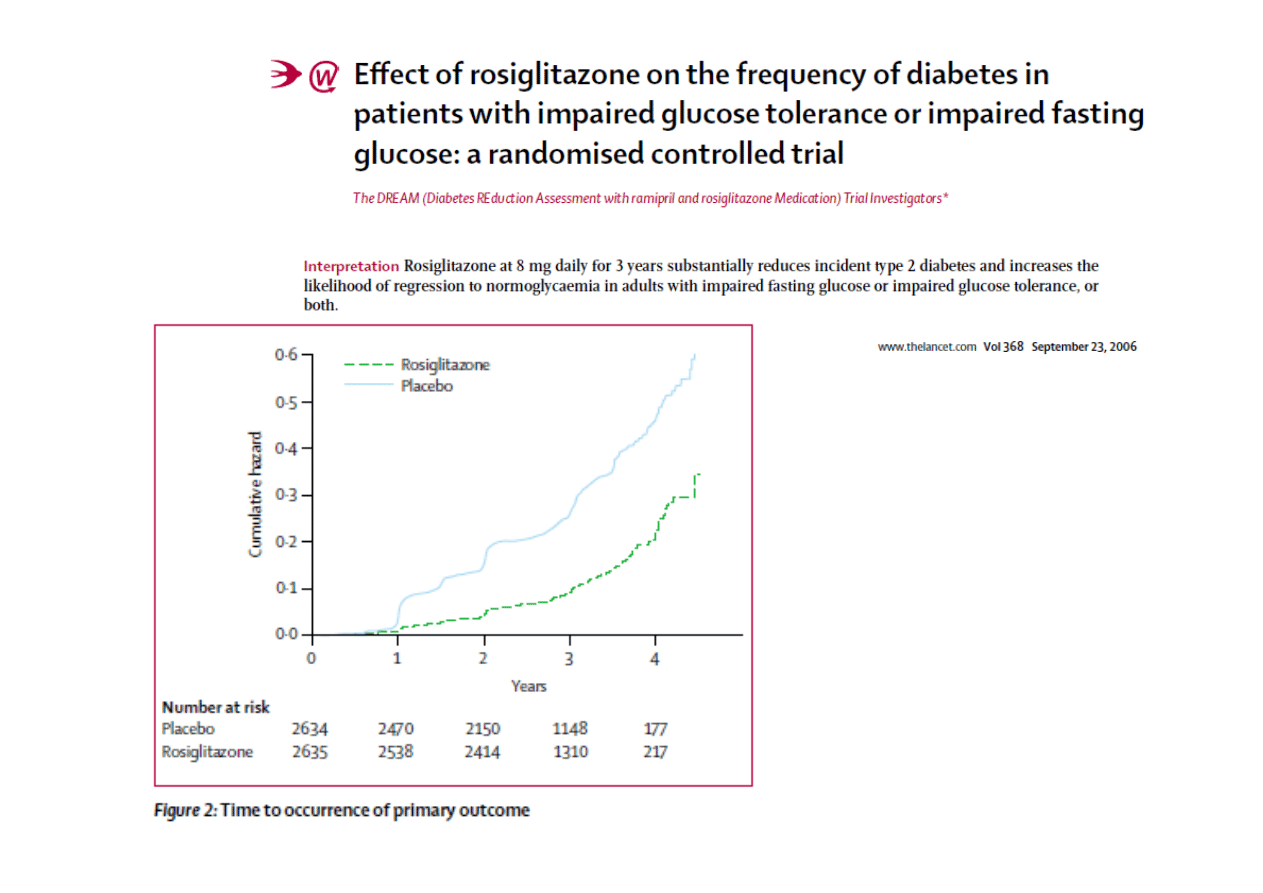
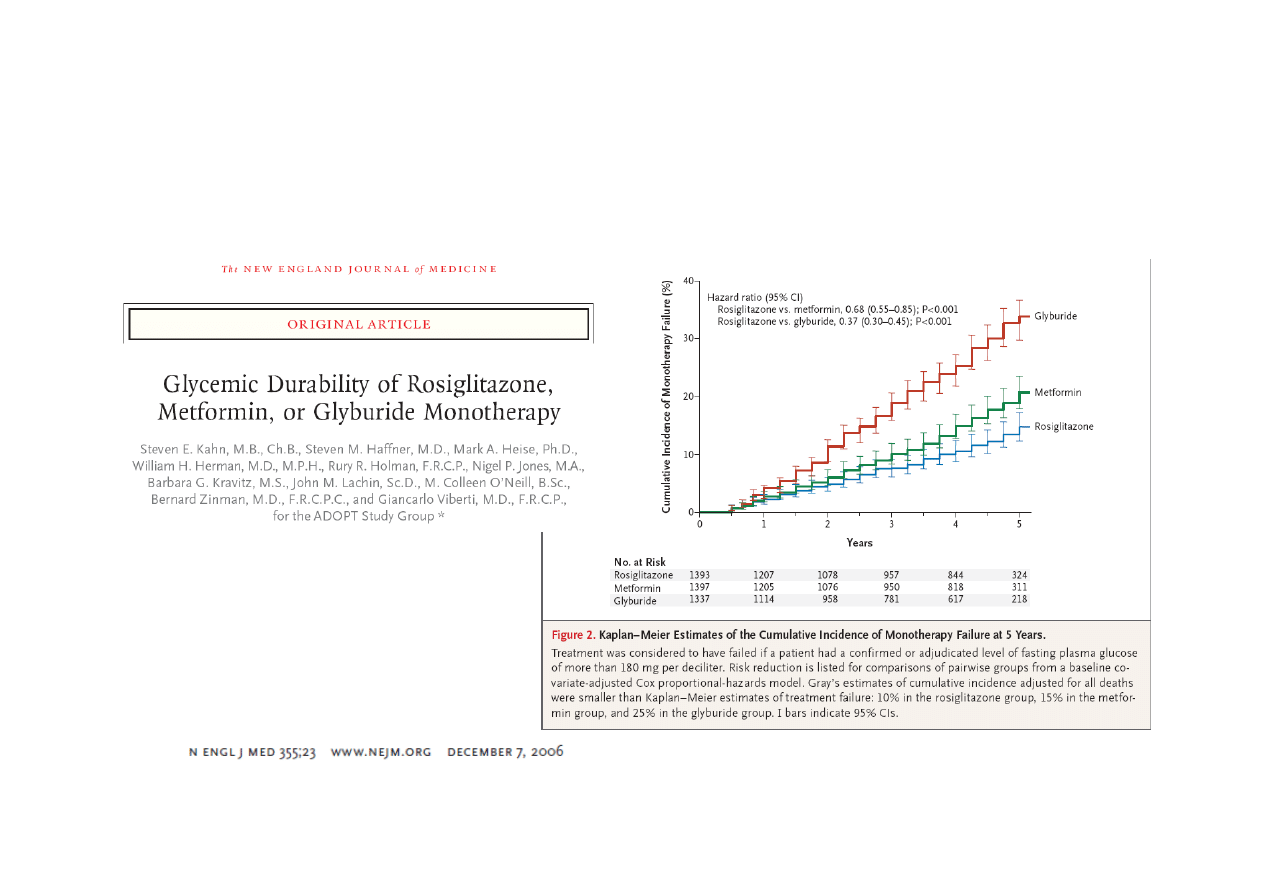
A Diabetes Outcome Progression Trial ADOPT



FDA Environment
Dr. Nissen
served as a member of the CardioRenal
Advisory
Panel of Food and Drug Administration (FDA)
for five years, and as chairman of the final year of his
membership. He continues to serve as a periodic advisor
to several FDA committees as a Special Government Employee.
Dr. Nissen
was also named in 2007 by
SmartMoney
Magazine as one of the "country’s 30 most
powerful forces in business and finance
.
Cardiovascular Medicine
Department Chair
Director, Joseph J. Jacobs Center for
Thrombosis and Vascular Biology
Phone: (216) 445-6852
Location: Cleveland Clinic Main Campus
Mail Code J2-3
9500 Euclid Avenue
Cleveland, OH 44195
Steven Nissen, M.D.

FDA Environment
Troglitazone
Rosiglitazone
Pioglitazone
23
13
5
12
Pooled TZDs
10
12
26
5
2
0
2
Matrix
metalloproteinase
12 –
20 LAT
(od znalezienie substancji aktywnej
do wprowadzenie jej do aptek)
500 000 mln
USD
(koszt całej operacji)

Badania podstawowe (2 -
7 lat)
określenie celu farmaceutycznego (choroby)
znalezienie substancji aktywnej biologicznie
-
źródła naturalne (rośliny)
-
synteza chemiczna
modyfikowanie substancji aktywnej (pochodne, sole)

Badania podstawowe (2 -
7 lat)
określenie celu farmaceutycznego (choroby)
znalezienie substancji aktywnej biologicznie
-
źródła naturalne (rośliny)
-
synteza chemiczna
modyfikowanie substancji aktywnej
Badania przedkliniczne
(2 -
3 lata)
farmakokinetyka
farmakodynamika
FARMAKOKINETYKA:
badanie procesu
wchłaniania danej substancji (biodostępność),
wiązania z białkami krwi, dystrybucji i usuwania
z ustroju
(tempo metabolizmu leku).
FARMAKODYNAMIKA:
zajmuje się
mechanizmem działania
substancji aktywnej,
działaniami niepożądanymi, interakcjami
z innymi lekami
oraz
toksycznością.

Badania podstawowe (2 -
7 lat)
określenie celu farmaceutycznego (choroby)
znalezienie substancji aktywnej biologicznie
-
źródła naturalne (rośliny)
-
synteza chemiczna
modyfikowanie substancji aktywnej
Badania przedkliniczne
(2 -
5 lata)
farmakokinetyka
farmakodynamika
toksyczność

Badania podstawowe (2 -
7 lat)
określenie celu farmaceutycznego (choroby)
znalezienie substancji aktywnej biologicznie
-
źródła naturalne (rośliny)
-
synteza chemiczna
modyfikowanie substancji aktywnej
Badania przedkliniczne
(2 -
3 lata)
farmakokinetyka
farmakodynamika
toksyczność
Badania kliniczne (5 -
10 lat)
Faza I
–
około 100 -
500 zdrowych ochotników
Faza II
–
około 1000 chorych
Faza III
–
kilka do kilkunastu tysięcy ochotników
(
najlepiej !!
) w różnych ośrodkach na świecie
(
przygotowanie wniosku o rejestrację
nowego leku
)
Faza IV –
poszerzenie wiedzy o stosowanym leku
Badania podstawowe (2 -
7 lat)
określenie celu farmaceutycznego (choroby)
znalezienie substancji aktywnej biologicznie
-
źródła naturalne (rośliny)
-
synteza chemiczna
modyfikowanie substancji aktywnej
Badania przedkliniczne
(2 -
3 lata)
farmakokinetyka
farmakodynamika
toksyczność
Badania kliniczne (5 -
10 lat)
Faza I
–
około 100 -
500 zdrowych ochotników
Faza II
–
około 1000 chorych
Faza III
–
kilka do kilkunastu tysięcy ochotników
(
najlepiej !!
) w różnych ośrodkach na świecie
(
przygotowanie wniosku o rejestrację
nowego leku
)
Faza IV –
poszerzenie wiedzy o stosowanym leku

Pre‐IND meeting – package content
Etap badań
podstawowych
w poszukiwaniu choroby: BADANIA NIEINTERWENCYJNE
Etap badań
podstawowych
w poszukiwaniu choroby: BADANIA NIEINTERWENCYJNE
[brak ingerencji w życie człowieka,
charakter wyłącznie pasywny
Etap badań
podstawowych
w poszukiwaniu choroby: BADANIA NIEINTERWENCYJNE
[brak ingerencji w życie człowieka,
charakter wyłącznie pasywny
całkowicie bierna obserwacja wybranej grupy
]
Etap badań
podstawowych
w poszukiwaniu choroby: BADANIA NIEINTERWENCYJNE
[brak ingerencji w życie człowieka,
charakter wyłącznie pasywny
całkowicie bierna obserwacja wybranej grupy
]
--
określanie związków przyczynowo-
skutkowych między danym czynnikiem a
wystąpieniem schorzenia
Etap badań
podstawowych
w poszukiwaniu choroby: BADANIA NIEINTERWENCYJNE
[brak ingerencji w życie człowieka,
charakter wyłącznie pasywny
całkowicie bierna obserwacja wybranej grupy
]
--
określanie związków przyczynowo-
skutkowych między danym czynnikiem a
wystąpieniem schorzenia
zaburzenie metaboliczne [
metabolizm dopaminy
] ----
zachowanie
palenie papierosów ----
rozwój nowotworów
dieta [
nadmiar węglowodanów
] ----
zespół
metaboliczny

Badania epidemiologiczne:
przekrojowe
--
zależność
między cechą
a schorzeniem
w określonym punkcie czasowym
obserwacyjne
--
obserwacja grupy osób [
konkretne schorzenie
]
przez dłuższy czas

Badania epidemiologiczne:
prospektywne
--
dane zbierane na bieżąco,
badanie trwa określoną
wcześniej długość
czasu
retrospektywnych
--
informacje z różnych baz danych
np. dokumentacja medyczna, także karty zgonu
punktem wyjścia jest PUNKT KOŃCOWY
KONTROLOWANE BADANIA EPIDEMIOLOGICZNE
T. Dyszynski, T. Lietz
E +
E -
Ekspozycja (E)
E= np. palenie tytoniu, dieta, tryb życia, stosowanie leków,
obecność czynników ryzyka danej choroby, czynniki
środowiskowe
osiągnięty
punkt
końcowy
osiągnięty
punkt
końcowy (np.
zawa serca)
Grupa eksponowana
Grupa nieeksponowana
CZAS
CZAS
Obserwacja )
Etap badań
podstawowych
poszukiwanie substancji aktywnych biologicznie
!
--
hamowanie całego procesu [GLUKONEOGENEZY]
--
przyspieszone utlenianie kwasów tłuszczowych
--
hamowanie [indukcja] szlaku sygnałowego
--
aktywacja [wyłączenie] konkretnego genu
--
hamowanie proliferacji komórek
Etap badań
podstawowych
poszukiwanie substancji aktywnych biologicznie
!
--
substancje naturalne [GŁÓWNIE] pochodzenia roślinnego [DIETA]
--
izolowanie i określenie struktury związku aktywnego
--
synteza analogów
Etap badań
podstawowych
poszukiwanie substancji aktywnych biologicznie
!
--
substancje naturalne [GŁÓWNIE] pochodzenia roślinnego [DIETA]
--
izolowanie i określenie struktury związku aktywnego
--
synteza analogów
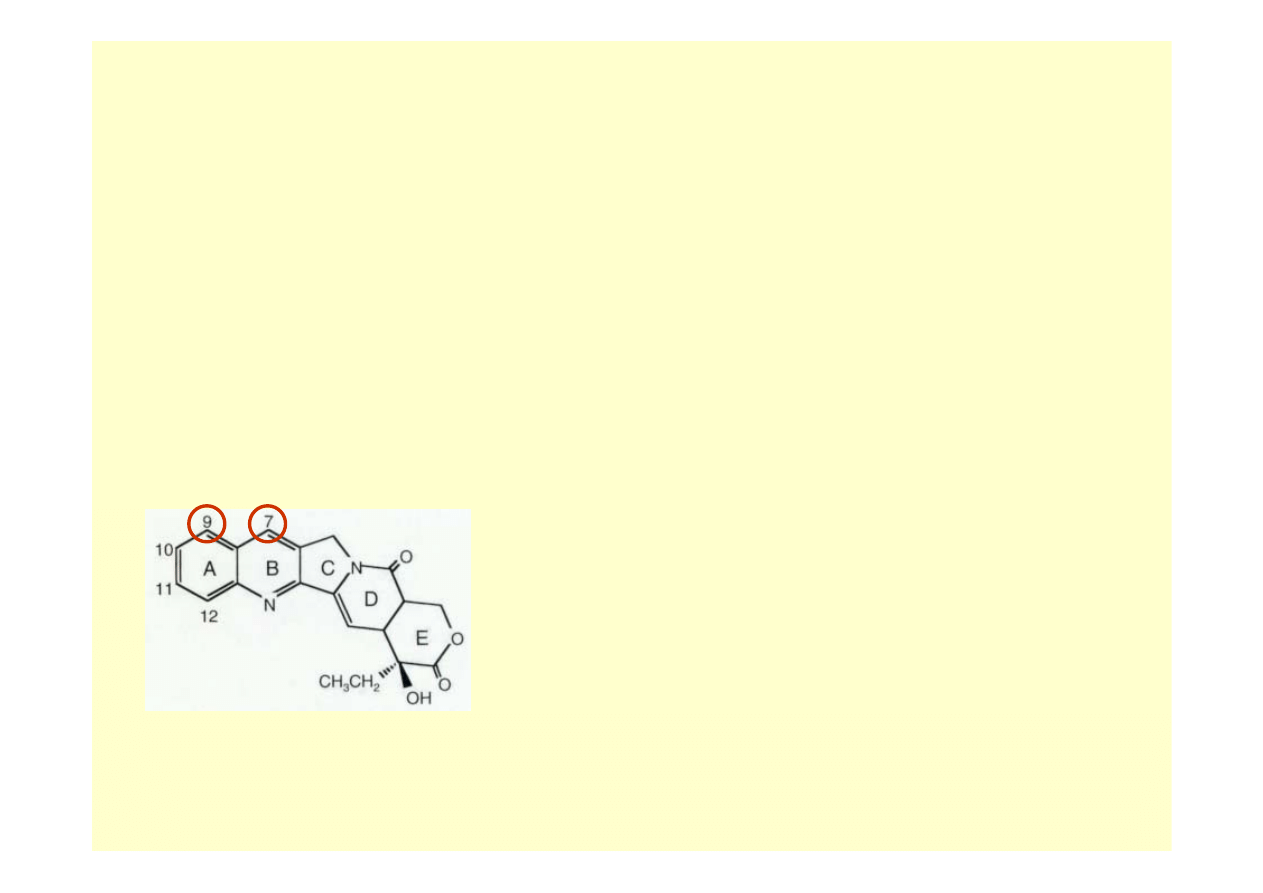
kamptotecyna
(CPT) Camptotheca acuminata – Xi Shu
Etap badań
podstawowych
poszukiwanie substancji aktywnych biologicznie
!
--
substancje naturalne [GŁÓWNIE] pochodzenia roślinnego [DIETA]
--
izolowanie i określenie struktury związku aktywnego
--
synteza analogów
kamptotecyna
(CPT) Camptotheca acuminata – Xi Shu
C11
C10
C9
C7
CPT
H
H
H
H
Etap badań
podstawowych
poszukiwanie substancji aktywnych biologicznie
!
--
substancje naturalne [GŁÓWNIE] pochodzenia roślinnego [DIETA]
--
izolowanie i określenie struktury związku aktywnego
--
synteza analogów
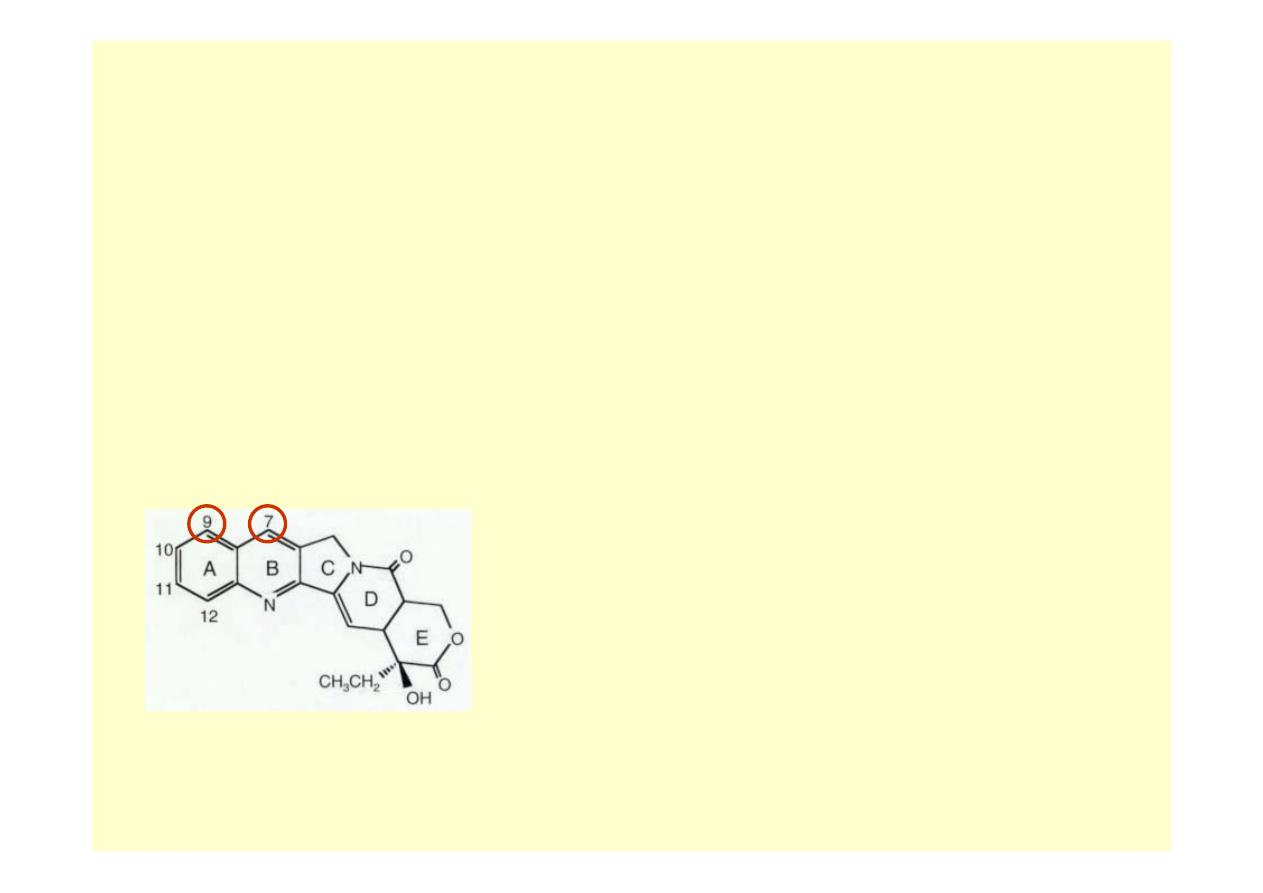
kamptotecyna
(CPT) Camptotheca acuminata – Xi Shu
C11
C10
C9
C7
CPT
H
H
H
H
topotecan
H
OH (CH3)2NHCH2
H
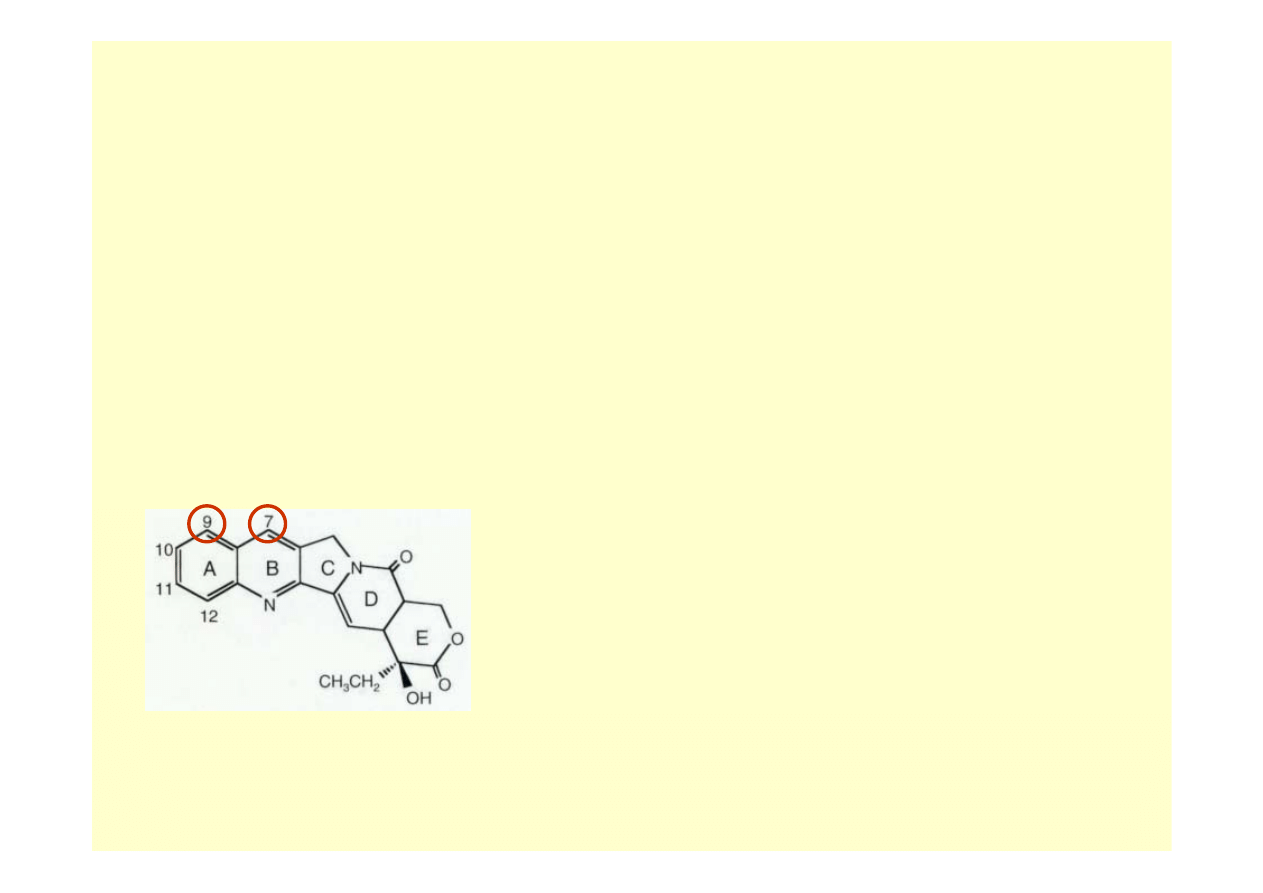
Etap badań
podstawowych
poszukiwanie substancji aktywnych biologicznie
!
--
substancje naturalne [GŁÓWNIE] pochodzenia roślinnego [DIETA]
--
izolowanie i określenie struktury związku aktywnego
--
synteza analogów
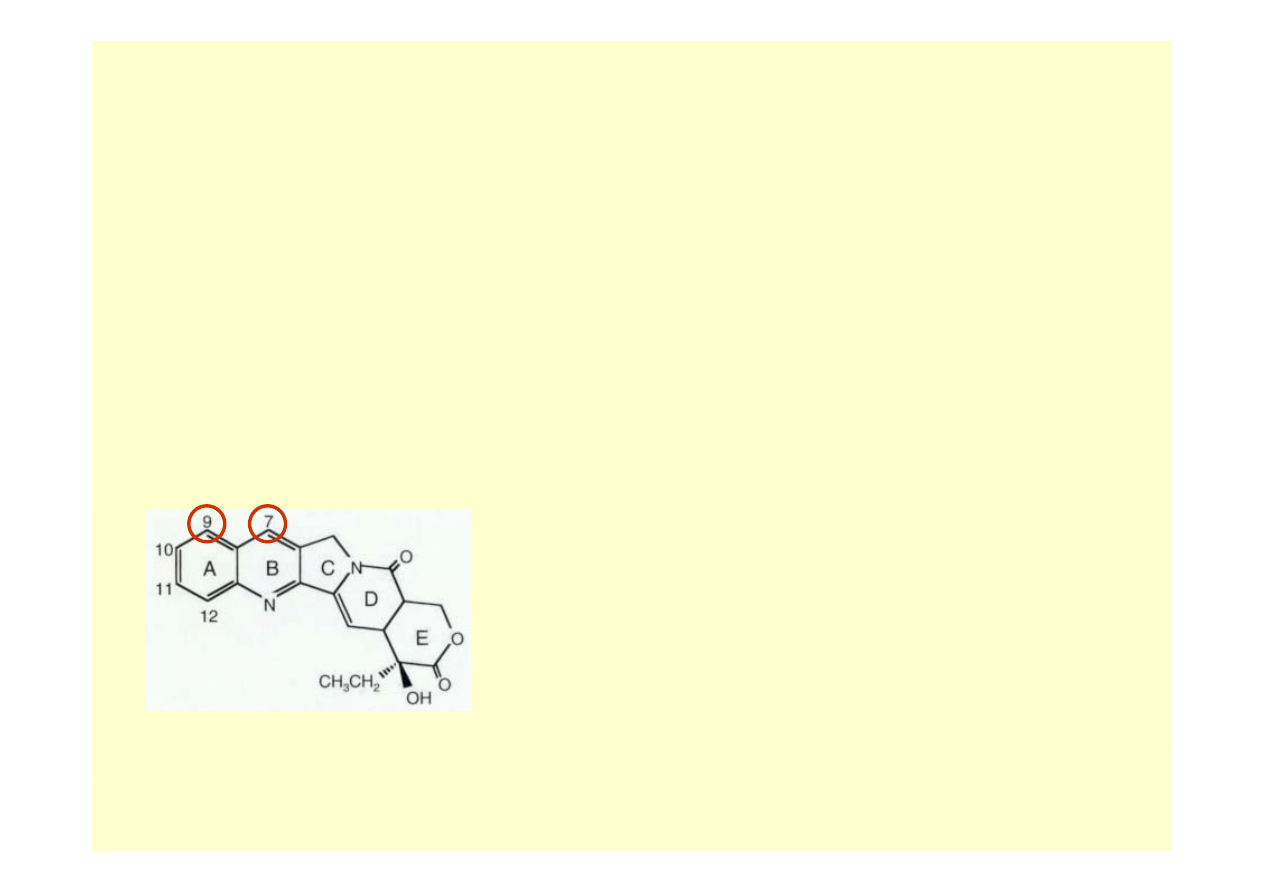
kamptotecyna
(CPT) Camptotheca acuminata – Xi Shu
C11
C10
C9
C7
CPT
H
H
H
H
topotecan
H
OH (CH3)2NHCH2
H
9-aminoCPT
H
H
NH2
H
Etap badań
podstawowych
poszukiwanie substancji aktywnych biologicznie
!
--
substancje naturalne [GŁÓWNIE] pochodzenia roślinnego [DIETA]
--
izolowanie i określenie struktury związku aktywnego
--
synteza analogów
kamptotecyna
(CPT) Camptotheca acuminata – Xi Shu
C11
C10
C9
C7
CPT
H
H
H
H
topotecan
H
OH (CH3)2NHCH2
H
9-aminoCPT
H
H
NH2
H
irinotecan
H
H
N-CH
3
CH
2
N
N
NCOO
-
Etap badań
podstawowych
poszukiwanie substancji aktywnych biologicznie
!
--
substancje naturalne [GŁÓWNIE] pochodzenia roślinnego [DIETA]
--
izolowanie i określenie struktury związku aktywnego
--
synteza analogów [DODAWANIE I WYMIANA GRUP BOCZNYCH]
Etap badań
podstawowych
poszukiwanie substancji aktywnych biologicznie
!
--
substancje naturalne [GŁÓWNIE] pochodzenia roślinnego [DIETA]
--
izolowanie i określenie struktury związku aktywnego
--
synteza analogów [DODAWANIE I WYMIANA GRUP BOCZNYCH]
!!
--
projektowanie i synteza substancji o przewidywanym działaniu
--
białka [ENZYMY]
--
lipidy błony komórkowej
--
kwasy nukleinowe [siRNA]
Etap badań
podstawowych
testowanie aktywności potencjalnych leków
--
in vitro np. hamowanie reakcji enzymatycznej
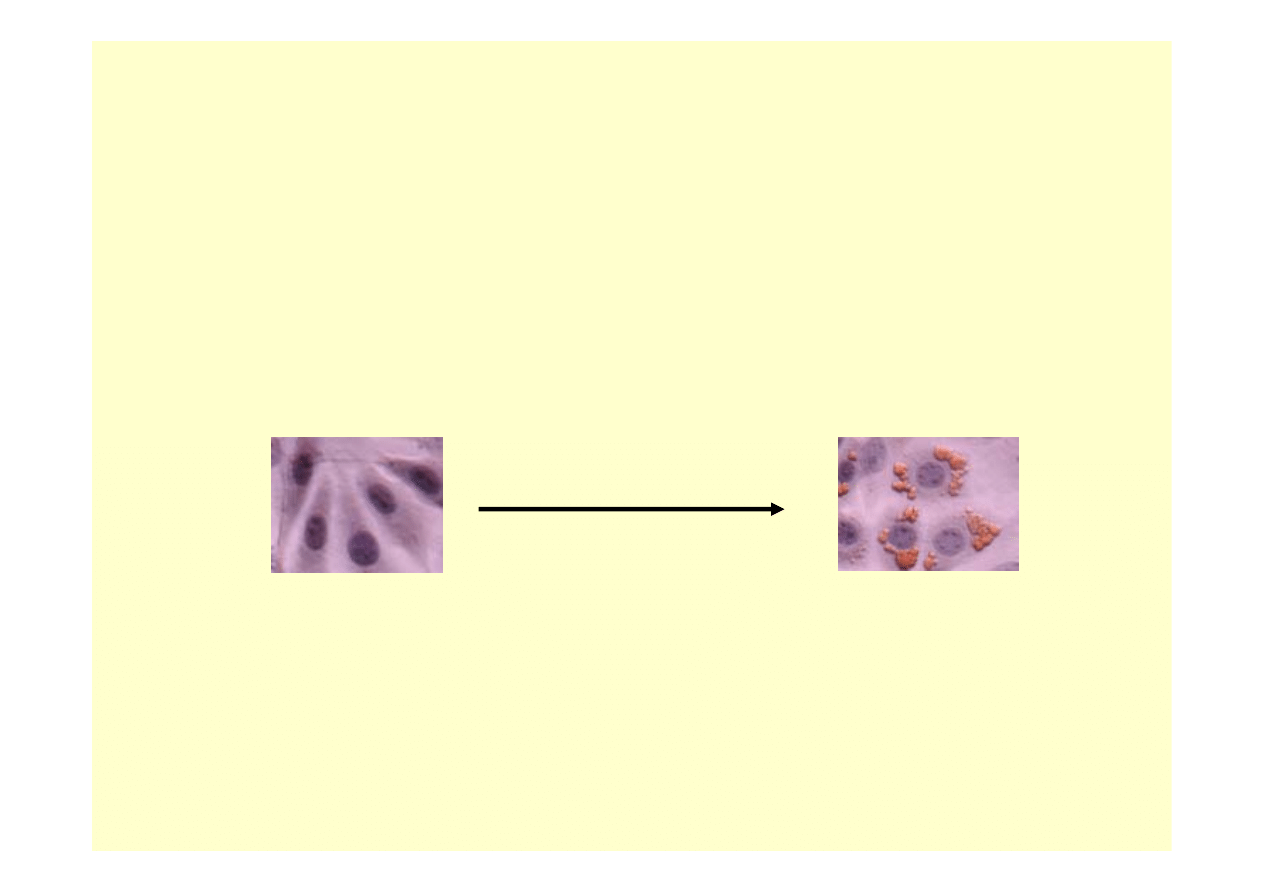
Etap badań
podstawowych
testowanie aktywności potencjalnych leków
--
in vitro np. hamowanie reakcji enzymatycznej
--
linie komórkowe [różnicowanie fibroblastów 3T3 L1 w adipocyty]
fibroblasty
adipocyty
aktywacja receptorów PPAR
Etap badań
podstawowych
testowanie aktywności potencjalnych leków
--
in vitro np. hamowanie reakcji enzymatycznej
--
linie komórkowe [różnicowanie fibroblastów 3T3 L1 w adipocyty]
--
izolowane hepatocyty
i kanaliki kory nerki [szybkość
syntezy glukozy]
Etap badań
podstawowych
testowanie aktywności potencjalnych leków
--
in vitro np. hamowanie reakcji enzymatycznej
--
linie komórkowe [różnicowanie fibroblastów 3T3 L1 w adipocyty]
--
izolowane hepatocyty
i kanaliki kory nerki [szybkość
syntezy glukozy]
--
linie komórkowe [zmiany aktywności genów, RealTimePCR, biomarkery]
Etap badań
podstawowych
testowanie aktywności potencjalnych leków
potencjalny lek
oceniamy szybkość
glukoneogenezy na
podstawie poziomu glukozy w medium

Etap badań
podstawowych
kontrola
potencjalny lek

Etap badań
podstawowych
kontrola
potencjalny lek
kontrola
+ rozpuszczalnik
(metanol)
(DMSO)

Etap badań
podstawowych
kontrola
potencjalny lek
kontrola
+ rozpuszczalnik
(metanol)
(DMSO)
Etap badań
podstawowych
testowanie aktywności potencjalnych leków
potencjalny lek
oceniamy szybkość
glukoneogenezy na
podstawie poziomu glukozy w medium
metoda oznaczania glukozy
Etap badań
przedklinicznych
FARMAKOKINETYKA:
badanie procesu
wchłaniania danej substancji (biodostępność),
wiązania z białkami krwi, dystrybucji i usuwania
z ustroju
(tempo metabolizmu leku).
FARMAKODYNAMIKA:
zajmuje się
mechanizmem działania
substancji aktywnej,
działaniami niepożądanymi, interakcjami
z innymi lekami
oraz
toksycznością
(LD50).
Etap badań
przedklinicznych
--
rozpuszczalność
[woda] [podawanie]
--
odporność
na soki trawienne
--
wchłanianie z jelita
--
odporność
na enzymy wątrobowe
--
wiązanie z białkami krwi [albumina]
--
wchłanianie do tkanki tłuszczowej
--
wydalanie z moczem
--
przenikanie przez błony komórkowe
--
bariera krew-mózg
Etap badań
przedklinicznych
--
rozpuszczalność
[woda] [podawanie]
--
odporność
na soki trawienne
--
wchłanianie z jelita
--
odporność
na enzymy wątrobowe
--
wiązanie z białkami krwi [albumina]
--
wchłanianie do tkanki tłuszczowej
--
wydalanie z moczem
--
przenikanie przez błony komórkowe
--
bariera krew-mózg
--
bakterie jelitowe
Etap badań
przedklinicznych
--
określenie dawki LD50
DAWKA POWODUJĄCA ŚMIERĆ
50% ZWIERZĄT DOŚWIADCZALNYCH
LD50 (mg/kg mc.) klasa toksyczności
< 25
bardzo toksyczna
< 200
toksyczna
< 2000
szkodliwa
2000 <
nieklasyfikowana
Etap badań
przedklinicznych
--
określenie dawki LD50
Philippus
Aureolus
Theophrastus
Bombastus
von Hohenheim
[XVI wiek]
chlorek sodu
200g
paracetamol
150 mg/kg mc. [10g]
"wszystko jest trucizną
i nic nie jest trucizną, bo
tylko dawka czyni truciznę"
Wyniki uzyskane na zwierzętach nie muszą
powtórzyć
się
na ludziach

Etap badań
klinicznych
BADANIA EKSPERYMENTALNE
--
mechanizm działania leków
[miejsce działania]
--
wpływ na metabolizm
--
toksyczność

Etap badań
klinicznych
BADANIA EKSPERYMENTALNE
--
mechanizm działania leków
[miejsce działania]
--
wpływ na metabolizm
--
toksyczność
BADANIA KLINICZNE
--
skuteczność
działania leków

Badania kliniczne
FAZA I
[wyłącznie zdrowe osoby
cytostatyki –
tylko chorzy
]
--
ocena bezpieczeństwa leku
[wchłanianie, metabolizm, wydalanie,
interakcje z innymi lekami i pożywieniem,
toksyczność]
--
ustalenie dawki

Badania kliniczne
FAZA II
[chorzy]
--
FIIa
ustalenie dawki w porównaniu do placebo
--
zależność
między dawka a efektem
--
wchłanianie, metabolizm i wydalanie w
odniesieniu do wieku i płci
--
FIIb
skuteczność
i bezpieczeństwo w porównaniu
do leku referencyjnego

Badania kliniczne
FAZA III
--
FIIIa
potwierdzenie skuteczności i bezpieczeństwa
--
porównanie krótko i długotrwałego
stosowania leku
--
FIIIb
informacje dla celów marketingowych

Badania kliniczne
FAZA IV
--
weryfikacja wcześniejszych ustaleń
--
poszerzenie wiedzy o działaniu danego związku

Badania kliniczne
[
ranga badania i jakość
uzyskanych wyników zależą
od tego jak
badanie zostało zaprojektowane
]

Badania kliniczne
[
ranga badania i jakość
uzyskanych wyników zależą
od tego jak
badanie zostało zaprojektowane
]
--
ilość
uczestników

Badania kliniczne
[
ranga badania i jakość
uzyskanych wyników zależą
od tego jak
badanie zostało zaprojektowane
]
--
ilość
uczestników
--
wiek i płeć
badanych

Badania kliniczne
[
ranga badania i jakość
uzyskanych wyników zależą
od tego jak
badanie zostało zaprojektowane
]
--
ilość
uczestników
--
wiek i płeć
badanych
--
czas trwania obserwacji

Badania kliniczne
[
ranga badania i jakość
uzyskanych wyników zależą
od tego jak
badanie zostało zaprojektowane
]
--
ilość
uczestników
--
wiek i płeć
badanych
--
czas trwania obserwacji
--
przypadki choroby podczas
prowadzenia badania

Badania kliniczne
[
ranga badania i jakość
uzyskanych wyników zależą
od tego jak
badanie zostało zaprojektowane
]
--
ilość
uczestników
--
wiek i płeć
badanych
--
czas trwania obserwacji
--
przypadki choroby podczas
prowadzenia badania
--
stosowanie
placebo
lub
leku referencyjnego

Badania kliniczne
[
ranga badania i jakość
uzyskanych wyników zależą
od tego jak
badanie zostało zaprojektowane
]
--
ilość
uczestników
--
wiek i płeć
badanych
--
czas trwania obserwacji
--
przypadki choroby podczas
prowadzenia badania
--
stosowanie
placebo
lub
leku referencyjnego
--
liczba analizowanych parametrów

Badania kliniczne
[
ranga badania i jakość
uzyskanych wyników zależą
od tego jak
badanie zostało zaprojektowane
]
--
ilość
uczestników
--
wiek i płeć
badanych
--
czas trwania obserwacji
--
przypadki choroby podczas
prowadzenia badania
--
stosowanie
placebo
lub
leku referencyjnego
--
liczba analizowanych parametrów
--
randomizacja badań

Badania kliniczne
[
ranga badania i jakość
uzyskanych wyników zależą
od tego jak
badanie zostało zaprojektowane
]
--
ilość
uczestników
--
wiek i płeć
badanych
--
czas trwania obserwacji
--
przypadki choroby podczas
prowadzenia badania
--
stosowanie
placebo
lub
leku referencyjnego
--
liczba analizowanych parametrów
--
randomizacja badań
--
podwójnie ślepa próba

Badania interwencyjne
[skuteczność
interwencji farmakologicznej]
[
ich wyniki mają
największy wpływ na rejestrację
nowych leków
]

Badania interwencyjne
[skuteczność
interwencji farmakologicznej]
[
ich wyniki mają
największy wpływ na rejestrację
nowych leków
]
„Złoty standard”
kontrolowane placebo badania randomizowane
przeprowadzone metodą
podwójnej ślepej próby

Badania interwencyjne
[skuteczność
interwencji farmakologicznej]
[
ich wyniki mają
największy wpływ na rejestrację
nowych leków
]
RANDOMIZACJA
--
losowy przydział
ochotników do grup badanych [kohort]
--
eliminacja wpływu lekarza na wybór uczestników badań

Badania interwencyjne
[skuteczność
interwencji farmakologicznej]
[
ich wyniki mają
największy wpływ na rejestrację
nowych leków
]
RANDOMIZACJA
--
losowy przydział
ochotników do grup badanych [kohort]
--
eliminacja wpływu lekarza na wybór uczestników badań
KONTROLA [placebo albo lek referencyjny]
--
placebo podawane identycznie jak badany związek

Badania interwencyjne
[skuteczność
interwencji farmakologicznej]
[
ich wyniki mają
największy wpływ na rejestrację
nowych leków
]
RANDOMIZACJA
--
losowy przydział
ochotników do grup badanych [kohort]
--
eliminacja wpływu lekarza na wybór uczestników badań
KONTROLA [placebo albo lek referencyjny]
--
placebo podawane identycznie jak badany związek
POSWÓJNIE ŚLEPA PRÓBA
--
neutralizacja oczekiwań
badanych osób
--
placaebo
i badany lek maja
taki sam wygląd
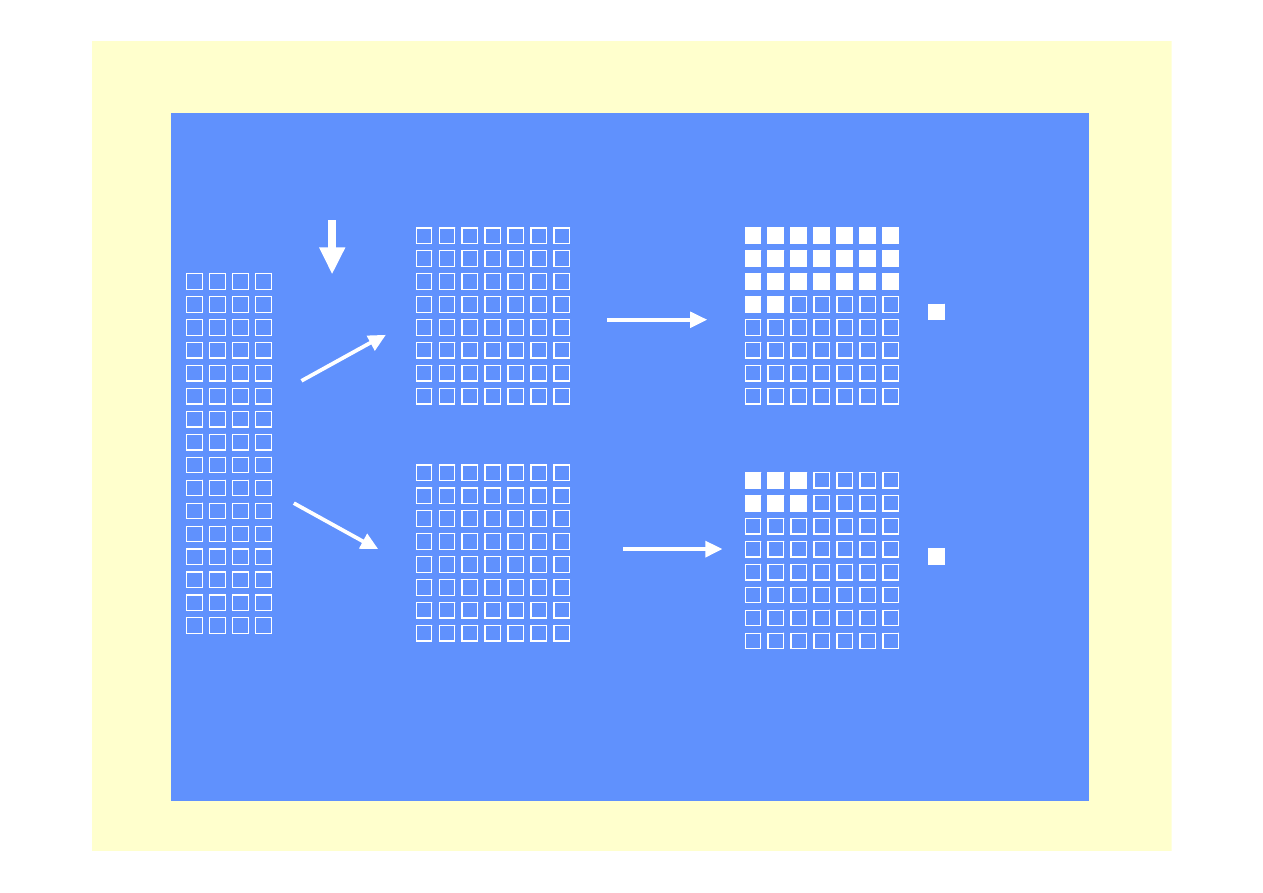
KONTROLOWANE PLACEBO BADANIA RANDOMIZOWANE
T. Dyszynski, T. Lietz
osiągnięty
punkt
końcowy (np.
cukrzyca typu
2)
osiągnięty
punkt
końcowy
Grupa kontrolna
Grupa leczona
aktywnie
CZAS
placebo
lek, dieta,
zmiana trybu
życia
CZAS
Randomizacja
Populacja
spełniająca
wymogi
uczestnictwa
w badaniu
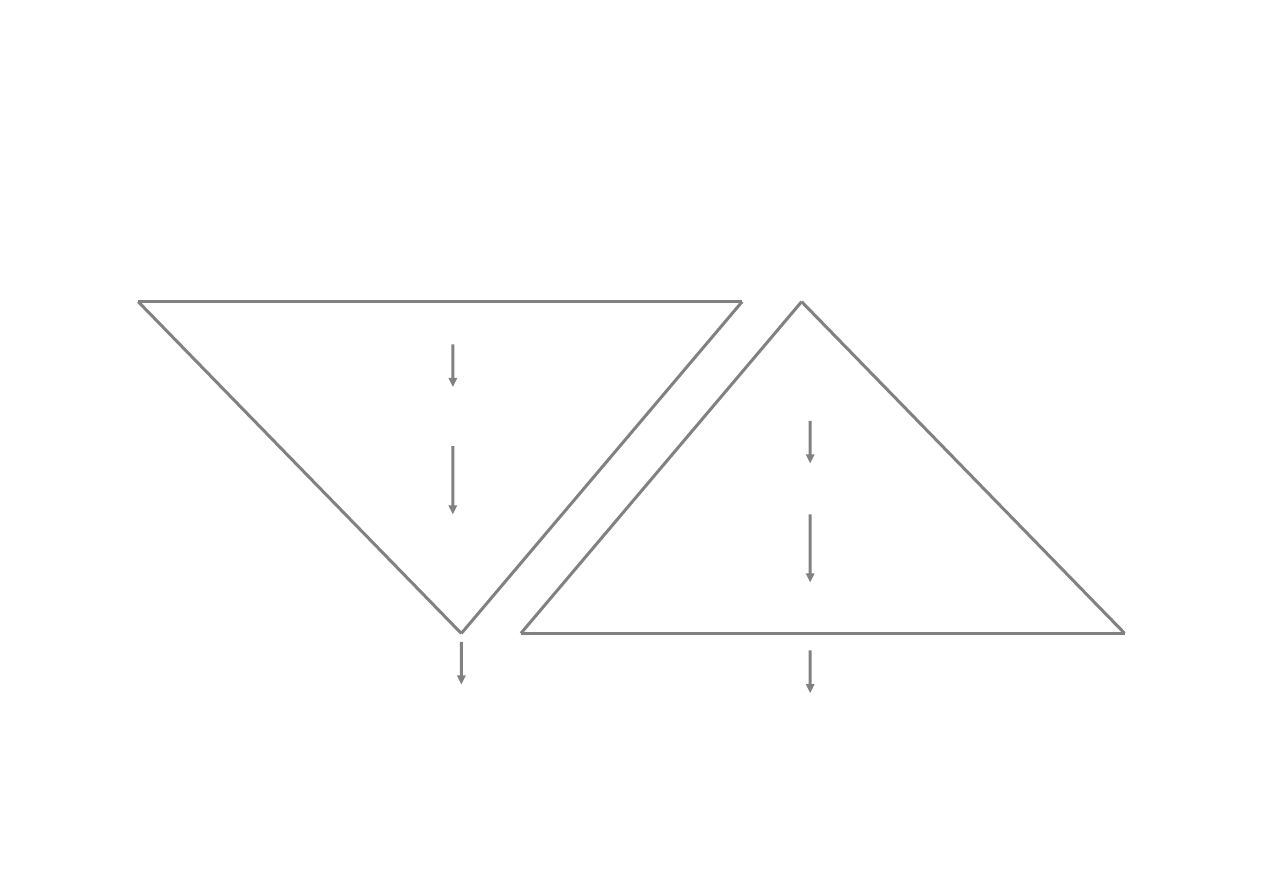
Clinical Development Program
Aim: NDA Approval / Partnership
Nonclinical Pharmacology, ADME, Toxicology Program
Clinical Program
Labeling
NDA / Partner
Nonclinical Pharmacology, ADME, Toxicology Program
Clinical Program
Label /TPP
Typical
Development
Plan
NDA
Smart
Development
Plan
Clinical
Trials
–
Phase
I
FIM ‐
Pilot
FIM ‐
SAD
SAD
PK and
safety
definition
MAD

Industry perspective: How to effectively deliver the preclinical
data now required
for regulatory submission
Dr Karen Cornelissen, Scientific Director, Covance, UK
Regulatory perspective on the pre‐clinical data required for Phase I approval ‐
gaining greater control
though translational medicine
Walter Janssens
PhD, Senior Assessor, Preclinical Department Research & Development,
Federal Agency for Medicinal and Health Products, Belgium
Comparing and contrasting European and FDA guidelines on risk mitigation in FIM studies
Anthea
Cromie, Head of Clinical, Pharmacology ‐
Europe, MDS Pharma
Services, UK
Designing efficient Phase I studies
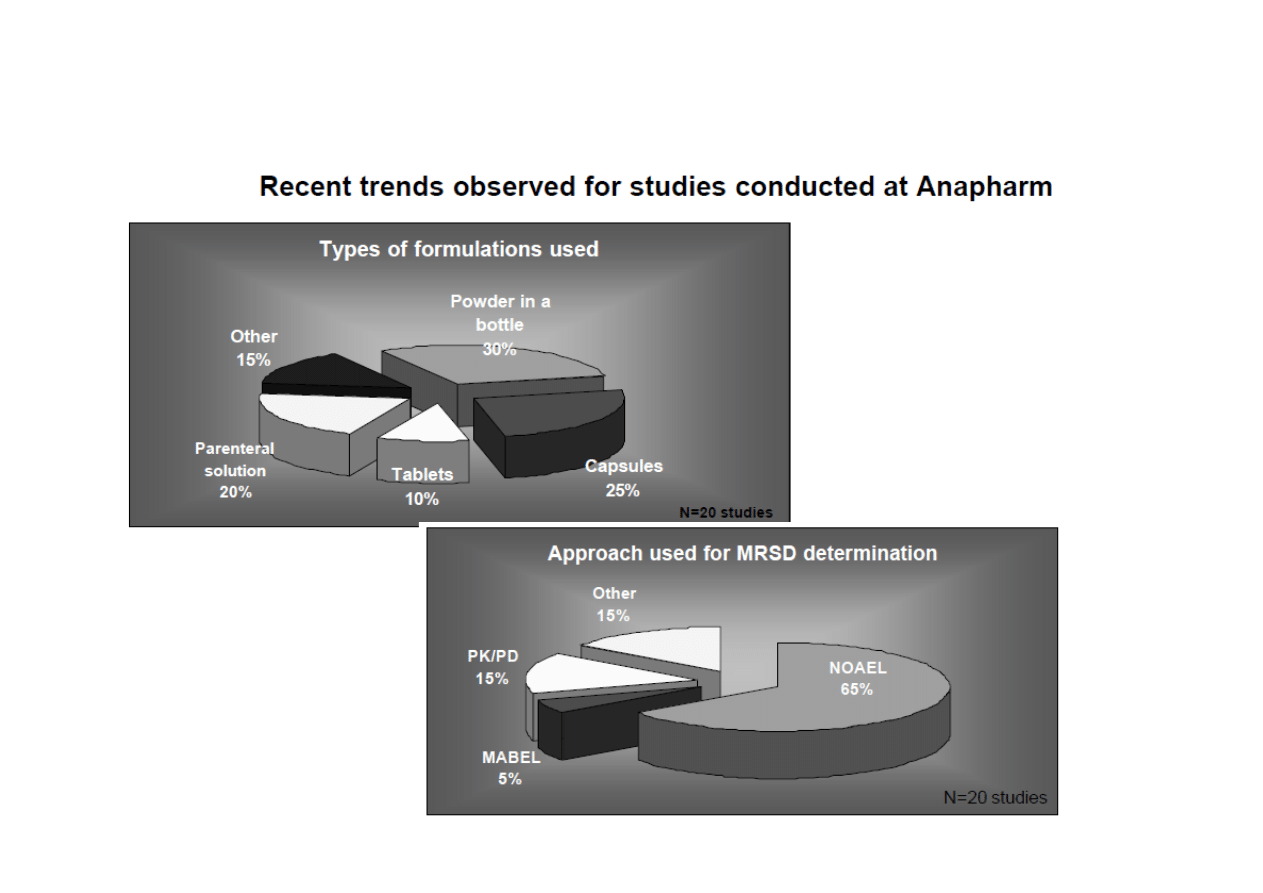
Mario Tanguay, B.Pharm, Ph.D, Vice President, Scientific & Regulatory Affairs, Anapharm
New thinking in overcoming FIM dosing challenges
James Dow PhD, Director of Clinical, Pharmacology & DMPK, (OSI) Prosidion, UK
Selecting the correct starting dose for FIM antibody studies
Peter Lloyd, Head of PKPD, Novartis Biologics, UK
Translational medicine
Translational medicine
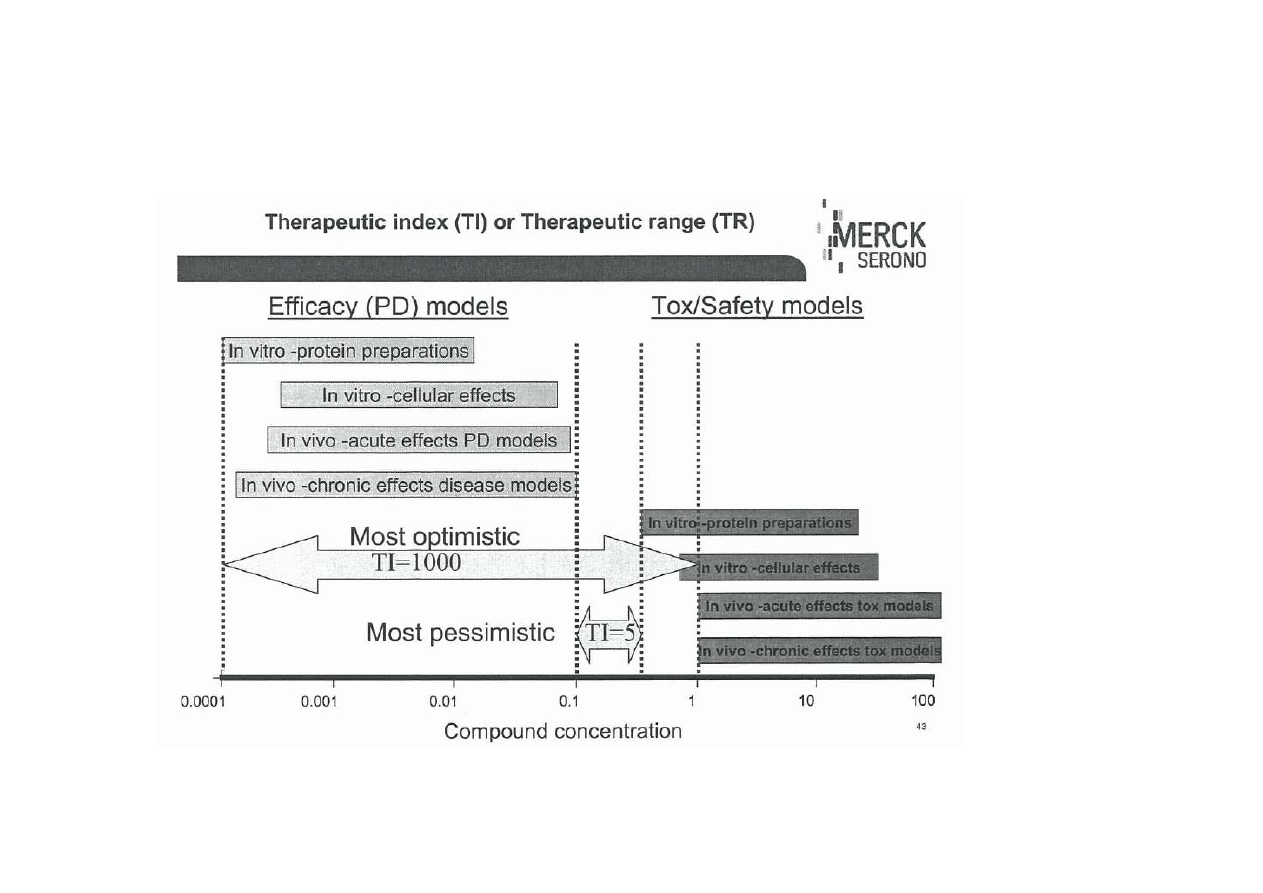
Translational medicine
?
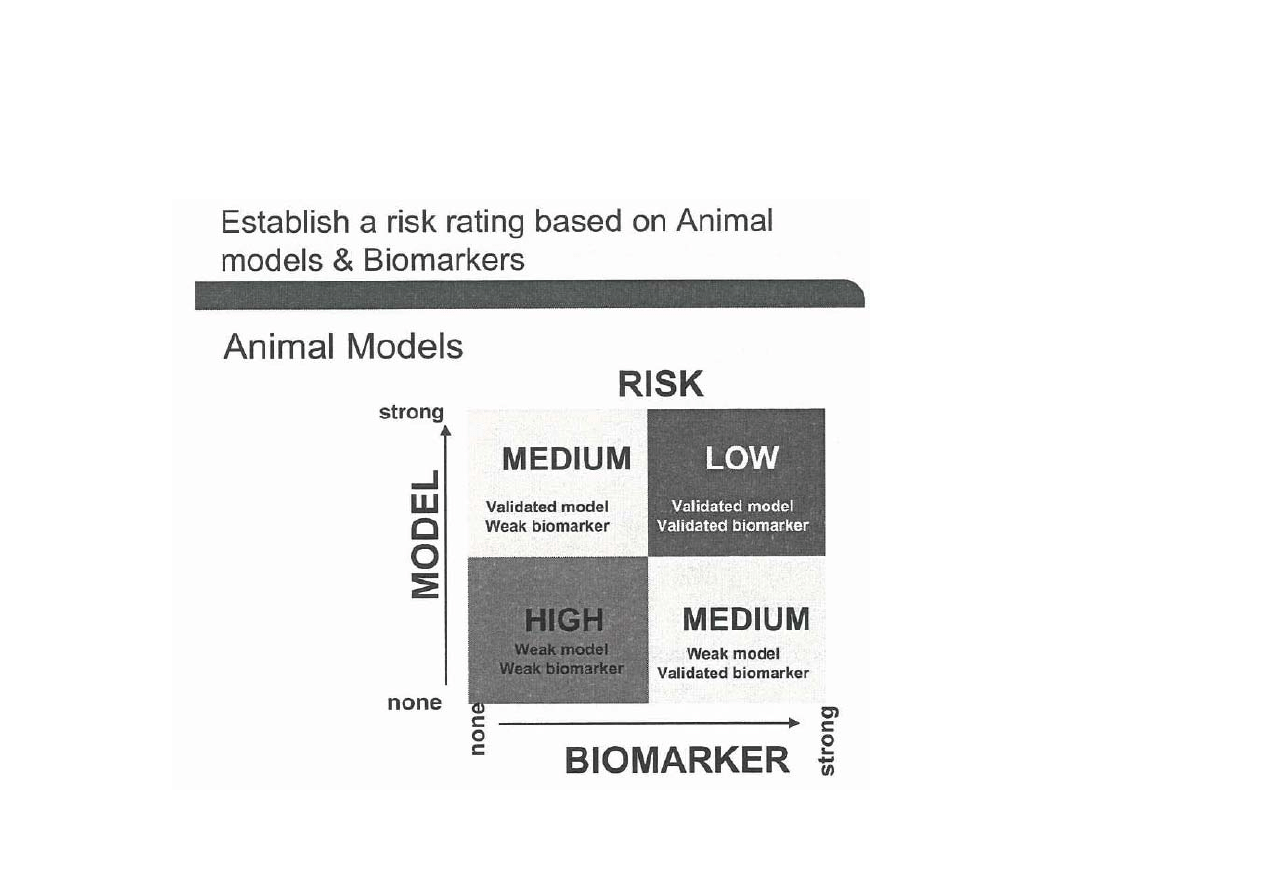
Translational medicine

Translational medicine
NOAEL
– 65%
MABEL
– 5%
PK/PD
– 15%
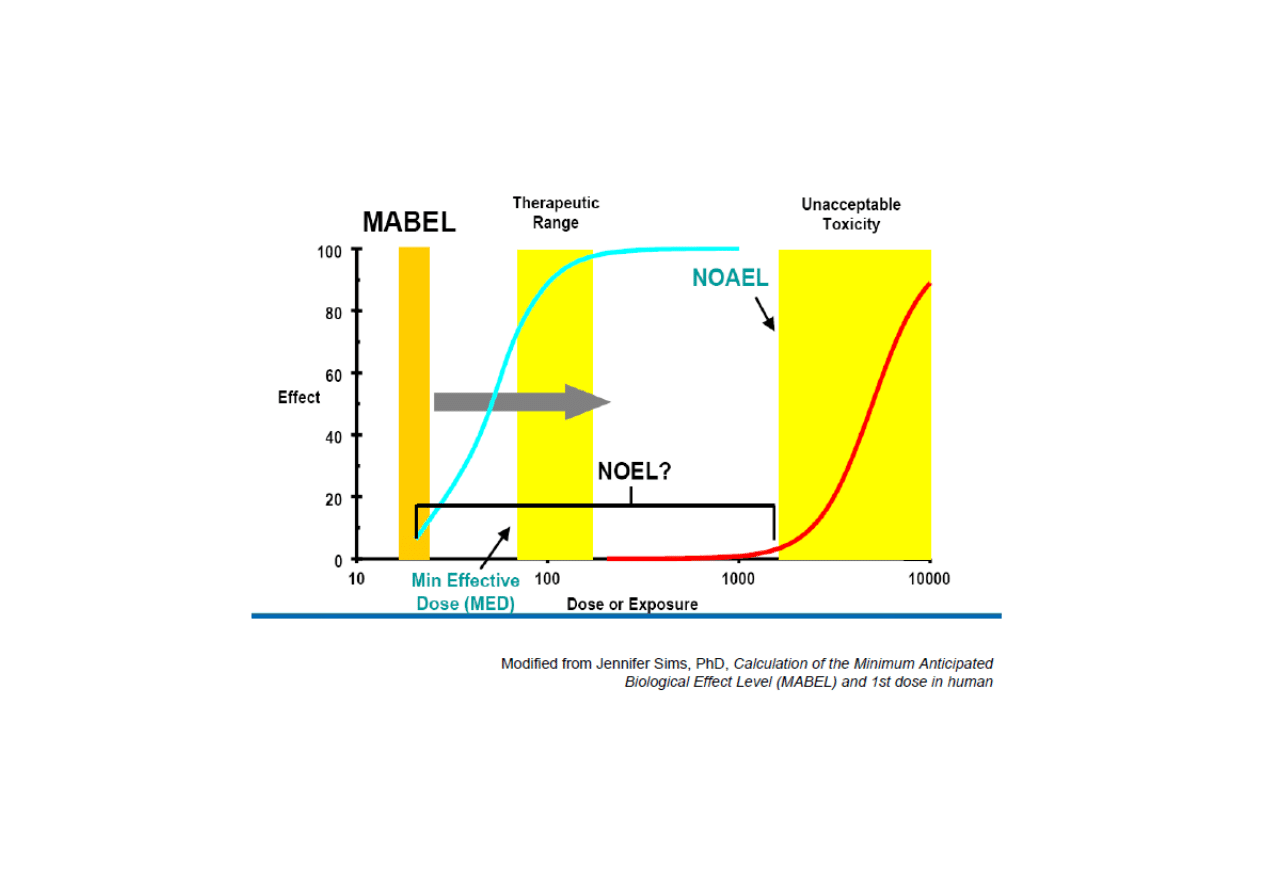

NOAEL
HED
Human
Equivalent
Dose
/10 Safety
Factor
MRSD
Maximum
Recommended
Safe
Dose
NOAEL –
50 mg/kg (psy)
50/1,8 = 2,7 mg/kg
27 * 60 kg = 1620 mg HED
/10 SF
= 160 mg MRSD
Translational medicine
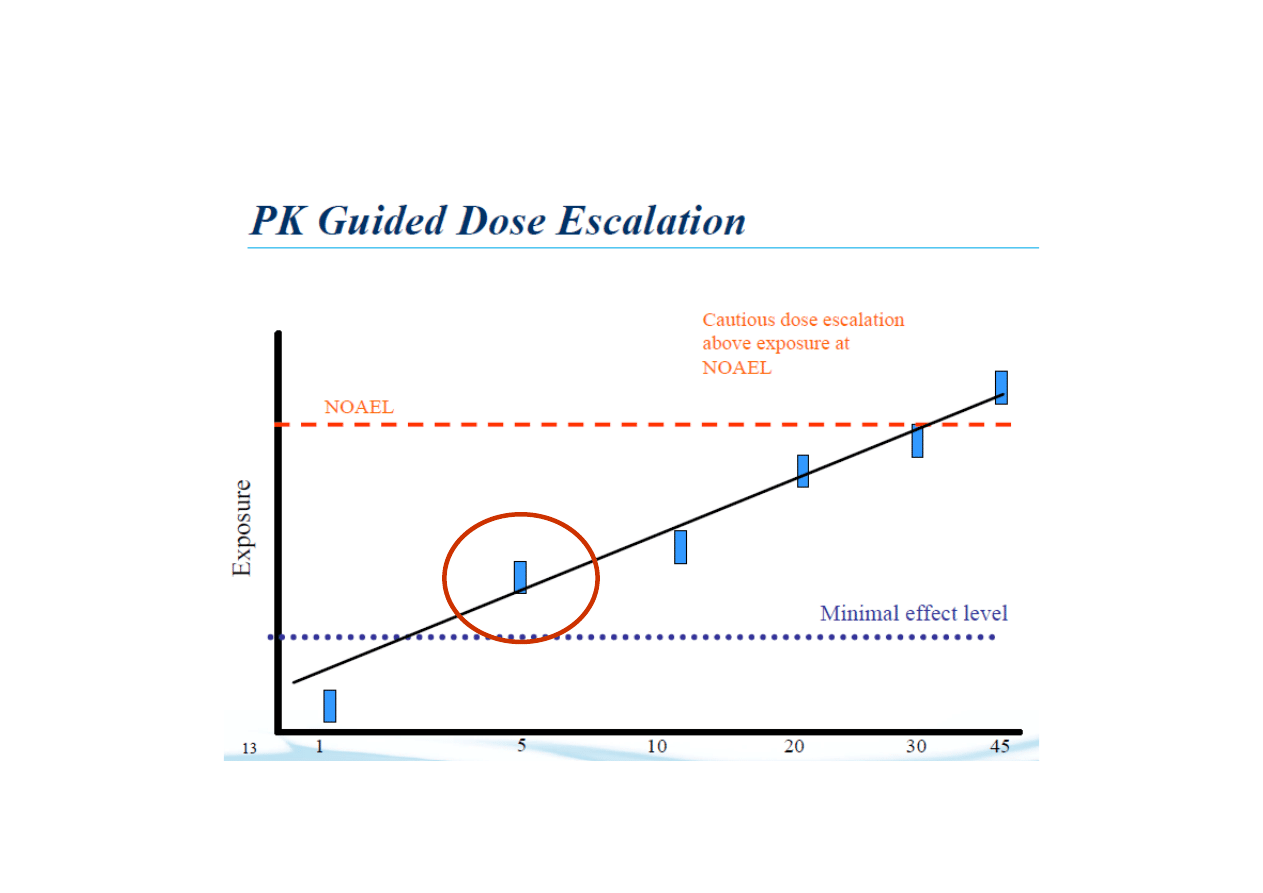

MRSD na podstawie NOAEL/10
MRSD na podstawie MABEL
(80 times
< NOAEL/10)



Pre‐IND meeting – package content

•
Tab A – Table of Contents
•
Tab B – List of Proposed Attendees
•
Tab C –
Introduction
–
Company’s
background, location, products
–
Meeting information (product name,
indication(s), sponsor, meeting date & time
•
Tab D –
Mechanism of action
•
Tab E –
Nonclinical Safety Studies
–
Table of all studies (safety & efficacy)
–
Summary of each safety study
–
Proposed additional studies:
proposed 4‐week study
(NOAEL)
•
Rat: 100, 500, 1000 mg/kg
•
Dog: 100, 500, 1000 mg/kg
•
Tab F – Previous Human Experience
–
Similar products (adverse effects)
•
Tab G – Clinical Program
–
Introduction (TPP)
–
Rationale for clinical studies
–
First Protocol (Single Dose)
–
Starting dose in grams/mass
–
Planned program
•
Tab H – CMC section
–
Short product description
& method of manufacture; analytical methods
–
API – 30 days stability
–
Formulation – 30 days stability
–
Proposals for ongoing and future
stability studies
–
Impurity Profile
•
Tab I ‐
Questions for FDA
Pre‐IND meeting – package content
Document Outline
- Slajd numer 1
- Slajd numer 2
- Slajd numer 3
- Slajd numer 4
- Slajd numer 5
- Slajd numer 6
- Slajd numer 7
- Slajd numer 8
- Slajd numer 9
- Slajd numer 10
- Slajd numer 11
- Slajd numer 12
- Opracowanie nowego leku i wprowadzenie go na rynek trwa około 20 lat i pochłania 2 miliardy zł
- Slajd numer 14
- Slajd numer 15
- Slajd numer 16
- Slajd numer 17
- Slajd numer 18
- Slajd numer 19
- Slajd numer 20
- Slajd numer 21
- Slajd numer 22
- Slajd numer 23
- Slajd numer 24
- Slajd numer 25
- FDA Environment
- FDA Environment
- Slajd numer 28
- Slajd numer 29
- Slajd numer 30
- Slajd numer 31
- Slajd numer 32
- Slajd numer 33
- Slajd numer 34
- Slajd numer 35
- Slajd numer 36
- Slajd numer 37
- Slajd numer 38
- Slajd numer 39
- Slajd numer 40
- Slajd numer 41
- Slajd numer 42
- Slajd numer 43
- Slajd numer 44
- Slajd numer 45
- Slajd numer 46
- Slajd numer 47
- Slajd numer 48
- Slajd numer 49
- Slajd numer 50
- Slajd numer 51
- Slajd numer 52
- Slajd numer 53
- Slajd numer 54
- Slajd numer 55
- Slajd numer 56
- Slajd numer 57
- Slajd numer 58
- Slajd numer 59
- Slajd numer 60
- Slajd numer 61
- Slajd numer 62
- Slajd numer 63
- Slajd numer 64
- Slajd numer 65
- Slajd numer 66
- Slajd numer 67
- Slajd numer 68
- Slajd numer 69
- Slajd numer 70
- Slajd numer 71
- Slajd numer 72
- Slajd numer 73
- Slajd numer 74
- Slajd numer 75
- Slajd numer 76
- Slajd numer 77
- Slajd numer 78
- Slajd numer 79
- Slajd numer 80
- Slajd numer 81
- Slajd numer 82
- Slajd numer 83
- Slajd numer 84
- Slajd numer 85
- Slajd numer 86
- Slajd numer 87
- Slajd numer 88
- Slajd numer 89
- Slajd numer 91
- Slajd numer 92
- Slajd numer 93
- Slajd numer 94
- Slajd numer 95
- Slajd numer 96
- Slajd numer 97
- Slajd numer 98
- Slajd numer 99
- Slajd numer 100
- Slajd numer 101
- Slajd numer 102
- Slajd numer 103
- Slajd numer 104
- Slajd numer 105
Wyszukiwarka
Podobne podstrony:
lek 2009 2010 porównanie genomu Pro i Eukar studenci
Diagnostyka laboratoryjna zaburzen gospodarki lek 2010
Konkurencja doskonała, ZiIP PP 2010-2011, Semestr I, Mikroekonomia
Pływanie, Doskonalenie pracy nóg do kraula na piersiach i na grzbiecie. Nauka pracy rak do kraula na
EGZ 2010 lek, I rok, Anatomia, cxrtsjxcgvhbjnkmugjyfghkjl, Anatomia egzamin, Egzaminy
testy patomotrfa, TEST LEK 2010 SFORMATOWANY, 1
Diagnostyka laboratoryjna zaburzen gospodarki lek 2010
KWARTALNY PLAN DOSKONALENIA ZAWODOWEGO kwartał I 2010
Plan II 2010 Kwartalny plan doskonalenia zawodowego
spis lab I sem 2010
2010 ZMP studenci
W4 2010
W01(Patomorfologia) II Lek
wyklad 14 15 2010
IV lek leczenie wspomagające w onkologii Żywienie
więcej podobnych podstron