
ANGIOPLASTYKA
W LECZENIU CHOROBY
WIEŃCOWEJ
Grzegorz J Horszczaruk
Grzegorz J Horszczaruk
I Katedra i Klinika Kardiologii AM w Warszawie
I Katedra i Klinika Kardiologii AM w Warszawie

Agioplastyka wieńcowa
(koronaroplastyka)
PTCA
PTCA= percutaneous transluminal
coronary angioplasty
PCI
PCI = percutaneous coronary
interventions
POBA
POBA= plain old balloon angioplasty

Kwalifikacja do
rewaskularyzacji (1)
Ocena kliniczna
wywiad dławicowy
ocena stabilności/niestabilności choroby
inne objawy mogące towarzyszyć niedokrwieniu
ocena wydolności serca
ocena dotychczasowego leczenia (farmakoterapia,
przebyte zabiegi)
choroby współistniejące i ocena ogólnego ryzyka zabiegu

Kwalifikacja do rewaskularyzacji wieńcowej
(2)
Obiektywna ocena niedokrwienia i krążenia
wieńcowego
zapis ekg
badania laboratoryjne (troponina, CK-MB)
próba wysiłkowa ekg
scyntygrafia wysiłkowa (SPECT)
metody echokardiograficzne (próba z dobutaminą,
ECHO kontrastowe)
ocena perfuzji za pomocą rezonansu magnetycznego
koronarografia
inne inwazyjne metody oceny krążenia wieńcowego
(IVUS; metody czynnościowa ocena zwężenia; próby farmakologiczne)

Technika POBA
Sprzęt
cewnik prowadzący
prowadnik (lider)
cewnik balonowy (balon)
Przebieg i ocena efektu
zabiegu
* predilatacja
* redilatacja
* zwężenie rezydualne
* obecność widocznej dyssekcji
* przepływ przez tętnicę
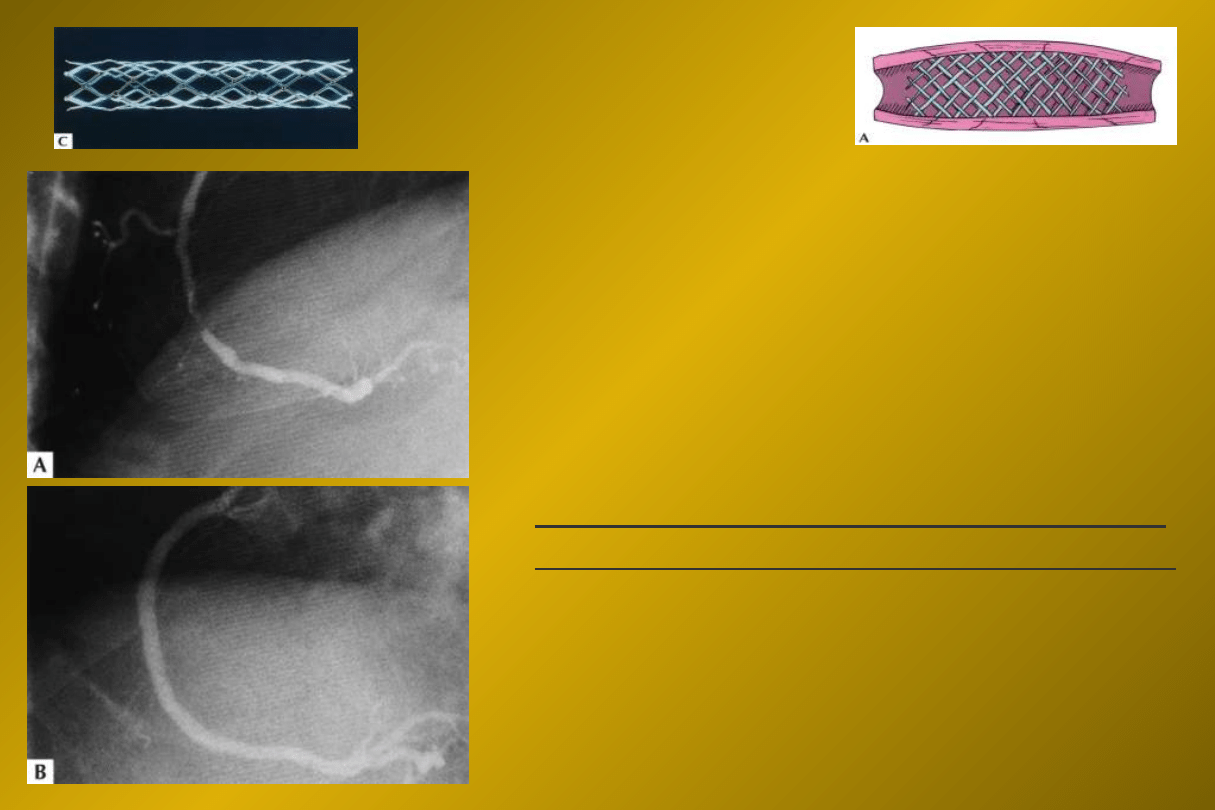
STENTY
Najważniejsze wskazania:
zagrażające zamknięcie tętnicy
(dyssekcja) - „bailout stenting”
po udrożnieniu przewlekle
niedrożnej tętnicy
suboptymalny efekt POBA
zmiany de novo w tętnicach nie
mniejszych niż 2,5 mm średnicy
zmiany restenotyczne
świeży zawał serca
krótkie zwężenie pomostu
wieńcowego
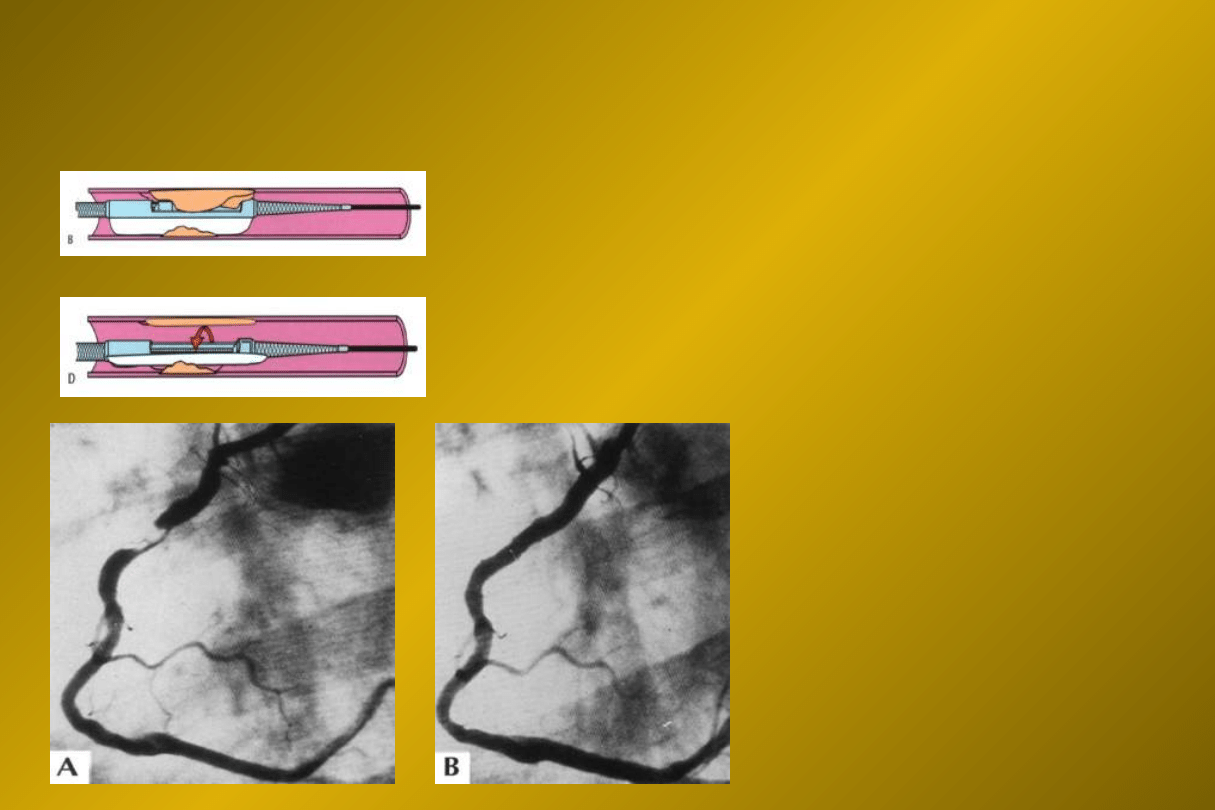
DCA - aterektomia
kierunkowa
zmiany
ekscentyryczne
zmiany w pomoście
żylnym
Obecnie bardzo
rzadko wykonywana
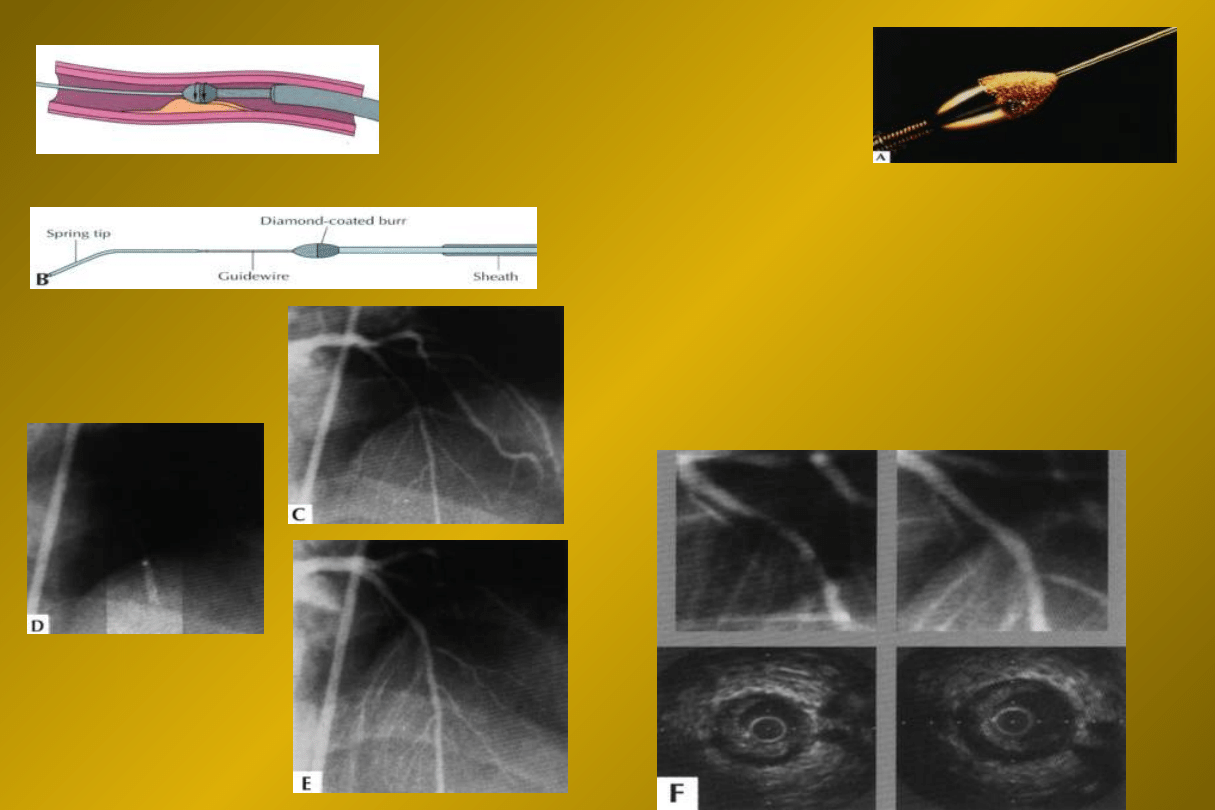
ROTA
ROTABLACJA
długie, zwapniałe
zwężenia
rozsiana restenoza w
stencie
Obecnie rzadko
wykonywana
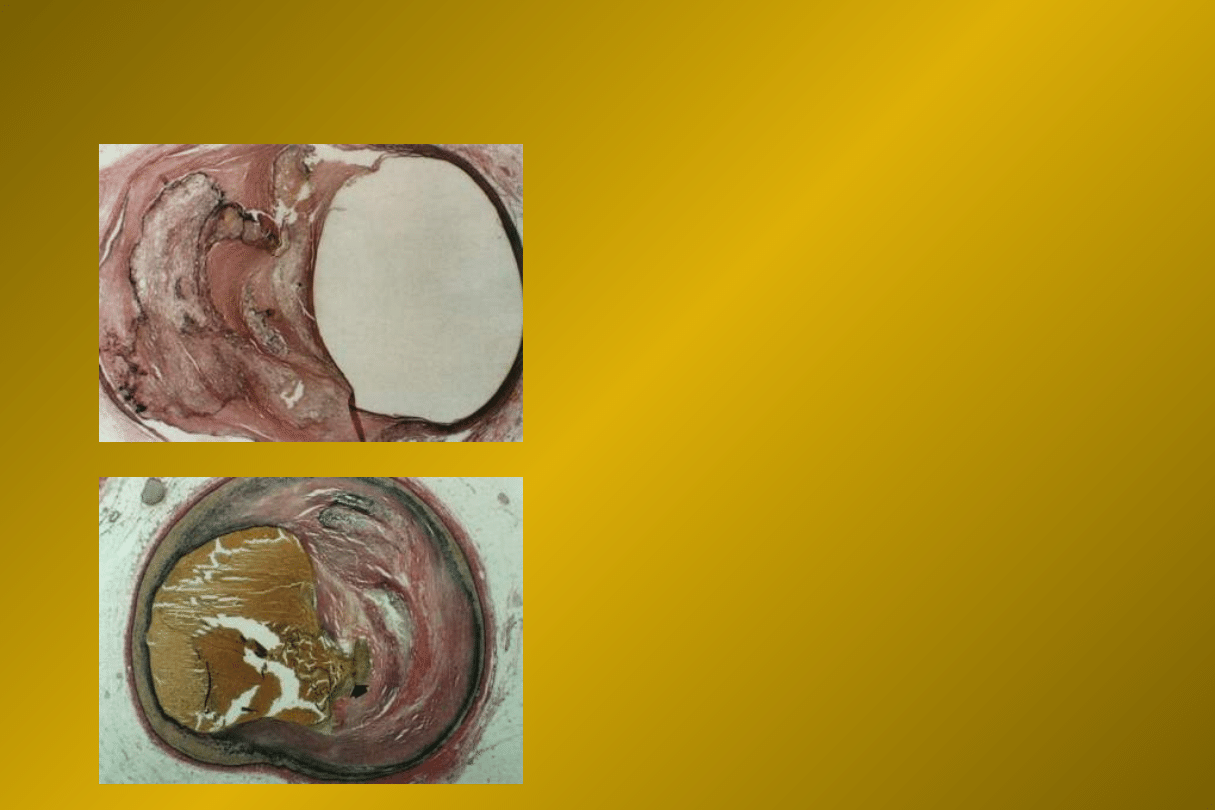
Mechanizm zabiegu
pęknięcie blaszki
kompresja blaszki
redystrybucja blaszki
rozciągnięcie ściany tętnicy
Usunięcie blaszki/skrzepliny – techniki
ateroablacyjne

Bezpośrednia skuteczność
PTCA
Kryteria skuteczności angiograficznej
zwężenie rezydualne < 50% (optymalnie <20%)
zmniejszenie zwężenia o co najmniej 20 %
prawidłowy przepływ przez tętnicę (TIMI 3)
nieobecność istotnej dyssekcji
Kryteria skuteczności klinicznej
ustąpienie (zmniejszenie) objawów niedokrwienia
nieobecność istotnych powikłań - zgon, zawał serca,
pilne CABG
70 - 98%
70 - 98% zabiegów - w zależności od anatomii zmian i sytuacji
klinicznej

LECZENIE INWAZYJNE

Wskazania do
koronaroplastyki
Stabilna choroba wieńcowa
Stabilna choroba wieńcowa
Nieskuteczność lub niepełna skuteczność farmakoterapii
Zagrożenie dużego obszaru mięśnia serca wykazane w
testach nieinwazyjnych
Duże prawdopodobieństwo powodzenia przy akceptowalnym
ryzyku zabiegu
Chory preferuje leczenie inwazyjne i jest dokładnie
poinformowany o indywidualnym ryzyku związanym z tym
leczeniem

Wskazania do
koronaroplastyki
Stabilna choroba wieńcowa
Stabilna choroba wieńcowa
Dławica CCS I-IV pomimo farmakoterapii i 1 VD –
klasa I A
Dławica CCS I-IV pomimo farmakoterapii i MVD u
chorych bez cukrzycy – klasa I A
Dławica o minimalnym nasileniu (CCS I) przy
farmakoterapii, zmiany 1,2 lub 3 naczyń, ale
obiektywnie wykazano duży obszar niedokrwienia –
klasa IIb C

Rokowanie u chorych leczonych farmakologicznie
a anatomia zmian w tt. wieńcowych
Anatomia zmian
5 –letnie
przeżycie
(%)
1 naczynie, 75% zwężenie
93
> 1 naczynie, zwężenie 50-74%
93
1 naczynie, 95%
91
2 naczynia
88
2 naczynia, oba zwężone 95%
86
1 naczynie, 95% zwężenie w proksymalnym segm. GPZ
83
2 naczynia, 95% zwężenie GPZ
83
2 naczynia, 95% zwężenie w proksymalnym segm. GPZ
79
3 naczynia
79
3 naczynia, przynajmniej jedno z 95% zwężeniem
73
3 naczynia, 75% zwężenie w proksymalnym segm. GPZ
67
3 naczynia, 95% zwężenie w proksymalnym segm. GPZ
59

PCI- rekomendacje ESC AD
2005
Obiektywnie stwierdzone rozległe
niedokrwienie (I A)
Rutynowe stentowanie zmian de novo
w natywnych tętnicach wieńcowych (I A)
Rutynowe stentowanie zmian de novo
w pomostach żylnych (I A)

Rekomendacje ESC AD 2005
Całkowita przewlekła niedrożność tętnicy
wieńcowej (IIa C)
Chory z wysokim ryzykiem
chirurgicznym, w tym LV-EF < 35% (IIa
B)

Rekomendacje ESC AD 2005
Choroba wielonaczyniowa/cukrzyca (IIb
C)
Zwężenie niezabezpieczonego pnia LTW
przy braku innych opcji rewaskularyzacji
(IIb C)

LECZENIE INWAZYJNE

Wskazania do
koronaroplastyki
Niestabilna choroba wieńcowa
Niestabilna choroba wieńcowa
Postępowanie inwazyjne – w zależności od wybranej
strategii
Chorzy wysokiego ryzyka
zidentyfikowana zmiana odpowiedzialna za niedokrwienie („culprit
lesion”)
akceptowana tzw. czynnościowa, niepełna rewaskularyzacja

UA/NSTEMI
strategie postępowania
Wczesna strategia inwazyjna: koronarografia
u wszystkich chorych bez przeciwwskazań do
rewaskularyzacji - wykonywana w ciągu
pierwszych 48 h hospitalizacji
Wczesna strategia zachowawcza:
koronarografia tylko, gdy: nawracająca
dławica CCS 4, duża dynamika zmian ST,
oporność na maksymalną faramakoterapię,
wybitnie dodatnie próby obciążeniowe

Wczesna strategia inwazyjna
Gdy koronarografia
natychmiast:
Możliwość bezzwłocznego
podjęcia odpowiedniego
leczenia u chorych ze
zwężeniem LMCA oraz
zmianami wielonaczyniowymi i
dysfunkcją LK
Chorzy bez istotnej patologii
tętnic wieńcowych mogą
szybko zostać przeniesieni z
OIOK
Gdy koronarografia odroczona
(o 12 – 48 h):
Czas na wdrożenie pełnej
farmakoterapii (ASA, LMWH,
blokery GP IIb/IIIa)
Możliwość pełniejszej obserwacji i
oceny chorego. Dokładniejsza
stratyfikacja ryzyka

Dokładna ocena kliniczna umożliwia
szybką stratyfikację ryzyka u danego
chorego:
Dławica CCS 4/niedokrwienie nawracające lub oporne, mimo
intensywnej farmakoterapii
Dławica/nawracające niedokrwienie z objawami CHF, S3, MR
EF<40% w ECHO
Wybitnie dodatnie testy nieinwazyjne przed hospitalizacją
Niestabilność hemodynamiczna
Groźne zaburzenia rytmu serca (sVT, VF)
PCI w ciągu poprzedzających 6 miesięcy
Stan po CABG
Kolejny epizod ACS, choć bez czynników najwyższego ryzyka
U chorych > 65 rż lub z obniżeniem ST lub podwyższonymi
wartościami markerów martwicy serca i bez
przeciwwskazań do rewaskularyzacji
ACC/AHA
ACC/AHA

Standardy ESC
AD 2003
kiedy wczesna strategia inwazyjna jest szczególnie
wskazana
Nawracające niedokrwienie (ból lub dynamika zmian ST – zwłaszcza
obniżenie lub krótkotrwałe uniesienie)
Wczesna dławica pozawałowa
Dodatni wynik testu troponinowego
Pojawienie się niestabilności hemodynamicznej w czasie obserwacji
Poważne zaburzenia rytmu serca (nawracający VT lub VF)
Chorzy z cukrzycą
EKG uniemożliwiające jednoznaczną ocenę ST (np. stymulator,
utrwalony LBBB)

Koronarografia wskazana
w ciągu pierwszej godziny
hospitalizacji
w przypadku chorych z:
z niestabilnością hemodynamiczną nie
reagującą na farmakoterapię
groźnymi komorowymi zaburzeniami rytmu
spoczynkową dławicą nie ustępującą mimo
podjęcia farmakoterapii
Standardy ESC 2003
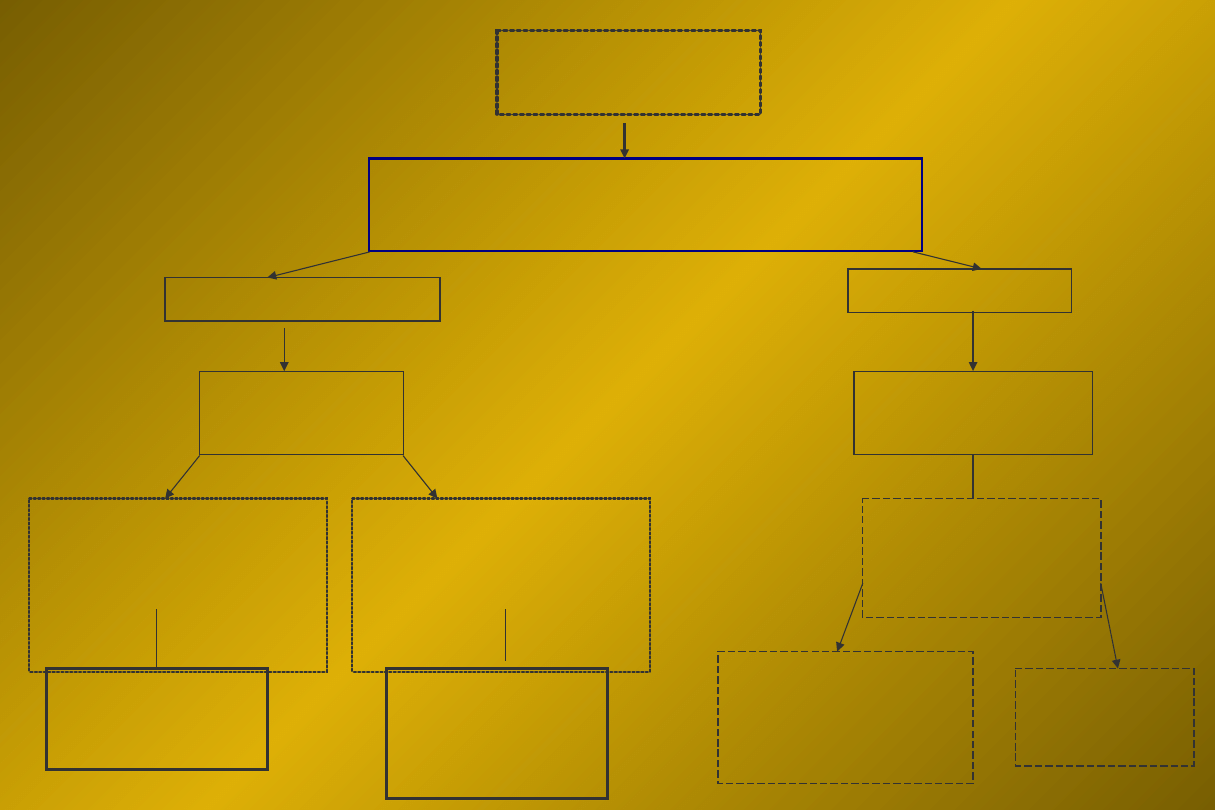
Objawy
NSTE - ACS
ASA/klopidogrel/heparyna/
beta-adrenolityk/ntg
Niskie ryzyko
Wysokie ryzyko
strategia
strategia
inwazyjna
inwazyjna
strategia
strategia
zachowawcza
zachowawcza
Koro w trybie
natychmiastowym
(< 2,5 h); IIb/IIIa GPI
– można się
wstrzymać
PCI
+
abciximab lub
eptifibatid
Koro w trybie
pilnym (< 48 h);
„upstream”
tirofiban lub
eptifibatid
IIa
Ia
PCI
+
kontynowac
tirofiban//eptifib
atid
Wczesne
testy
nieinwazyjne
PCI
ewentualnie z
tirofibanem/eptifbatid
em
tylko
farmakotera
pia

LECZENIE INWAZYJNE

Rozwój strategii leczenia ostrego STEMI
Rozwój strategii leczenia ostrego STEMI
(zmodyf. wg Van der Werf, Circulation 2002)
Podstawowe,
zachowawcze
lityczne
Pierwotna
PCI
Tlen, spoczynek, walka z bólem,
monitorowanie/leczenie arytmii
opcje
LBA, leczenie
przeciwkrzepliwe
Przewidywana
śmiertelność
30 dniowa
Przewidywany czas
hospitalizacji
Kierunki rozwoju
10 %
co
najmniej
7 dni
Bolus/wlew
UFH/LMWH
ASA
PCI - jeśli
utrzymuje się
dławica
6-7 %
5-7 dni
Nowe preparaty,
antytrombiny,
Inhibitory
IIb/IIIa
Heparyna, ASA,
klopidogrel,
czas do pPCI < 120
min
Stent, inhibitor
IIb/IIIa,
trombektomia, IABP
3-4%
Niekiedy ~2 %
3-5 dni
Ułatwiona PCI, ochrona przed
embolizacją, ochrona przed
uszkodzeniem reperfuzyjnym
Hipotermia, hiperoksemia
dowieńcowa

Wskazania do
koronaroplastyki
Świeży zawał serca
Świeży zawał serca
leczenie z wyboru - „primary PCI”
w przypadku przeciwwskazań do fibrynolizy
brak reperfuzji po fibrynolizie („rescue PCI”)
reokluzja po leczeniu fibrynolitycznym
wstrząs kardiogenny

Wskazania do pPCI w STEMI (wg ESC
AD
2003
)
Jeśli pPCI niemożliwe do wykonania przez doświadczony zespół, w czasie < 90 minut
od pierwszego kontaktu z lekarzem – fibrynoliza (gdy brak p/wskazań) – klasa I a
rekomendacja
Klasa I
IIa
IIb
III
Dowody
naukow
e
pPCI
pPCI
Preferowany terapia, jeśli wykonywana przez
Preferowany terapia, jeśli wykonywana przez
doświadczony zespół, w czasie < 90 minut od
doświadczony zespół, w czasie < 90 minut od
pierwszego kontaktu z lekarzem
pierwszego kontaktu z lekarzem
X
A
Wskazana dla chorych we wstrząsie oraz dla
chorych z przeciwwskazaniami do fibrynolizy
X
C
pPCI bez stentu i z inhibitorem IIb/IIIa
X
A
pPCI ze stentem i z inhibitorem IIb/IIIa
X
A
Rescue PCI – gdy rozległy zawał i
nieskuteczne leczenie trombolityczne
X

PCI
po leczeniu fibrynolitycznym
jest wskazane w przypadku:
(pod warunkiem, że anatomia zmian jest
odpowiednia do wykonania PCI)
Dorzut zawału - obiektywnie potwierdzony
Spontanicznego lub sprowokowanego
niedokrwienia we wczesnym okresie po
zawale
Wystąpienia objawów niestabilności
hemodynamicznej lub wstrząsu
kardiogennego

Wykonanie PCI
po leczeniu
fibrynolitycznym
jest także uzasadnione, gdy:
Obecne są objawy niewydolności serca,
EF 40%.
Występują poważne komorowe zaburzenia
rytmu
W ostrej fazie zawał występowały objawy
niewydolności serca, nawet jeśli następnie
wycofały się, a EF > 40%

PCI
po leczeniu fibrynolitycznym
PCI może być wykonane planowo jako
część przyjętej strategii inwazyjnej po
leczeniu fibrynolitycznym

STEMI
STEMI
w ciągu 12 godzin od pojawienia się objawów
chory w szpitalu
z dostępnością PCI
Pierwotna PCI
chory w szpitalu bez dostępności PCI
3 – 12 godzina
< 3 godziny
natychmiastowy
transport
Tromboliza
nieskuteczna
Ratunkowa
PCI
skuteczna
dostępność PCI
24 h
Post-
trombolityczna
PCI
brak dostępności PCI
24 h
ocena niedokrwienia
przed wypisaniem
PCI
-
jeśli
niedokrwienie
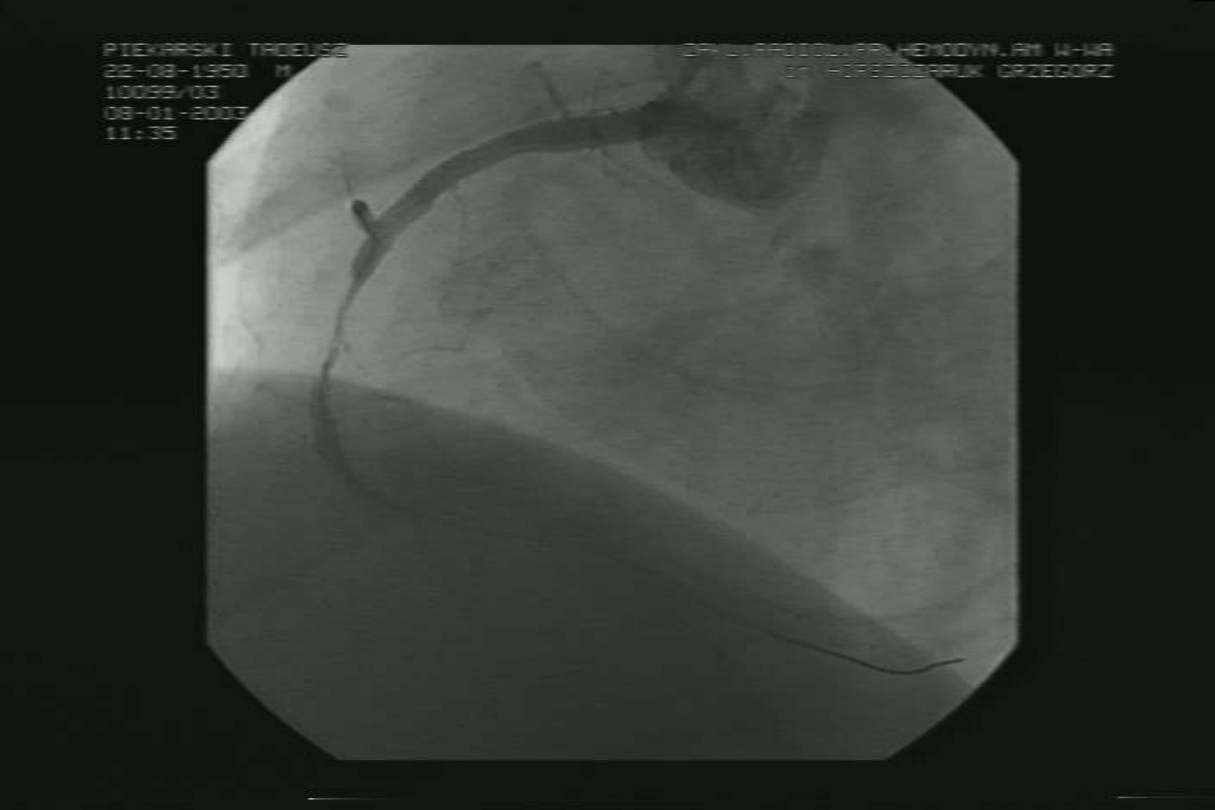
Pierwotna PCI - AMI
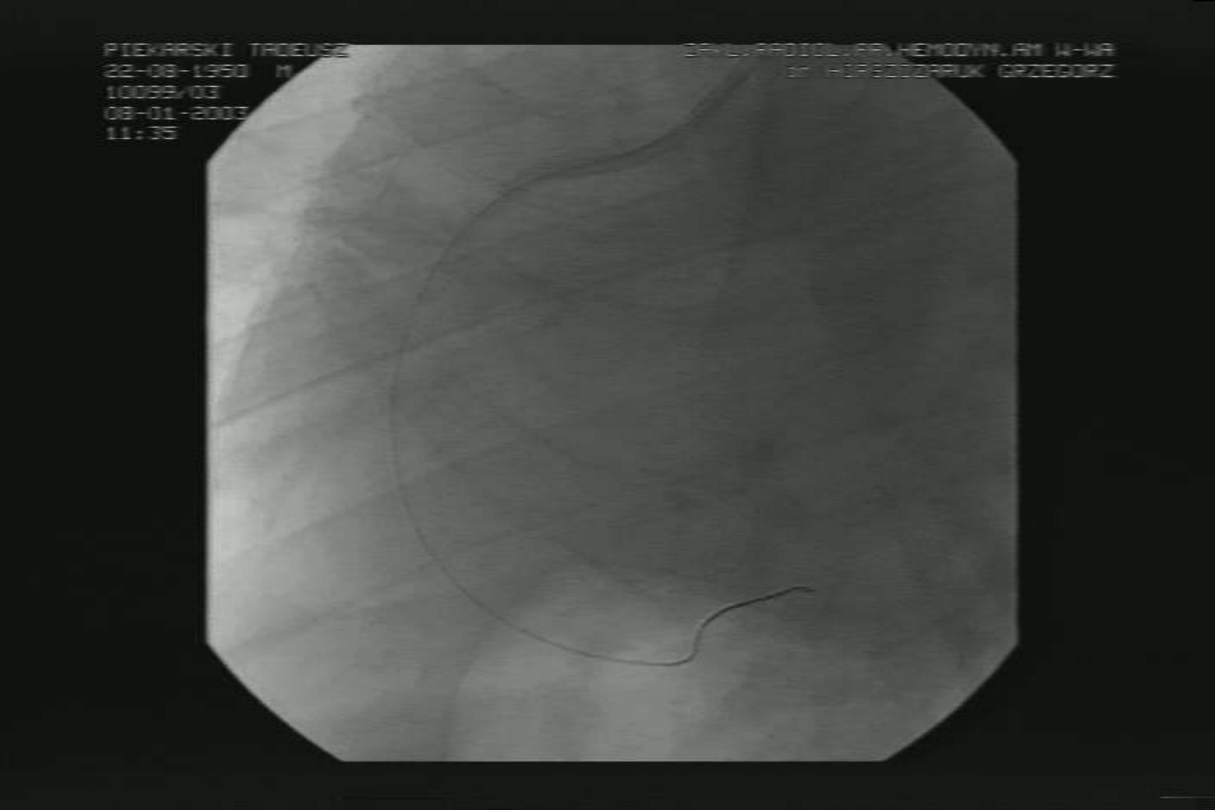
Pierwotna PCI - AMI

Pierwotna PCI w STEMI, efekt
końcowy
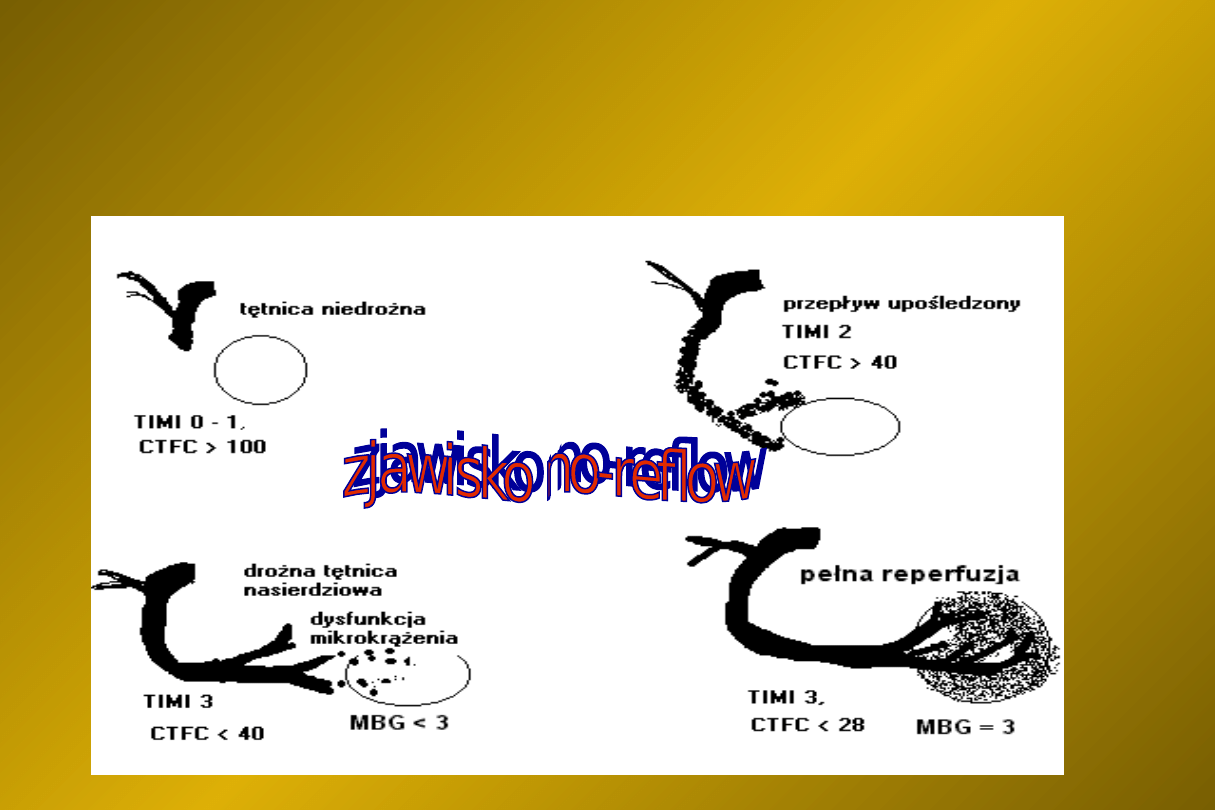
CEL:
drożna tętnica + perfuzja mikrokrażenia

Zjawisko angiograficznego „no-
reflow” (1)
Definicja:
upośledzony (
TIMI 2) przepływ przez
tętnicę odpowiedzialną za zawał
(culprit artery), po jej rekanalizacji –
występujący lub utrzymujący się,
pomimo braku mechanicznej
przeszkody w tętnicy nasierdziowej

Zjawisko angiograficznego „no-
reflow” (2)
Jeśli no-reflow, wówczas we wczesnym okresie częściej
występuje :
Zgon (p=0,002)
Niewydolność serca (p < 0,0001)
Złośliwa arytmia (p=0.038)

WSTRZĄS

Wstrząs kardiogenny-
rozpoznanie
Można rozpoznać wstrząs kardiogenny, jeśli skurczowe ciśnienie tętnicze utrzymuje się poniżej
90
mmHg przez
nie mniej niż 1 godzinę oraz:
Nie reaguje na dożylne podawanie płynów
Jest wtórne do dysfunkcji mięśnia serca lub
Występują objawy tkankowej hipoperfuzji lub
PCWP > 18 mmHg oraz CI < 2,2 l/min/m
2
Rozpoznanie można rozważać nawet jeśli ciśnienie skurczowe w ciągu 1 godziny po włączeniu
katecholamin wzrosło powyżej 90 mmHg.
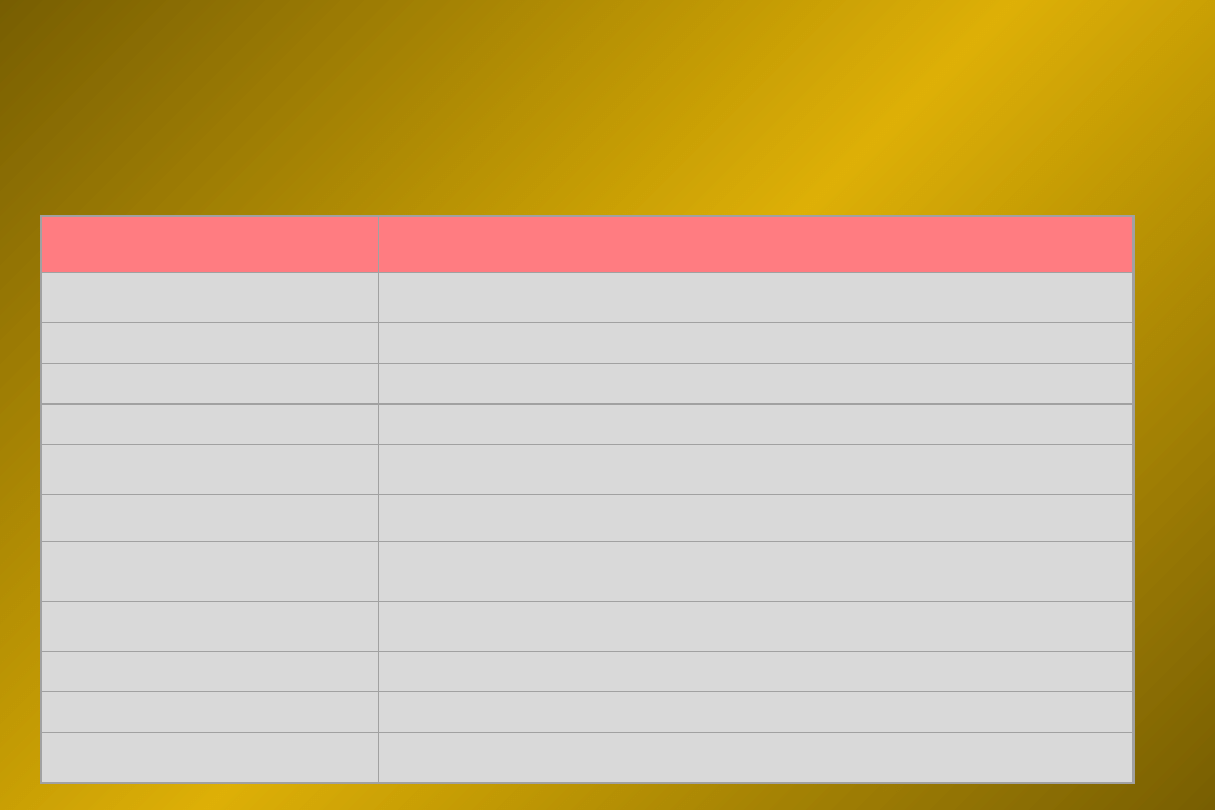
Wstrząs kardiogenny -
postępowanie
DIAGNOSTYKA
POSTĘPOWANIE
Wywiad i badanie przedmiotowe
Dostęp żylny (także centralny)
EKG
Zacewnikowanie pęcherza moczowego i pomiar diurezy
ECHO serca
Monitorowanie ekg, ciśnienia tętniczego oraz pulsoksymetria
Badania laboratoryjne
Tlenoterapia, ewentualnie intubacja i wentylacja mechaniczna
RTG klatki piersiowej
Korekcja zaburzeń metabolicznych z uwzględnieniem dyselektrolitemii i zaburzeń
kwasowo-zasadowych
Inwazyjna ocena
hemodynamiczna
Walka z bólem (morfina, fentanyl) oraz sedacja
Leczenie ewentualnych zaburzeń rytmu
(leki, kardiowersja)
i przewodzenia (stymulacja endokawitarna)
Odstawienie leków mogących nasilać hipotensję (w tym: beta-adrenolityki, azotany,
inhibitory konwertazy angiotensyny)
Uzupełnianie płynów – o ile nie ma obrzęku płuc
Katecholaminy
Diuretyki w przypadku zastoju w krążeniu płucnym
(uwaga na hipotensję!)

Wspomaganie lewej
komory w zabiegach PCI
IABP - kontrapulsacja
wewnątrzaortalna
przy EF < 30%, w niestabilnej dławicy, w AMI
przezskórne krążenie pozaustrojowe
przy EF < 20%
(chorzy zdyskwalifikowani od CABG)
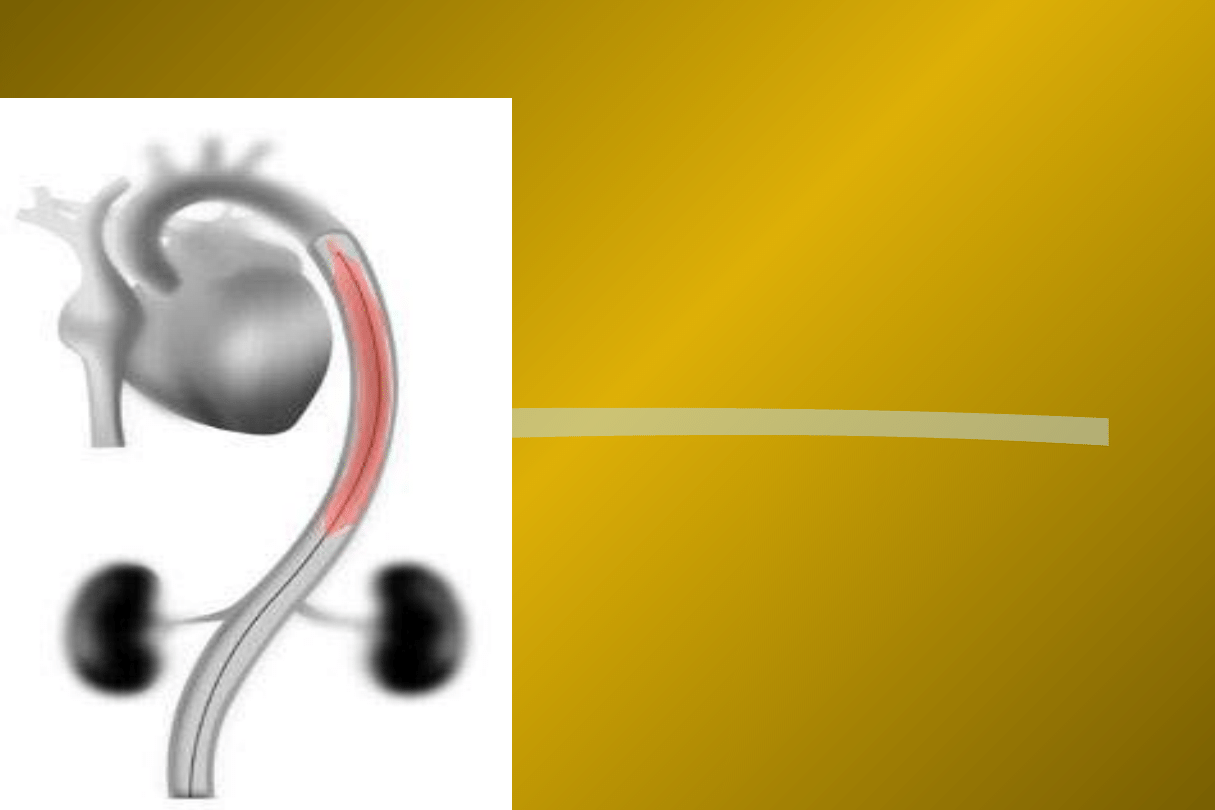
IABP = kontrapulsacja wewnątrzaortalna
Zasada działania IABP:
•
balon wypełnia się (
inflacja balonu
) w
momencie zamknięcia zastawki aortalnej
• poprawa przepływu krwi w tętnicach
wieńcowych i mózgowych
•
deflacja balonu
(tuż przed skurczem
komór) powoduje obniżenie ciśnienia
tętniczego krwi w aorcie – zjawisko
„zasysania” – spadek obciążenia
następczego lewej komory – odciążenie
lewej komory
• max. wzrost o 1 l/min
• uzyskanie stabilności hemodynamicznej
umożliwiającej wykonanie zabiegów
rewaskualryzacyjnych
•
kilka godz – kilka/kilkanaście dni
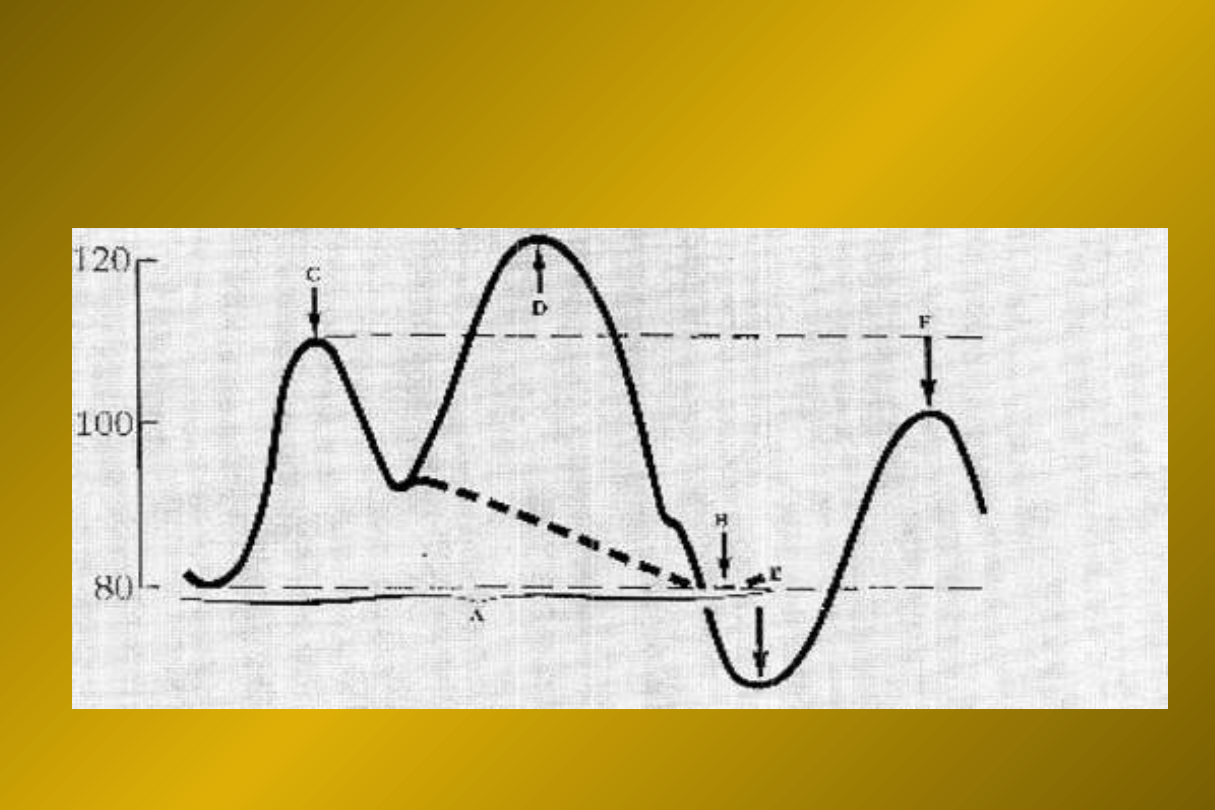
IABP – zasada działania
mmHg
A- pełny cykl sercowy
B – ciśnienie końcoworozkurzcowe w aorcie – bez wspomagania
C – ciśnienie skurczowe – bez wspomagania
D – wzmocnienie diastoliczne
E – ciśnienie końcoworozkurczowe w aorcie - wspomagane
Wzrost perfuzji
wieńcowej
Zmniejszenie
zapotrzebowania
serca na tlen

IABP – skutki zastosowania:
Znaczny wzrost systemowego ciśnienia
rozkurczowego
Redukcja ciśnienia napełniania LK o 5-10 mmHg
Wzrost objętości wyrzutowej i wskaźnika
sercowego
Wzrost przepływu systemowego i wieńcowego,
wkrótce po rozpoczęciu kontrapulsacji


Wskazania do
koronaroplastyki
Dławica u chorych po pomostowaniu tętnic
Dławica u chorych po pomostowaniu tętnic
wieńcowych
wieńcowych
1.
Objawy niedokrwienia w ciągu 30 dni po operacji
2.
Progresja miażdżycy w natywnych tt. wieńcowych
(w tym także poszerzanie zwężenia pnia LTW)
3.
Zwężenie pomostu
(raczej przeciwwskazane udrażnianie przewlekle zamkniętych pomostów
żylnych)

Wskazania do
koronaroplastyki
Dławica u chorych po pomostowaniu tętnic
Dławica u chorych po pomostowaniu tętnic
wieńcowych
wieńcowych – cd.
w przypadku nieobecności rozsianych zmian w pomoście
Stenty !
Profilaktyka mikroembolizacji (często !) - „filtry”
Inhibitory IIb/IIIa nie zmniejszają występowania MI przy PCI
pomostów żylnych !

Co jest ważne przy wyborze
sposobu rewaskularyzacji?
Morfologia i lokalizacja zwężenia
Ilość zajętych naczyń
Anatomia obwodowych odcinków naczyń
Wydolność lewej komory serca
Choroby zwiększające ryzyko operacji
Obecność cukrzycy !
Wcześniej przebyte zabiegi na naczyniach
wieńcowych

PCI czy CABG ?
PCI
Mniejsza inwazyjność - większy
komfort dla chorego
Mniejsze ograniczenia związane z
chorobami towarzyszącymi
Większa dostępność procedury (AMI
!)
Uruchomienie chorego wkrótce po
zabiegu
Możliwość rewaskularyzacji w kilku
etapach
Powtórny zabieg nie jest związany z
istotnie większym ryzykiem
powikłań
CABG
Na ogół pełna rewaskularyzacja
Znacznie rzadsza potrzeba
reinterwencji
Rzadsze nawroty dolegliwości po
zabiegu
Przewaga w zaawansowanej
chorobie wieńcowej
Przewaga u chorych z cukrzycą
oraz ciężką dysfunkcją lewej
komory serca

PCI vs CABG obserwacje odległe – 20 lat
(Serruys, Eur Heart J 2002)
W ciągu pierwszego roku po zabiegu – więcej
reinterwencji po PCI
Po 7-8 latach większość reinterwencji u chorych po CABG
Podobna częstość zgonów i zawałów

Ilość zwężonych naczyń a
kwalifikacja do
rewaskularyzacji –
„wskazania klasyczne”
Choroba jednonaczyniowa -
PTCA
PTCA
(wyjątek - zwężenie pnia LTW; dyskusyjne - krytyczne zwężenie
proksymalnej LAD
Choroba dwunaczyniowa i EF > 40% - raczej
PTCA
PTCA
Choroba wielonaczyniowa i obniżona EF < 40% - raczej
CABG
CABG
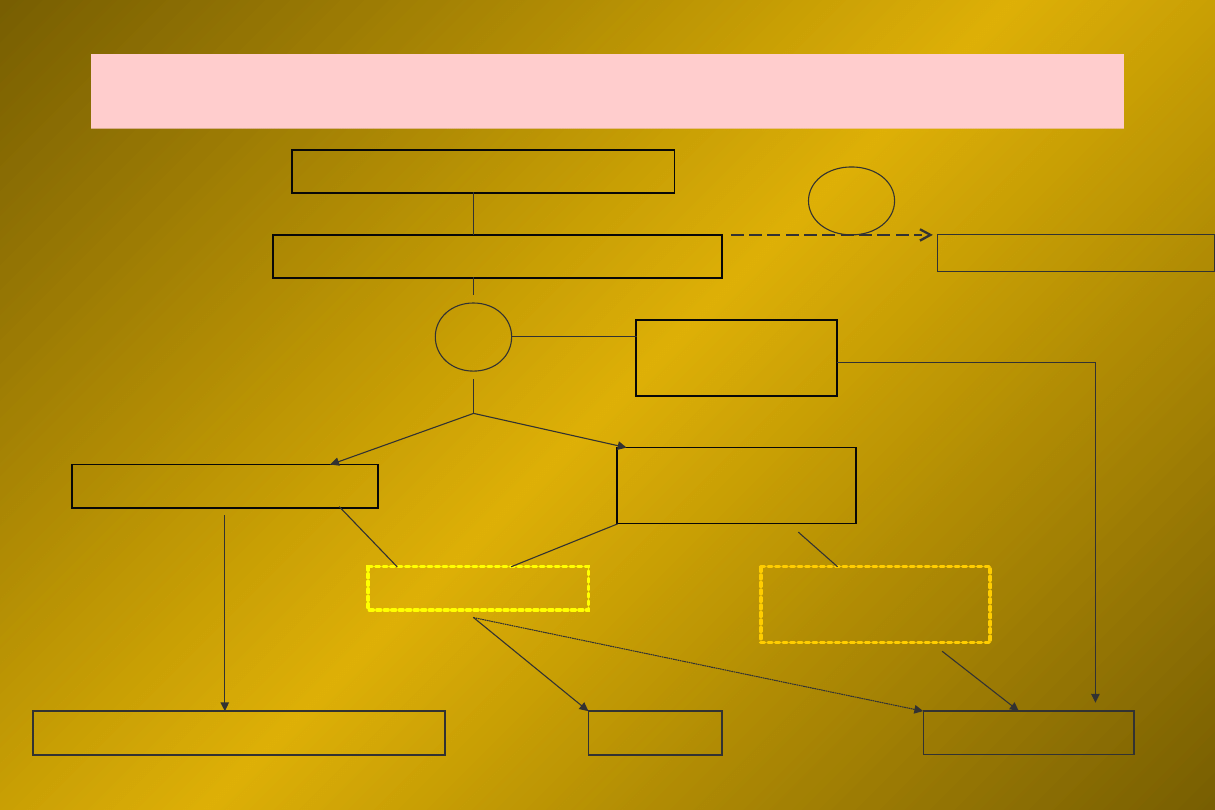
Anatomia naczyń a preferowana metoda rewaskularyzacji
wieńcowej
KORONAROGRAFIA
Obecność istotnego zwężenia
leczenie zachowawcze
Zwężenie
pnia LTW
CABG
Zwężone 1 naczynie
PCI lub farmakoterapia
Prox. GPZ?
PCI
Zmiany w 2 lub
3 naczyniach
Cukrzyca lub
EF < 45%
TAK
NIE

Przeciwwskazania do PCI
a) bezwzględne
zwężenie < 50 % średnicy naczynia
rozsiane zwężenia tętnicy
istotne zwężenia pnia, przy braku drożnego pomostu do GO lub
GPZ (!?)
b) względne
poszerzanie jedynej drożnej tętnicy wieńcowej
poszerzanie tętnicy nieodpowiadającej za zawał (u chorych ze
STEMI)
brak zabezpieczenia kardiochirurgicznego
rozsiane zmiany w pomoście żylnym
istotna koagulopatia, w tym INR > 2

Powikłania PCI
„duże powikłania” - ostre zamknięcie tętnicy
zgon (średnio nie więcej niż 1 % chorych)
zawał serca (w tym zawał bez Q = 3 x wzrost CK-MB) -
około 4 %
konieczność pilnego CABG (nie więcej niż 3 %)
„mniejsze” powikłania - około 5 - 7%
zamknięcie gałęzi bocznej, konieczność defibrylacji lub elektrostymulacji,
udar mózgu, krwawienia, tamponada serca, powikłania w miejscu nakłucia
tętnicy udowej (promieniowej), reakcja alergiczna na kontrast

Ważniejsze czynniki ryzyka
wystąpienia powikłań PCI
A) kliniczne:
wiek > 65 lat
niestabilna choroba wieńcowa lub AMI
wstrząs kardiogenny
niewyrównana niewydolność serca
uprzedni zabieg CABG
B) angiograficzne:
niekorzystna morfologia zwężenia
choroba wielonaczyniowa
duży obszar zagrożenia serca („jeopardy score”)
EF < 35%
nagłe zamknięcie tętnicy w czasie zabiegu

Farmakoterapia w okresie
okołozabiegowym PCI (1)
heparyna
(UFH) –
50-70 U/kg m. ciała - bolus na
początku zabiegu, a następnie ewentualne dawki dodatkowe
pod kontrolą ACT;
(przyszłość
(przyszłość ? - heparyny drobnocząsteczkowe
(
enoxaparyna
) oraz
biwalirudyna)
antagoniści receptora IIb/IIIa
:
abciximab,
tirofiban, eptifibatid
leki podawane dowieńcowo:
NTG - gdy skurcz tętnicy wieńcowej
adenozyna - w przypadku „no reflow” oraz przy czynnościowej ocenie
przepływu wieńcowego
werapamil - w przypadku skurczu nie reagującego na NTG
nitroprusydek sodu – w przypadku ”no-reflow”

Farmakoterapia w okresie
okołozabiegowym PCI (2)
1.
Kwas acetylosalicylowy
-
dawki standardowe
2.
klopidogrel
-
300 mg
(600 mg)
– dawka nasycająca i
następnie 75 mg/d,
minimum – 1 miesiąc (nawet do roku)
(alternatywnie:
tiklopidyna
-
2 x 250 mg/d - najlepiej co najmniej
3 dni przed zabiegiem, po implantacji stentu - kontynuacja przez 4 -6 tyg.)
3. Leki przeciwdławicowe
- w dawkach standardowych
azotany - do rozważenia odstawienie, w przypadku pełnej rewaskularyzacji
LBA u chorego po zawale – wg zaleceń
antagoniści wapnia - można rozważyć ich stosowanie przez kilka miesięcy po
zabiegu, zwłaszcza w przypadku tendencji do skurczu tętnicy

Heparynizacja chorego poddawanego terapii inwazyjnej/PCI
w NSTE_ACS
NSTE-ACS
rozpoznane,
rozpoczęta terapia
LMWH
Wczesna terapia inwazyjna albo obecne są wskazania do pilnej koronarografii w strategii wcześnie
zachowawczej
Koronarografia/PC
Koronarografia/PC
I < 8 godzin po
I < 8 godzin po
ostatniej dawce
ostatniej dawce
LMWH
LMWH
Koro/PCI pomiędzy 8 – 12 godziną po
Koro/PCI pomiędzy 8 – 12 godziną po
ostatniej dawce LMWH
ostatniej dawce LMWH
Bez dodatkowej dawki
LMWH/UFH
+/_Terapia
inhibitorem
IIb/IIIa
+ inhibitor
IIb/IIIa
Bez
inhibitora
IIb/IIIa
Dożylnie UFH 50
U/kg,
Podczas zabiegu
utrzymywać ACT
200 – 250 s
Dodatkowy
bolus
LMWH IV
0,3mg//kg
Dodatkowy
bolus
LMWH IV
0,3-0,5
mg/kg
Dożylnie UFH
60 U/L,
Podczas
zabiegu
utrzymywać
ACT 250-300
s


ZWĘŻENIA AGIOGRAFICZNIE
GRANICZNE
40 - 70 %
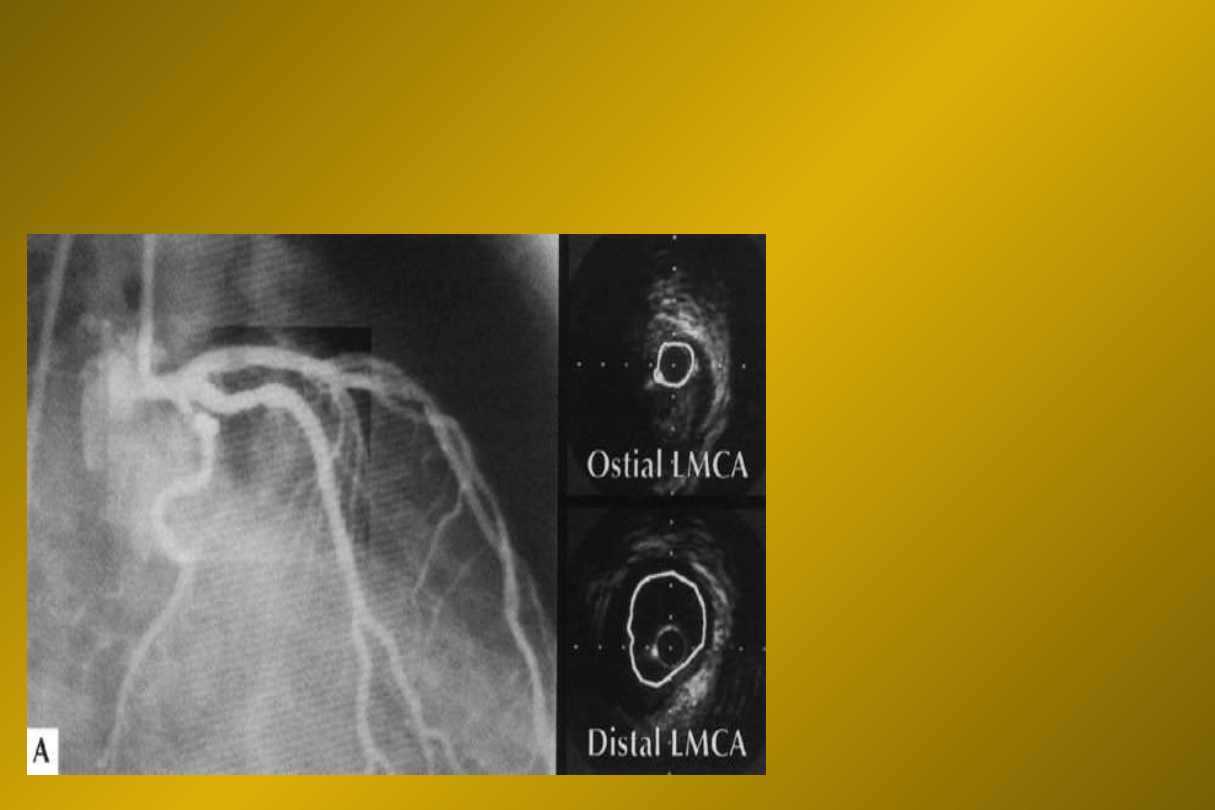
Ultrasonografia
wewnątrznaczyniowa
IVUS
IVUS (1)
Diagnostyka:
uwidocznienie
prawdziwej objętości
blaszki miażdżycowej i
światła naczynia
ocena zmian
wątpliwych
angiograficznie
(fot.)
ocena remodelingu
tętnicy
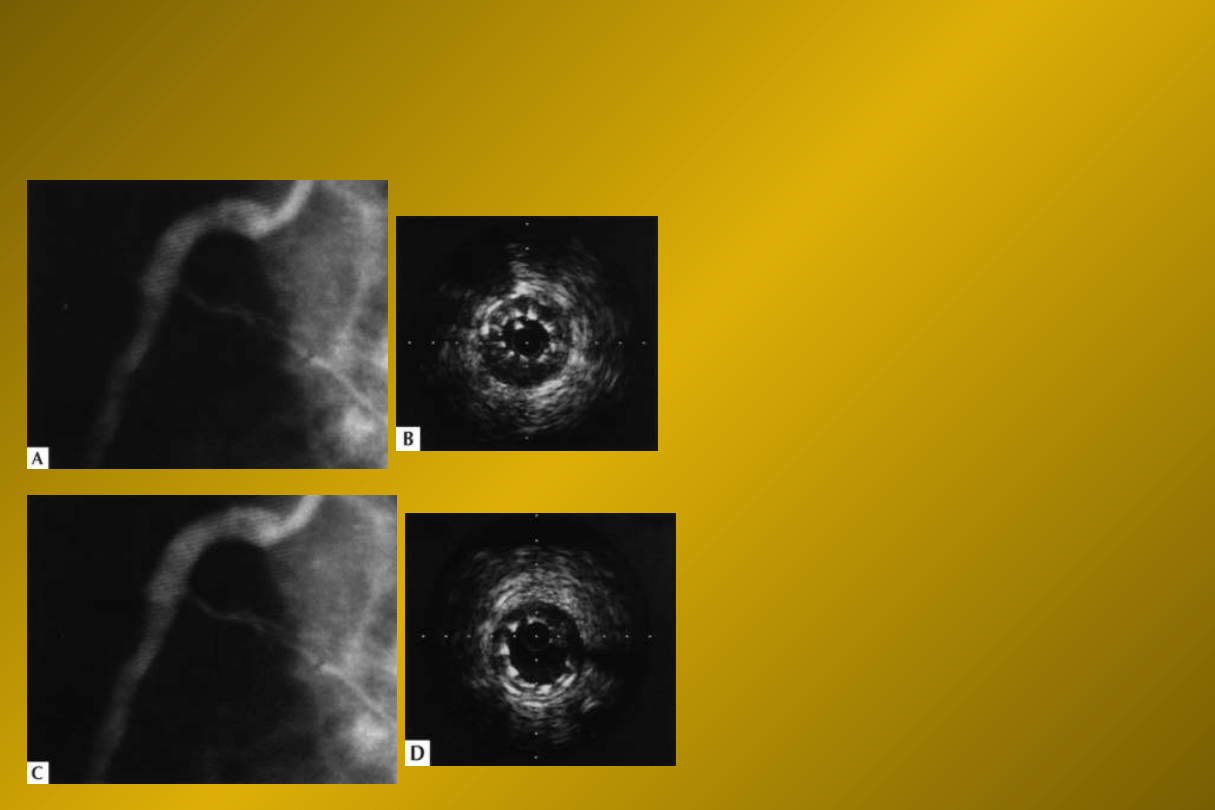
Ultrasonografia
wewnątrznaczyniowa
IVUS
IVUS (2)
Optymalizacja
zabiegu:
ocena prawdziwej średnicy
naczynia oraz zwężenia
rezydualnego
wykrycie niewidocznej
agiograficznie dyssekcji
ocena stentu po rozprężeniu
potwierdzenie obecności
prowadnika w prawdziwym
albo fałszywym świetle

Wskazania do inwazyjnej oceny zwężenia
za pomocą metody cząstkowej rezerwy przepływu
(FFR)
50-70% zwężenie
niedokrwienia nie udokumentowano
/ nie wykonano SPECT
FFR
> 0,8
odroczyć PCI
< 0,75
wykonać PCI

Nattawut et al. Am J Cardiol 2005;96:877–884


RESTENOZA (1)
Definicje:
kliniczna
– dolegliwości wieńcowe spowodowane
nawrotem zwężenia (konieczność powtórnej
rewaskularyzacji – TLR)
angiograficzna
– ponowne zwężenie, powyżej 50 %
redukcji światła, w uprzednio poszerzanym miejscu
Najczęściej pierwsze 3 miesiące po PCI, do 6-9
miesięcy - rzadko później
Średnio u
15-20%
po założeniu stentu
(20- 40 % chorych po POBA )

RESTENOZA (2)
mechanizm:
okres wczesny – elastic recoil
zakrzep w miejscu poszerzanym i jego
organizacja
negatywny remodeling tętnicy
proliferacja tzw. „neointimy” ( w tym przerost
błony wewnętrznej) – restenoza w stencie !

RESTENOZA (3)
ważniejsze czynniki ryzyka:
Cukrzyca
Wąskie naczynie (średnica < 3 mm)
Długa zmiana (> 15 mm)
Większa ilość wszczepionych stentów
Suboptymalny efekt zabiegu (
„bigger is
better”
!)
Przewlekła niewydolność serca
Przewlekła niewydolnośc nerek

RESTENOZA (4)
A) prewencja restenozy
optymalizacja zabiegu
optymalizacja zabiegu
odpowiednia kwalifikacja do zabiegu
odpowiednia kwalifikacja do zabiegu (!)
stenty z substancjami antyproliferacyjnymi (
Drug-
eluting stents
)
(np. rapamycyna, paclitaksel)
brachyterapia wieńcowa – coraz rzadziej stosowana
farmakoterapia - jak dotąd, nie wykazano jednoznacznej
skuteczności
B) leczenie restenozy
re - PCI
CABG
intensyfikacja farmakoterapii przeciwdławicowej

Wskazania do stentów
uwalniających leki
- DES (
IIa C
)
Małe naczynia
Całkowita przewlekła niedrożność
Bifurkacje/zmiany ostialne
Zwężenia w pomostach
DM insulinozależna
MVD
Niezabezpieczony pień LTW
Restenoza w stencie

Stenty uwalniające leki (DES)
Nie powinno się wszczepiać DES
jeśli planuje się wykonanie
zabiegu chirurgicznego w trybie
pilnym/przyspieszonym
Konieczne leczenie przeciwpłytkowe:
ASA + tienopirydyna, przez 6 – 12 miesięcy po
zabiegu
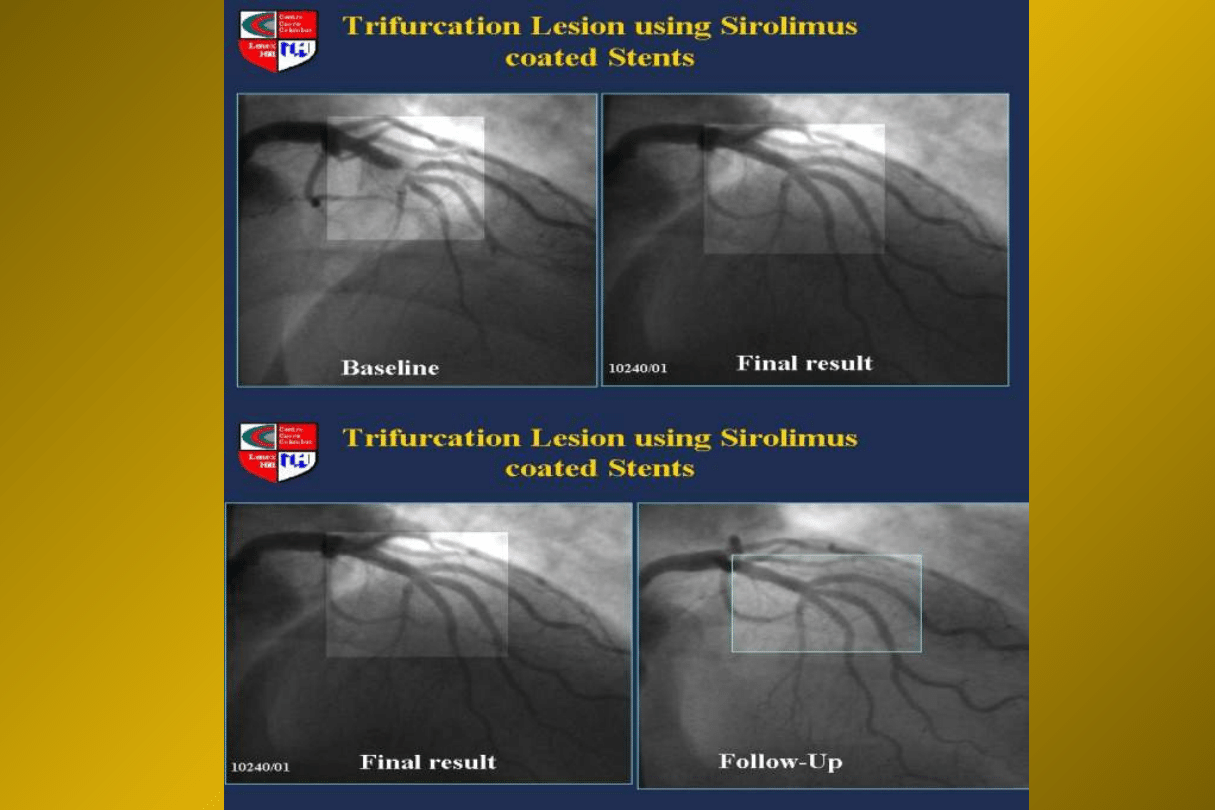

Postępowanie z chorym po
rewaskularyzacji wieńcowej (1)
Wykonywanie testów obciążeniowych rutynowo, u
wszystkich chorych po zabiegach, nie jest obecnie
zalecane
Dla weryfikacji objawów ewentualnej restenozy –
preferowane badania obrazowe (SPECT lub ECHO z
dobutaminą)
Próba wysiłkowa EKG - dla oceny ogólnej wydolności
fizycznej chorego i zaplanowania rehabilitacji

Postępowanie z chorym po
rewaskularyzacji wieńcowej (2)
Modyfikacja czynników ryzyka ChNS
Całkowite zaprzestanie palenia tytoniu
Redukcja masy ciała (cel: BMI 21- 25 kg/m2)
Trening fizyczny (rekreacja – 30 minut, 3 –4 x / tydzień)
Kontrola ciśnienia tętniczego
(cel: < 130/85 mmHg)
Kontrola lipidogramu
(cel: LDL < 100mg/dL,
HDL > 35mg/dL, TG <
200mg/dL)
Kontrola cukrzycy
(cel: dążenie do normoglikemii oraz HbA1c < 7
g/dL)
Postępowanie z chorym po
rewaskularyzacji wieńcowej (3)
Farmakoterapia
Kwas acetylosalicylowy (ASA) – bezterminowo u chorych bez
przeciwwskazań
Po implantacji stentu: ASA + tiklopidyna/klopidogrel – przez
minimum 4 tygodnie [klopidogrel – optimum 6-12 mcy po
PCI]
Leki hipolipemizujące (statyny !)
Inhibitory ACE
Beta adrenolityki
Antagoniści wapnia (amlodypina) ?

Strategia w kompleksowych zabiegach PCI
1.
1.
Oceń ryzyko
Oceń ryzyko
2.
2.
Użyj odpowiedniego sprzętu
Użyj odpowiedniego sprzętu
3.
3.
Oceń grunt, po którym się poruszasz
Oceń grunt, po którym się poruszasz
4.
4.
Nie bądź zbyt ambitny, być może
Nie bądź zbyt ambitny, być może
ostateczny cel jest teraz nieosiągalny
ostateczny cel jest teraz nieosiągalny



Chorzy objawowi z już rozpoznaną ChNS
wskazania do koronarografii
Dławica CCS 1-2, objawy niewydolności
LK (EF <45%), przy dodatnim, lecz nie
wybitnie, wyniku testu nieinwazyjnego
Wątpliwym wynik testu
obciążeniowego, nie pozwalający na
określenie dalszego rokowania

Stabilni chorzy bez/skąpoobjawowi
wskazania do koronarografii
Chory z niepewnym rozpoznaniem ChNS, po wykonanych testach
obciążeniowych, u którego pewne postawienie rozpoznania
usprawiedliwa wykonanie diagnostyki inwazyjnej (ryzyko, koszt)
Chory, u którego nie można wykonać testów obciążeniowych z powodu
chorób towarzyszących, niemożności wykonania wysiłku, patologicznej
otyłości
Chory wykonujący zawód, który wymaga pewnego
potwierdzenia/wykluczenia ChNS
Chory, u którego ze względu na wystąpienie objawów w młodym wieku,
podejrzewa się niemiażdżycowe tło ChNS (ch. Kawasaki, anomalie tt.
wieńcowych, vasculopatię)
Chorzy, u których podejrzewa się naczynioskurczową postać ChNS i
konieczne jest wykonanie inwazyjnego testu prowokującego skurcz tt.
wieńcowych
Chorzy z wysokim prawdopodobieństwem (klinicznym) zaawansowanej
ch wieńcowej – zwężenia pnia lub MVD

Chorzy objawowi z już rozpoznaną ChNS
wskazania do koronarografii
Dławica CCS 1 – 2, EF >45%,
bez wybitnie dodatniego wyniku testu
nieinwazyjnego
Początkowo dławica CCS 3 – 4, która
zmniejszyła się do CCS 1-2 po włączeniu
farmakoterapii
Dławica CCS 1 – 2, przy złej
tolerancji/poważnych efektach
niepożądnych farmakoterapii

Chorzy stabilni z niepewnym rozpoznaniem
wskazania do koronarografii
Chorzy wielokrotnie hospitalizowani z
powodu bólów w klatce piersiowej,
wymagających postawienia ostatecznego
rozpoznania
Chorzy bardzo żądający ostatecznego
rozpoznania/wykluczenia ChNS, u których
istnienie tej choroby jest prawdopodobne
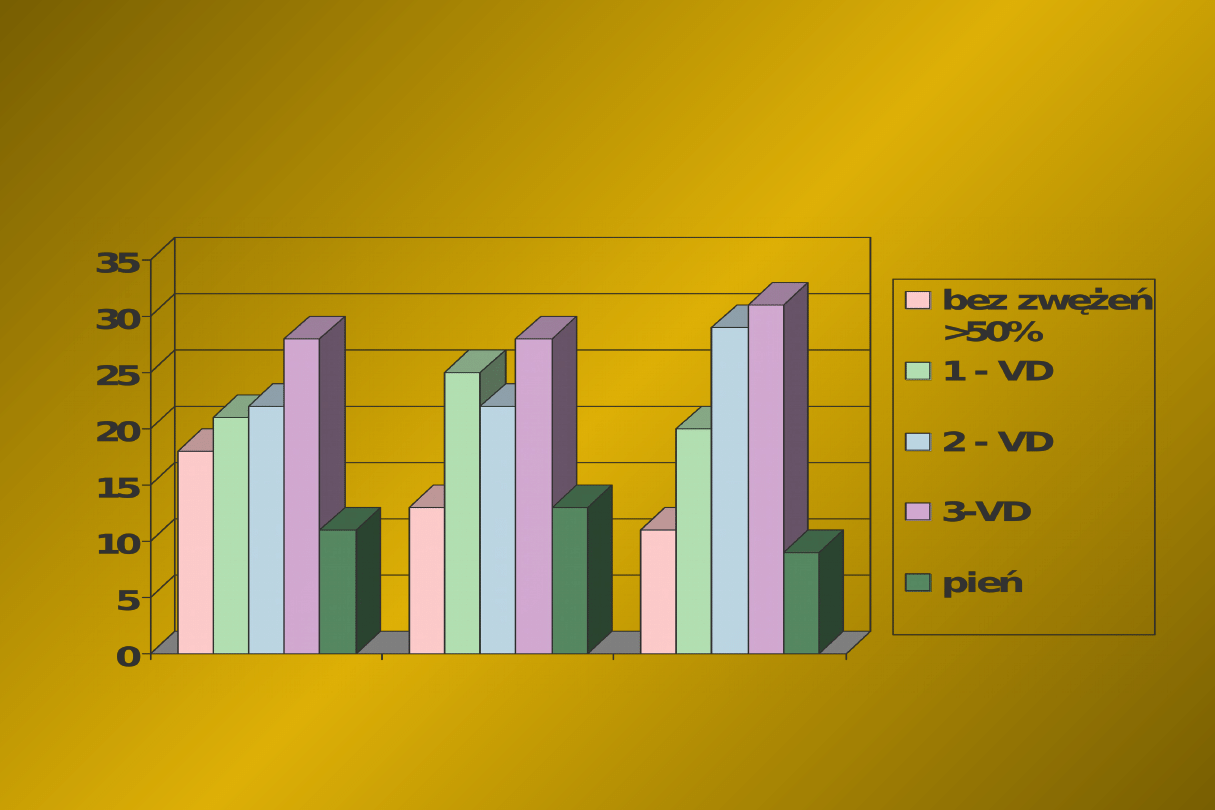
Anatomia zmian w tętnicach wieńcowych
u mężczyzn ze stabilną dławicą
um
ia
rk
ow
an
a
Z
na
cz
ni
e
na
si
lo
na
N
as
ila
ją
ca
s
ię
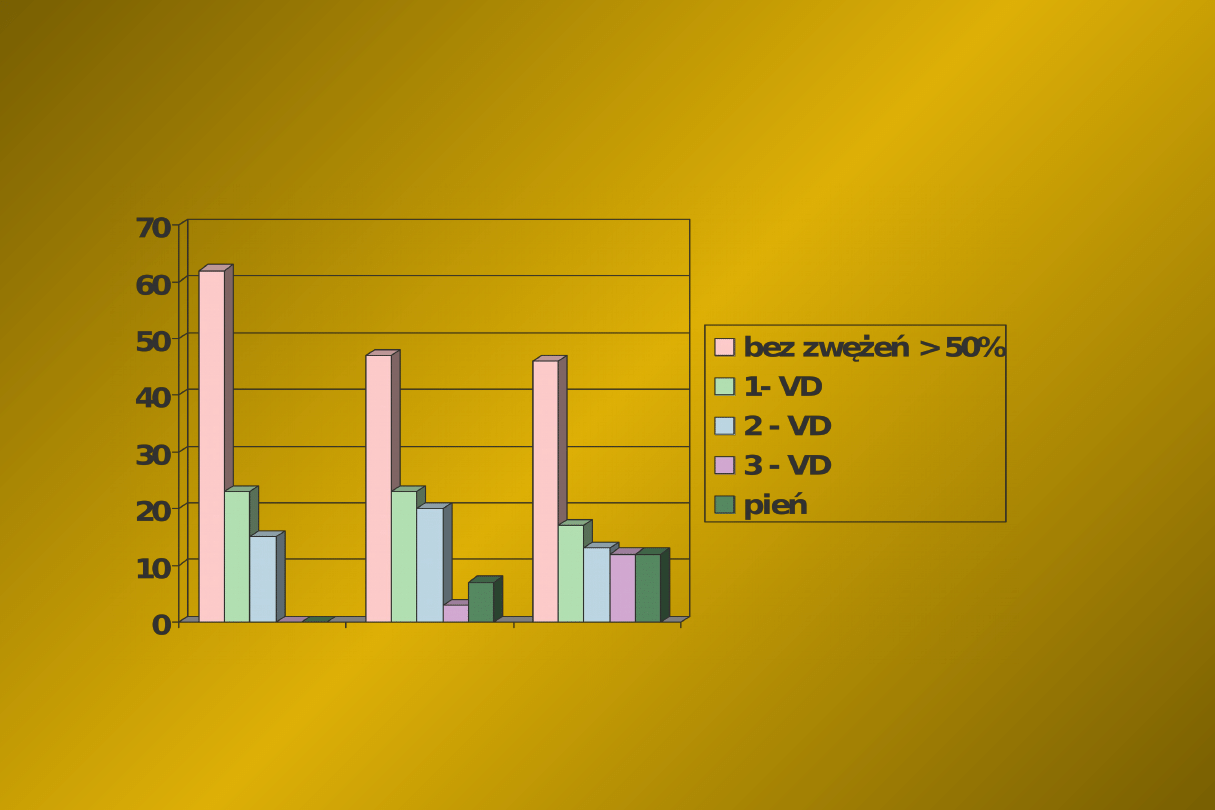
Anatomia zmian w tętnicach wieńcowych
u kobiet ze stabilną dławicą
um
ia
rk
ow
an
a
zn
ac
zn
ie
na
si
lo
na
na
si
la
ją
ca
s
ię

No – reflow: zapobieganie
Jak najkrótszy czas od początku objawów do
rekanalizacji naczynia !
Antagoniści IIb/IIIa !
Mechaniczne zapobieganie embolizacji –
protection devices
? Ułatwiona angioplastyka !
? IABP - wspomaganie pracy LK !
? Farmakologiczny preconditioning (nicorandil, adenozyna, opiaty) ?
? Stopniowana reperfuzja i/czy direct stenting ?

No – reflow: leczenie
Antagoniści IIb/IIIa (bolus ic lub iv + wlew
iv.)
Adenozyna ic.
NTG ic.
Nitroprusydek sodu ic.
Werapamil ic
Papaveryna ic.
Nicorandil ic.

UA/NSTEMI
strategie postępowania
Wczesna strategia inwazyjna: koronarografia
u wszystkich chorych bez przeciwwskazań do
rewaskularyzacji - wykonywana w ciągu
pierwszych 48 h hospitalizacji
Wczesna strategia zachowawcza:
koronarografia tylko, gdy: nawracająca
dławica CCS 4, duża dynamika zmian ST,
oporność na maksymalną faramakoterapię,
wybitnie dodatnie próby obciążeniowe

PCI - techniki zmierzające do
skrócenia czasu zabiegu i
hospitalizacji
Bezpośrednie wszczepianie
stentów
(czas zabiegu – ok. 30 minut)
Zabiegi z dostępu
transradialnego
(uruchomienie chorego – natychmiast,
wypisanie do domu – po 6 godzinach)

Wczesna strategia inwazyjna -
na pewno, kiedy:
Dławica CCS 4/niedokrwienie nawracające lub oporne, mimo
intensywnej farmakoterapii
Dławica/nawracające niedokrwienie z objawami CHF, S3, MR
EF<40% w ECHO
Wybitnie dodatnie testy nieinwazyjne przed hospitalizacją
Niestabilność hemodynamiczna
Groźne zaburzenia rytmu serca (sVT, VF)
PCI w ciągu poprzedzających 6 miesięcy
Stan po CABG
Kolejny epizod ACS, choć bez czynników najwyższego ryzyka
U chorych > 65 rż lub z obniżeniem ST lub podwyższonymi
wartościami markerów martwicy serca i bez
przeciwwskazań do rewaskularyzacji
ACC/AHA

Kwalifikacja do
rewaskularyzacji (2)
Obiektywna ocena niedokrwienia i krążenia
wieńcowego
zapis ekg
badania laboratoryjne
(troponina, CK-MB)
próba wysiłkowa ekg
scyntygrafia wysiłkowa (SPECT)
echokardiograficzna próba z dobutaminą
koronarografia
inne inwazyjne metody oceny krążenia wieńcowego
(IVUS; metody czynnościowa ocena zwężenia; próby farmakologiczne)

Chorzy ze stabilną ChNS
wskazania do PCI
Krótkie zwężenie żylnego pomostu aortalno-wieńcowego
Wielopunktowe zwężenie pomostu aortalno-wieńcowego u
chorych nie będących dobrymi kandydatami
do re-CABG
Choroba 2 – lub 3 tętnic, bez istotnego zwężenie
proksymalnej GPZ, z umiarkowanie rozległym obszarem
zaopatrzenia i niedokrwieniu wykazanym w teście
nieinwazyjnym
Choroba 1-naczyniowa z zajęciem proksymalnego odcinka
GPZ

Chorzy ze stabilną ChNS
wskazania do PCI
Choroba 2 – lub 3 tętnic , z istotnym zwężeniem
proksymalnej GPZ i korzystną dla PCI
morfologią zmian, u chorego z cukrzycą lub
dysfunkcja LK
Zwężenie pnia LTW u chorego, który nie może
być zakwalifikowany do CABG (pod warunkiem
odpowiedniej morfologii zmiany)
Choroba 2 lub 3 – naczyniowa u chorego, który
po przebytym NZK lub z utrwalonymi VT
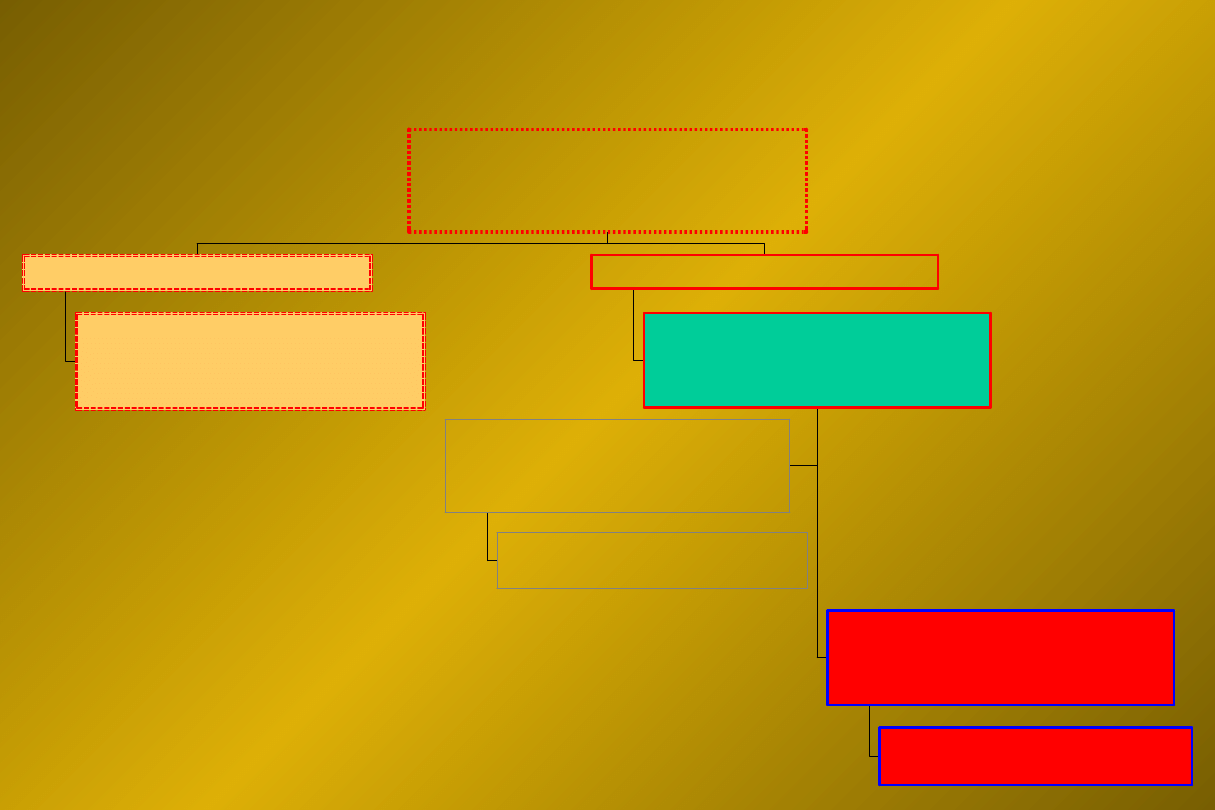
ALGORYTM POSTĘPOWANIA W ACS (wg. ESC)
(Eur. Heart J. 2000 21:1406-1432)
F i b r y n o l i z a
i / l u b
A n g i o p l a s t y k a
P r z e t r w a ł e u n i e s i e n i e S T
E T T / S P E C T / E C H O z d o b u ta m in ą
( p r z e d w y p is a n ie m lu b a m b u la to r y jn ie )
T r o p o n in a - p r a w id ło w a
( o c e n a p r z y p r z y ję c iu o r a z p o 6 - 1 2 h )
B l o k e r G P I I b /I I I a
K o r o n a r o g r a fi a i r e w a s k u l a r y z a c j a
T r o p o n i n a p o d w y ż s z o n a
N a w r a c a j ą c a d ł a w i c a , d ł a w i c a p o z a w a ł o w a
N i e s t a b i l n o ś ć h e m o d y n a m i c z n a
Z a b u r z e n i a r y t m u z w i ą z a n e z n i e d o k r w i e n i e m
A S A
A z o t a n y i v .
B e t a a d r e n o l i t y k
H e p a r y n a ( L M W H )
B e z p r z e t r w a ł e g o u n i e s i e n i a S T
O b j a w y k l i n i c z n e s u g e r u j ą c e A C S :
1 . B a d a n i e k l i n i c z n e
2 . E K G
3 . P o b r a n i e k r w i d o b a d a ń

Zjawisko angiograficznego
„no-reflow” (2)
No – reflow występuje częściej częściej, gdy:
Przepływ przez culprit artery bezpośrednio przed
interwencją < TIMI 2
Nieobecność dławicy prodromalnej – w ciągu
ostatnich 48 h
Znacznie upośledzona funkcja LK
(WMS śr < 19, klasa
Killipa >2)

Chorzy objawowi z już rozpoznaną CHD
wskazania do koronarografii
Dławica CCS3 pomimo leczenia
farmakologicznego
Wybitnie dodatni wynik testu wysiłkowego (lub
innego testu nieinwazyjnego), niezależnie od
aktualnego nasilenia dławicy
Dławica u chorego po przebytym NZK z
powodów kardiologicznych oraz groźnymi
komorowymi zaburzeniami rytmu
Chorzy z dławicą i objawami niewydolności
serca
Przy objawach klinicznych wskazujących na
wysokie ryzyko znacznego zaawansowania
choroby wieńcowej
ACC/AHA 2002

Chorzy bezobjawowi lub
skąpoobjawowi
z niepewnym rozpoznaniem
Wskazania do koronarografii
Chory po przebytym nagłym
zatrzymaniu krążenia, z wstępnie
rozpoznawaną lub podejrzewaną
dławicą piersiową.
ACC/AHA 2002

Chorzy stabilni, z niepewnym
rozpoznaniem
koronarografia nie jest zalecana
Chorzy obciążeni poważnymi chorobami,
u których ryzyko koronarografii
przewyższa korzyść z jej wykonania
Pacjenci żądający postawienia
ostatecznej diagnozy, przy bardzo małym
prawdopodobieństwem istnienia ChNS
ACC/AHA 2002

Chorzy ze stabilną ChNS
wskazania do PCI
Choroba 2 - lub 3 tętnic wieńcowych, także z zajęciem
proksymalnego segmetu GPZ, z morfologią zmian korzystną
dla PCI, u chorego bez cukrzycy i z prawidłową funkcją LK.
PCI/CABG w chorobie 2 lub 3 tętnic, ale bez zajęcia
proksymalnego odcinka GPZ, zaopatrujących znaczny obszar
żywego miokardium, przy wybitnie dodatnim wyniku testów
nieinwazyjnych
Nawrót zwężenia po PCI, wykonanym w naczyniu
zaopatrującym duży obszar żywego miokardium lub przy
wybitnie dodatnim wyniku testu nieinwazyjnego
Nieskuteczność farmakoterapii przeciwdławicowej u
chorych, którzy mogą być poddani leczeniu inwazyjnemu
z akceptowalnym poziomem ryzyka
ACC/AHA 2002

Randomizowane badania stent vs CABG
PCI
CABG
PCI
CABG
PCI
CABG
Śmiertelność (%)
0,9
5,7
2,5
2,8
2,5
0,8 (!?)
Ponowna
rewaskularyzacja
(%)
16,8
4,8
16,8
3,5
17
3,2
Typ stentu
GR II
Crown,
Cross Flex
róźne
Stentowanie mnniej kosztowne, MACE- bez różnicy, istotnie więcej
reinterwncji po PCI
ARTS
ERACI II
SOS

Chorzy ze stabilną ChNS
PCI nie jest zalecana
Dławica CCS 1 – 2 dobrze
kontrolowana farmakologicznie, przy
ujemnym wyniku testów
nieiwazyjnych
Chory, który woli uniknąć leczenia
inwazyjnego
ACC/AHA 2002

Chorzy ze stabilną ChNS
PCI nie jest zalecana
Choroba 2 lub 3 tętnic wieńcowych, bez zajęcia
proksymalnej GPZ, u chorych demonstrujących
niewielkie objawy prawdopodobnie niezwiązane z
niedokrwieniem serca lub nie otrzymujący
odpowiedniej farmakoterapii, o ile:
nie stwierdzono niedokrwienia w testach nieinwazyjnych
obszar ulegający niedokrwieniu jest mały
Graniczne (50-60%) zwężenie zlokalizowane poza
pniem LTW przy nie wykazaniu niedokrwienia w
testach nieinwazyjnych
Zwężenie nieistotne hemodynamicznie ( < 50 %)
Istotne zwężenie pnia LTW, u chorego będącego dobrym
kandydatem do CABG
ACC/AHA 2002
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
- Slide 59
- Slide 60
- Slide 61
- Slide 62
- Slide 63
- Slide 64
- Slide 65
- Slide 66
- Slide 67
- Slide 68
- Slide 69
- Slide 70
- Slide 71
- Slide 72
- Slide 73
- Slide 74
- Slide 75
- Slide 76
- Slide 77
- Slide 78
- Slide 79
- Slide 80
- Slide 81
- Slide 82
- Slide 83
- Slide 84
- Slide 85
- Slide 86
- Slide 87
- Slide 88
- Slide 89
- Slide 90
- Slide 91
- Slide 92
- Slide 93
- Slide 94
- Slide 95
- Slide 96
- Slide 97
- Slide 98
- Slide 99
- Slide 100
- Slide 101
- Slide 102
- Slide 103
Wyszukiwarka
Podobne podstrony:
Chirurgiczne leczenie choroby wieńcowej, pięlęgniarstwo, mgr
maloinwazyjne metody w leczeniu choroby wiencowej
LECZENIE CHOROBY WIEŃCOWEJ
Chirurgiczne leczenie choroby wieńcowej w świeżym zawale mięśnia serca
W06 SZ W06 Leki stosowane w leczeniu choroby wieńcowej (Marta E )
Leczenie chorob pasozytniczych, FARMACJA, Farmakologia z el. chemii leków
03 0000 039 02 Leczenie choroby Lesniowskiego Crohna u dzieci
Leczenie chorób tarczycy, fizjoterapia
Choroba wieńcowa, FIZJOTERAPIA
Leczenie chorób tarczycy, Patologia i choroby
chirurgiczne leczenie choroby wrzodowej, Chirurgia ogólna
więcej podobnych podstron