
Instytut Materiałów Inżynierskich i
Biomedycznych
Zakład Odlewnictwa
Wydział Mechaniczny
Technologiczny
POLITECHNIKA ŚLĄSKA W
GLIWICACH
Odlewnictwo
Krystalizacja i krzepnięcie
Odlewnictwo
Krystalizacja i krzepnięcie
GLIWICE – ROK
2005
Mirosław
Cholewa

Literatura:
Literatura:
Crosley P., Douglas A., Mondolfo L.: Interfacial Energies in Heterogeneous
Crosley P., Douglas A., Mondolfo L.: Interfacial Energies in Heterogeneous
Nucleation,The Solid. of Metals, The Iron and Steel Inst. nr 110, London 1968, s.10
Nucleation,The Solid. of Metals, The Iron and Steel Inst. nr 110, London 1968, s.10
Bramfitt B.: The effect of Carbide and Nitride Addition on the heterogeneous
Bramfitt B.: The effect of Carbide and Nitride Addition on the heterogeneous
Nucleation Behavior of Liquid Iron, Metall. Trans., 1970, s. 1987
Nucleation Behavior of Liquid Iron, Metall. Trans., 1970, s. 1987
Gliksman M., Childs W.: Nucleation Catalysis in Supercooled Liquid Tin, Acta Metall.
Gliksman M., Childs W.: Nucleation Catalysis in Supercooled Liquid Tin, Acta Metall.
1962, s.925
1962, s.925
Fraś E.: Teoret. Podst. Kryst., cz. 1, skr. uczeln. nr 930 Kraków 1984, s 82
Fraś E.: Teoret. Podst. Kryst., cz. 1, skr. uczeln. nr 930 Kraków 1984, s 82
Oostdijk J.,
Oostdijk J.,
C.: Van kiem tot kristalliet. Pr. Dokt. Delft, Drukkerij J., H. Pasmans, 1967
C.: Van kiem tot kristalliet. Pr. Dokt. Delft, Drukkerij J., H. Pasmans, 1967
Chalmers B.: Principles of Solidification
Chalmers B.: Principles of Solidification
,
,
John Wiley & Sons, New York 1964, s.68
John Wiley & Sons, New York 1964, s.68
Verma A. R.: Crystal growth and dislocations. Butterworths Scientific Publications,
Verma A. R.: Crystal growth and dislocations. Butterworths Scientific Publications,
London 1953,
London 1953,
Missol W.: Energia powierzchni rozdziału faz, Wyd. „Śląsk”. Katowice 1975
Missol W.: Energia powierzchni rozdziału faz, Wyd. „Śląsk”. Katowice 1975
Braszczyński J., Krystalizacja odlewów, WNT, Warszawa 1991
Braszczyński J., Krystalizacja odlewów, WNT, Warszawa 1991
Jones H., Leak M.G.: The surface entropy of solid metals, Metall. Sci. v. 1, 1967, s. 211
Jones H., Leak M.G.: The surface entropy of solid metals, Metall. Sci. v. 1, 1967, s. 211
Jones H.: The surface energy of solid metals. Metall. Sci. v. 5, 1971, s. 15
Jones H.: The surface energy of solid metals. Metall. Sci. v. 5, 1971, s. 15
Jones H.: The grain boundary term in surface energy measurement by zero creep,
Jones H.: The grain boundary term in surface energy measurement by zero creep,
Scripta Met. v. 6, 1972, s. 423Allen B.C.: Effect of crystallographic orientation on the
Scripta Met. v. 6, 1972, s. 423Allen B.C.: Effect of crystallographic orientation on the
surface free energy and surface self-diffusion of solid molybdenum. Trans. Metall. Soc.
surface free energy and surface self-diffusion of solid molybdenum. Trans. Metall. Soc.
AIME v. 245, 1969, s. 2089
AIME v. 245, 1969, s. 2089
Guggenheim E.A.: Termodynamics, Amsterdam, North-Holland Publ.Co 1950
Guggenheim E.A.: Termodynamics, Amsterdam, North-Holland Publ.Co 1950
Burden M.H., Hunt J.D., J. Cryst. Growth, Trans., vol. 22, 1974, s. 109.
Burden M.H., Hunt J.D., J. Cryst. Growth, Trans., vol. 22, 1974, s. 109.
Tiller W., Grain size control during ingot solidification, Trans, of the Metall. Soc., v.
Tiller W., Grain size control during ingot solidification, Trans, of the Metall. Soc., v.
224, s. 448.
224, s. 448.
Witzke S., Riquet J., Durand F., Acta Metallurgica, vol.29, 1981, s. 365
Witzke S., Riquet J., Durand F., Acta Metallurgica, vol.29, 1981, s. 365
Fredrikson H., Hillert M., On formation of the central equiaxed zone in ingots.
Fredrikson H., Hillert M., On formation of the central equiaxed zone in ingots.
Met.Trans., v. 3, 1972, s. 565
Met.Trans., v. 3, 1972, s. 565
Elliot R., The formation of the equiaxed crystal zone during solidification. The British
Elliot R., The formation of the equiaxed crystal zone during solidification. The British
Foundryman, No.10, 1964, p. 164
Foundryman, No.10, 1964, p. 164
Bałandin G., Formirowanije kristalliczeskowo strojenija otliwok, Maszinistr., Moskwa
Bałandin G., Formirowanije kristalliczeskowo strojenija otliwok, Maszinistr., Moskwa
1973.
1973.
Flemings M., Solidification processing, Met. Trans., vol,5, 1974, s. 2121.
Flemings M., Solidification processing, Met. Trans., vol,5, 1974, s. 2121.
Southin R.T., Trans,TMS-AIME, v.236, 1967, s.220.
Southin R.T., Trans,TMS-AIME, v.236, 1967, s.220.
Fraś E., Krzepnięcie metali i stopów, WN PWN, Warszawa 1992.
Fraś E., Krzepnięcie metali i stopów, WN PWN, Warszawa 1992.
Kurz W., Fisher D. J., Fundamentals solidification, Trans, Tech. Publ., Paris 1984.
Kurz W., Fisher D. J., Fundamentals solidification, Trans, Tech. Publ., Paris 1984.
Chalmers B., The structure of ingots, J. Aust. Int. Met.,vol.8, 1963, s. 224.
Chalmers B., The structure of ingots, J. Aust. Int. Met.,vol.8, 1963, s. 224.
Southin R., Nucleation of equiaxed zone i cast metals, TMS-AIME, vol.229, 1967,
Southin R., Nucleation of equiaxed zone i cast metals, TMS-AIME, vol.229, 1967,
s.220.
s.220.
Ohno A., The solidification of metals. Chijin Shoken, Tokyo 1980.
Ohno A., The solidification of metals. Chijin Shoken, Tokyo 1980.
Jackson K., Hunt J., Uhlmann D., Soward T., Trans. TMS-AIME, vol. 236, 1967, p. 149.
Jackson K., Hunt J., Uhlmann D., Soward T., Trans. TMS-AIME, vol. 236, 1967, p. 149.
Langenberg F.C., Prestel G., Honeycutt C.R., Trans.
Langenberg F.C., Prestel G., Honeycutt C.R., Trans.
TMS-AIME, vol. 221, 1961, p. 993.
TMS-AIME, vol. 221, 1961, p. 993.

Kinetyka krzepnięcia
odlewów
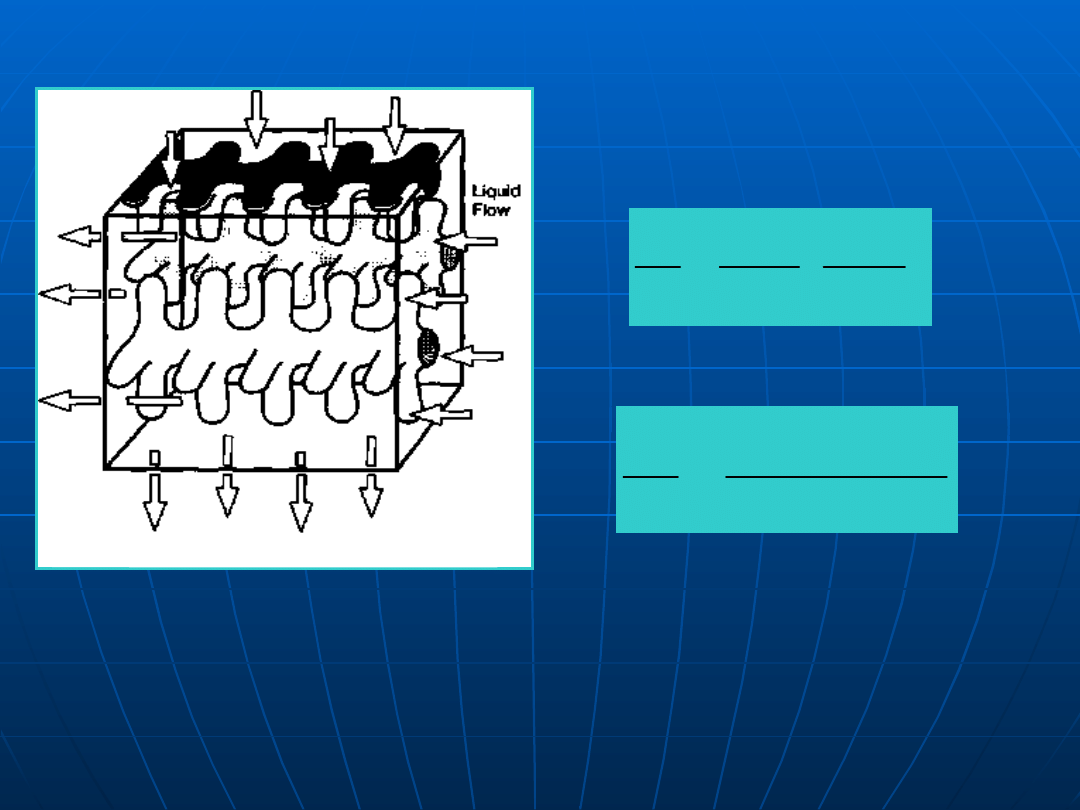
Równoważność oddziaływań fizycznych i
chemicznych
e
e
O
l
k
k
D
mC
v
G
1
D
C
C
m
v
G
O
E
l
gdzie:
G
l
- gradient temperatury w cieczy, v - prędkość krystalizacji.
C
O
, C
E
- stężenie
cieczy i dendrytów, m - nachylenie linii
likwidus, D - współczynnik dyfuzji
obszar jednofazowy
obszar dwufazowy

Funkcję Gibbsa, funkcję stanu można przedstawić
w następującej postaci:
A
PV
TS
U
G
Zapis dotyczy całego, dowolnego układu złożonego obejmującego
parametry ekstensywne i intensywne. Przyjmowane założenia dotyczą
zawsze ustalania jednego z nich i zmienności drugiego.
Energię swobodną rozłożono na składowe: objętościową i
powierzchniową, przy czym objętość przypisano sumie objętości
składników przed tworzeniem stopu jak i po jego wytworzeniu wraz z
powstałymi produktami reakcji między nimi. Mamy zatem dla:
objętości:
V=Vi+Vi-n (VA=0)
energii wewnętrznej:
U=UV+UA
entropii:
S=SV+SA
energii swobodnej
F=FV+FA
liczby moli
ni=nVi+nAi
zależności:

W technologiach wykorzystujących dodatkowe
W technologiach wykorzystujących dodatkowe
oddziaływania fizyczne jak np.: pola elektryczne,
oddziaływania fizyczne jak np.: pola elektryczne,
magnetyczne konieczne jest ich uwzględnienie w
magnetyczne konieczne jest ich uwzględnienie w
ogólnym bilansie energetycznym:
ogólnym bilansie energetycznym:
)
(
)
(
)
(
)
(
i
A
i
A
A
A
i
V
i
V
V
V
A
A
V
V
V
i
i
n
d
Ad
dT
S
A
F
d
dG
n
d
VdP
dT
S
PV
F
d
dG
A
F
G
PV
TS
U
G
dn
Ad
VdP
SdT
dG
dA
dn
BdM
Qd
VdP
SdT
dG
i
i
gdzie: S - entropia, T - temperatura, V - objętość, P - ciśnienie, Q
- ładunek elektryczny, ψ- potencjał elektryczny, M - moment
magnetyczny, B - indukcja magnetyczna, μi- potencjał chemiczny
składnika, ni - ilość składnika i (mol), ω – energia
powierzchniowa, A - powierzchnia.
Wszystkie procesy dynamicznego oddziaływania na kąpiel
Wszystkie procesy dynamicznego oddziaływania na kąpiel
można rozpatrywać jako wzrost energii Fermiego, a także
można rozpatrywać jako wzrost energii Fermiego, a także
energii wewnętrznej cieczy. Powiększa się, zatem także
energii wewnętrznej cieczy. Powiększa się, zatem także
metastabilność układu przyspieszając w ten sposób
metastabilność układu przyspieszając w ten sposób
krystalizację. Makroskopowe lub lokalne zwiększanie
krystalizację. Makroskopowe lub lokalne zwiększanie
ciśnienia w kąpieli jest termodynamicznie analogiczne do
ciśnienia w kąpieli jest termodynamicznie analogiczne do
zwiększania stopnia przechłodzenia. Znajduje to
zwiększania stopnia przechłodzenia. Znajduje to
potwierdzenie w teorii W.A. Tillera dotyczącej zarodkowania
potwierdzenie w teorii W.A. Tillera dotyczącej zarodkowania
w metalach i stopach a opisanych równaniem Clausiusa-
w metalach i stopach a opisanych równaniem Clausiusa-
Clapeyrona:
Clapeyrona:
L
V
T
dp
dT
V
T
dH
dT
dp
E
f
E
f
E
gdzie: dp wzrost ciśnienia, dTE- rzeczywiste zwiększenie
przechłodzenia, dHf – molowe ciepło topnienia, ΔVf -zmiana
jednostkowej objętości cieczy przy krzepnięciu, L - ciepło
krystalizacji

Wyznaczając następnie temperaturę T
Wyznaczając następnie temperaturę T
E
E
i
i
wstawiając ją do zależności na krytyczny promień
wstawiając ją do zależności na krytyczny promień
zarodka homogenicznego lub heterogenicznego, w
zarodka homogenicznego lub heterogenicznego, w
klasycznym rozumieniu uzyskuje się odpowiedni
klasycznym rozumieniu uzyskuje się odpowiedni
promień krytyczny (r
promień krytyczny (r
x
x
) powstały w nowych
) powstały w nowych
warunkach:
warunkach:
sin
2
2
T
T
L
G
r
E
dp
dT
T
V
r
sin
2
gdzie: ω i Θ to odpowiednio - swobodna energia
powierzchniowa między kryształem a cieczą i kąt
zwilżania

Korzystając z zależności na energię swobodną – funkcji
Korzystając z zależności na energię swobodną – funkcji
Helmholtza i potencjału termodynamicznego Herringa
Helmholtza i potencjału termodynamicznego Herringa
można wykazać współzależność i równoważność
można wykazać współzależność i równoważność
oddziaływań fizycznych i chemicznych, głównie w strefie
oddziaływań fizycznych i chemicznych, głównie w strefie
granicznej reprezentowanej przez powierzchnię kontaktu,
granicznej reprezentowanej przez powierzchnię kontaktu,
lecz także w objętości otaczającej powierzchnię kontaktu:
lecz także w objętości otaczającej powierzchnię kontaktu:
Z energii swobodnej Helmholtza:
Z energii swobodnej Helmholtza:
TS
U
F
energia swobodna powierzchni:
A
TS
U
F
A
A
A
Ad
dT
S
n
VdP
dT
S
n
n
A
A
F
G
n
PV
F
G
TS
U
F
A
i
iA
V
i
iV
i
iA
A
A
i
iV
V
V
V
V
V
)
(
energia użyteczna powierzchni:
gdzie: σ - napięcie powierzchniowe

W obszarze międzyfazowym gęstość, ciśnienie, skład chemiczny i
W obszarze międzyfazowym gęstość, ciśnienie, skład chemiczny i
właściwości fizyczne zmieniają się w zakresie od wartości
właściwości fizyczne zmieniają się w zakresie od wartości
charakterystycznych dla cieczy do wartości typowych dla
charakterystycznych dla cieczy do wartości typowych dla
kryształów. Dla zastosowań związanych z układami wielofazowymi,
kryształów. Dla zastosowań związanych z układami wielofazowymi,
wskazane byłoby posługiwanie się koncepcją Guggenheima
wskazane byłoby posługiwanie się koncepcją Guggenheima
uwzględniającą niezerową grubość fazy powierzchniowej o
uwzględniającą niezerową grubość fazy powierzchniowej o
cechach i własnościach dodatkowej fazy objętościowej.
cechach i własnościach dodatkowej fazy objętościowej.
Zróżnicowanie energii powierzchniowej występuje zarówno na
Zróżnicowanie energii powierzchniowej występuje zarówno na
różnych płaszczyznach krystalograficznych tego samego metalu,
różnych płaszczyznach krystalograficznych tego samego metalu,
ale także na różnych kierunkach krystalograficznych należących
ale także na różnych kierunkach krystalograficznych należących
do wspólnej płaszczyzny.
do wspólnej płaszczyzny.
Jeśli przyjąć, że energia powierzchniowa jest proporcjonalna do
Jeśli przyjąć, że energia powierzchniowa jest proporcjonalna do
niewysycenia wiązań atomowych wówczas minimalną energię
niewysycenia wiązań atomowych wówczas minimalną energię
powierzchniową będą posiadały płaszczyzny krystalograficzne
powierzchniową będą posiadały płaszczyzny krystalograficzne
gęstego upakowania atomów
gęstego upakowania atomów
Lokalny dodatkowy efekt energetyczny pozostający w związku z
Lokalny dodatkowy efekt energetyczny pozostający w związku z
topografią i morfologią kryształów wpływa na inicjowanie i
topografią i morfologią kryształów wpływa na inicjowanie i
przebieg generowania dyfuzyjnej strefy przejściowej między cieczą
przebieg generowania dyfuzyjnej strefy przejściowej między cieczą
a kryształami.
a kryształami.
Przykładowo wielkość energii krawędziowej w atmosferze
Przykładowo wielkość energii krawędziowej w atmosferze
powietrza w temperaturze 900
powietrza w temperaturze 900
o
o
C dla srebra wynosi: λ(100)=38
C dla srebra wynosi: λ(100)=38
pJ/m, λ(111)=57 pJ/m. Miedź w atmosferze wodoru w
pJ/m, λ(111)=57 pJ/m. Miedź w atmosferze wodoru w
temperaturze 1000oC posiada: λ(100)=20 pJ/m i λ(111)=34 pJ/m
temperaturze 1000oC posiada: λ(100)=20 pJ/m i λ(111)=34 pJ/m

Dla zaistnienia zarodkowania niezbędne jest stworzenie
Dla zaistnienia zarodkowania niezbędne jest stworzenie
właściwego przechłodzenia cieczy przed frontem krystalizacji.
właściwego przechłodzenia cieczy przed frontem krystalizacji.
Zarodki znajdujące się w innych obszarach odlewu powstają na
Zarodki znajdujące się w innych obszarach odlewu powstają na
granicach faz - między innymi przez kontakt ciekłego metalu z
granicach faz - między innymi przez kontakt ciekłego metalu z
elementami formy, w tym głównie układu wlewowego. Modele
elementami formy, w tym głównie układu wlewowego. Modele
opisujące ten zakres dziedziny zarodkowania to między innymi:
opisujące ten zakres dziedziny zarodkowania to między innymi:
Chalmersa – tzw. „big bang” oparty na idei zarodkowania poprzez
Chalmersa – tzw. „big bang” oparty na idei zarodkowania poprzez
kryształy zamrożone powstałe na wewnętrznej powierzchni wnęki
kryształy zamrożone powstałe na wewnętrznej powierzchni wnęki
formy
formy
Ohno – polegający na zarodkotwórczym działaniu kryształów
Ohno – polegający na zarodkotwórczym działaniu kryształów
oderwanych od powierzchni wnęki formy
oderwanych od powierzchni wnęki formy
Jaksona i in. – według, których powstaje w kąpieli dyspersja
Jaksona i in. – według, których powstaje w kąpieli dyspersja
kryształów poprzez ich nadtapianie i rozmnażanie
kryształów poprzez ich nadtapianie i rozmnażanie
Southina – w którym zarodki powstają na powierzchni ciekłego
Southina – w którym zarodki powstają na powierzchni ciekłego
metalu. Jest tzw. model deszczowy
metalu. Jest tzw. model deszczowy
Tillera lub Witzkego– o zarodkowaniu przed frontem krystalizacji
Tillera lub Witzkego– o zarodkowaniu przed frontem krystalizacji
Uwzględniające zewnętrzne pola siłowe – wymuszoną konwekcję i
Uwzględniające zewnętrzne pola siłowe – wymuszoną konwekcję i
w jej następstwie fragmentację dendrytów na skutek
w jej następstwie fragmentację dendrytów na skutek
•
-fluktuacji temperatury
-fluktuacji temperatury
•
-mechanicznego działania ciekłego metalu
-mechanicznego działania ciekłego metalu
•
-połączonego wpływu czynników: kinetycznego, stężeniowego i
-połączonego wpływu czynników: kinetycznego, stężeniowego i
cieplnego
cieplnego

W procesie zarodkowania, przy wspomaganiu zwilżania
W procesie zarodkowania, przy wspomaganiu zwilżania
fizycznymi oddziaływaniami, sumaryczna powierzchnia
fizycznymi oddziaływaniami, sumaryczna powierzchnia
międzyfazowa nie dość, że jest wielokrotnie większa niż w
międzyfazowa nie dość, że jest wielokrotnie większa niż w
tradycyjnych stopach to jeszcze dodatkowo aktywowana
tradycyjnych stopach to jeszcze dodatkowo aktywowana
może zmieniać swoją powierzchnię kontaktu w zależności
może zmieniać swoją powierzchnię kontaktu w zależności
od temperatury, lokalnego składu chemicznego,
od temperatury, lokalnego składu chemicznego,
chwilowego stężenia i intensywności zewnętrznego pola
chwilowego stężenia i intensywności zewnętrznego pola
siłowego.
siłowego.
Podsumowując można postawić tezę:
Podsumowując można postawić tezę:
zwiększenie energii powierzchniowej jest
zwiększenie energii powierzchniowej jest
skutkiem poprawnego zwilżania oraz
skutkiem poprawnego zwilżania oraz
właściwej adhezji i dyfuzji, powodując
właściwej adhezji i dyfuzji, powodując
minimalizację naprężeń i ich homogenizację
minimalizację naprężeń i ich homogenizację

Trajektoria ruchu
Trajektoria ruchu
pojedynczego jonu Fe w
pojedynczego jonu Fe w
temperaturze 1823 K
temperaturze 1823 K
rzutowana na płaszczyznę
rzutowana na płaszczyznę
poziomą YOX
poziomą YOX
jest on związany z ruchem
jest on związany z ruchem
dużej grupy sąsiednich
dużej grupy sąsiednich
jonów, co prowadzi do
jonów, co prowadzi do
stabilności lokalnej
stabilności lokalnej
struktury w czasie 6
struktury w czasie 6
·
·
10
10
-3
-3
s.
s.
Jon w tym czasie może
Jon w tym czasie może
znajdować się w stanie
znajdować się w stanie
ruchu drgającego
ruchu drgającego
względem prawie
względem prawie
nieruchomego środka
nieruchomego środka
równowagi, a następnie
równowagi, a następnie
wykonuje przeskok do
wykonuje przeskok do
nowego ośrodka drgań.
nowego ośrodka drgań.

Charakterystyki struktur atomowych
Charakterystyki struktur atomowych
metali w stanie stałym i ciekłym
metali w stanie stałym i ciekłym
Metal
Stan skupienia
stały
ciekły
Liczba
koordyna-
cyjna
Średnia
odległość
miedzy
atomami
l0
-1
nm
Temperatu
ra
K
Liczba
koordynacy
jna
Średnia
odległość
między
atoniami
10
-1
nm
Al
12
2,86
973
10,6
2,96
Zn
6—6
2,16—2,90
763
11
2,94
Hg
6—6
3,47—3,00
293
12
3,30
Na
8
3,72
373
8
4,38
Ge
4
2,34
1273
8
2,70
Bi
3—3
3,09—3,46
613
7—8
3,32

Z tabl. wynika, że dla czystych metali (Al, Zn, Hg, Na) liczba
Z tabl. wynika, że dla czystych metali (Al, Zn, Hg, Na) liczba
koordynacyjna przy roztapianiu nie zmienia się lub
koordynacyjna przy roztapianiu nie zmienia się lub
zmniejsza w niewielkim stopniu. Dla nich upakowanie w
zmniejsza w niewielkim stopniu. Dla nich upakowanie w
stanie ciekłym i stałym odpowiada jednej klasie struktur.
stanie ciekłym i stałym odpowiada jednej klasie struktur.
Dla innych metali (Bi, Ge) liczba koordynacyjna przy
Dla innych metali (Bi, Ge) liczba koordynacyjna przy
roztapianiu wzrasta. W stanie stałym metale te mają
roztapianiu wzrasta. W stanie stałym metale te mają
strukturę o mniejszym stopniu upakowania (defekty
strukturę o mniejszym stopniu upakowania (defekty
struktury), a w ciekłym — bardziej gęstą, odnoszącą się już
struktury), a w ciekłym — bardziej gęstą, odnoszącą się już
do drugiej klasy struktur. Roztapianie powoduje częściowe
do drugiej klasy struktur. Roztapianie powoduje częściowe
rozerwanie połączeń między atomami, co pozwala zapełnić
rozerwanie połączeń między atomami, co pozwala zapełnić
atomami „pustki" krystalograficzne, istniejące w sieci ciała
atomami „pustki" krystalograficzne, istniejące w sieci ciała
stałego. Wreszcie część metali, mających w stanie stałym
stałego. Wreszcie część metali, mających w stanie stałym
sieć tetragonalną (Zn, Hg, Bi), traci tetragonalność po
sieć tetragonalną (Zn, Hg, Bi), traci tetragonalność po
roztopieniu.
roztopieniu.
Ogólnie stwierdza się, że metale po stopieniu rozszerzają
Ogólnie stwierdza się, że metale po stopieniu rozszerzają
się tylko o 3 - 5% (Bi nawet się kurczy), tak że liczba i
się tylko o 3 - 5% (Bi nawet się kurczy), tak że liczba i
upakowanie najbliższych sąsiadów nie mogą ulegać
upakowanie najbliższych sąsiadów nie mogą ulegać
poważniejszym zmianom
poważniejszym zmianom
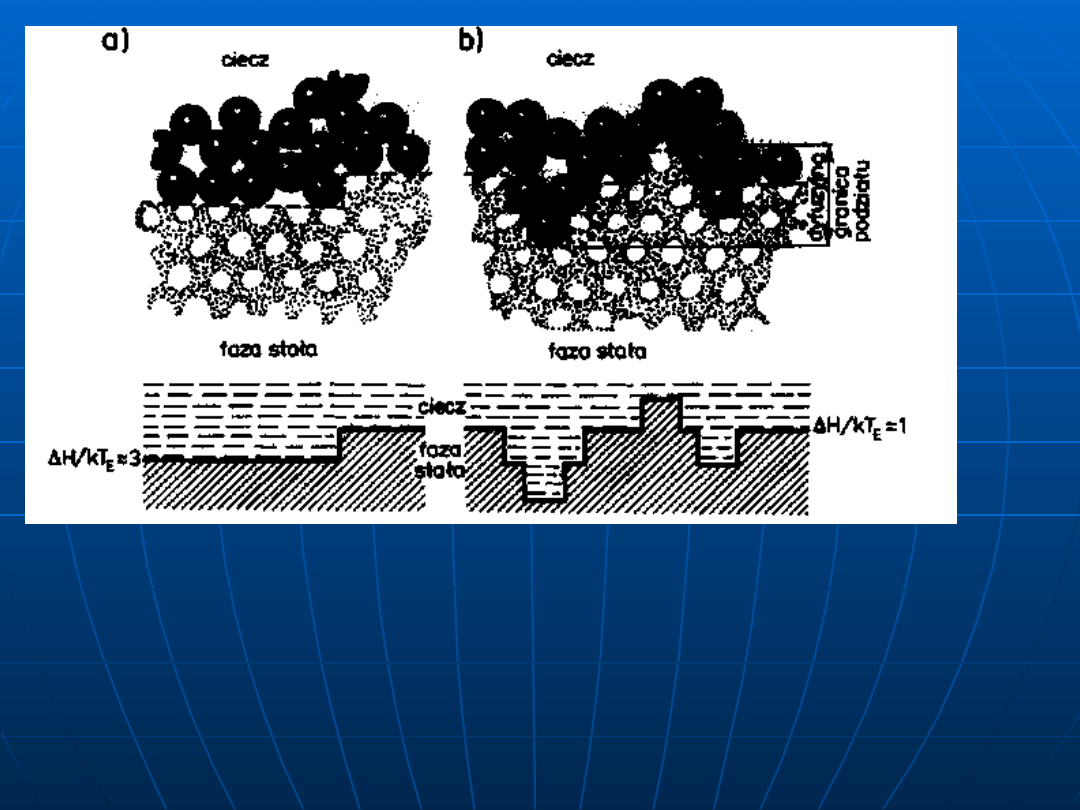
Model rozłożenia atomów w cieczy (ciemne kule) i w fazie stałej
Model rozłożenia atomów w cieczy (ciemne kule) i w fazie stałej
(jasne kule) na powierzchni:
(jasne kule) na powierzchni:
a) atomowogładkiej, b) szorstkiej — rozmytej;
a) atomowogładkiej, b) szorstkiej — rozmytej;
H
H
— entalpia,----- umowna granica rozdziału faz: ciecz — faza stała
— entalpia,----- umowna granica rozdziału faz: ciecz — faza stała
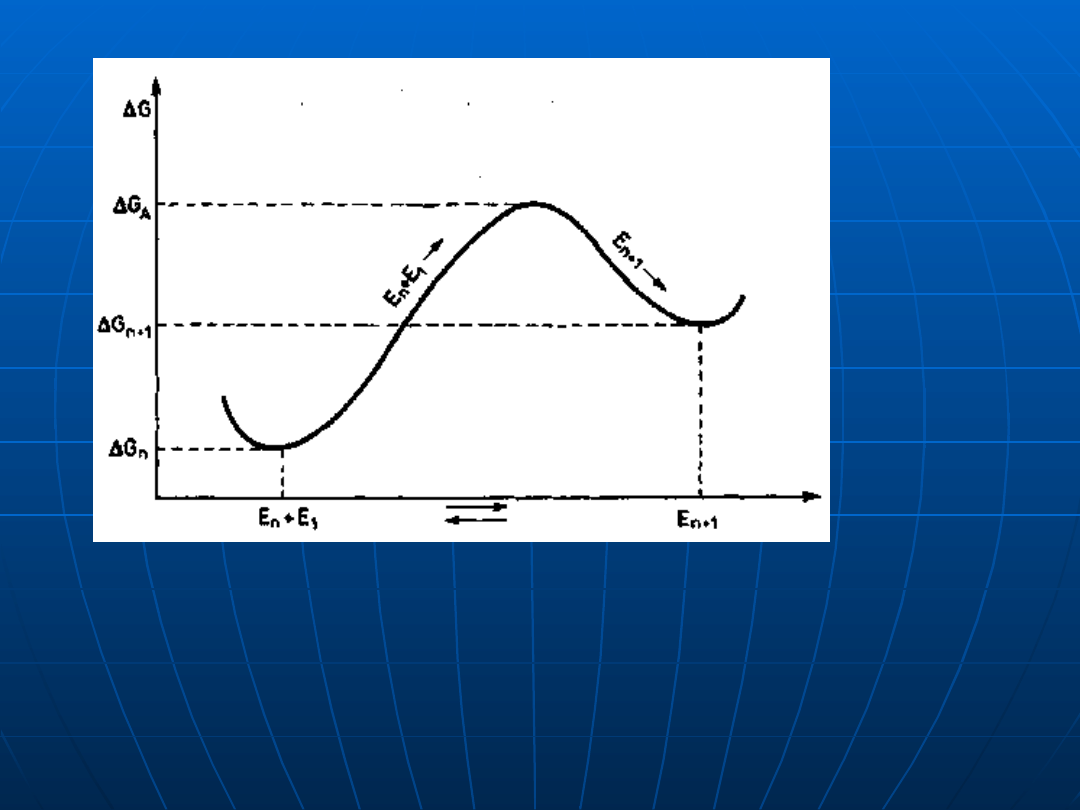
Energia swobodna układu
Energia swobodna układu
Δ
Δ
G w funkcji zmiany rozmieszczenia
G w funkcji zmiany rozmieszczenia
atomów, spowodowanej przyłączeniem nowego atomu E
atomów, spowodowanej przyłączeniem nowego atomu E
1
1
do
do
fluktuacji
fluktuacji
E
E
n
n
wg J.W. Christiana
wg J.W. Christiana
Δ
Δ
G
G
A
A
— energia stanu aktywowanego,
— energia stanu aktywowanego,
Δ
Δ
G
G
n
n
— energia fluktuacji
— energia fluktuacji
n
n
atomów,
atomów,
Δ
Δ
G
G
n+1
n+1
— energia fluktuacji
— energia fluktuacji
n +
n +
1 atomów
1 atomów
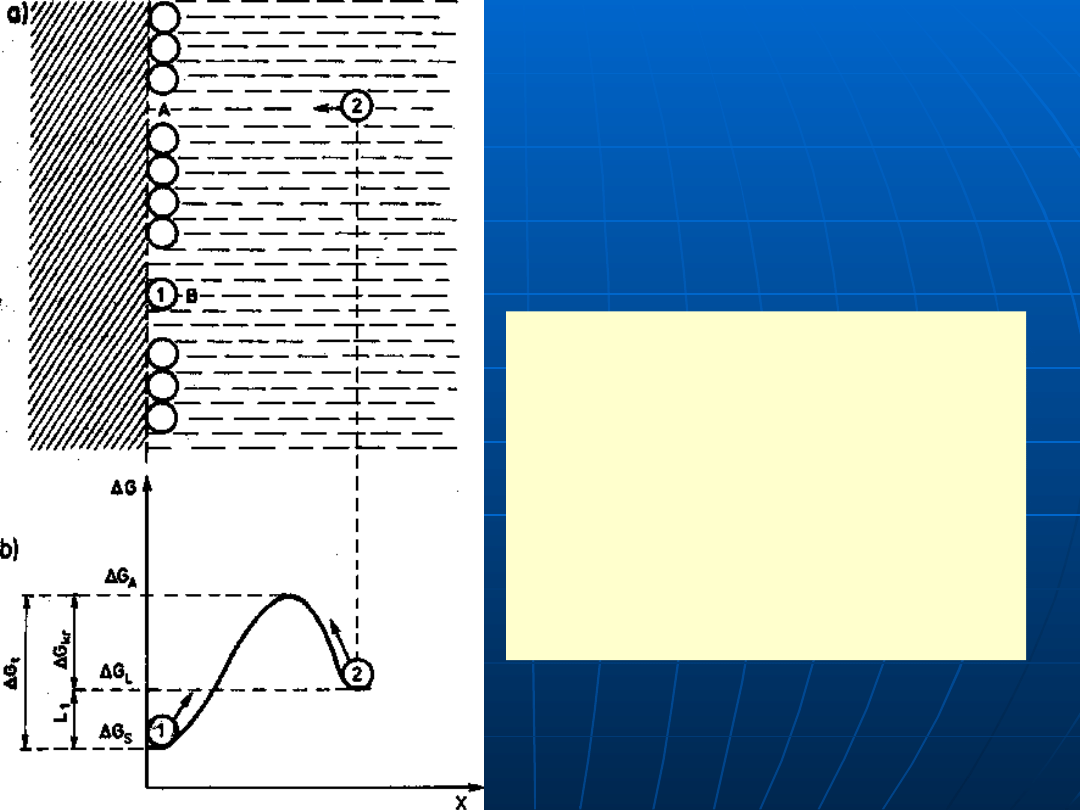
Topnienie i krystalizacja:
Topnienie i krystalizacja:
a) w układzie atomowym,
a) w układzie atomowym,
b) energetycznym;
b) energetycznym;
l
l
— atom w procesie topnienia,
— atom w procesie topnienia,
2 —
2 —
atom w procesie krystalizacji,
atom w procesie krystalizacji,
Δ
Δ
GL,
GL,
Δ
Δ
GS — energia swobodna
GS — energia swobodna
atomów w fazie ciekłej i stałej,
atomów w fazie ciekłej i stałej,
Δ
Δ
G
G
t
t
,
,
Δ
Δ
G
G
kryst
kryst
— energia aktywacji
— energia aktywacji
topnienia i krystalizacji, L
topnienia i krystalizacji, L
1
1
—
—
utajone ciepło krzepnięcia,
utajone ciepło krzepnięcia,
x
x
—
—
odległość od frontu krzepnięcia
odległość od frontu krzepnięcia
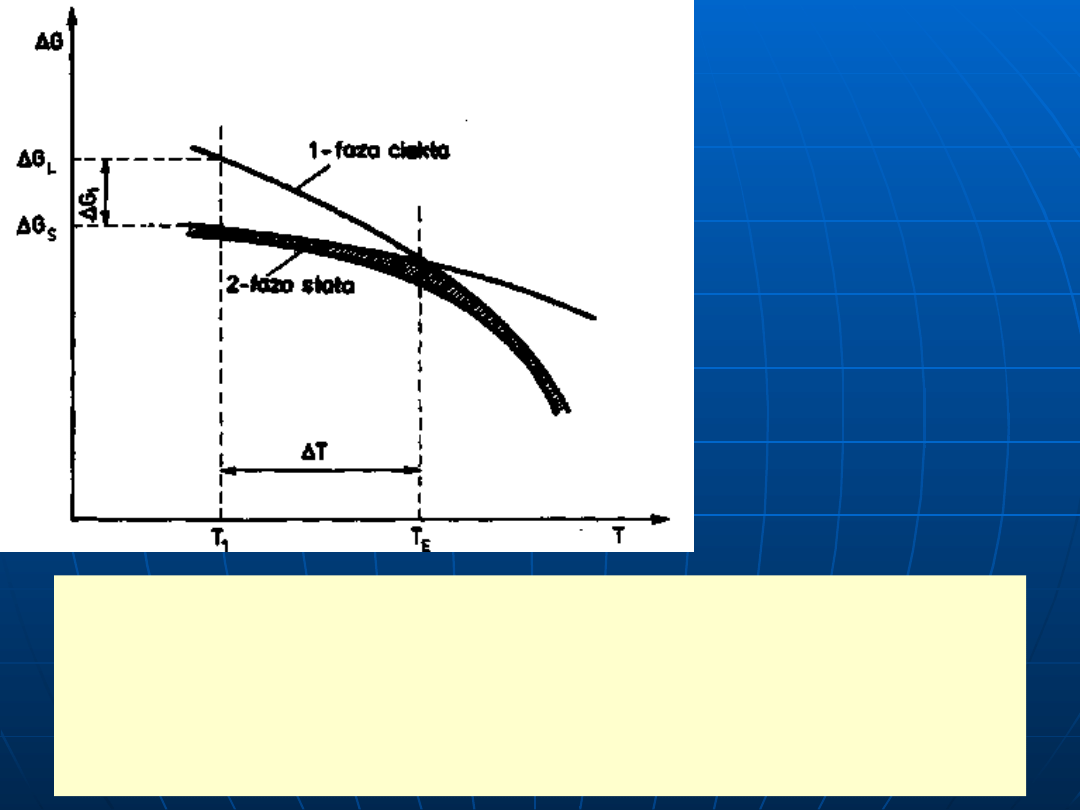
Zależność energii swobodnej fa zy stałej
Zależność energii swobodnej fa zy stałej
Δ
Δ
G
G
S
S
, i ciekłej
, i ciekłej
Δ
Δ
G
G
L
L
od
od
temperatury
temperatury
T;
T;
Δ
Δ
Gi — termodynamiczny potencjał
Gi — termodynamiczny potencjał
przemiany (krystalizacji), odpowiadający przechłodzeniu
przemiany (krystalizacji), odpowiadający przechłodzeniu
Δ
Δ
T,
T,
T
T
E
E
— temperatura równowagowa
— temperatura równowagowa
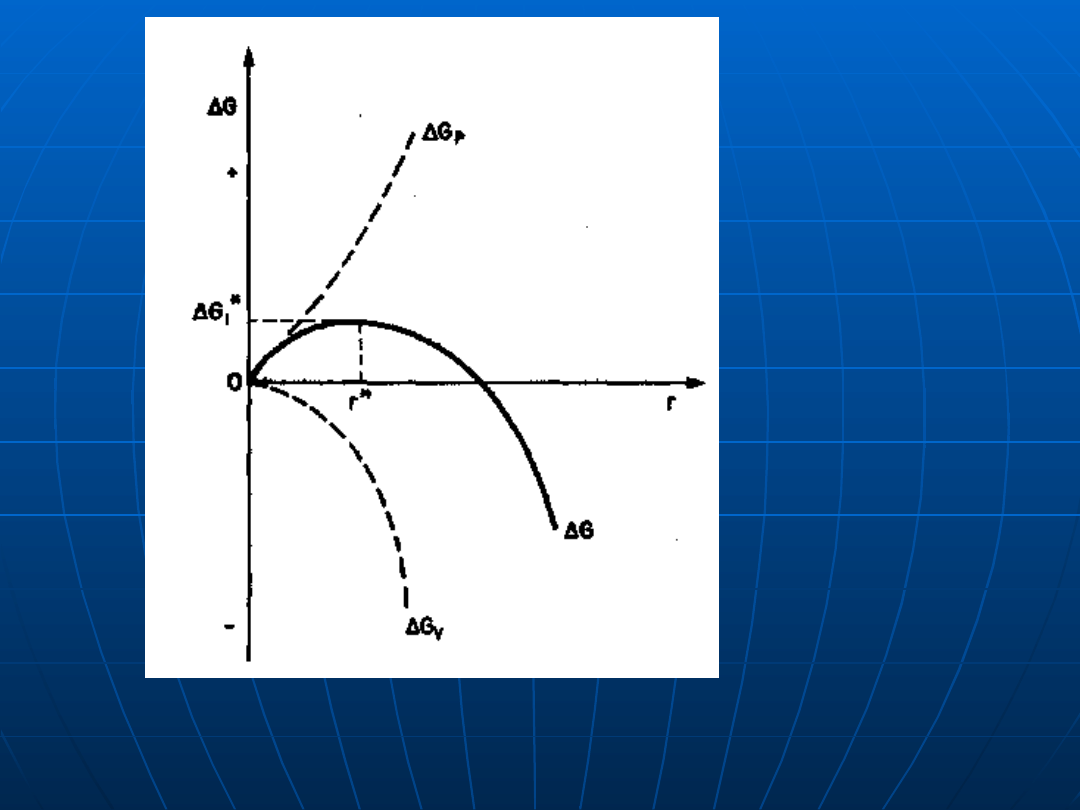
Zmiana energii swobodnej
Zmiana energii swobodnej
Δ
Δ
G, przy tworzeniu zarodka
G, przy tworzeniu zarodka
kulistego o promieniu
kulistego o promieniu
r; r*
r; r*
— promień krytyczny zarodka,
— promień krytyczny zarodka,
Δ
Δ
G
G
i
i
* — krytyczna energia swobodna zarodkowania
* — krytyczna energia swobodna zarodkowania
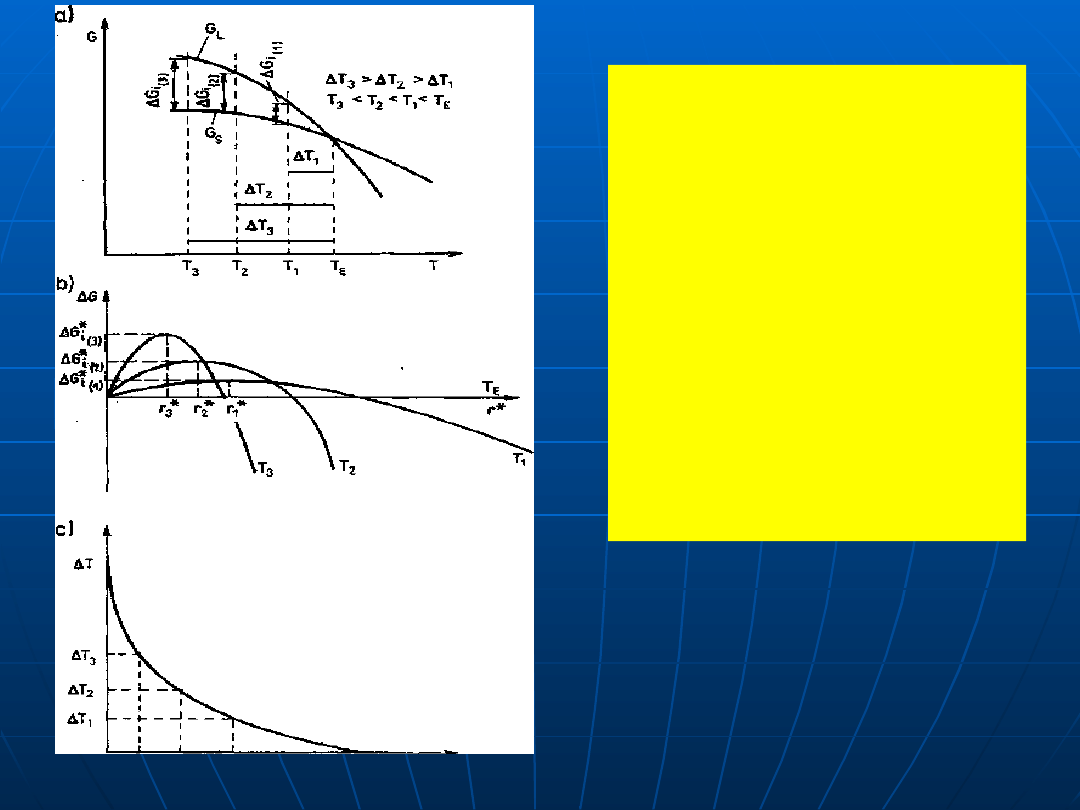
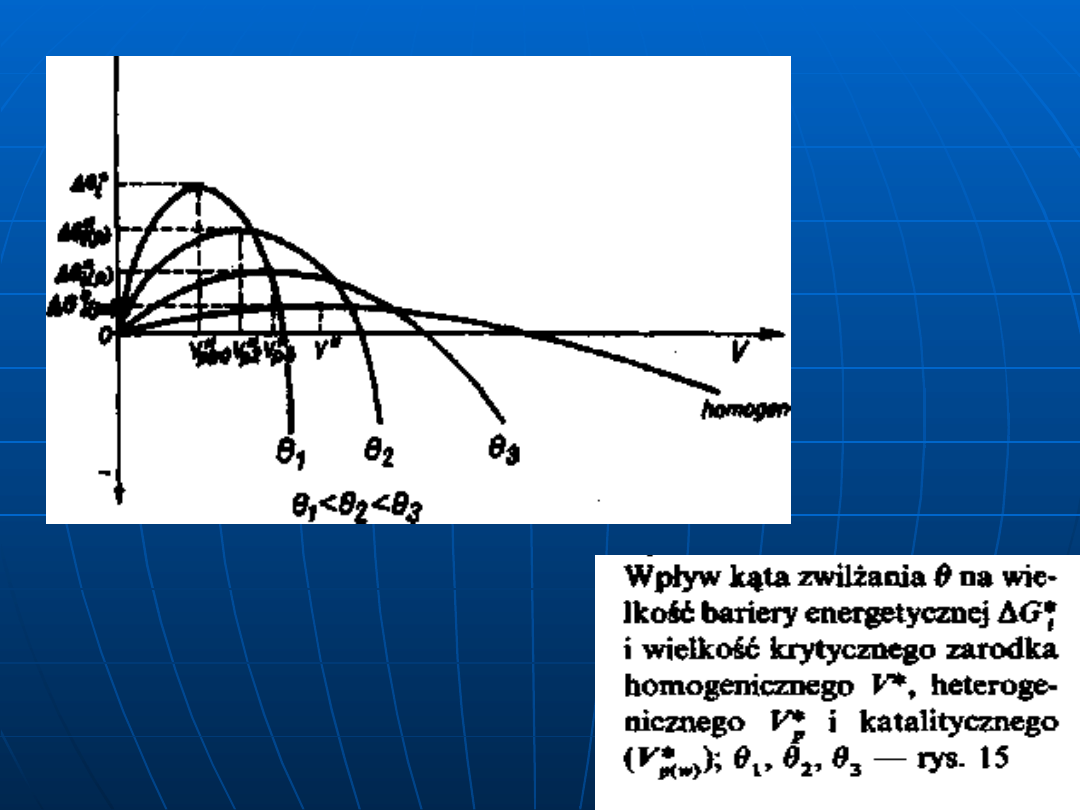
Wpływ przechłodzenia ΔT
i energii swobodnej
zarodkowania ΔG na
promień krytyczny
zarodka r*:
a) zależność
termodynamicznego
potencjału zarodkowania
ΔGi od przechłodzenia
ΔT1;
b) zależność promienia
zarodka krytycznego od
krytycznej energii
swobodnej zarodkowania
ΔGi*
i
i temperatury T;
c) zależność wielkości
zarodka krytycznego od
przechłodzenia ΔT
r*

Metal
Temperatura K
Nap. Pow.
10
-3
N/m
Metal
Temperatura K
Nap. Pow.
10
-3
N/m
Aluminium
933
860±20
Molibden
2893
2240
Antymon
900,5
395 ±20
Nikiel
1823
1924
Bizmut
544
380±10
Ołów
600
410 + 5
Chrom
1888
1420
Platyna
2273
1819
Cyna
505
525 ±10
Potas
373
573; 773
98
75; 54
Cynk
692,5
750±20
Rtęć
234,63 ;
273
373
473
573
623
500+15
470
450
430
410
400
Cyrkon
2173
1380
Gal
303
725 ±10
Iryd
2623
2310
Sód
373; 475
573
723
190; 180
171
156
Kadm
504
550±10
Kobalt
1823
1768
1936
1740
Srebro
1233,5
923
Krzem
1723
725 ±800
Srebro w fazie
stałej
1040
1235
Lit
459
430
Tytan
1998
1325
Magnez
923
520±10
Uran
1423
1020
Mangan
1533
1050
Wanad
1983
1710
Miedź -
1473
1300
Wapń
1083
255
Miedź w fazie
stałej
1100
1852
Wolfram
3653
2680
Złoto
1336
1128
Złoto w fazie
stałej
1260
1610
Żelazo
1823
1835
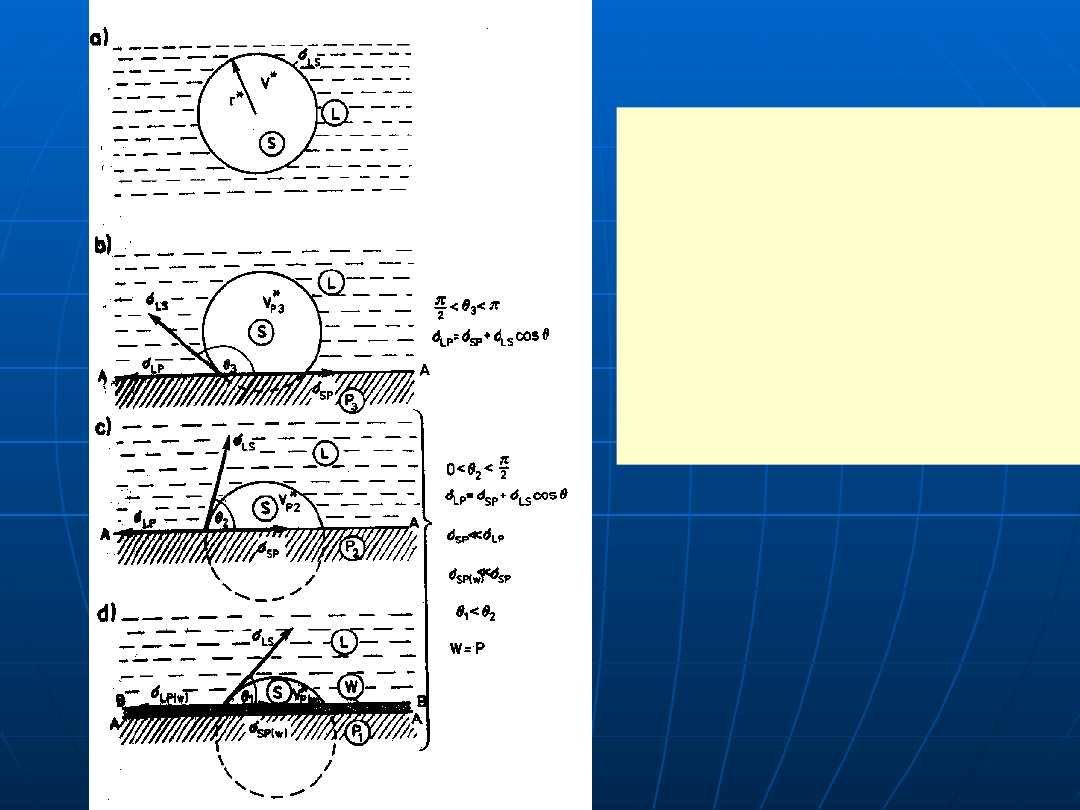
Schemat zarodka:
Schemat zarodka:
a) homogenicznego,
a) homogenicznego,
b), c), heterogenicznego,
b), c), heterogenicznego,
d) katalitycznego;
d) katalitycznego;
L — faza ciekła,
L — faza ciekła,
S
S
— faza
— faza
stała,
stała,
P
P
— podłoże,
— podłoże,
W
W
— warstwa przejściowa,
— warstwa przejściowa,
V*,r*
V*,r*
— objętość i promień
— objętość i promień
zarodka krytycznego
zarodka krytycznego
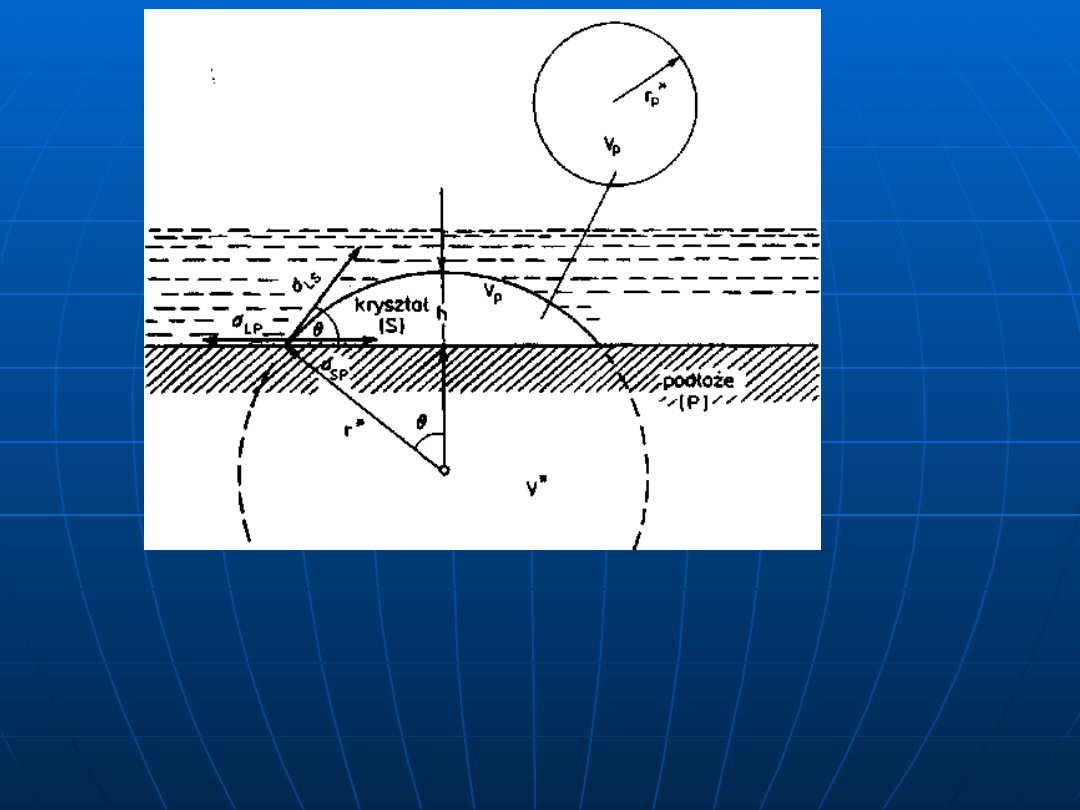
Zarodkowanie heterogeniczne (na podłożu
Zarodkowanie heterogeniczne (na podłożu
P); r*, V*
P); r*, V*
— promień i
— promień i
objętość zarodka homogenicznego, r
objętość zarodka homogenicznego, r
p
p
*,
*,
V
V
p
p
*
*
— promień i objętość
— promień i objętość
zarodka heterogenicznego (wycinka kulistego o wysokości
zarodka heterogenicznego (wycinka kulistego o wysokości
h
h
sprowadzonego do kuli)
sprowadzonego do kuli)
—_ciecz (L)
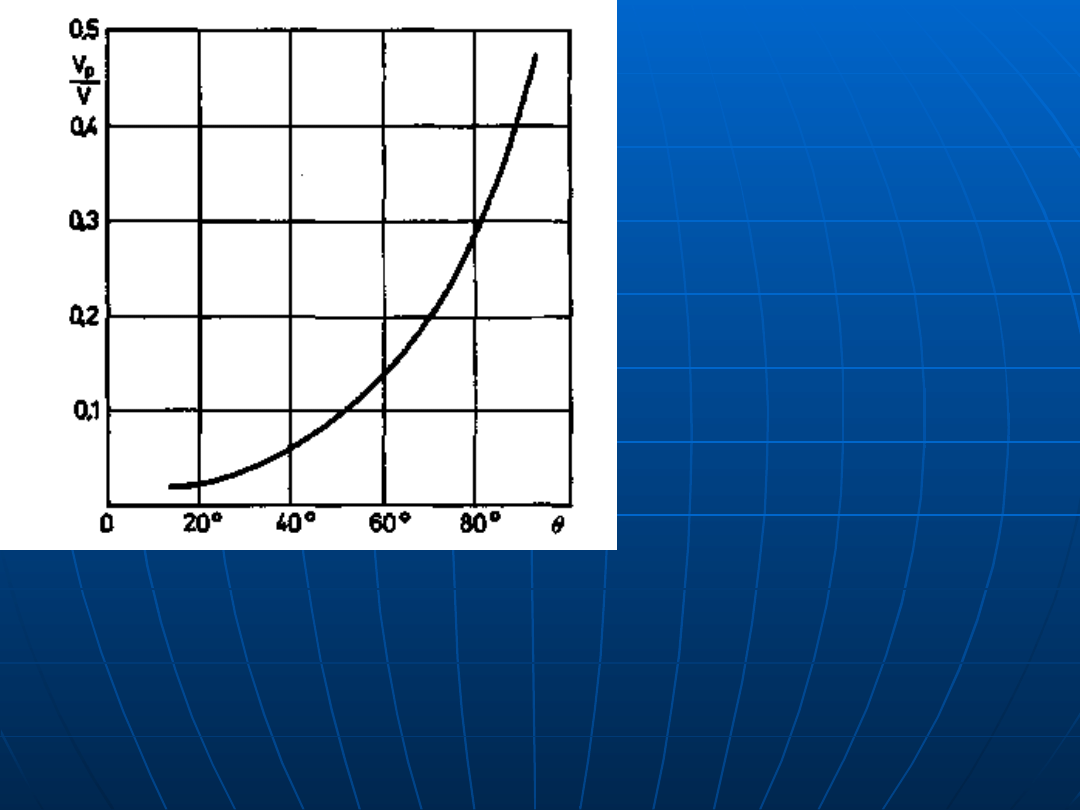
Zależność między stosunkiem objętości zarodka
Zależność między stosunkiem objętości zarodka
heterogenicznego
heterogenicznego
V*p
V*p
i homogenicznego
i homogenicznego
V
V
* a
* a
krawędziowym kątem zwilżania
krawędziowym kątem zwilżania
Θ
Θ
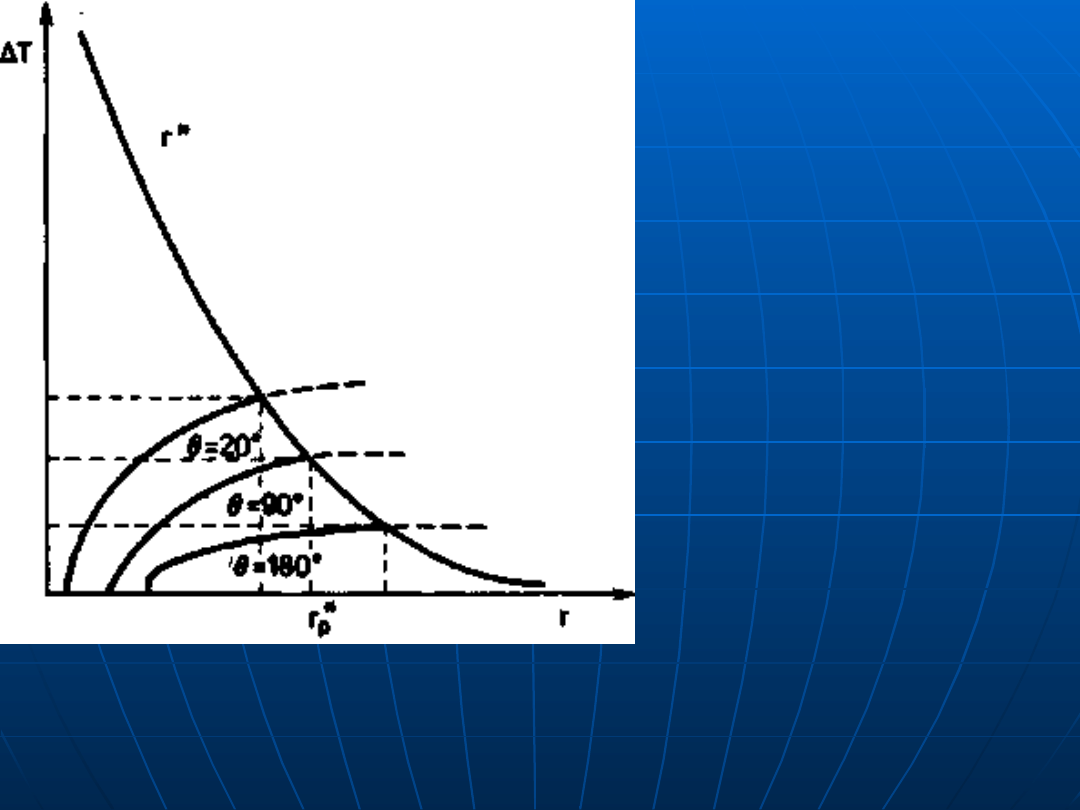
Schemat warunków zarodkowania
Schemat warunków zarodkowania
heterogenicznego w funkcji przechłodzenia
heterogenicznego w funkcji przechłodzenia
Δ
Δ
T i
T i
krawędziowego kąta zwilżania
krawędziowego kąta zwilżania

Energetyczna nadrzędność heterogenicznego zarodkowania
Energetyczna nadrzędność heterogenicznego zarodkowania
jest tak znaczna, iż nawet w czystych metalach przeważa
jest tak znaczna, iż nawet w czystych metalach przeważa
pierwszeństwo w tworzeniu zarodków heterogenicznych.
pierwszeństwo w tworzeniu zarodków heterogenicznych.
Miarą tych różnic może być wielkość przechłodzenia w
Miarą tych różnic może być wielkość przechłodzenia w
stosunku do zarodkowania homogenicznego. W badaniach
stosunku do zarodkowania homogenicznego. W badaniach
eksperymentalnych, gdzie z założenia dąży się do
eksperymentalnych, gdzie z założenia dąży się do
minimalizacji badanych objętości, chociażby dla
minimalizacji badanych objętości, chociażby dla
zmniejszenia prawdopodobieństwa oddziaływań wtrąceń
zmniejszenia prawdopodobieństwa oddziaływań wtrąceń
mogących być podkładką zarodkotwórczą, różnice w
mogących być podkładką zarodkotwórczą, różnice w
wielkości przechłodzenia mogą wynosić kilkadziesiąt stopni.
wielkości przechłodzenia mogą wynosić kilkadziesiąt stopni.
Dla przykładu podstawiając do wzoru na wielkość krytyczną
Dla przykładu podstawiając do wzoru na wielkość krytyczną
zarodka:
zarodka:
można wyznaczyć promień r* jako funkcję wielkości
można wyznaczyć promień r* jako funkcję wielkości
przechłodzenia. Przykładowa zależność dla miedzi:
przechłodzenia. Przykładowa zależność dla miedzi:
2
*
2
v
G
R
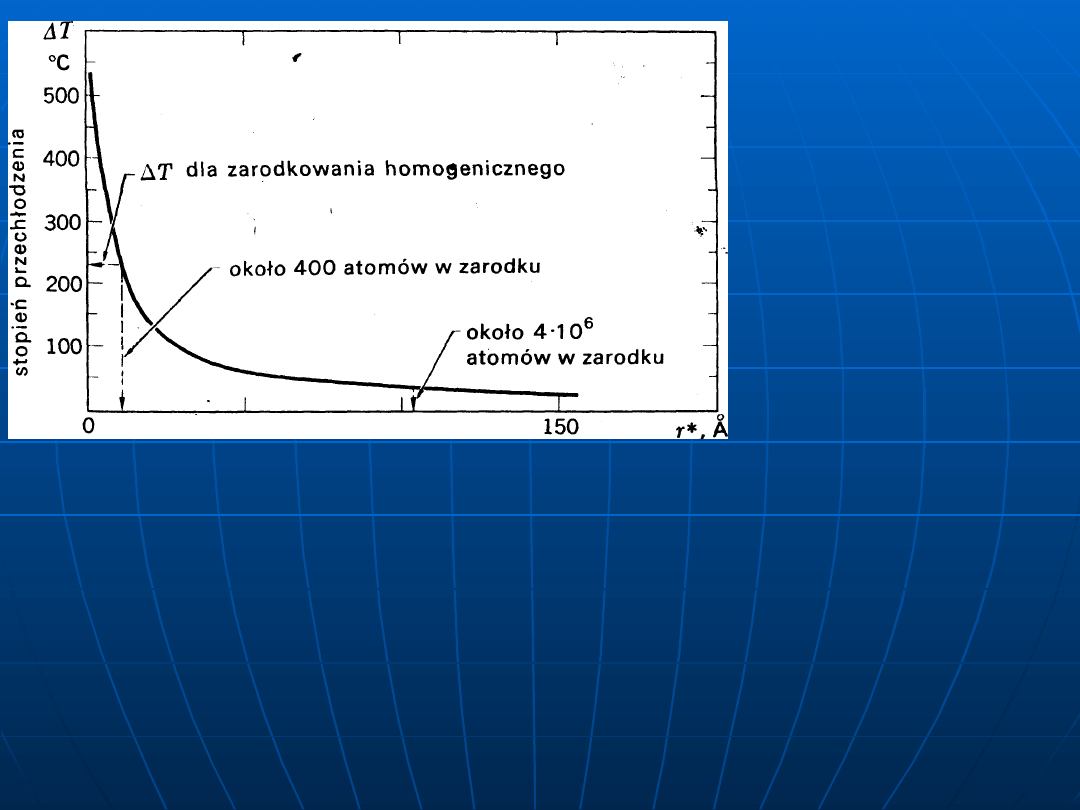
Zależność wielkości
Zależność wielkości
promienia
promienia
krytycznego
krytycznego
zarodka miedzi w
zarodka miedzi w
zależności od
zależności od
stopnia
stopnia
przechłodzenia ΔT
przechłodzenia ΔT
Podstawą analiz powinny być ze względu na procesy zarodkowania
Podstawą analiz powinny być ze względu na procesy zarodkowania
wielkości rzędu: {kilkudziesięciu ÷ kilkuset [Å]}. Wynika to z wielkości
wielkości rzędu: {kilkudziesięciu ÷ kilkuset [Å]}. Wynika to z wielkości
zarodków rzędu kilku – kilkudziesięciu [nm].
zarodków rzędu kilku – kilkudziesięciu [nm].
Na rysunku poniżej zakreskowany obszar oznacza intensywne
Na rysunku poniżej zakreskowany obszar oznacza intensywne
zarodkowanie dla kątów od 0÷25
zarodkowanie dla kątów od 0÷25
o
o
na płaszczyźnie, dla kątów 25÷45
na płaszczyźnie, dla kątów 25÷45
o
o
dla
dla
progów, krawędzi oraz 45÷90
progów, krawędzi oraz 45÷90
o
o
w szczelinach oraz 90÷120
w szczelinach oraz 90÷120
o
o
w we
w we
wgłębieniach 90÷120
wgłębieniach 90÷120
o
o
. Przy czym w większości przypadków głębokość
. Przy czym w większości przypadków głębokość
defektów powierzchniowych jest rzędu ok. 100 [Å]
defektów powierzchniowych jest rzędu ok. 100 [Å]
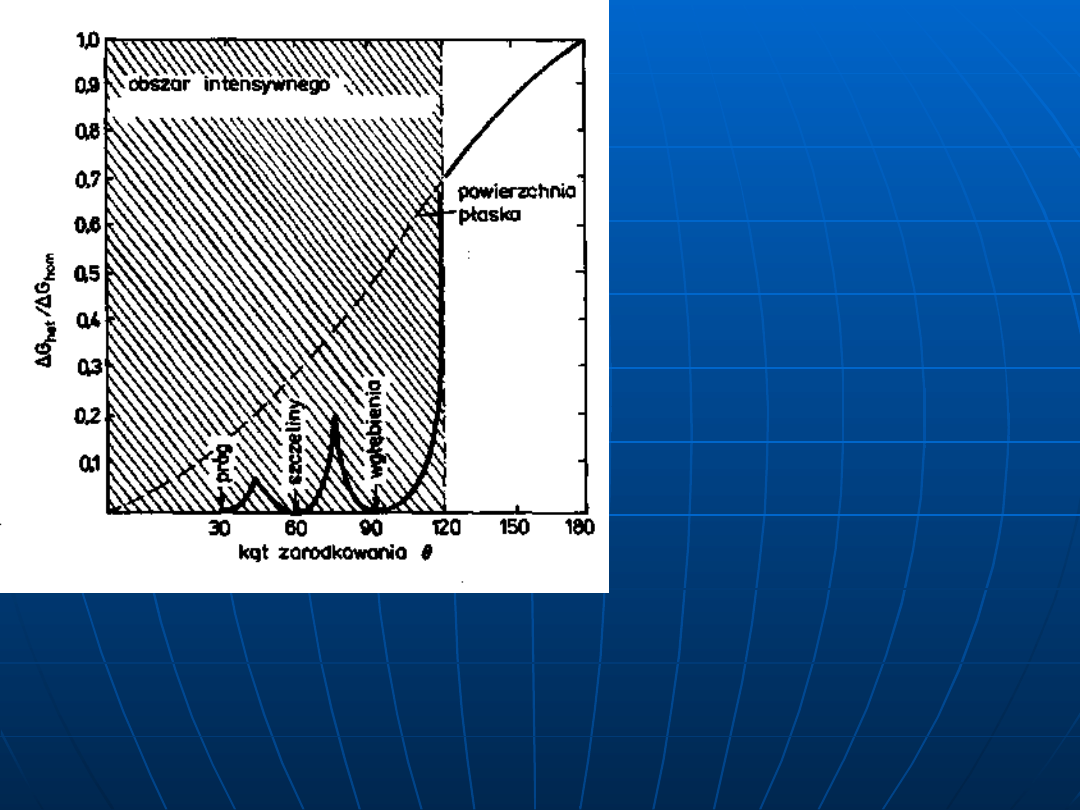
Porównanie energii stanu aktywowanego, niezbędnej do zarodkowania
Porównanie energii stanu aktywowanego, niezbędnej do zarodkowania
homogenicznego i heterogenicznego w zależności od nierówności na powierzchni
homogenicznego i heterogenicznego w zależności od nierówności na powierzchni
rozdziału fazy stałej i ciekłej
rozdziału fazy stałej i ciekłej
wg W. Missola
wg W. Missola
zarodkowania
heterogenicznego
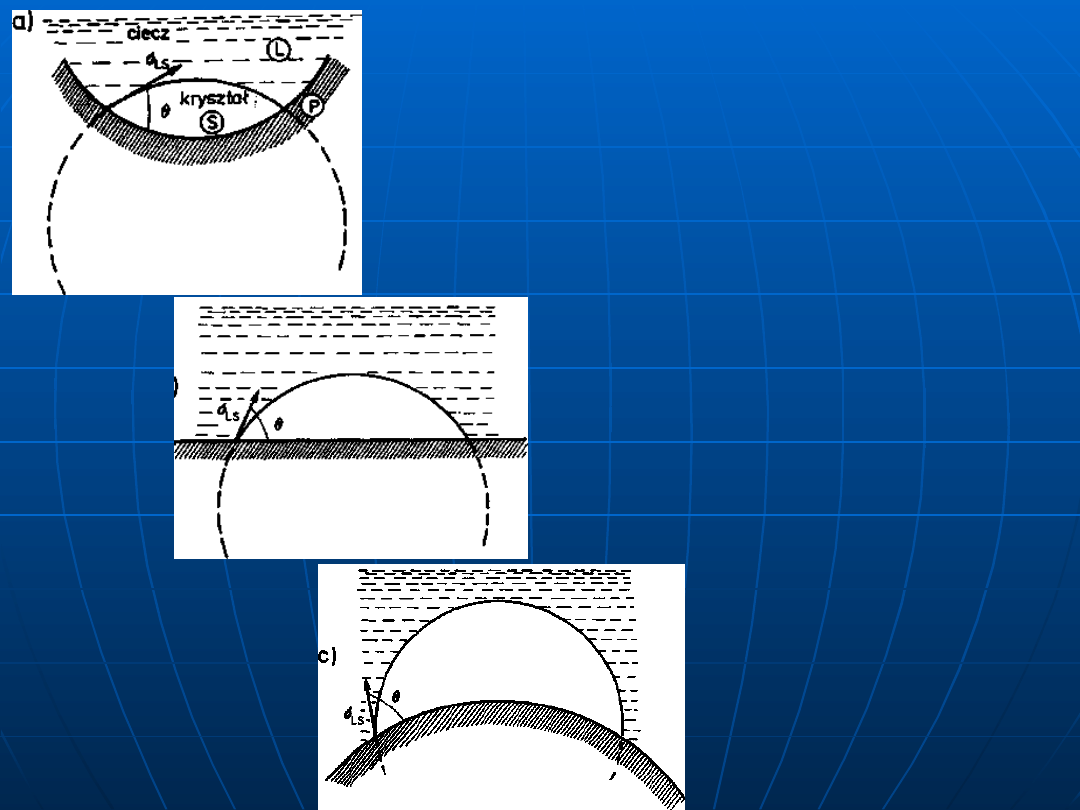
Tworzenie
Tworzenie
kryształów na
kryształów na
powierzchni
powierzchni
podłoża
podłoża
:
:
a) wklęsłej,
a) wklęsłej,
b) płaskiej
b) płaskiej
c) wypukłej
c) wypukłej
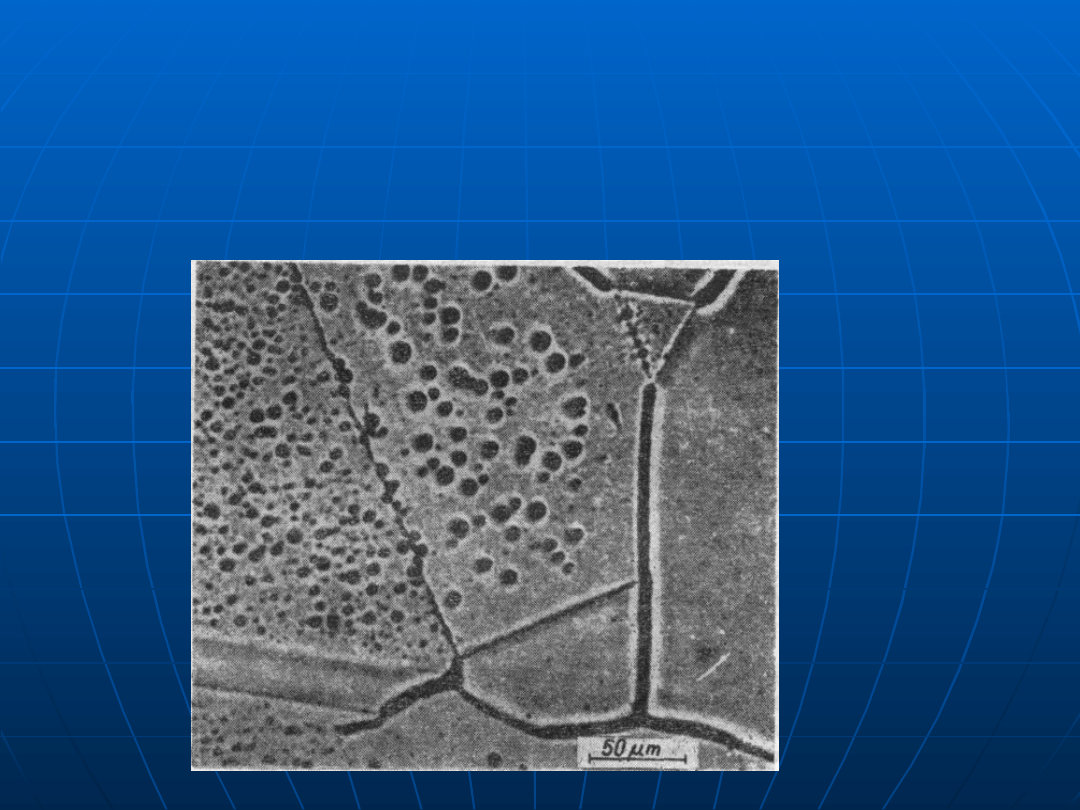
Przykładowe tworzenie jamek trawienia
Przykładowe tworzenie jamek trawienia
cieplnego na płaszczyznach (111) i (100)
cieplnego na płaszczyznach (111) i (100)
polikrystalicznego srebra (40 h, 700°C,
polikrystalicznego srebra (40 h, 700°C,
PH
PH
2
2
O/PH
O/PH
2
2
= 0,08)
= 0,08)

Kształt powierzchni międzyfazowej ciecz metaliczna – kryształ
Kształt powierzchni międzyfazowej ciecz metaliczna – kryształ
zależy m. in. od gradientu temperatury w pobliżu frontu
zależy m. in. od gradientu temperatury w pobliżu frontu
krystalizacji. Tiller dokonał szacunkowej oceny wpływu dyfuzji
krystalizacji. Tiller dokonał szacunkowej oceny wpływu dyfuzji
składnika oraz transportu ciepła [81]. Odległość, na którą
składnika oraz transportu ciepła [81]. Odległość, na którą
następuje dyfuzja w jednostce czasu przy jednostkowym
następuje dyfuzja w jednostce czasu przy jednostkowym
gradiencie stężenia jest około sto razy mniejsza niż droga
gradiencie stężenia jest około sto razy mniejsza niż droga
przemieszczenia frontu krystalizacji. Natomiast odległość, na którą
przemieszczenia frontu krystalizacji. Natomiast odległość, na którą
przenoszone jest ciepło w jednostce czasu przy jednostkowym
przenoszone jest ciepło w jednostce czasu przy jednostkowym
gradiencie temperatury jest ok. sto razy większa niż wielkość
gradiencie temperatury jest ok. sto razy większa niż wielkość
przemieszczenia frontu krystalizacji. Powierzchnia międzyfazowa,
przemieszczenia frontu krystalizacji. Powierzchnia międzyfazowa,
która szybciej reaguje na zmianę warunków termodynamicznych
która szybciej reaguje na zmianę warunków termodynamicznych
dominuje w kształtowaniu struktury
dominuje w kształtowaniu struktury
Rozwinięta powierzchnia międzyfazowa może być definiowana za
Rozwinięta powierzchnia międzyfazowa może być definiowana za
pomocą promienia krzywizny. Może być rozpatrywana w
pomocą promienia krzywizny. Może być rozpatrywana w
kategoriach przyrostu temperatury lub ciśnienia lub też zmiany
kategoriach przyrostu temperatury lub ciśnienia lub też zmiany
stężenia – głównych czynników krystalizacyjnych. Jeśli w
stężenia – głównych czynników krystalizacyjnych. Jeśli w
analizowanej przestrzeni napięcie powierzchniowe σ jest
analizowanej przestrzeni napięcie powierzchniowe σ jest
izotropowe wówczas przyrost energii swobodnej spowodowanej
izotropowe wówczas przyrost energii swobodnej spowodowanej
obecnością powierzchni zakrzywionej o promieniu r wynosi:
obecnością powierzchni zakrzywionej o promieniu r wynosi:
H
G
2
gdzie:
H
to uśredniona krzywizna
ΔGρ – zmiana energii swobodnej wywołana krzywizną
ΔGρ – zmiana energii swobodnej wywołana krzywizną
ρ1 ρ2, - zorientowane promienie główne prostopadłych krzywizn
ρ1 ρ2, - zorientowane promienie główne prostopadłych krzywizn
powierzchni kryształu.
powierzchni kryształu.
Klasyczna postać równania Gibbsa-Thomsona pokazuje zależność
Klasyczna postać równania Gibbsa-Thomsona pokazuje zależność
równowagowej temperatury krystalizacji powierzchni płaskiej Te i
równowagowej temperatury krystalizacji powierzchni płaskiej Te i
zakrzywionej Tρ frontu krystalizacji. Zależność odnosi się zasadniczo
zakrzywionej Tρ frontu krystalizacji. Zależność odnosi się zasadniczo
do czystych metali. Zakłada się równość równowagowych
do czystych metali. Zakłada się równość równowagowych
współczynników rozdziału składnika między cieczą i kryształem
współczynników rozdziału składnika między cieczą i kryształem
zakrzywionym i płaskim. Jeśli przyjąć, że promienie
zakrzywionym i płaskim. Jeśli przyjąć, że promienie
r
r
prostopadłe
prostopadłe
krzywizn są równe, co odpowiada powierzchni sferycznej wówczas
krzywizn są równe, co odpowiada powierzchni sferycznej wówczas
przyrost temperatury zależąc od promienia krzywizny r jest dwa razy
przyrost temperatury zależąc od promienia krzywizny r jest dwa razy
wyższy niż w przypadku powierzchni jednokrotnie zakrzywionej – np.
wyższy niż w przypadku powierzchni jednokrotnie zakrzywionej – np.
walcowej. Przykład wpływu obu przypadków wskazuje na skalę
walcowej. Przykład wpływu obu przypadków wskazuje na skalę
oddziaływań. Wzrost rozwinięcia powierzchni heterogenicznego
oddziaływań. Wzrost rozwinięcia powierzchni heterogenicznego
zarodkowania a tym samym wzrost powierzchni frontu wzrostu
zarodkowania a tym samym wzrost powierzchni frontu wzrostu
kryształów oraz minimalizacja promienia krzywizn celowo
kryształów oraz minimalizacja promienia krzywizn celowo
kształtowanych powierzchniowo komponentów zbrojących, prowadzi
kształtowanych powierzchniowo komponentów zbrojących, prowadzi
do zmniejszania równowagowej temperatury krystalizacji.
do zmniejszania równowagowej temperatury krystalizacji.
F
F
dF
dF
H
2
1
1
1
2
1
H
L
T
T
e
2
Promień krzywizny powierzchni międzyfazowej
Promień krzywizny powierzchni międzyfazowej
ciecz-ciało stałe można wyznaczyć korzystając z
ciecz-ciało stałe można wyznaczyć korzystając z
warunku
warunku
x
dx
dT
T
T
e
x
T
T
T
e
x
gdzie: T
x
– temperatura powierzchni rozdziału ciecz- ciało stałe,
dx
dT
- gradient temperatury, Δx – przemieszczenie względem izotermy T
e
;
T
e
równowagowa temperatura krystalizacji czystego metalu
Po podstawieniu:
e
x
T
T
H
L
T
e
2
e
x
T
T
F
F
e
F
F
e
dF
dF
L
T
dF
dF
L
T
2
1
2
1
1
1
1
1
1
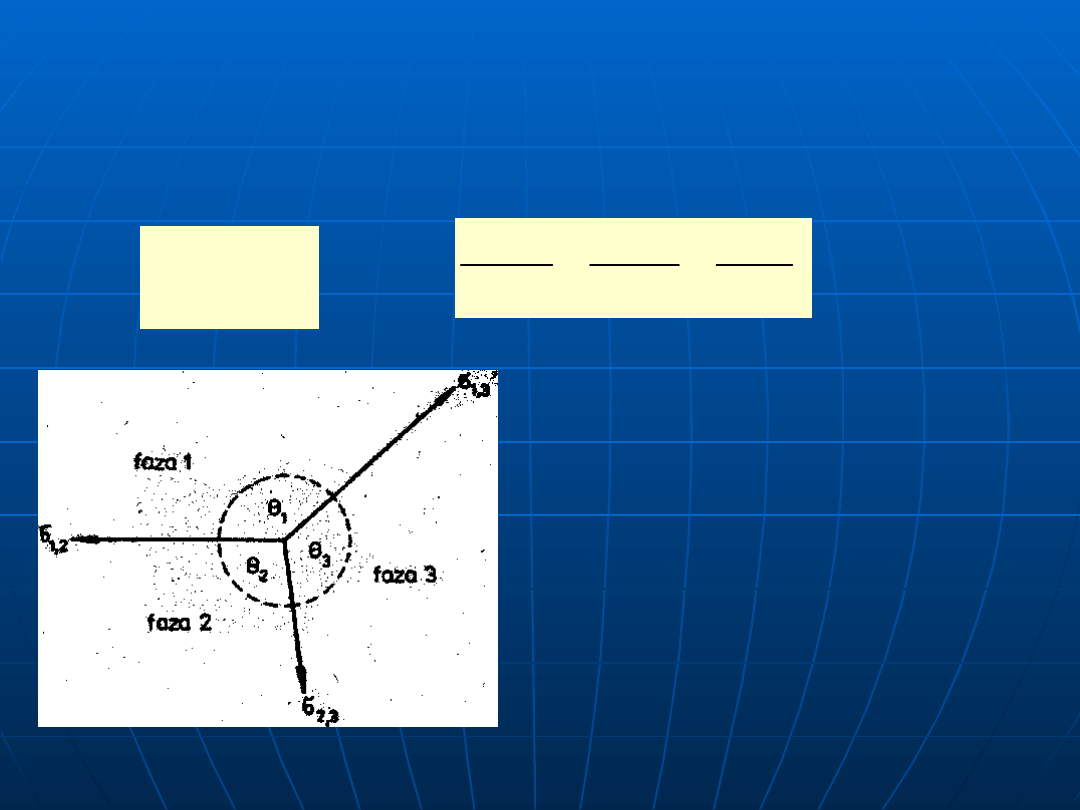
Rozpatrując prosty przypadek równowagi sił
Rozpatrując prosty przypadek równowagi sił
powierzchniowych dwufazowej osnowy i
powierzchniowych dwufazowej osnowy i
cząstki zbrojącej spełniony musi być
cząstki zbrojącej spełniony musi być
warunek Neumana, równości napięć
warunek Neumana, równości napięć
powierzchniowych:
powierzchniowych:
0
1
i
2
31
1
23
3
12
sin
sin
sin
Równowaga granic rozdziału w
Równowaga granic rozdziału w
układzie trójfazowym
układzie trójfazowym
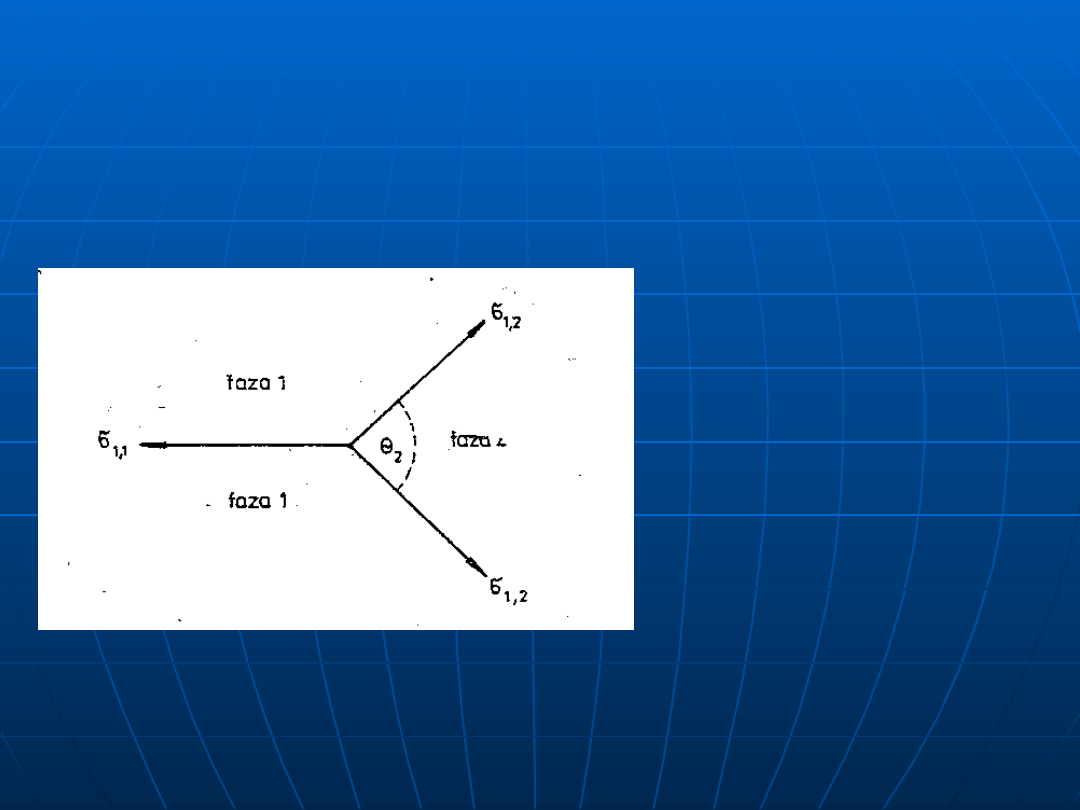
Granice między ziarnami tej samej fazy mają
Granice między ziarnami tej samej fazy mają
jednakowe energie powierzchniowe, natomiast
jednakowe energie powierzchniowe, natomiast
granice między ziarnami różnych faz mają inne
granice między ziarnami różnych faz mają inne
wartości energii powierzchniowych i inne napięcia
wartości energii powierzchniowych i inne napięcia
powierzchniowe
powierzchniowe
Równowagowy dwuścienny kąt zwilżania Θ2 na
styku dwóch ziarn jednej fazy z drugą fazą

Uzyskanie płaskich ścian jest możliwe
Uzyskanie płaskich ścian jest możliwe
tylko wówczas, gdy układ ma
tylko wówczas, gdy układ ma
zrównoważone nadmiary
zrównoważone nadmiary
powierzchniowe energii, czyli jest
powierzchniowe energii, czyli jest
stabilny. Kąty tetraedryczne dążą do
stabilny. Kąty tetraedryczne dążą do
wartości 109,5
wartości 109,5
o
o
. Warunki związane z
. Warunki związane z
wypełnieniem przestrzeni i
wypełnieniem przestrzeni i
równowagi napięć powierzchniowych
równowagi napięć powierzchniowych
spełniają ziarna w postaci
spełniają ziarna w postaci
czternastościanów
czternastościanów
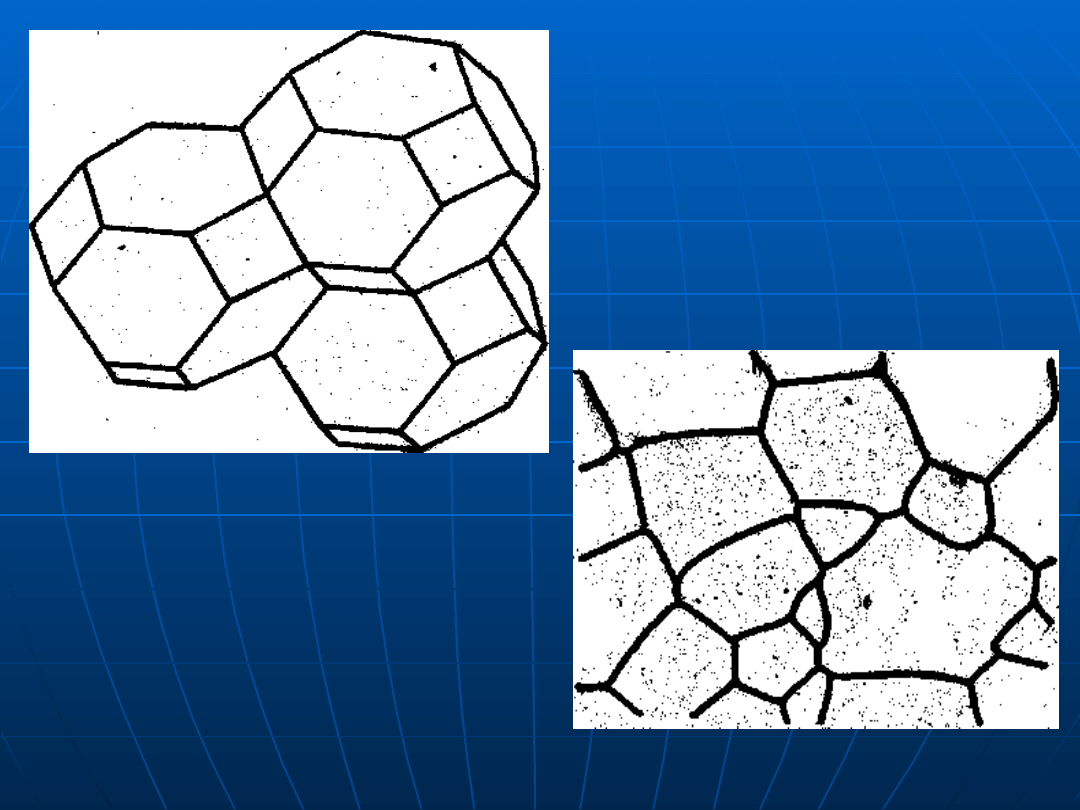
Ułożenie i kształt ziarn
wypełniających przestrzeń w pełni
przy zachowaniu płaskich ścian:
model czternastościany
oraz
powierzchnia odpowiadającego
modelowi zgładu

Przy krystalizacji pojedynczych kryształów
Przy krystalizacji pojedynczych kryształów
równowagowy kształt odpowiada minimalnej
równowagowy kształt odpowiada minimalnej
energii powierzchniowej przy stałej objętości.
energii powierzchniowej przy stałej objętości.
Wynika to z prawa Gibbsa:
Wynika to z prawa Gibbsa:
Kształt kulisty jest uprzywilejowany z
Kształt kulisty jest uprzywilejowany z
założenia w warunkach izotropowego pola
założenia w warunkach izotropowego pola
napięcia powierzchniowego. Przy anizotropii
napięcia powierzchniowego. Przy anizotropii
napięcia powierzchniowego spowodowanego
napięcia powierzchniowego spowodowanego
odmiennością energii powierzchniowych w
odmiennością energii powierzchniowych w
zależności od orientacji krystalograficznej na
zależności od orientacji krystalograficznej na
powierzchnia kryształu wystąpią granice o
powierzchnia kryształu wystąpią granice o
niesferycznych kształtach. Kształt ziarna wg
niesferycznych kształtach. Kształt ziarna wg
Wulfa pokazany na rysunku powiązany z
Wulfa pokazany na rysunku powiązany z
energiami i napięciami powierzchniowymi:
energiami i napięciami powierzchniowymi:
i
i
i
F min
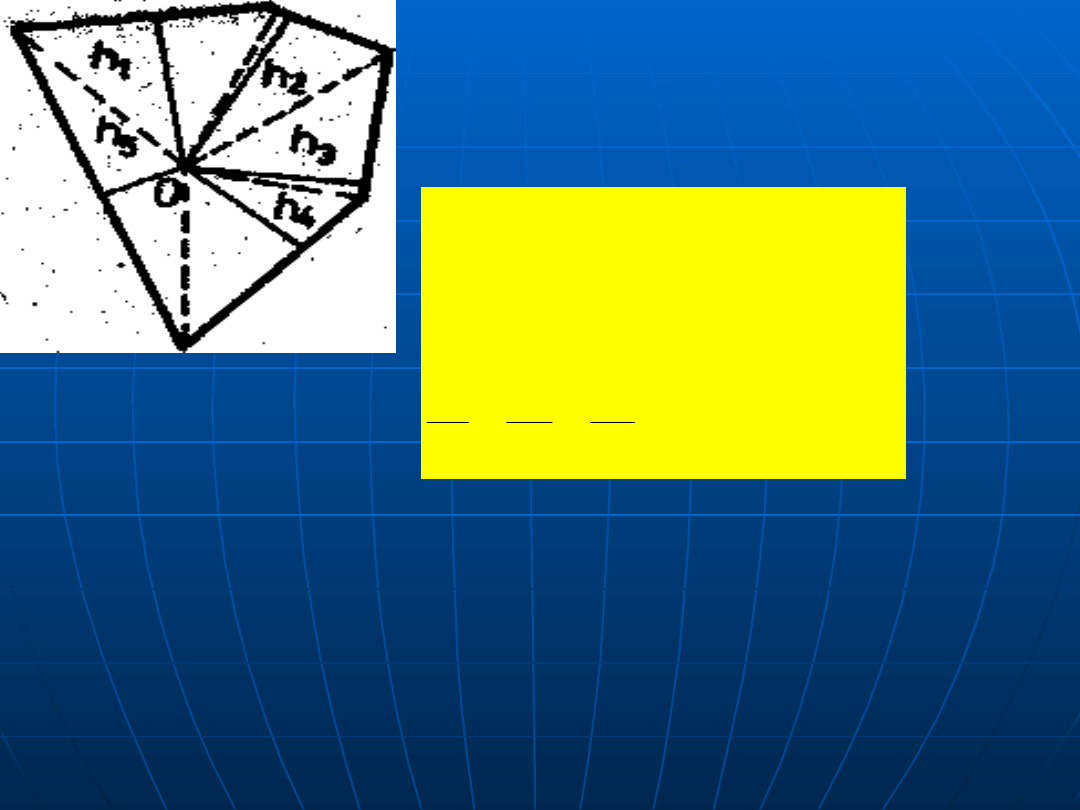
Kryształ Wulfa
Kryształ Wulfa
const
h
h
h
h
h
h
b
E
h
h
h
d
V
h
h
h
b
F
....
...)
(
...)
(
...)
(
3
3
2
2
1
1
2
3
3
2
2
2
2
1
1
3
3
3
2
3
1
2
3
2
2
2
1
gdzie: F, V, odpowiednio powierzchnia całkowita , objętość
kryształu, b, d – stałe zależne od kształtu, σi napięcie
powierzchniowe na ścianie przy wysokości hi zgodnie z
rysunkiem
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
Wyszukiwarka
Podobne podstrony:
opracowanie zerowego z MiO, Politechnika Poznańska (PP), Metalurgia i Odlewnictwo, Wykłady
Odlewnictwo wykład 1
Odlewnictwo wykład 3
Pytania kontrolne dla IMM Mechatron, Politechnika Poznańska, Mechatronika, Semestr 01, Metalurgia i
Opracowanie3, POLITECHNIKA ŚLĄSKA Wydział Mechaniczny-Technologiczny - MiBM POLSL, Inżynierskie, Sem
Odlewnictwo wykład I i II
MATERIAŁY PRODUKCYJNE ODLEWNICTWO WYKŁAD
mio-test, Politechnika Poznańska (PP), Metalurgia i Odlewnictwo, Wykłady
Pytania kontrolne, Politechnika Poznańska, Mechatronika, Semestr 01, Metalurgia i odlewnictwo - wykł
Odlewnictwo wykłady, Studia, pomoc studialna, odlewnictwo i spawalnictwo, spawalnictwo odlewnictwo,
Odlewnictwo wykład 2
Odlewnictwo wykład 4
Wykład MO 21.11.10, Mechatronika, Metalurgia i Odlewnictwo, Wykłady
Odlewnictwo wykład
więcej podobnych podstron