
ZWIĄZKI KARBONYLOWE
POCHODNE
KWASÓW
KARBOKSYLOWYCH
-
ESTRY,
HALOGENKI KWASOWE, AMIDY
Znanych jest wiele pochodnych kwasów
karboksylowych, omówione będą trzy
wymienione w tytule. Do grupy acylowej
przyłączony jest elektroujemny atom
albo podstawnik
R C
O
OH
R C
O
X
R C
O
NH
2
R C
O
OR
kwas karboksylowy
halogenek kwasowy X=Cl, Br, F, I
amid
ester
R C
O
grupa acylowa
ZWIĄZKI KARBONYLOWE
POCHODNE
KWASÓW
KARBOKSYLOWYCH
-
ESTRY,
HALOGENKI KWASOWE, AMIDY
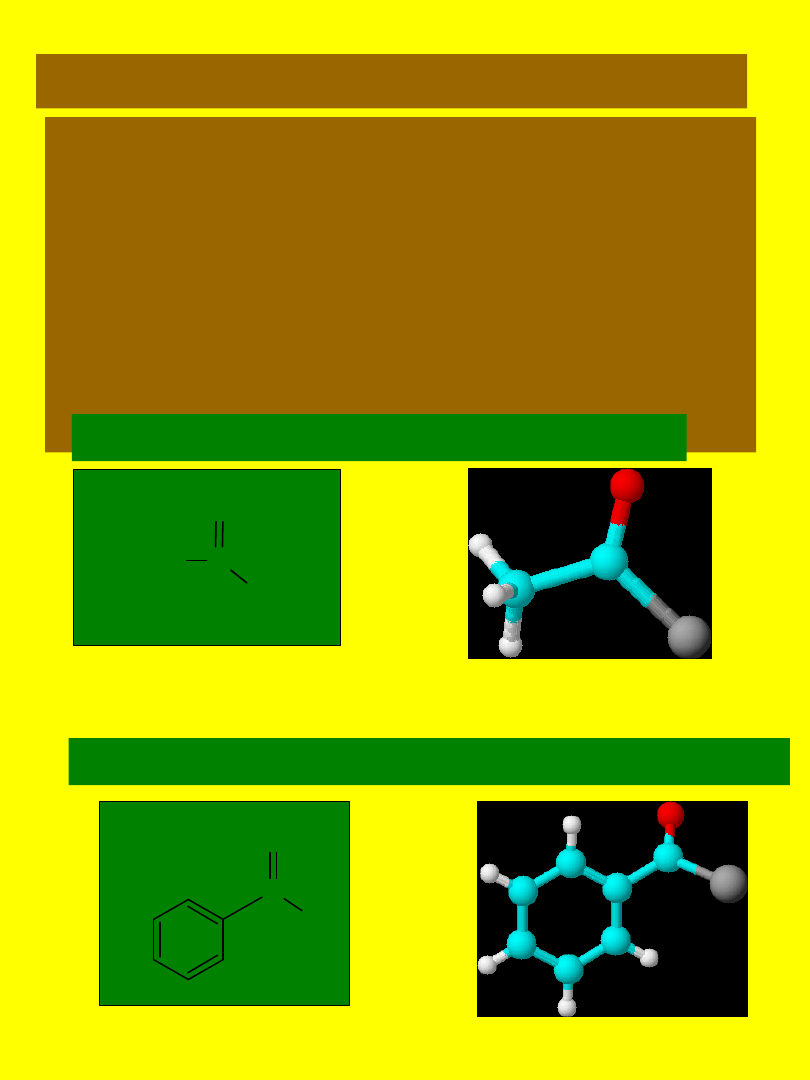
NAZEWNICTWO HALOGENKÓW
KWASOWYCH
Nazewnictwo rozpoczyna się od nazwy
halogenku, a następnie dodaje się nazwę
grupy acylowej.
C
H
3
C
O
Cl
bromek benzoilu - z kwasu benzoesowego
C
O
Br
chlorek acetylu - z kwasu octowego
ZWIĄZKI KARBONYLOWE
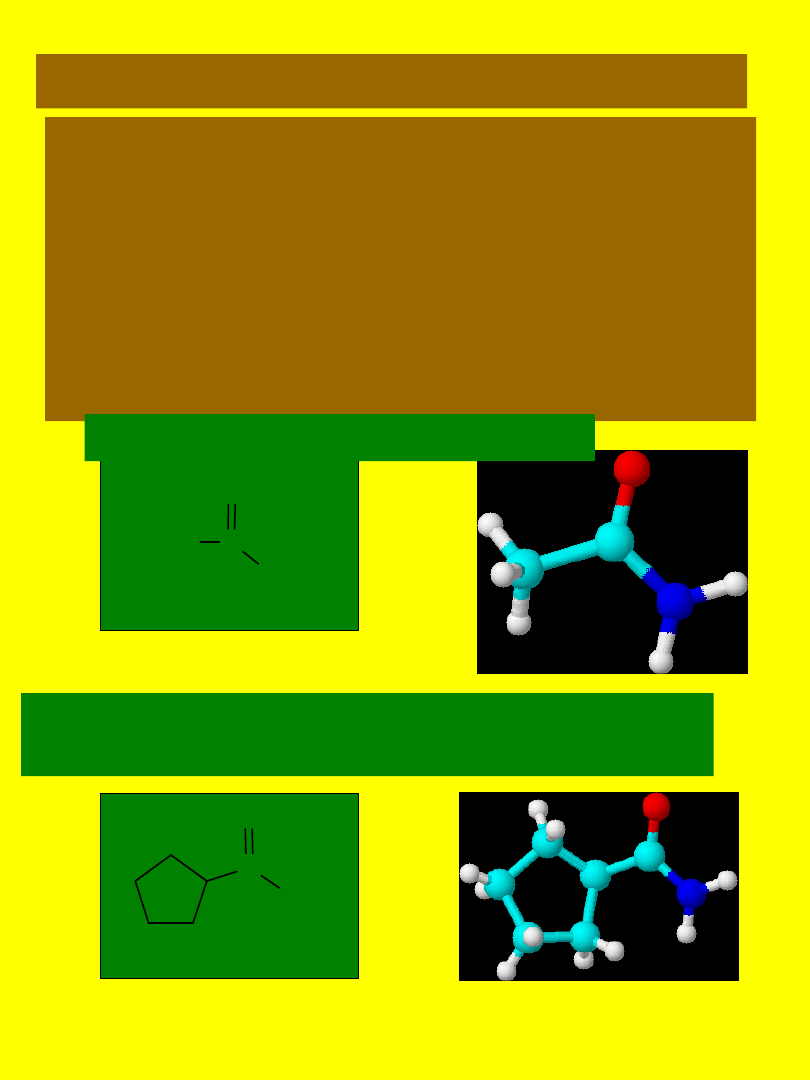
NAZWY AMIDÓW
Nazwy
amidów,
zawierające
nie
podstawioną grupę NH
2
tworzy się z
nazw systematycznych lub zwyczajowych
odpowiednich kwasów, zmieniając kwas
karboksylowy na karboksyamid lub
zmieniając końcówkę -oil (-yl) w nazwie
grupy acylowej na przyrostek amid.
C
H
3
C
O
NH
2
acetamid - z kwasu octowego
C
O
NH
2
Cyklopentanokarboksyamid
- z kwasu cyklopentanokarboksylowego
ZWIĄZKI KARBONYLOWE
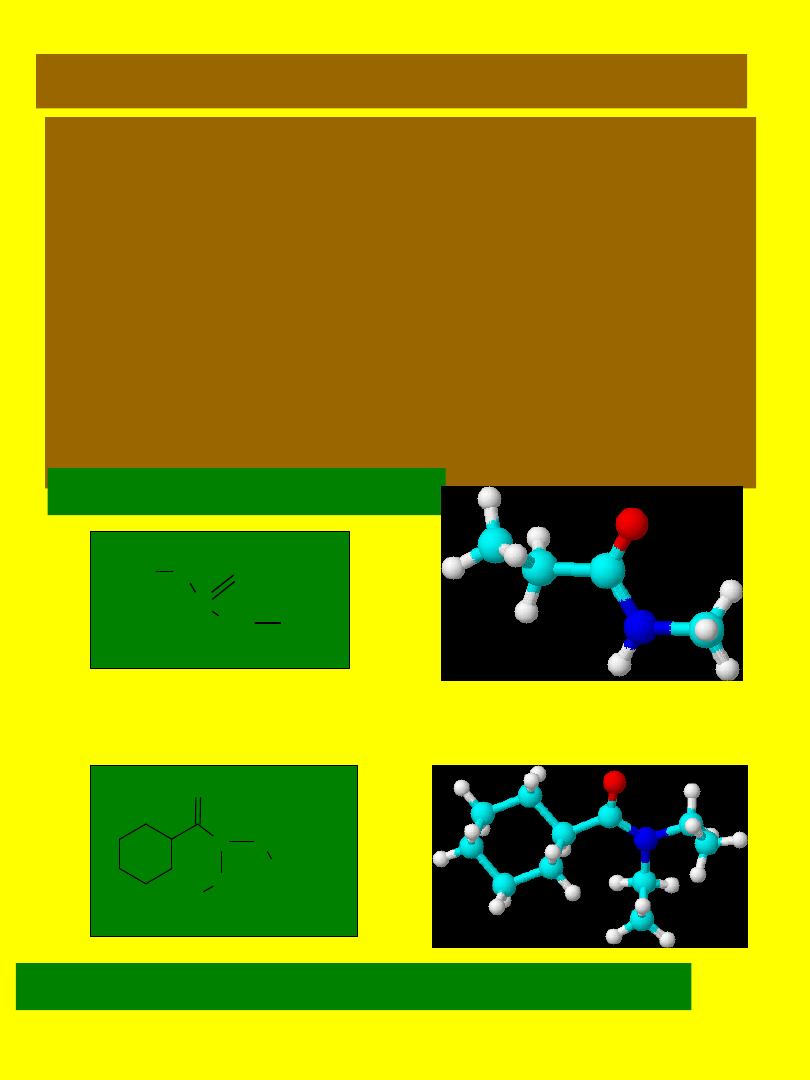
NAZWY AMIDÓW
Jeżeli atom azotu w amidzie jest
podstawiony innymi grupami, to w
nazwie najpierw określa się, jakie to
podstawniki, a dopiero potem podaje
nazwę macierzystego amidu. Nazwę
podstawników
przy
atomie
azotu
poprzedza się literą N, co oznacza
jednoznacznie
bezpośrednie
podstawienie przy atomie azotu.
N-metylopropanoamid
C
H
3
CH
2
C
O
NH
CH
3
O
N
CH
2
CH
3
CH
2
C
H
3
N,N-dietylocykloheksanokarboksyamid
ZWIĄZKI KARBONYLOWE
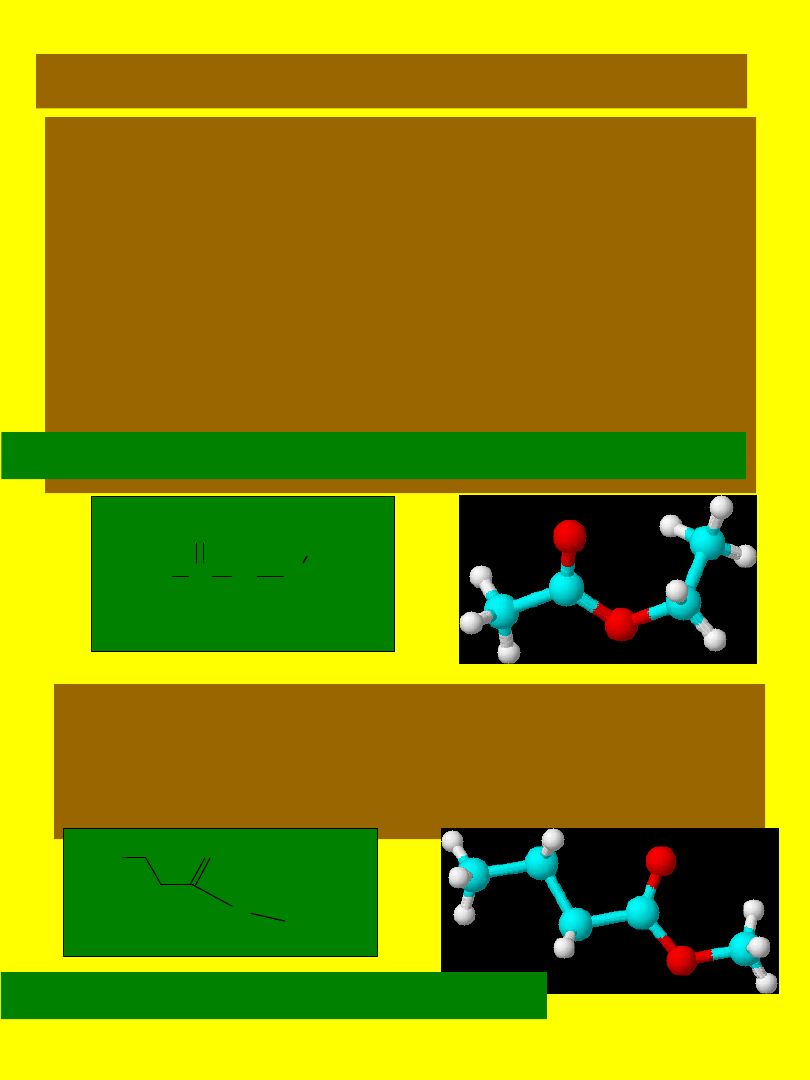
ESTRY
Wzór ogólny estrów RCO
2
R’
Nazwy estrów tworzy się określając, z
jakiego kwasu karboksylowego one
powstały oraz jakie grupy alkilowe
zostały wprowadzone do cząsteczki w
miejsce atomu wodoru w kwasie. Nazwa
estru ma końcówkę -an dodaną w
miejsce
końcówki
-owy
w
przymiotnikowej części nazwy kwasu.
octan etylu ester etylowy kwasu octowego
C
H
3
C
O
O CH
2
CH
3
Wiele prostych estrów to ciecze o bardzo
przyjemnym
zapachu,
które
są
odpowiedzialne za zapach wielu owoców
i kwiatów.
C
H
3
O
CH
3
O
butanian metylu - w ananasach
ZWIĄZKI KARBONYLOWE
C
H
3
O
O
CH
3
CH
3
octan izopentylu - w bananach
Połączenia estrowe występują także w
tłuszczach zwierzęcych oraz w wielu
cząsteczkach
o
ważnym
znaczeniu
biologicznym
C
H
2
O
C
O
R
C
H
O
O
R
C
H
2
O
O
R
tłuszcz
R = łańcuchy C
11-17
Estry można hydrolizować w wodnym
roztworze zasady. Produktem jest kwas
karboksylowy oraz alkohol. Reakcja ta
zwana jest reakcją zmydlania.
R C
O
O
R
NaOH, H
2
O
R C
O
OH
+
ROH

ZWIĄZKI KARBONYLOWE
ALDEHYDY I KETONY
Aldehydy i ketony należą do najczęściej
spotykanych
typów
związków
organicznych, zarówno w przyrodzie, jak
i w przemyśle chemicznym. Wiele
substancji
potrzebnych
żywym
organizmom zawiera grupę funkcyjną
aldehydową lub ketonową. W przemyśle
chemicznym proste aldehydy i ketony są
produkowane w dużych ilościach do
późniejszego
wykorzystania
zarówno
jako rozpuszczalniki, jak i substraty do
otrzymywania
innych
związków
chemicznych.
aldehyd
C
O
R
H
C
O
R
R
keton
ZWIĄZKI KARBONYLOWE
ALDEHYDY I KETONY
Nazwę aldehydu tworzy się od nazwy
odpowiedniego alkanu, do której dodaje
się przyrostek -al. Łańcuch macierzysty
musi zawierać grupę -CHO i atom węgla
tej grupy numeruje się jako C1.
2-etylo-4-metylopentanal
C
H
3
CH
O
C
H
3
5
4
3
2
CH
1
O
C
H
3
CH
3
etanal acetaldehyd
CH
2
O
Metanal albo formaldehyd to
najprostszy
aldehyd,
produkowany
w
przemyśle w dużych ilościach,
między
innymi
stosowany
do
produkcji żywic, do spajania płyt
wiórowych i sklejki
ZWIĄZKI KARBONYLOWE
ALDEHYDY I KETONY
Nazwy ketonów tworzy się od nazwy
odpowiedniego alkanu, do której dodaje
się -on. Najdłuższy łańcuch, w którym
znajduje się grupa ketonowa, jest
łańcuchem
macierzystym,
a
numerowanie rozpoczyna się od końca
najbliższego
karbonylowego
atomu
węgla.
propanon - aceton
C
H
3
C
CH
3
O
C
H
3
6
5
4
3
2
CH
3
1
O
4-heksen-2-on
C
H
3
6
5
4
3
2
CH
3
1
O
O
2,4-heksanodion

ZWIĄZKI KARBONYLOWE
ALDEHYDY I KETONY
Aldehydy
łatwo
ulegają
reakcji
utleniania do kwasów karboksylowych,
natomiast ketony w zasadzie są odporne
na działanie utleniaczy. Różnica ta jest
konsekwencją struktury: aldehydy w
przeciwieństwie do ketonów, zawierają
atom wodoru w grupie -CHO, który może
zostać usunięty w reakcji utleniania.
Utlenianie
można
przeprowadzić
odczynnikiem Jonesa (CrO
3
w wodnym
roztworze kwasu siarkowego). Reakcja
utleniania z odczynnikiem Jonesa
zachodzi
szybko
w
temperaturze
pokojowej z dobra wydajnością.
heksanal
kwas heksanowy
C
O
R
H
C
O
R
OH
[O]
C
H
3
CH
O
C
H
3
C
O
OH
ZWIĄZKI KARBONYLOWE
ALDEHYDY I KETONY
Utlenianie
aldehydów można także
przeprowadzić
stosując
wodny,
amoniakalny roztwór tlenku srebra
Ag
2
O, znany jako odczynnik Tollensa.
Aldehydy sa utleniane tym odczynnikiem
z dużą wydajnością, bez naruszenia
wiązań podwójnych węgiel-węgiel lub
innych grup funkcyjnych obecnych w
cząsteczce.
Podczas
utleniania
odczynnikiem
Tollensa
na
ściankach
naczynia
reakcyjnego odkłada się błyszczące
lustro metalicznego srebra., stanowiące
test
jakościowy
na
obecność
aldehydowej
grupy
funkcyjnej
w
cząsteczce związku o nieznanej budowie.
benzaldehyd
kwas benzoesowy
CH
O
C
O
OH
Ag
2
O
NH
4
OH, H
2
O)
+
Ag
Document Outline
Wyszukiwarka
Podobne podstrony:
07 Dewiacja organizacyjne
organizacja uslug hotelarskich wyklad 07.03.2010, GWSH, organizacja usług w hotelarstwie
07 Organizowanie procesu gospod Nieznany
Krwawe ataki (organizacja State of Iraq) (09 07 2009)
07 Planowanie żywienia odpowiednio do potrzeb organizmu
07 Metody syntezy organicznej VI s1 2011 [tryb zgodnosci]id 6901
07 Organizowanie procesu gospodarczego przedsiębiorstwa
organizacja uslug hot. 07.03.2010, GWSH TiR, Organizacja usług hotelarskich
BOTANIKA WYK+üAD 07, Organizmy zarodnikowe i rośliny nasienne
07 Organizacja pracy biurowejid Nieznany (2)
Rachunkowość - wykłady - 07, Formalne, prawne i organizacyjne aspekty prowadzenia rachunkowości
07 Organizowanie procesu inwestycyjnego
2013-14-OTZ OT 07 organizator, TRANSPORT UTP BYDGOSZCZ, VI semestr - Organizacja Transportu, Organiz
07 Dewiacja organizacyjne
Petycje pl Nr 7621 26 07 2011 Żywność organiczna na naszym stole
07 Planowanie żywienia odpowiednio do potrzeb organizmu 2
więcej podobnych podstron