Fizyka jądrowa
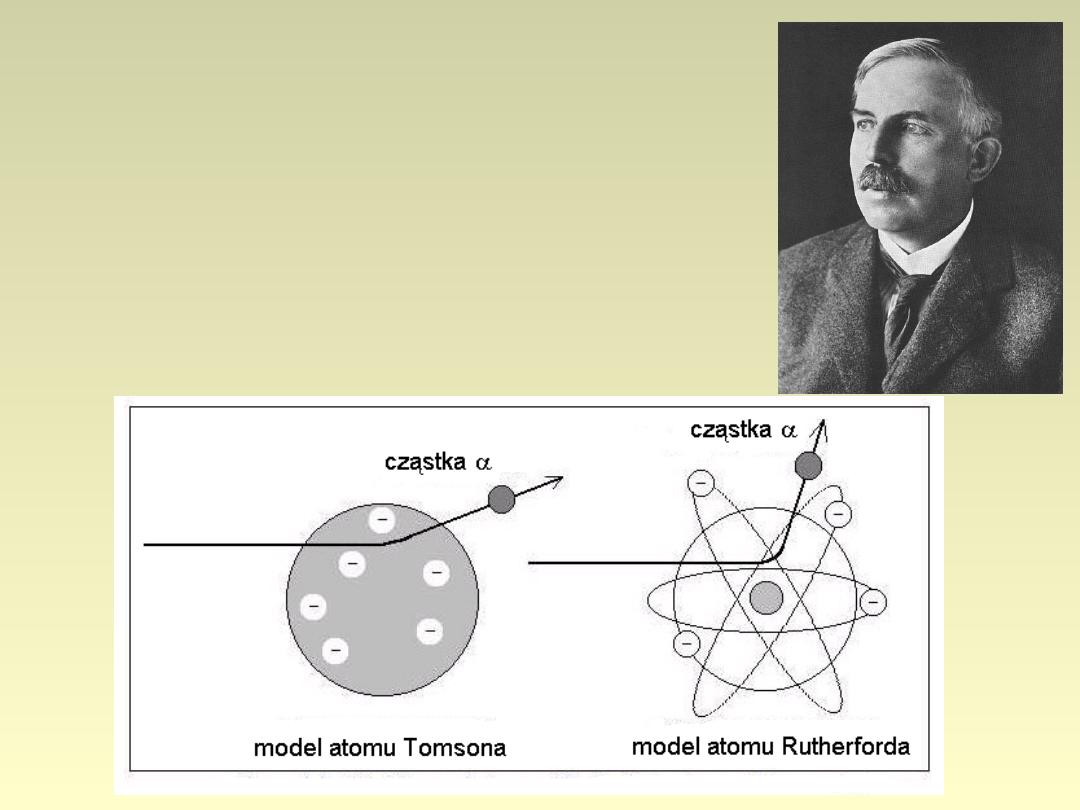
Doświadczenie
Rutherforda (1911)
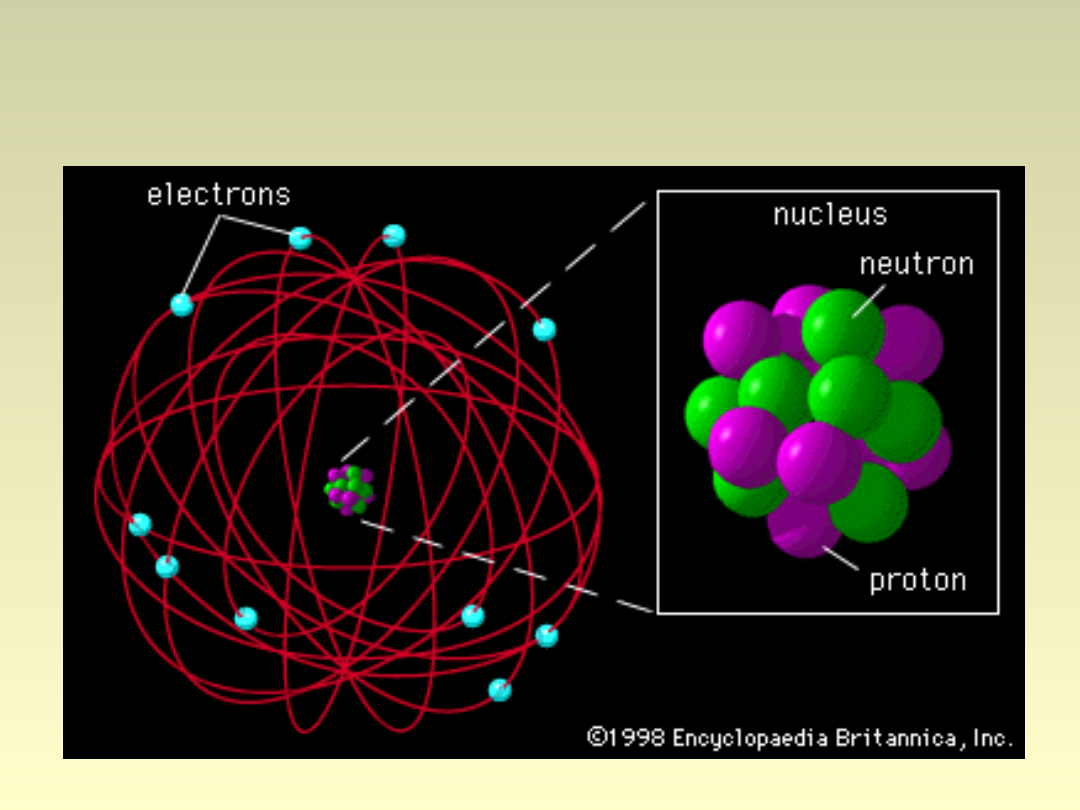
Budowa jądra atomowego

Budowa jądra atomowego
• Jądro atomowe składa się z
nukleonów
:
protonów
i
neutronów
;
• Liczba masowa
A
= liczba
nukleonów
;
• Liczba atomowa lub porządkowa
Z
= liczba
protonów
;
• Liczba
neutronów N
= A – Z;
• Proton ma ładunek dodatni i masę:
• Neutron nie ma ładunku elektrycznego i ma
masę:
C
e
19
10
6
,
1
kg
m
p
27
10
672
,
1
kg
m
n
27
10
674
,
1

Budowa jądra atomowego
• Kombinacja określonej liczby protonów i
neutronów -
nuklid
.
• Zapis:
np.
• Nuklidy o tej samej liczbie
Z – izotopy
;
• Nuklidy o tej samej liczbie
A – izobary
;
• Nuklidy o tej samej liczbie
N – izotony
.
X
A
Z
U
238
92

Budowa jądra atomowego
• Jądro atomowe jest
dużo
mniejsze od
atomu:
• Masa jądra:
• Gęstość materii jądrowej:
3
1
15
10
7
,
1
3
,
1
A
m
R
j
a
j
m
m
a
j
R
R
5
10
3
18
10
m
kg
j

Siły jądrowe
• Jądro utrzymuje się w całości dzięki
siłom jądrowym
;
• Siły jądrowe mają bardzo
krótki
zasięg
→ małe rozmiary jąder;
• Oddziałują ze sobą tylko najbliższe
nukleony;
• Siły jądrowe nie zależą od ładunków
nukleonów;
• Neutrony pełnią rolę „kleju” – czym
jądro większe, tym więcej neutronów.

Modele jądrowe
• Model kroplowy
:
oddziaływanie pomiędzy
nukleonami jest silne, że
ich ruchy są skorelowane;
jądro traktuje się jak kroplę
cieczy.
• Model powłokowy
: nukleon
oddziałuje z wypadkowym
polem potencjalnym.
Oba modele nie tłumaczą
wszystkich efektów, tylko niektóre
np. model powłokowy istnienie jąder
magicznych.

Energia wiązania jądra
• Dokładny pomiar mas atomowych
spektrometrem masowym → bilans masy
jądra:
• ∆m –
defekt masy
;
• Z Einsteina:
• E
w
–
energia wiązania jądra
; średnio na
jeden nukleon:
0
,
Z
A
M
m
Z
A
Zm
m
n
p
w
E
mc
E
2
MeV
A
E
w
8
7
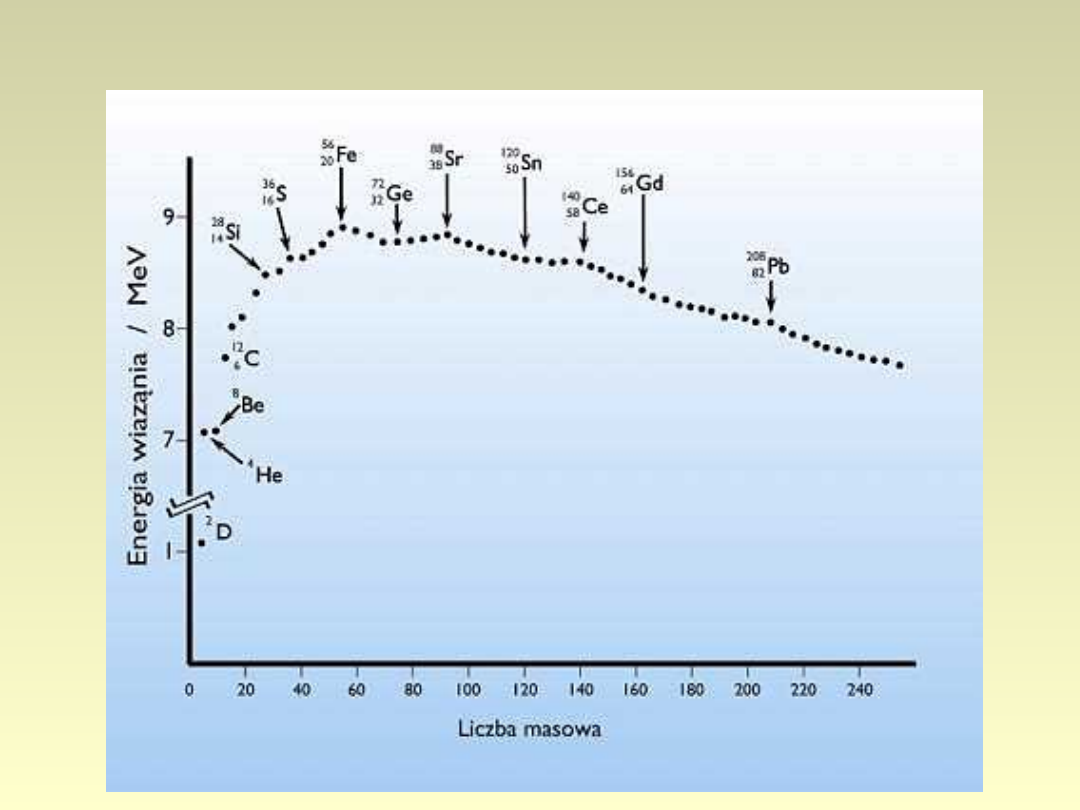
Energia wiązania jądra
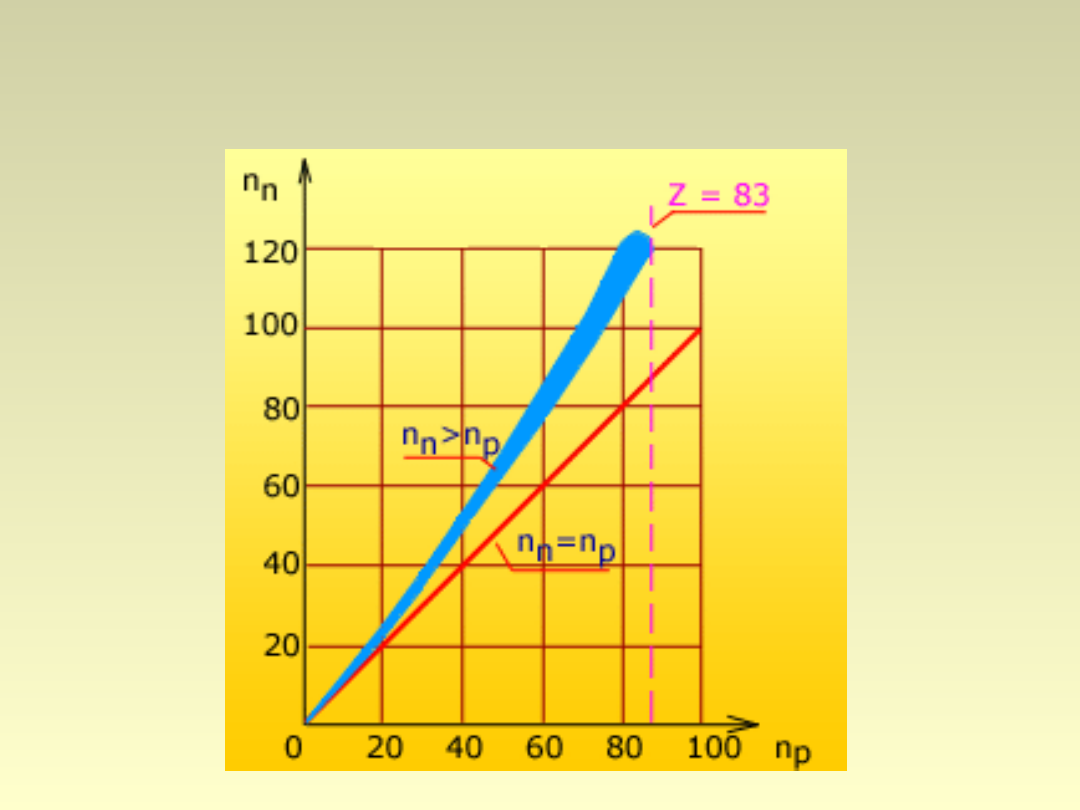
Systematyka nuklidów
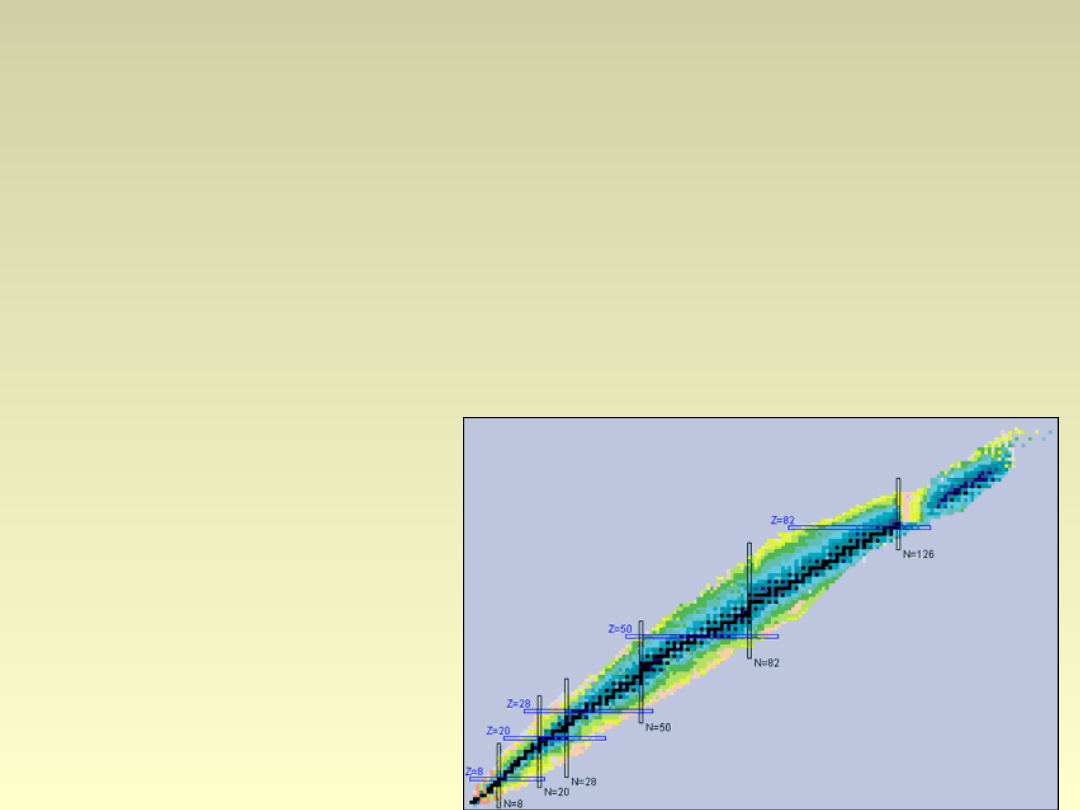
Systematyka nuklidów
•Pierwiastki o parzystej liczbie protonów – więcej
izotopów niż te o nieparzystej;
•87% masy Ziemi – jądra parzysto-parzyste;
•Udział neutronów rośnie wraz ze wzrostem A;
•Wyjątkowo trwałe są jądra magiczne (2, 8, 20, 28,
50, 82, 126, 152).
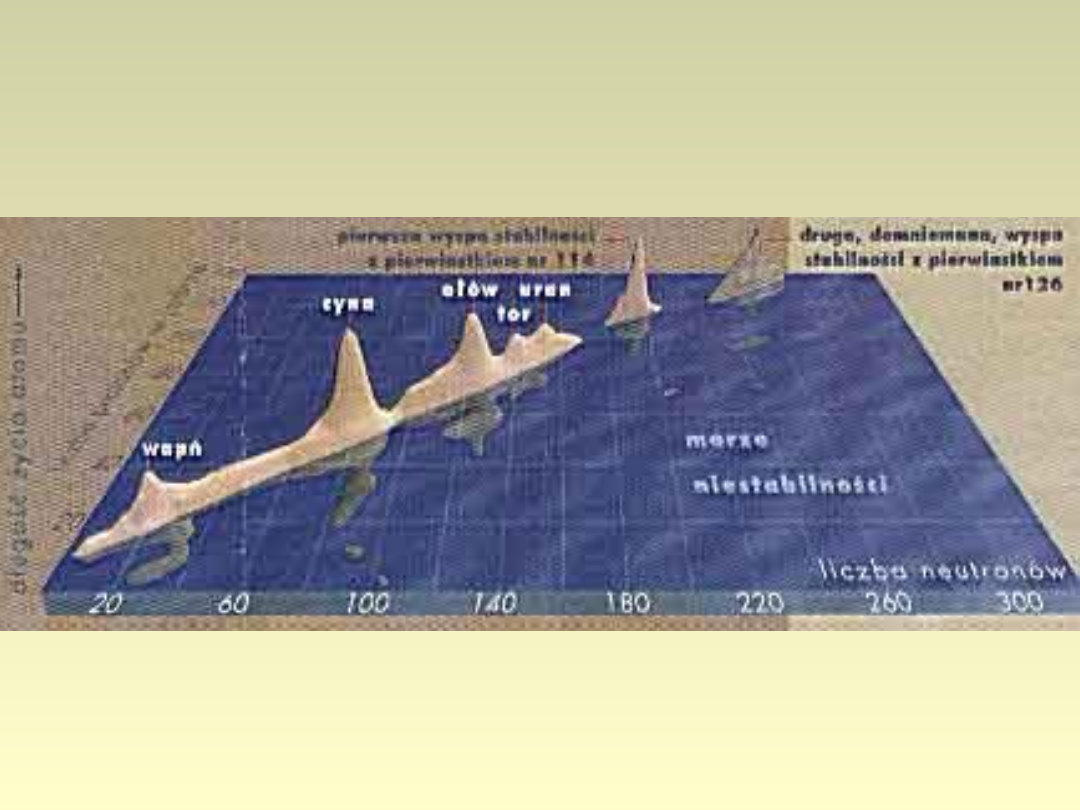
Systematyka nuklidów

Promieniotwórczość
Promieniotwórczość
naturalna została odkryta
przez Bequerela (1896) i
małżeństwo Curie (1898)
w rudach uranu (polon i
rad).

Promieniotwórczość
• Można zaobserwować trzy rodzaje
promieniowania:
• -
jądra He
• -
elektrony
• -
fale elektromagnetyczne
• Naturalne izotopy długożyciowe:
238
U
(4,5·10
9
l),
40
K (1,3·10
9
l);
• Naturalne izotopy krótkożyciowe
wytworzone przez promieniowanie
kosmiczne:
3
H (12,3 l),
14
C (5730 l).
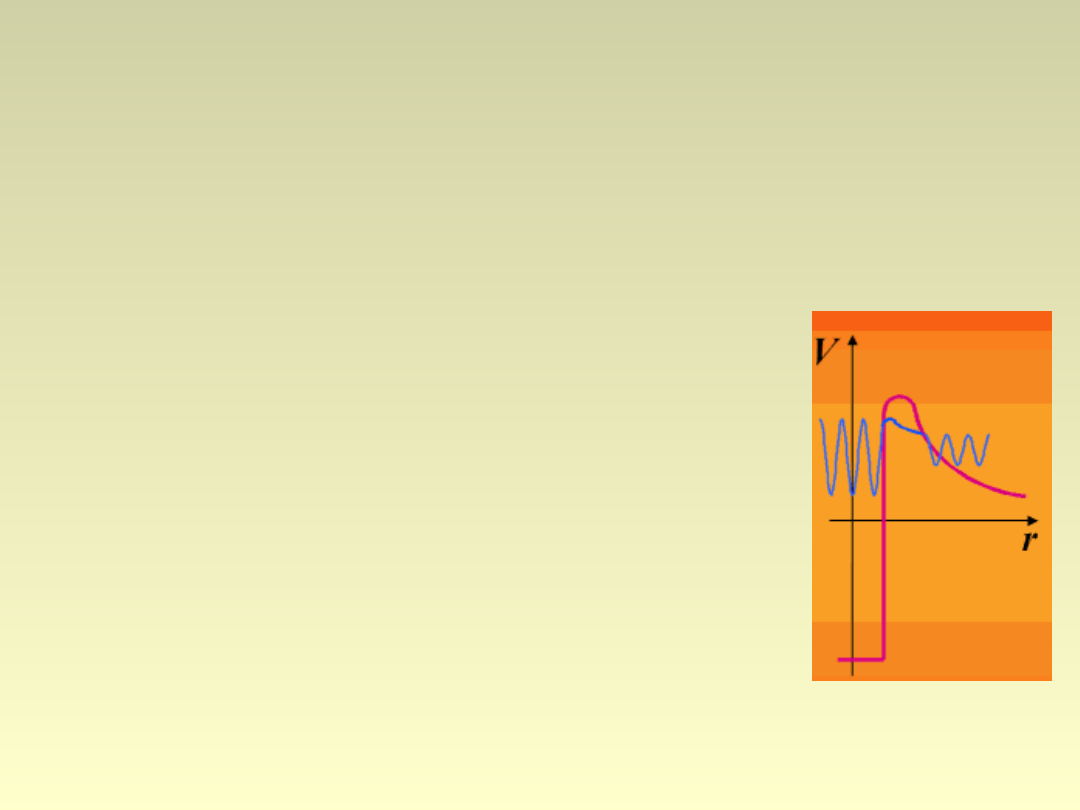
Rozpad
•Jądro macierzyste emituje jądro He;
•Zachodzi dla ciężkich pierwiastków (od
Bi), które mają zbyt dużo protonów, aby
być stabilne;
•Cząstka
przenika barierę potencjału
kulombowskiego jądra w
efekcie
tunelowym
;
•Energię przemiany unoszą produkty;
•Przykład:
He
Y
X
A
Z
A
Z
4
2
4
2
He
Th
U
4
2
234
90
238
92

Rozpad
~
0
1
1
1
1
0
e
p
n
e
n
p
0
1
1
0
1
1
e
Y
X
A
Z
A
Z
0
1
1
•Dwa rodzaje przemian w jądrze
+
i
-
:
•Przykłady:
•Hipoteza
neutrina
(Pauli 1930) – żeby spełnić
zasadę zachowania energii i pędu w rozpadzie .
Neutrina zostały odkryte w reaktorze jądrowym w
1956 r.
e
Ne
Na
0
1
22
10
22
11
~
0
1
60
28
60
27
e
Ni
Co
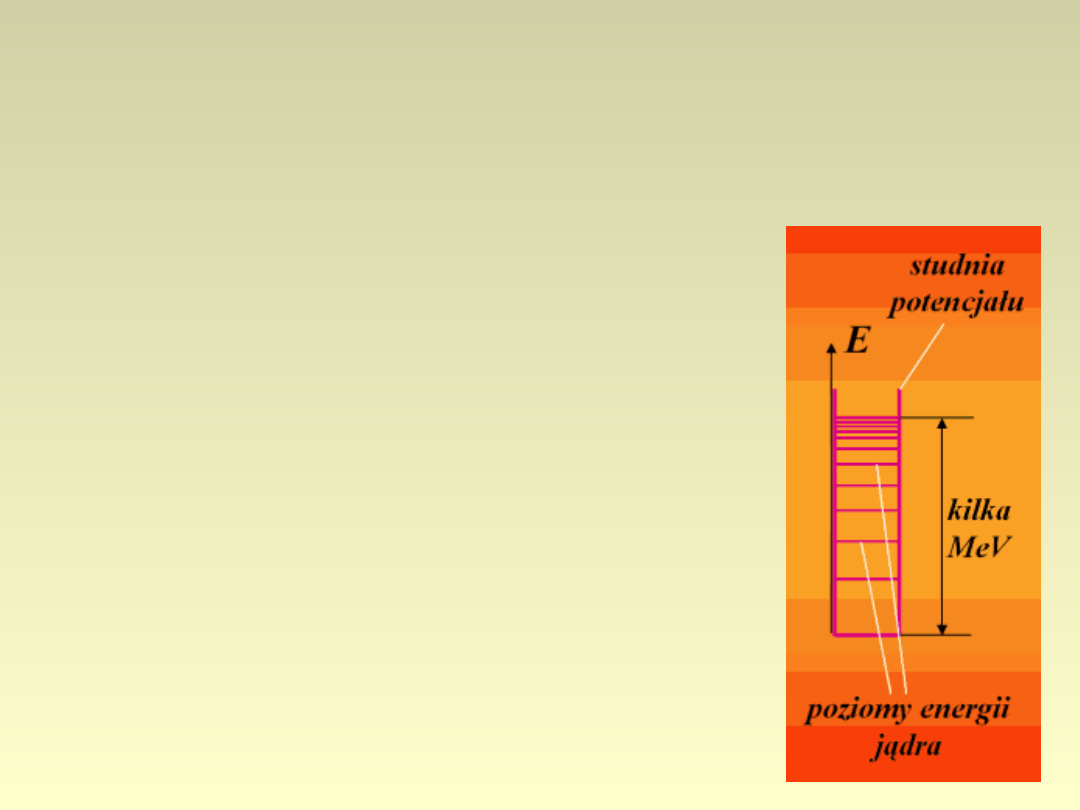
Przemiana
X
X
A
Z
A
Z
*
•
Po rozpadzie i jądra
pozostają w stanie
wzbudzonym – aby
pozbyć się nadmiaru
energii emitują
promieniowanie
.
• Średnie czasy życia
stanów wzbudzonych: 10
-
12
– 10
5
s.

Prawo rozpadu
promieniotwórczego
Liczba rozpadających się jąder jest
proporcjonalna do ich liczby:
Prawo rozpadu promieniotwórczego:
- stała rozpadu
N
dt
dN
t
N
N
dt
N
dN
0
0
t
e
N
N
0
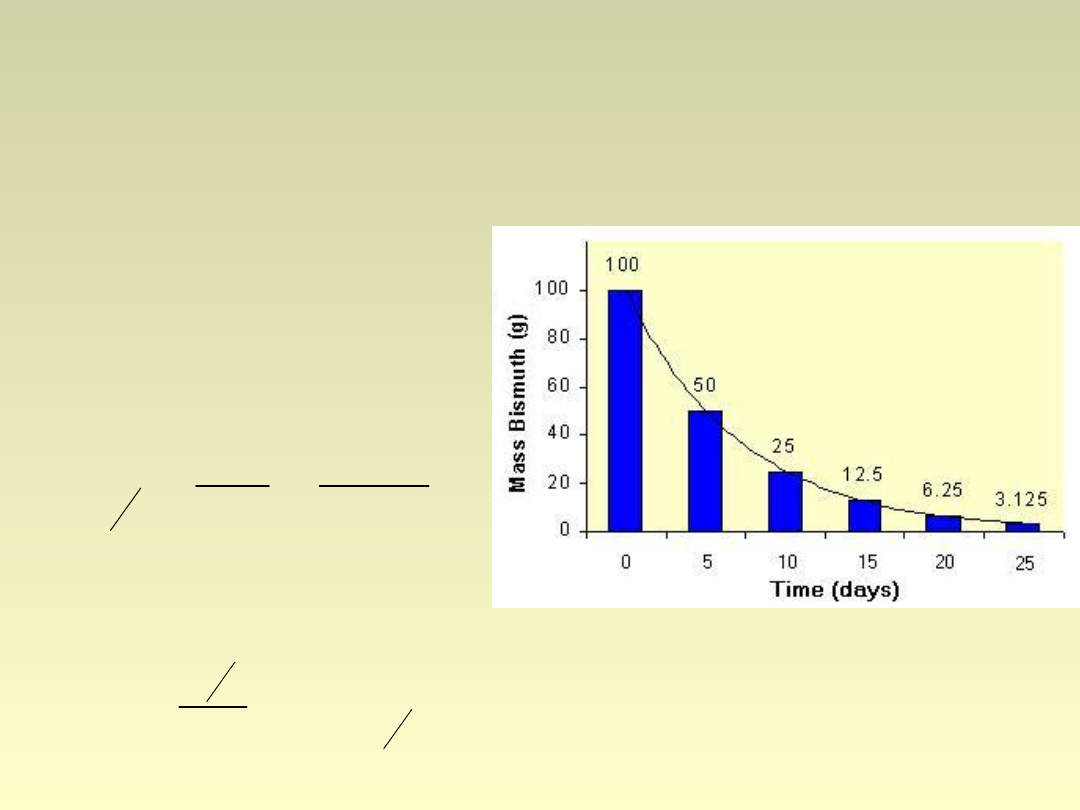
Prawo rozpadu
promieniotwórczego
Czas połowicznego
rozpadu T
1/2
– czas po
którym rozpadnie się
połowa początkowej
liczby jąder N
0
/2:
Czas życia jąder
:
693
,
0
2
ln
2
1
T
2
1
2
1
44
,
1
2
ln
T
T
Prawo rozpadu
promieniotwórczego
Aktywność
– liczba rozpadów w jednostce czasu
(jednostką jest bekerel):
Aktywność izotopów obecnych w człowieku:
t
e
N
N
dt
dN
A
0

Reakcje jądrowe
↑
Przemiana jąder na skutek oddziaływania
cząstek z jądrami:
• Źródło neutronów:
• Reakcja egzoenergetyczna:
• Sztuczna promieniotwórczość:
n
C
He
Be
1
0
12
6
4
2
9
4
Zawsze musi być spełniona zasada zachowania
ładunku i liczby nukleonów!
MeV
n
He
H
H
6
,
17
1
0
4
2
2
1
3
1
0
0
110
47
1
0
109
47
Ag
n
Ag
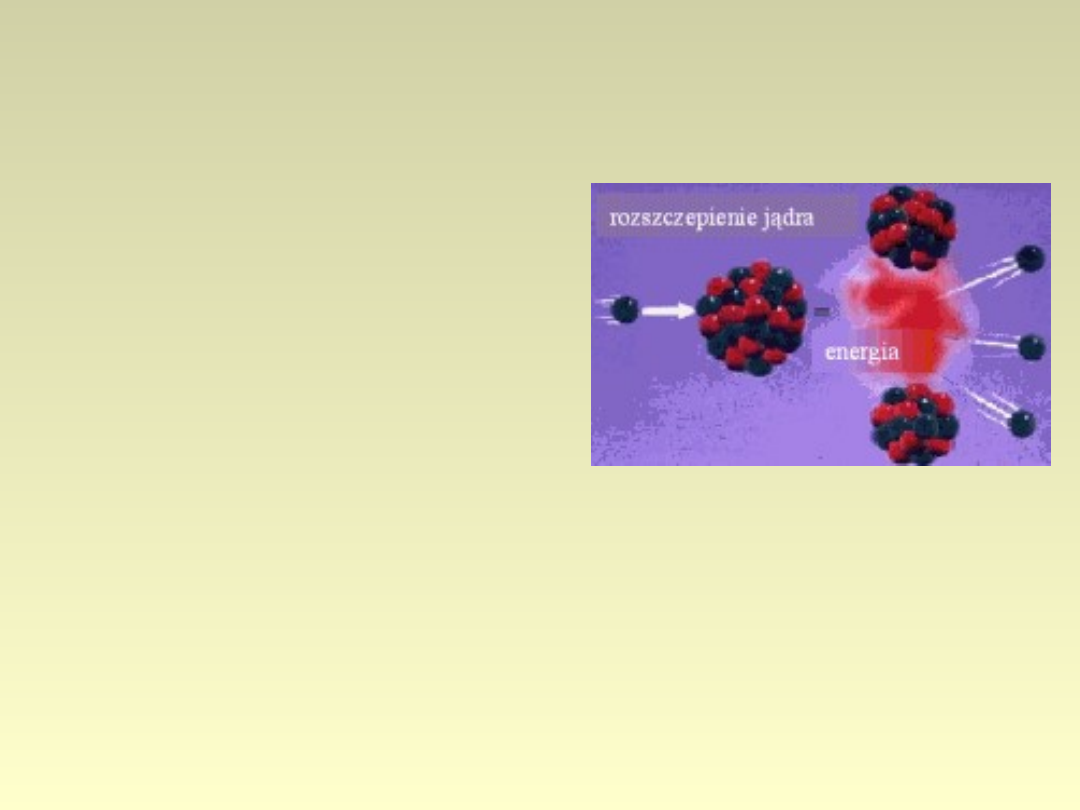
Rozszczepienie
•Hahn i Strassman (1938)
– U może się „zmieniać” w
Ba;
•Frish i Meitner – U po
przyłączeniu neutronu
tworzy wiele pierwiastków;
•Przykładowa reakcja:
MeV
n
La
Br
U
n
U
200
2
1
0
146
57
88
35
236
92
1
0
235
92
Neutrony otrzymane w wyniku rozszczepienia
mogą być wykorzystane do
reakcji
łańcuchowej
.
MeV
e
n
Xe
Mo
U
n
U
200
4
2
0
1
1
0
136
54
98
42
236
92
1
0
235
92
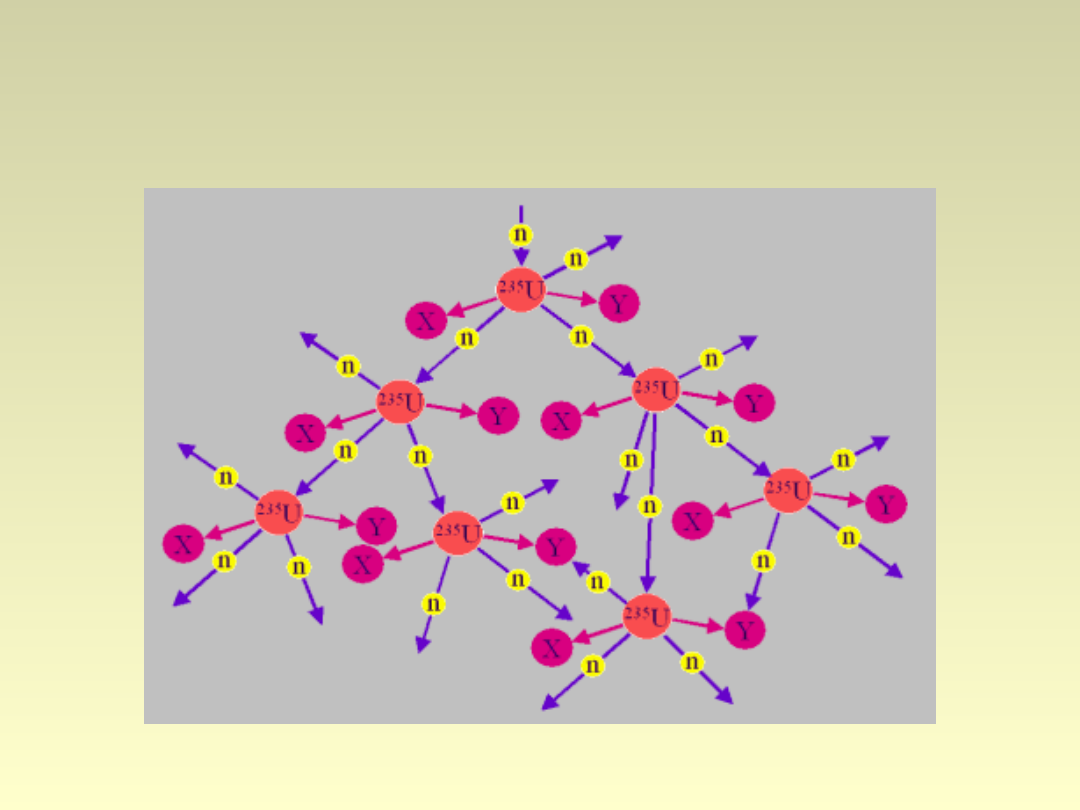
Reakcja łańcuchowa

Reakcja łańcuchowa
• Zbyt mała masa próbki – neurony
wylatują na zewnątrz i nie ma reakcji
łańcuchowej;
• Jeżeli masa próbki jest równa
masie
krytycznej
(dla 43 kg) – reakcja
łańcuchowa ze stałą prędkością (
reaktor
jądrowy
);
• dla mas większych niż krytyczna –
lawinowa reakcja łańcuchowa z
wydzieleniem ogromnych ilości energii
(
bomba atomowa
).
U
235
92

Reaktor jądrowy
• Paliwo jądrowe
- wzbogacony
(0,7-3,5%).
• Moderator
(H
2
O, D
2
O, grafit) –
pozwala na wychwyt neutronów.
• Reaktory służą do:
U
235
92
U
238
92
–produkcji energii
(17% energii na
świecie);
–badań naukowych;
–produkcji sztucznych
izotopów (np. dla
medycyny).
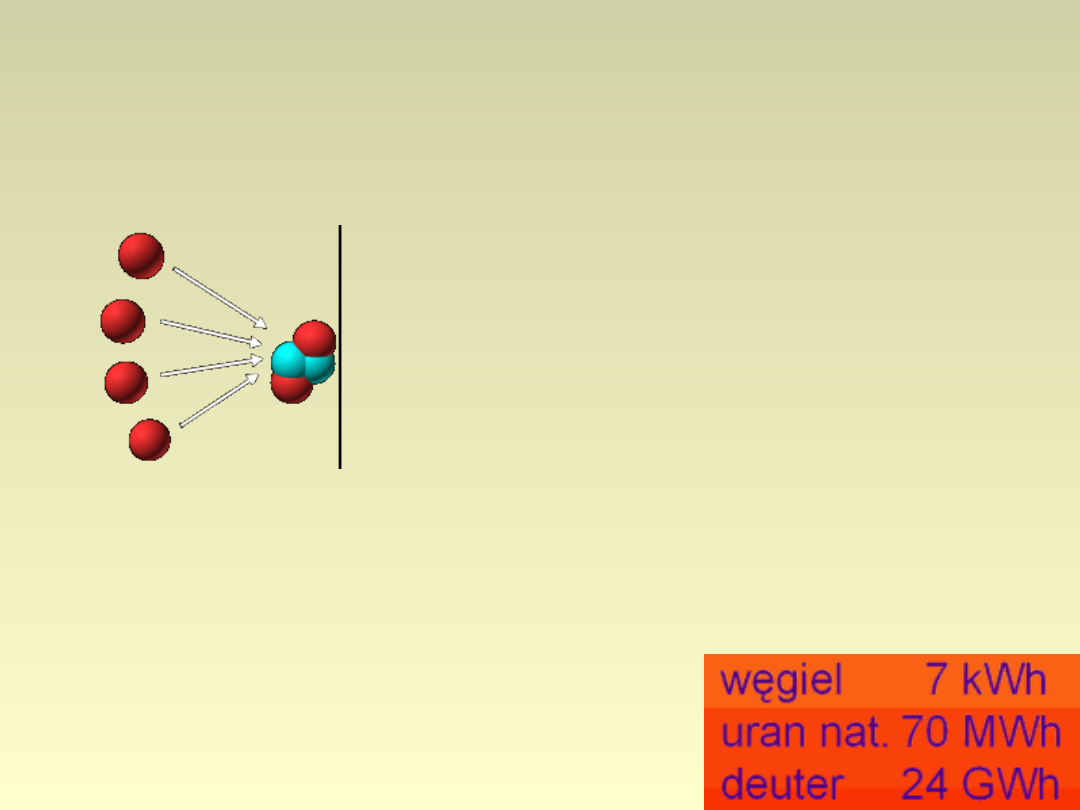
Synteza jądrowa
• Synteza jądrowa – egzoenergetyczna reakcja
łączenia jąder lekkich pierwiastków w cięższe:
• Źródło energii Słońca, na Ziemi – problem z
utrzymaniem wysokotemperaturowej plazmy
w jednej części;
• Użyta w bombie termojądrowej;
• Porównanie energii
otrzymanej z 1kg substancji
:
MeV
n
He
H
H
6
,
17
1
0
4
2
3
1
2
1
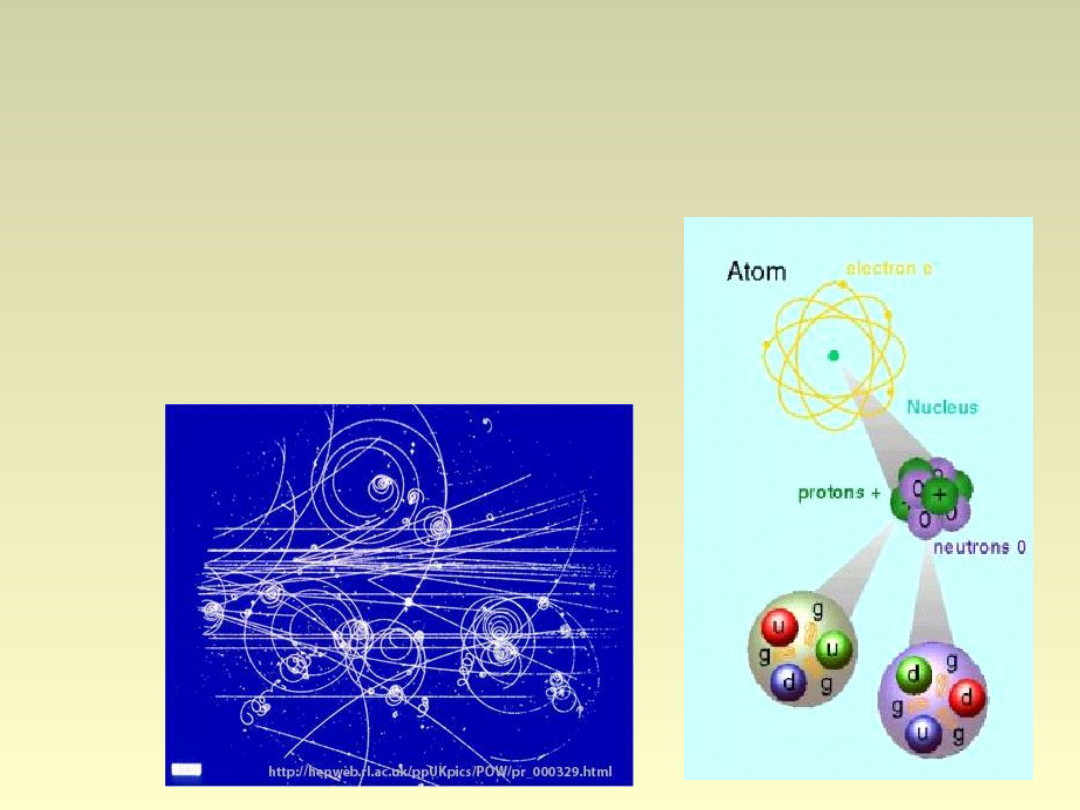
Cząstki elementarne
Odkryto kilkaset cząstek
„elementarnych”, obserwując
ich oddziaływanie z materią.
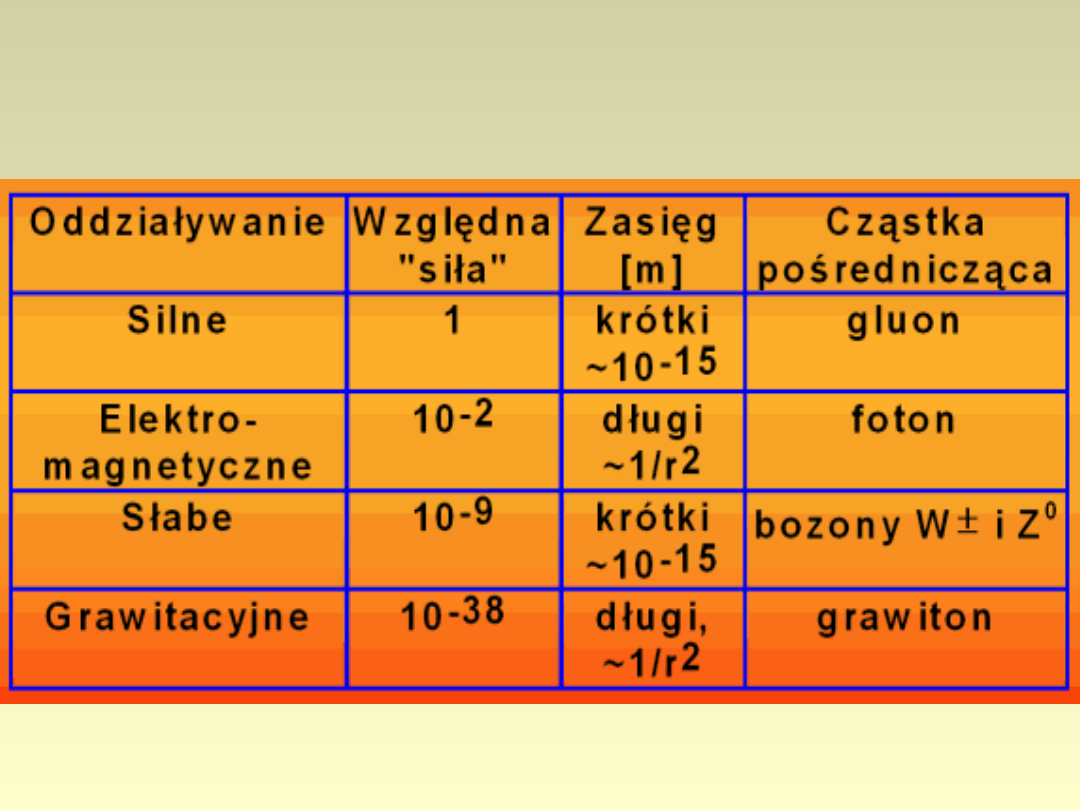
Siły natury
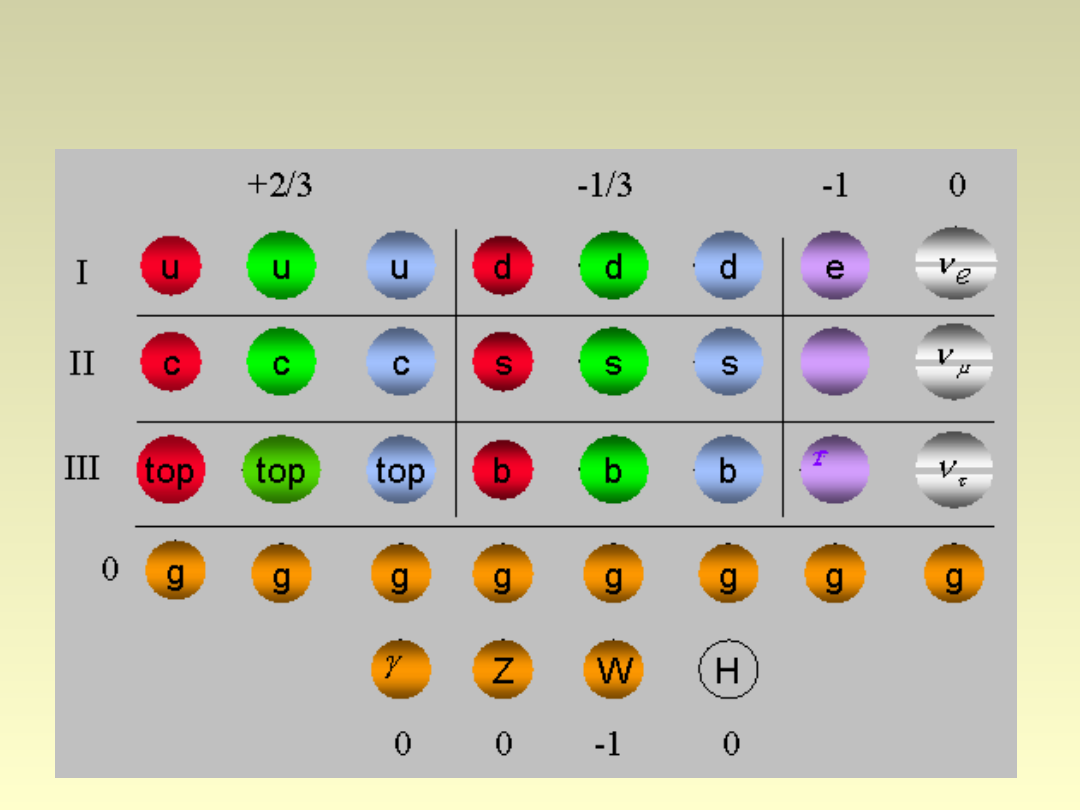
Kwarki, leptony, bozony
pośredniczące

Klasyfikacja cząstek
• Leptony
(bez struktury): elektrony,
miony i taony.
• Hadrony
(zbudowane z kwarków):
– mezony, np. piony i kaony;
– bariony np. nukleony.
• Cząstki pośredniczące
: foton, gluony,
W i Z, grawiton.
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
Wyszukiwarka
Podobne podstrony:
Fizyka jadrowa
Raport 398, Fizyka jądrowa, Dozymetria
CZARNOBYL W STRONĘ POLSKI, Fizyka, Fizyka jądrowa
Fizyka Jądrow1
24 fizyka jadrowa
Fizyka jadrowa 4 6
23 fizyka jadrowa id 30068 Nieznany
Fizyka jadrowa 12
Fizyka jądrowa arkusz poziom podstawowy
Fizyka jadrowa 11
38 fizyka jądrowa
Fizyka jądrowa
WYKLAD z fizyki atomowej i mol w3-4 2008, Fizyka, 13.Fizyka jądrowa, mat ch1
Fizyka jądrowa wzory
FIZYKA JĄDROWA
fizyka jądrowa
fizyka jądrowa, Szkoła
więcej podobnych podstron