
Infekcje HPV,
immunoprofilaktyka
Wykonanie: Martyna Orman

Wirus brodawczaka
ludzkiego (HPV) jest
szeroko rozpowszechniony.
Obecnie znanych jest 120
typów wirusa HPV, z których
większość jest relatywnie
nieszkodliwa, a zakażenie
przebiega bezobjawowo i
ustępuje samoistnie. Około
30 typów wirusa HPV jest
odpowiedzialnych za
infekcje narządów moczowo-
płciowych kobiet i mężczyzn
(przenoszone droga
kontaktów seksualnych).
Czym jest HPV?
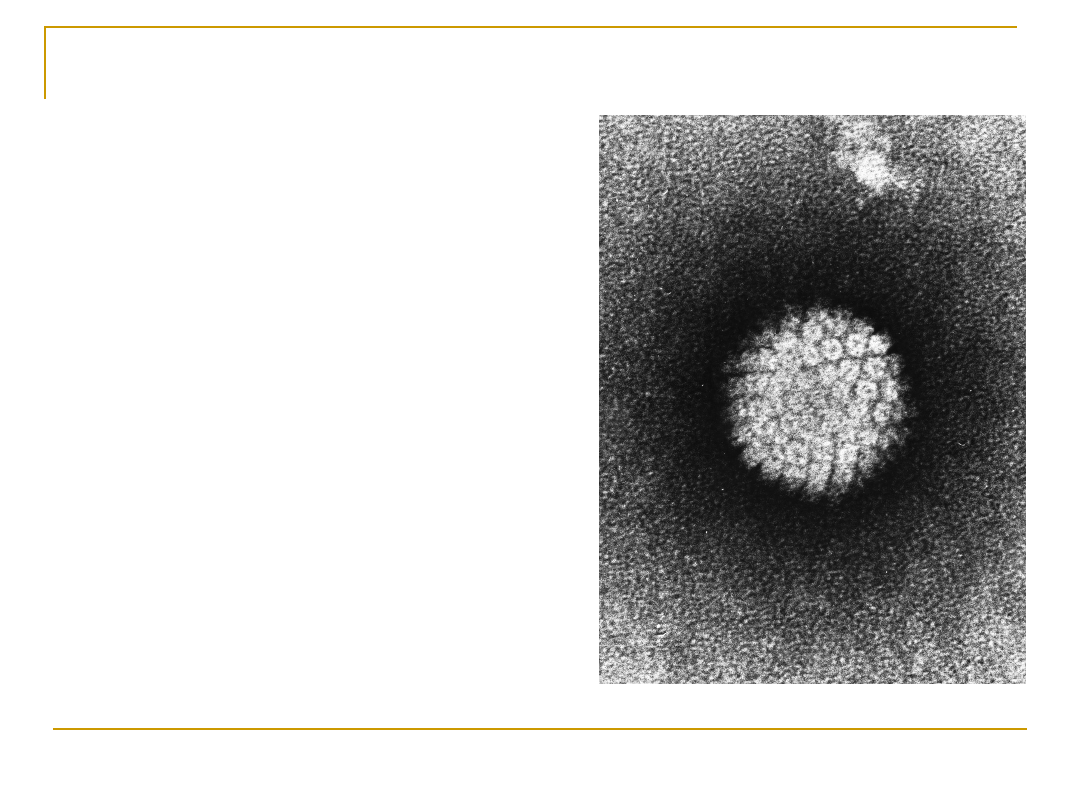
Budowa
•
Wirus DNA o ok. 8000 par
nukleotydów
•
Białkowy kapsyd o kształcie
dwudziestościanu
foremnego
•
Zawiera jedynie 7 genów
pośród których dwa - E6 i
E7 - to onkogeny
•
Po włączeniu tych
fragmentów do DNA
komórek nabłonka
dochodzi do blokowania
anty-onkogennych białek
p53 i pRb
Niskoonkogenne
(niskiego
ryzyka)-
odpowiedzialne są
za powstawanie
łagodnych zmian
brodawkowatych
narządów
rozrodczych
(określanych jako
kłykciny
kończyste)
zarówno u kobiet
jak i mężczyzn
Wysokoonkogenne
(wysokiego ryzyka)
prowadzą najczęściej
do powstawania raka
szyjki macicy (ponad
90% zachorowań
wywołanych jest przez
wysokoonkogenne
odmiany HPV).
Zakażenie typami HPV
wysokoonkogennym
związane jest również
z występowaniem
innych, rzadziej
występujących
nowotworów narządów
moczowo-płciowych,
takich jak rak odbytu,
pochwy i sromu
Typy
wirusa
HPV
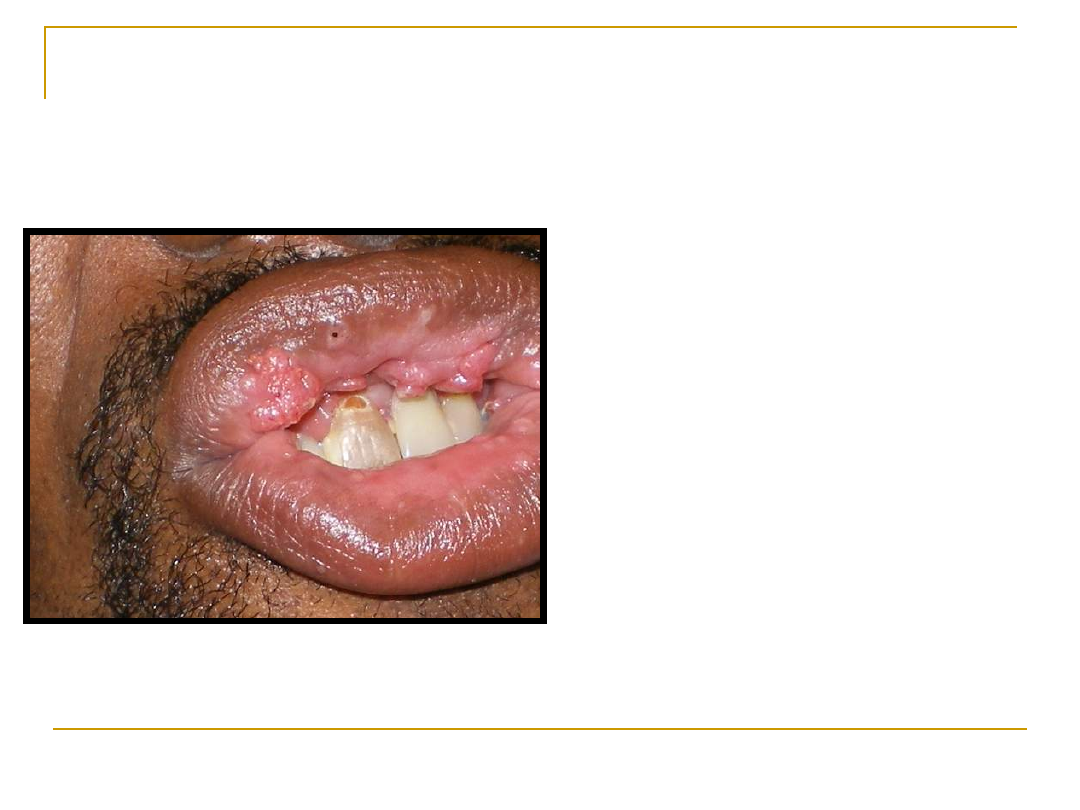
Skutki zakażenia
Kłykciny kończyste -to
drobnobrodawkowate wykwity
najczęściej na śluzówce przedsionka
pochwy, ścianach pochwy i odbycie.
Brodawczaki płaskonabłonkowe-
przylegają niewielką szypułą do
powierzchni nabłonka, a w części
obwodowej mają bardzo
pofałdowaną, brodawkowatą
powierzchnię. Często są pokryte
zrogowaciałym nabłonkiem, przez co
układ naczyń jest gorzej widoczny.
Rogowacenie białe (Leukoplakia
zwykła)
Zmiany te powstają w wyniku
rogowacenia nabłonka, który
fizjologicznie nie rogowacieje.
Zmiany takie występują na pokrytej
nabłonkiem wielowarstwowym
płaskim nierogowaciejącym
śluzówce przedsionka pochwy, na
ścianach pochwy, na tarczy szyjki
macicy.
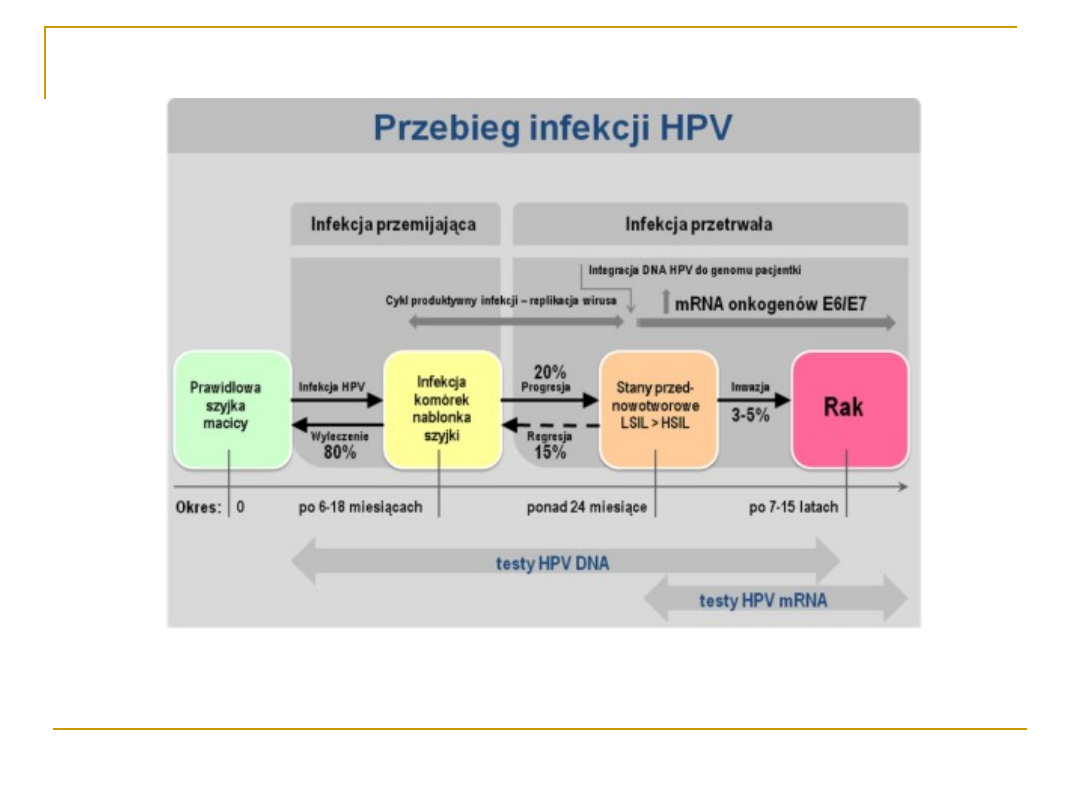

Immunoprofilaktyka
Radykalną pomoc w wyeliminowaniu
zakażeń HPV oferuje szczepionka
profilaktyczna, zapobiegająca
całkowicie długotrwałym infekcjom
HPV typami 16 i18 - związanymi z
rozwojem 70% raków szyjki macicy,
oraz typami 6 i 11 - wywołującymi
brodawki narządów płciowych.
Immunoprofilaktyka
Może zapobiec zakażeniu niektórymi gatunkami
związanego z rozwojem
i kilku
rzadziej występujących nowotworów(odbytu, sromu, pochwy i
pracia).
Szczepionki obecne na rynku to Gardasil ( w Polsce znany pod
nazwą Silgard) i Cervarix Obie szczepionki chronią przed
dwoma typami wirusa HPV (HPV-16 i HPV-18). Silgard chroni
łącznie przed czterema typami wirusa HPV (6, 11, 16 i 18).
Typy 6 i 11 odpowiedzialne są w 90-ciu procentach za
brodawki narządów płciowych. Ponadto wykazano, że mogą
być stosowane w profilaktyce raka jamy
ustnej wywołanegoprzez onkogenne
wirusy HPV.

Silgard
To szczepionka zawierająca adiuwant, niezakaźna, rekombinowana,
czterowalentna szczepionką otrzymana z wysokooczyszczonych,
wirusopodobnych cząsteczek (ang. virus-like particles, VLP) głównego
białka L1 kapsydu wirusów HPV typu 6, 11, 16 i 18. Wirusopodobne
cząsteczki nie zawierają wirusowego DNA, dlatego nie mają zdolności
zakażania komórek, namnażania się ani wywoływania choroby. HPV
zakaża tylko ludzi, lecz badania na zwierzętach dotyczące
analogicznych papillomawirusów sugerują, że skuteczność
szczepionek opartych na L1 VLP jest związana z rozwojem
immunologicznej odpowiedzi humoralnej.
Skład jakościowy i ilościowy substancji czynnych:
Białko L12,3 wirusa brodawczaka ludzkiego1 typu 6 20 mikrogramów
Białko L12,3 wirusa brodawczaka ludzkiego1 typu 11 40
mikrogramów
Białko L12,3 wirusa brodawczaka ludzkiego1 typu 16 40
mikrogramów
Białko L12,3 wirusa brodawczaka ludzkiego1 typu 18 20
mikrogramów.

Szczepienie-kiedy?
Najbardziej odpowiednim
momentem szczepienia
jest, podanie szczepionki przed
pierwszym kontaktem z
wirusem czyli najlepiej przed
inicjacją seksualną.
Szczepieniem mogą zostać objęte
dziewczęta od 11-12 roku życia
(najwcześniej od 9 tego roku życia,
ponieważ nie zostało
udokumentowane bezpieczeństwo
stosowania poniżej 9 r. ż.).
Oczywiście zaszczepić mogą się
także kobiety aktywne seksualnie,
gdyż nie wiadomo czy są one, czy
nie, zakażone wirusem HPV.
Nie ma konieczności wykonywania
u osób aktywnych seksualnie
badania na obecność wirusa HPV w
wymazie z szyjki macicy.
Pierwszy cykl szczepień
składa się z 3 oddzielnych 0,5
ml dawek, podawanych
zgodnie z następującym
schematem: 0, 2, 6 miesięcy.
Jeśli konieczny jest inny
schemat szczepienia, druga
dawka powinna być podana co
najmniej jeden miesiąc po
pierwszej dawce, a trzecia
dawka powinna być podana co
najmniej 3 miesiące po dawce
drugiej. Wszystkie trzy dawki
należy podać w ciągu 1 roku.
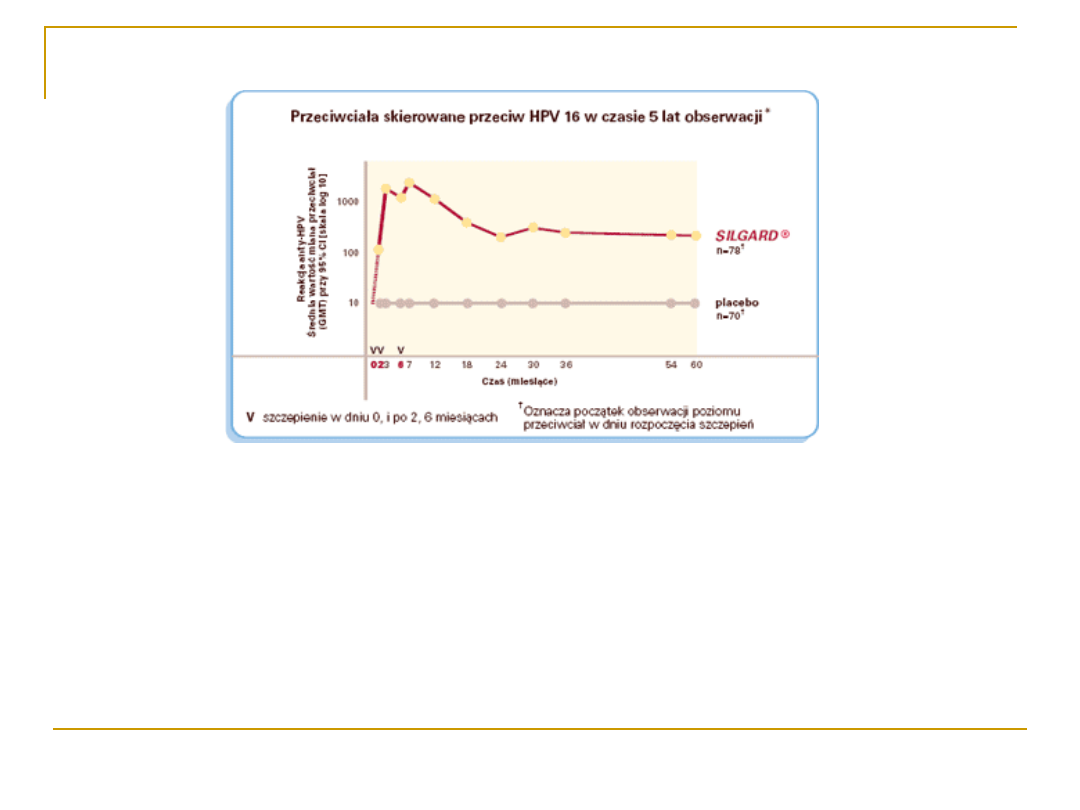
Stwierdzono, że po szczepieniu poziom przeciwciał jest
kilkadziesiąt lub nawet ponad sto razy wyższy niż w
przebiegu naturalnego zakażenia. Po podaniu dawki
przypominającej wzrasta on dodatkowo do 40 razy.
Przeciwciała utrzymują się w organizmie człowieka przez
okres 5 lat i tak samo długo działa pamięć
immunologiczna – tzn. podanie dawki przypominającej
po tym okresie wyzwala produkcję dużej ilości nowych
przeciwciał.

Cervarix
Szczepionka Cervarix zawiera oczyszczone białka L1 dla
dwóch typów wirusa HPV – typu 16 i 18. Białka zawarte w
szczepionce Cervarix są wytwarzane metodą określaną jako
„technika rekombinacji DNA”: są one wytwarzane przez
komórki, które otrzymały odpowiedni gen (DNA),
umożliwiający im wytwarzanie białek L1. Białka te są łączone
w „cząsteczki przypominające wirusa” (są to struktury, które
wyglądają podobnie do wirusa HPV, dzięki czemu organizm
może je rozpoznać). Szczepionkę wytwarza się z
zastosowaniem „systemu adiuwantowego” zawierającego
MPL – oczyszczony lipid (substancja tłuszczopodobna )
wyekstrahowany z bakterii, który działa jako substancja
immunostymulująca: stymuluje on odpowiedź układu
immunologicznego przeciwko szczepionce. Szczepionka jest
„adsorbowana”, co oznacza, że zawierające białko L1
cząsteczki przypominające wirusa oraz MPL są przyłączone
do związku glinu w celu skuteczniejszego stymulowania
odpowiedzi immunologicznej.
Dawkowanie
Szczepionka Cervarix jest
przeznaczona do stosowania
u kobiet i dziewcząt powyżej
10 roku życia.
Łącznie są podane trzy dawki
szczepionki, zgodnie z
poniższym schematem:
Pierwsza dawka: w dowolnie
wybranym terminie
Druga dawka: 1 miesiąc po
pierwszej dawce
Trzecia dawka: 6 miesięcy po
pierwszej dawce

Szczepionki
szczepionki żywe (zawierają żywe drobnoustroje),
czego przykładem jest doustna szczepionka
przeciw poliomyelitis (OPV), szczepionka przeciw
odrze, śwince i różyczce (MMR),
szczepionki zabite/inaktywowane (zawierają zabite
drobnoustroje), np. pełnokomórkowa składowa
krztuścow,
szczepionki rekombinowane (zawierają antygeny
otrzymane metodami inżynierii genetycznej),
toksoidy/anatoksyny (zawierają produkty
metabolizmu komórek bakteryjnych),
szczepionki podjednostkowe (zawierają rozbite
drobnoustroje lub ich fragmenty);

Zasady wykonywania
szczepień
Nie wykonuje się szczepień żywymi i zabitymi szczepionkami
w (zgodnie z zaleceniami WHO):
ostrych stanach chorobowych
zaostrzeniu przewlekłego procesu chorobowego
Szczepienia powinny być odroczone do momentu ustąpienia
ostrych objawów chorobowych a w chorobach przewlekłych
niezwłocznie podjęte w okresie stabilizacji przewlekłego procesu
chorobowego.
Stosowanie szczepień ochronnych u chorych z zaburzeniami
odporności jest ograniczone ze względu na możliwość wystąpienia
powikłań poszczepiennych wywołanych przez żywe szczepionki.
Częstą przyczyną niepowodzeń w profilaktyce chorób zakaźnych
jest także, wynikająca z zaburzeń immunologicznych,
niewystarczająca odpowiedź na szczepienia lub jej brak.

Stany przebiegające z ciężkimi
zaburzeniami odporności, będące
przeciwwskazaniem do stosowania żywych
szczepionek:
ciężkie wrodzone i nabyte
niedobory odporności
białaczka
chłoniaki
uogólniony proces
nowotworowy
terapia lekami o działaniu
alkilującym,
antymetabolicznym,
radioterapia oraz wysokie
dawki sterydów
przeszczepy szpiku
transplantacje narządów

Stan zaburzonej odporności a
bezpieczeństwo stosowania żywych
szczepionek
Żywa szczepionka
Ciężkie wrodzone i
nabyte zaburzenia
odporności
przeciwwskazana
Zakażenie wirusem
HIV
z ograniczeniem
Niewielkie,
izolowane wrodzone
i nabyte zaburzenia
odporności
bez ograniczeń

Szczepionki inaktywowane są w
takim samym stopniu bezpieczne w
stanach zaburzonej odporności, jak u
osób z prawidłową odpornością.
Efektywność ich jest bardzo różna w
zależności od stopnia niedoborów
odporności oraz rodzaju szczepionki.

Ocena układu odporności, która
pozwala na podjęcie decyzji
zakwalifikowania lub zwolnienia z
planowanych szczepień:
Układ odporności humoralnej:
Stężenie gównych klas immunoglobulin/ IgG, IgA, IgM.
Układ odporności komórkowej:
Odsetek i liczba bezwzględna limfocytów T
Test transformacji blastycznej
Test skórny na nadwrażliwość typu opóźnionego z
tuberkuliną,antygenami bakteryjnymi i grzybiczymi
Układ granulocytarny:
Odsetek i liczba bezwzględna neutrofilów.
Test NBT
Układ dopełniacza:
CH50
Kompleksy immunologiczne
Kwalifikacja do szczepień żywymi szczepionkami na
podstawie prawidłowych wyników w/w testów jest
wystarczająca.

Bibliografia
www.wikipedia.com
http://cyto.igabinet.pl
http://www.test-hpv.pl
http://www.obgmanagement.com
www.hpv.pl
http://www.szczepienia.czd.pl
http://www.google.pl/imghp?hl=pl&tab=wi
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
Wyszukiwarka
Podobne podstrony:
Infekcja HPV a rak szyjki macicy
W7 IMMUNOLOGIA INFEKCJI
Immunologia Infekcyjna Wykład
IMMUNOLOGIA INFEKCJI
W7 IMMUNOLOGIA INFEKCJI ppt
W7 IMMUNOLOGIA INFEKCJI
Czy wiêcej znaczy lepiej Rozwa¿ania immunologiczne o skutecznooeci szczepionek przeciw HPV — kopia
Perspektywy immunoprofilaktyki HPV u kobiet po 40 roku ¿ycia
SEMINARIUM IMMUNOLOGIA Prezentacja
Testy immunologiczne
Seminarium 6 Immunologia transplantacyjna farmacja 2
Cw 7 IMMUNOLOGIA TRANSPLANTACYJNA
Immunologia nowotworów
więcej podobnych podstron