|
Wydział Elektroniki Politechniki Wrocławskiej
|
Laboratorium Fizyki ogólnej |
||
Wykonał Sowa Mariusz
|
Grupa 6 |
Ćw. nr 25 |
Prowadzący dr Kumala |
|
Temat : Wyznaczanie ciepła topnienia lodu
|
Data wykonania 20.03.2001 |
Data oddania 27.03.2001 |
Ocena
|
|
Cel ćwiczenia:
Zapoznanie się z techniką pomiarów kalometrycznych oraz ocena dokładności tych pomiarów.
Wiadomości wstępne:
Mierzeniem ilości ciepła zajmuje się dział nauki zwany kalorymetrią. Kalorymetria opiera się na kilku zasadach, które można wyrazić następująco:
![]()
- ilość ciepła ![]()
oddana przez ciało badane jest równa ilości ciepła ![]()
pobranej przez ciała otaczające;
- ilość ciepła pobrana przez ciało podczas ogrzewania jest równa ilości ciepła oddanej podczas ostygania w tym samym zakresie temperatur jeśli ciało przechodzi w odwrotnym porządku przez te same stany pośrednie;
- ilość ciepła Q oddana bądź pobrana przez ciało jednorodne jest proporcjonalna do jego masy, a przy niewielkich zmianach temperatury - do przyrostu temperatury ![]()
.
Ciepłem topnienia nazywamy ilość ciepła potrzebną do zamiany 1 kg ciała stałego ![]()
o temperaturze topnienia na ciecz o tej samej temperaturze.
Ilość ciepła Q potrzebna do stopienia masy m ciała o temperaturze topnienia wyraża się wzorem ![]()
, gdzie ![]()
- ciepło topnienia.
Temperatura topnienia T zależy od ciśnienia, przy którym zachodzi przemiana ciała stałego
w ciecz. Ciepło topnienia lodu wyznaczymy z bilansu cieplnego dla procesu stopienia pewnej ilości lodu w kalorymetrze wodnym. Ciepła potrzebnego do stopienia lodu ΔQ1 oraz ogrzania
powstałej z niego wody ΔQ2 dostarczają woda zawarta w naczyniu kalorymetrycznym ΔQ3, naczynie kalorymetryczne wraz z mieszadłem ΔQ4 oraz zanurzona część termometru ΔQ5
- którą w tym przypadku pomijamy Według równania bilansu cieplnego mamy więc zależność ![]()
ΔQ1 + ΔQ2 = ΔQ3 + ΔQ4 + ΔQ5
Podstawiając odpowiednie wartości do powyższego wzoru otrzymujemy następujące równanie:
cxml + cwml (Tk - Tt) = cwmw (Tw - Tk) + ckmk (Tw - Tk)
z którego znajdujemy szukane ciepło topnienia lodu:
![]()
gdzie: cx - ciepło topnienia lodu
ml - masa lodu
cw - ciepło właściwe wody
mw - masa wody (przed wrzuceniem lodu)
ck - ciepło właściwe naczynia kalorymetrycznego
mk - masa naczynia kalorymetrycznego wraz z mieszadłem
Tw - temperatura początkowa wody w kalorymetrze
Tk - temperatura końcowa układu
Tt - 273,15 K - temperatura topnienia lodu
Część doświadczalna (pomiary wykonano 3x):
Kalorymetr wodny:
- Po zważeniu na wadze laboratoryjnej pustego suchego naczynia kalorymetrycznego wraz
z mieszadłem, napełniono 2/3 obj. wodą i ponownie zważono.
- Po wstawieniu naczynia do kalorymetru i zanurzeniu termometru, przez ok. 5min odczytywano temperaturę.
POMIAR 1
czas[min] |
temp.[C] |
0 |
33,5 |
1 |
33,3 |
2 |
33,2 |
3 |
33,0 |
4 |
32,9 |
5 |
32,8 |
- Po otworzeniu kalorymetru, wrzuceniu lodu (1/4 obj.), mieszając wodę odczytywano temperaturę co 1015s.
czas[s] |
temp.[C] |
0'00'' |
25,0 |
15” |
22,1 |
30” |
20,4 |
45” |
19,4 |
1'00” |
18,5 |
1'15” |
17,9 |
1'30” |
17,4 |
1'45” |
16,4 |
2'00” |
16,2 |
2'15” |
15,8 |
2'30” |
15,6 |
2'45” |
15,4 |
3'00” |
15,2 |
3'15” |
15,0 |
3'30'' |
14.6 |
4'00'' |
13,7 |
4'15'' |
14,2 |
4'30'' |
14,4 |
5'15'' |
14,8 |
5'30' |
15,0 |
6'15'' |
15.2 |
7'00'' |
15.4 |
7'45” |
15,6 |
10'45” |
15,8 |
- Zważono naczynie kalorymetryczne.
masa naczynia |
89,9 g |
masa naczynia z wodą |
285,7 g |
masa wody |
195,8 |
masa naczynia z wodą+lód |
326,2 g |
masa lodu |
40,5 |
POMIAR 2
czas[min] |
temp.[C] |
0 |
33 |
1 |
32,8 |
2 |
32,7 |
3 |
32,6 |
4 |
32,5 |
5 |
32,5 |
- Po otworzeniu kalorymetru, wrzuceniu lodu (1/4 obj.), mieszając wodę odczytywano temperaturę co 1015s.
czas[s] |
temp.[C] |
0 |
31,5 |
10” |
30,0 |
20” |
29,0 |
30” |
27,1 |
40” |
25,6 |
1'00” |
24,,8 |
1'10” |
24,3 |
1'20” |
24,2 |
3'00” |
24,2 |
4'00” |
24,2 |
5'00” |
24,3 |
6'00” |
24,3 |
7'00” |
24,3 |
8'00” |
24,4 |
10'00” |
24,5 |
- Zważono naczynie kalorymetryczne.
masa naczynia |
89,9 g |
masa naczynia z woda |
259,8 g |
masa wody |
169,9 |
masa naczynia z wodą+lód |
326,2 |
masa lodu |
66,4 |
POMIAR 3
czas[min] |
temp.[C] |
0 |
30 |
0,5 |
29,6 |
1 |
29,5 |
1,5 |
29,4 |
2 |
29,4 |
- Po otworzeniu kalorymetru, wrzuceniu lodu (1/4 obj.), mieszając wodę odczytywano temperaturę co 1015s.
czas[s] |
temp.[C] |
0 |
29,3 |
10” |
28 |
20” |
24,7 |
30” |
23,8 |
40” |
23,4 |
50” |
22,6 |
1'00'' |
22,5 |
1'10” |
22,4 |
1'20” |
22,3 |
1'30” |
22,2 |
1'40” |
22,1 |
1'50” |
22,1 |
2'00” |
22,1 |
3'00'' |
22,0 |
4'00'' |
22,1 |
5'00” |
22,2 |
6'00” |
22,3 |
9'00'' |
22,4 |
- Zważono naczynie kalorymetryczne.
masa naczynia |
89,9 |
masa naczynia z woda |
236,8 |
masa wody |
146,9 |
masa naczynia z wodą+lód |
249,7 |
masa lodu |
12,9 |
Część obliczeniowa :
Wartości stałe:
CX ciepło topnienia lodu
mL masa lodu
CW ciepło właściwe wody
mW masa wody w kalorymetrze
CK ciepło właściwe kalorymetru
mK masa kalorymetru z mieszadełkiem
TW temperatura początkowa wody w kalorymetrze
TK temperatura końcową układu
TT temperatura topnienia lodu równa 273.15 K =0,00 °C
Wyznaczenie ciepła topnienia lodu z równania bilansu cieplnego:
Po podstawieniach:
![]()
![]()
![]()
![]()
Otrzymałem:
![]()
Teraz mogę wyliczyć ciepło topnienia lodu Cx :
![]()
Błąd Cx obliczę z różniczki zupełnej:
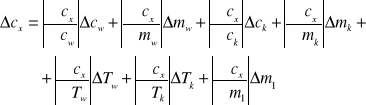
Wartości jakie przyjąłem do obliczeń:
mL = 0,0129 kg mL = 0.0001 kg
CW= 4185 J/kg K CW = 8 J/kg K
mW = 0,01469 kg mW = 0.0001 kg
CK = 879 J/kg K CK = 1 J/kg K
mK = 0,0899 kg mK = 0.0001 kg
TW = 302,45 K TW = 0.1 K
TK = 295,15 K TK = 0.1 K
Tt = 273.15 K
Z obliczeń:
Cx = 320 541.7584 J/kg
Cx = 12 453.92341 J/kg
Ostatecznie Cx=(320 500 +-12 500) J/kg
Błąd względny : ![]()
Wnioski :
Celem ćwiczenia było zmierzenie ciepła topnienia lodu. Pomiary dały wynik 320500 J/kg. Wartość ciepła topnienia podawana w tablicach fizycznych wynosi 340000 J/kg. Błąd bezwzględny wyniku to 12453 J/kg co jest sporą wartością, lecz jako błąd względny daje ostatecznie 3.88 %
Na kształt charakterystyk ma wpływ bezwładność cieplna wszystkich elementów biorących udział praktycznie w wymianie ciepła, wiec : kalorymetr, woda, mieszadełko kalorymetru, powietrze w kalorymetrze i poza nim, stół na którym stal kalorymetr. Największy wpływ na zaokrąglenie charakterystyki miały czynniki bezpośrednio stykające się z lodem. Pomiar ciepła topnienia lodu był pośredni (nie można zmierzyć tego bezpośrednio - należy wyliczyć ze wzoru). W związku z tym, że wzór był dość rozbudowany i składał się z wielu zmiennych. Na błąd pomiaru wpływało wiele czynników takich jak :
dokładność pomiaru mas (kalorymetru, kalorymetru z woda, kolorymetru z wodą i lodem)
dokładność pomiaru temperatury w rożnych chwilach
Spośród tych rożnych przyczyn największy wpływ na błąd miały : dokładność pomiaru temperatury końcowej całego układu i dokładność pomiaru temperatury początkowej wody w kalorymetrze. Generalnie na błędy najbardziej wpłyną pomiar temperatury.
Aby podać wynik z większą dokładnością należało by dokonać dokładniejszych pomiarów temperatury, gdyż to ona właśnie w największym stopniu wpływa na błąd pomiarów i obliczeń
7
ciepło właściwe wody Cw=
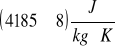
termometru
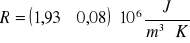
ciepło właściwe kalorymetru: aluminiowego
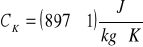
Wyszukiwarka
Podobne podstrony:
Mech- Wyznaczanie ciepła topnienia lodu(1), Sprawozdania - Fizyka
Wyznaczanie ciepła topnienia lodu, Emilia Wieteska
spraw, 24, Wyznaczanie ciepla topnienia lodu
Mech- Wyznaczanie ciepła topnienia lodu, Sprawozdania - Fizyka
wyznaczanie ciepła topnienia lodu
fizyka, Ciepło topnienia lodu 2 (inne spr.), Temat ćwiczenia nr 32:Wyznaczanie ciepła topnienia lodu
Wyznaczanie ciepła topnienia lodu ćw nr 11, PWSZ Krosno budownictwo, Fizyka
WYZNACZANIE CIEPLA TOPNIENIA LODU, Sprawozdania
C1- Wyznaczanie ciepła topnienia lodu przy pomocy kalorymetru. sprawozdanie, Sprawozdania
Wyznaczanie ciepła topnienia lodu przy pomocy kalorymetru, Studia, Pracownie, I pracownia
Wyznaczanie ciepła topnienia lodu, topnienie lodu
C1 - Wyznaczanie ciepła topnienia lodu metoda kalorymetryczn, Sprawozdania
wyznaczanie ciepła topnienia lodu, Sprawozdania
wyznaczanie ciepla topnienia lodu, Budownictwo PG, Semestr 2, Fizyka, Laborki Fizyka, Laborki - chom
Wyznaczanie ciepła topnienia lodu, Sprawozdania - Fizyka
Wzyanczanie ciepła topnienia lodu przy pomocy kalorymetru, Studia, Pracownie, I pracownia, 27 Wyznac
spr od diany wyznaczanie ciepla topnienia lodu, biologia uj, biologia II, fizyka
więcej podobnych podstron