
Numer ćwiczenia:
6
Dział analizy i temat ćwiczenia:
Sporządzanie i mianowanie
roztworu Na
2
S
2
O
3
o stężeniu
0,1mol/L
Data wykonania ćwiczenia:
14.04.2014
Data oddania sprawozdania:
28.04.2014
Grupa i sala:
Imię i nazwisko:
Nazwisko sprawdzającego:
Uwagi:
Ocena:

I WSTĘP TEORETYCZNY:
Tiosiarczanu sodu nie wolno traktować jako substancji wzorcowej. Składa się na to
kilka czynników. Po pierwsze tiosiarczan jako hydrat nie zachowuje takiej samej ilości wody
hydratacyjnej, odpowiadającej tej we wzorze. Po drugie wpływ na stężenie tiosiarczanu mają
bakterie zawarte w roztworze i reakcja tiosiarczanu z kwasem węglowym znajdującym się w
wodzie. Po trzecie miano roztworu zmienia się, dlatego należy go mianować dopiero po
upływie ok. dwóch tygodni od sporządzenia. Jeżeli w roztworze pojawi się osad należy go
przesączyć za pomocą lejka Buchnera.
Mianowanie tiosiarczanu zalicza się do metod jodometrycznych. Tiosiarczan ma za
zadanie odmiareczkować wydzielający się w reakcji jod wg równania:
Wskaźnikiem stosowanym w jodometrii jest skrobia, która z jodem tworzy związek koloru
granatowego. Metody jodometryczne mają bardzo szerokie zastosowanie, ze względu na
dokładność ustalenia punktu końcowego miareczkowania, który przeprowadzonym
doświadczeniu objawiał się odbarwieniem roztworu po jednej kropli.
Tiosiarczan można zmianować za pomocą kilku substancji wzorcowych. W tym
doświadczeniu użyto do tego celu przygotowanego wcześniej roztworu KBrO3 o stężeniu
0,0166mol/L. Przebieg doświadczenia opisany zostanie w punkcie II.
II CZĘŚĆ DOŚWIADCZALNA:
1. Stosowane odczynniki, szkło, przyrządy laboratoryjne:
a) Przygotowany ok. 2 tygodni wcześniej Na
2
S
2
O
3
b) przygotowany tydzień wcześniej KBrO
3
c) 3x kolba stożkowana zamykana doszlifowanym korkiem
d) Woda destylowana
e) 6x naczynka wagowe
f) Stały KBr
g) Stały KI
h) Roztwór HCl (c=2mol/L)
i) Skrobia
j) Biureta
k) Statyw
l) Lejek

2. Przebieg doświadczenia:
Sporządzanie roztworu tiosiarczanu:
Na wadze technicznej odważono w naczynku wagowym 12,52g stałego
hydratu tiosiarczanu. Następnie przeniesiono ilościowo do kolby o pojemności
0,5L, rozpuszczono i uzupełniono woda destylowaną do kreski. Otrzymany
roztwór przelano do ciemnej butelki, Zakręcono, odpowiednio opisano i
pozostawiono w szafce na okres dwóch tygodni.
Mianowanie roztworu:
Przygotowano 3 odważki KBr (po ok. 0,5g każda) i 3 odważki KI (po ok. 2g
każda) i zważono je w naczynkach wagowych na wadze technicznej. Następnie do
każdej z trzech kolb stożkowych za pomocą kalibrowanej pipety 25mL
przeniesiono porcję mianowanego roztworu KBrO
3
i rozcieńczono woda
destylowaną do objętości ok. 50mL. Następnie do każdej z kolb przeniesiono
ilościowo za pomocą lejka po jednej odważce KBr i jednej odważce KI. Do kolb
dodano za pomocą cylindra miarowego po ok. 15mL HCl (c=2mol/L). Kolby
zamknięto doszlifowanym korkiem tak szybko by jak najbardziej ograniczyć
kontakt roztworu z powietrzem. Roztwory wymieszano i odstawiono na ok. 5min.
W tym czasie przygotowano biuretę na stojaku. Przemyto ją trzykrotnie niewielką
ilością wody destylowanej, a następnie trzykrotnie niewielką ilością roztworu
tiosiarczanu. Następnie biureta została napełniona roztworem tiosiarczanu do zera
tak by menisk dolny dotykał kreski. Następnie wydzielający się jod w kolbach
mianowano roztworem tiosiarczanu, dodając pod koniec miareczkowania (kiedy
roztwór miał kolor słomkowy) skrobi. Wyniki miareczkowania zestawiono w
tabeli (1).
III OPRACOWANIE DANYCH:
Tabela 1
Nr
Masa naczynka [g]
Masa naczynka
z odważką [g]
Masa odważki
[g]
Objętość
Na
2
S
2
O
3
[mL]
KBr
KI
KBr
KI
KBr
KI
1
15,72
15,47
16,34
17,45
0,62
1,98
24,5
2
15,72
15,48
16,29
17,63
0,57
2,15
24,4
3
7,76
7,70
8,29
9,50
0,53
1,80
24,5
Z trzech otrzymanych wyników obliczono średnią arytmetyczną.

Stężenie Na
2
S
2
O
3
obliczono ze wzoru (2):
[mol/L]
(2)
gdzie:
– objętość bromianu(V) potasu [mL]
– stężenie bromianu(V) potasu [mL/L]
- objętość tiosiarczanu [mL]
[mol/L]
NIEPEWNOŚĆ POMIARU
Niepewność pomiaru liczy się wg wzoru:
(
)
√(
̅̅̅̅̅̅̅̅̅̅̅
)
(
)
(
)
Niepewności związane z roztworem Na
2
S
2
O
3:
Pomiar objętości titranta (roztwór Na
2
S
2
O
3
):
- niepewność kalibracji biurety (0,1 mL)
- niepewność kropli (0,05 mL)
- niepewność odczytu (0,05 mL)
- poprawka temperaturowa objętości szkła (0,0025 mL)
u
1
(V) = 0,1 mL /
√ = 0,058 mL
u
2
(V) = 0,05 mL /
√ = 0,029 mL
u
3
(V) = 0,05 mL /
√ = 0,029 mL
Niepewność systematyczną objętości u(V)
syst
obliczono ze wzoru:
√
√
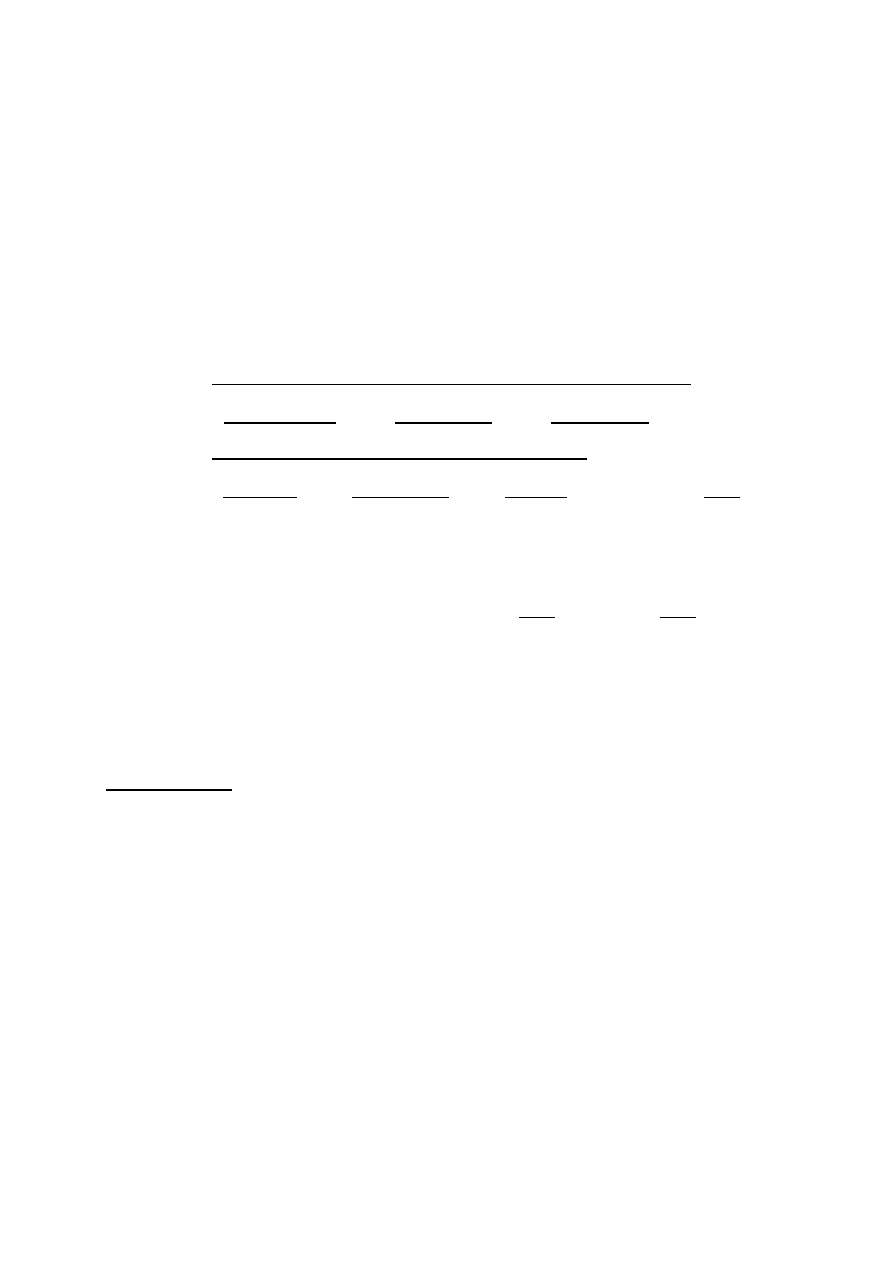
Niepewności związane z roztworem KBrO3:
(Dane zaczerpnięte ze sprawozdania numer 5)
Niepewność stężenia tiosiarczanu sodu:
(
)
√(
(
̅̅̅̅̅̅̅̅̅̅̅)
)
(
(
)
)
(
(
)
)
√(
)
(
)
(
)
[
]
Niepewność rozszerzona k=2:
(
) [
]
Wynik:
IV WNIOSKI
Przygotowana odważka miała masę 12,52g, dlatego teoretycznie stężenie roztworu
powinno wynieść 0,1000mol/L. Otrzymane stężenie różni się od zadanego o 0,018mol/L i nie
mieści się w granicach wyznaczonego błędu. Wykracza jednak poza przedział niepewności
niewiele. Przyczyną może być nietrwałość związku jakim jest tiosiarczan. Rozszerzona
niepewność stanowi ok. 1,47% wyniku.
Wyszukiwarka
Podobne podstrony:
Tiosiarczan sodu - odtrutka (prawie) na wszystko, + TWOJE ZDROWIE -LECZ SIE MĄDRZE -tu pobierasz bez
Mianowanie roztworu tiosiarczanu sodu
10 Tiosiarczan sodu zastosowanie
Sodu tiosiarczan 5 hydrat techn
Sodu tiosiarczan 5 hydrat
Sodu tiosiarczan?zw czda
Sodu tiosiarczan?zwodny
Sodu tiosiarczan 5×hydrat czda
Sodu tiosiarczan 0,1 N odważka
p toluenosulfonian sodu
03 0000 034 02 Leczenie immunosupresyjne mykofenolanem mofetylu lub mykofenolanem sodu
istan Wodorotlenek sodu, BHP, Instrukcje-Stanowiskowe
Sodu wodorotlenek 0,5 r r mianowany
Sodu fluorek cz
Sodu chlorek
Sodu pirogronian
więcej podobnych podstron