
Acta Haematologica Polonica 2009, 40, Nr 2, str. 305–311
PRACA POGLĄDOWA – Review Article
WIESŁAW WIKTOR JĘDRZEJCZAK
Aktualne wskazania do przeszczepiania krwiotwórczych
komórek macierzystych
Current indications for the transplantation of hematopoietic stem
cells
Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawskiego Uniwersytetu
Medycznego w Warszawie
Kierownik: Prof. dr hab. med. Wiesław W. Jędrzejczak
STRESZCZENIE
Wskazania do przeszczepiania komórek krwiotwórczych ulegają stopniowej ewolucji. Rozsze-
rzenie wskazań wynika z wprowadzenia nowych form zabiegu takich, jak przeszczepianie po
kondycjonowaniu niemieloablacyjnym, lepszego doboru dawców niespokrewnionych, a także
wykorzystywania nowych źródeł komórek krwiotwórczych takich, jak krew pępowinowa oraz
dawcy haploidentyczni. Zmniejszenie śmiertelności związanej z przeszczepieniem umożliwia też
rozszerzenie wskazań na schorzenia występujące głownie u osób starszych takie, jak przewlekła
białaczka limfocytowa i mielofibroza. Z drugiej strony, wprowadzenie skutecznych terapii far-
makologicznych (np. imatinib w przewlekłej białaczce szpikowej i zespole hypereozynofilo-
wym) ogranicza wskazania do przeszczepiania komórek krwiotwórczych, jako metody znacznie
bardziej toksycznej. Te dane zostały wykorzystane w przygotowaniu zaproponowanej zmodyfi-
kowanej tabeli wskazań zgodnej z wiedzą z roku 2009.
SŁOWA KLUCZOWE: Przeszczepianie szpiku – Ostre białaczki – Przewlekłe białaczki – Choroby
komórek plazmatycznych
SUMMARY
Indications for transplantation of hematopoietic cells undergo constant evolution. Some indica-
tions become broadened owing to the introduction of new forms of procedures such as transplan-
tation after non-myeloablative conditioning, better tissue matching, and utilization of newer
forms of sources of hematopoietic cells such as cord blood and haploidentical donors. Decrease
in transplantation related mortality has allowed for broadening of indications to include disorders
of elderly such as chronic lymphocytic leukemia and myelofibrosis. On the other hand, introduc-
tion of effective pharmacological therapies (e.g. imatinib in chronic myeloid leukemia and hy-
pereosinophilic syndrome) limited indications to the transplantation of hematopoietic cells as
much more toxic method. These data have been used in preparation of proposal of modified indi-
cation table according to the state of the art for 2009.
KEY WORDS: Bone marrow transplantation – Acute leukemia – Chronic leukemia – Plasma cell
disorders

W.W. JĘDRZEJCZAK
306
Wskazania do przeszczepiania krwiotwórczych komórek macierzystych ulegają
stałej ewolucji. Wynika to zarówno z rozwoju samego przeszczepiania, jak i rozwoju
metod alternatywnych. Od kilku lat [8], jako wykładnię aktualnych wskazań do prze-
szczepiania komórek krwiotwórczych przyjmuje się wskazania opracowane przez Eu-
ropejską Grupę ds. Przeszczepiania Krwi i Szpiku (EBMT). Są one sukcesywnie aktu-
alizowane i ostatnie wersje tych dokumentów pochodzą z lat 2006 i 2008 [1, 10, 11].
Muszą one jednak być nieco skorygowane w oparciu o inne piśmiennictwo przede
wszystkim dlatego, że nie obejmują oddzielnych wskazań do przeszczepień po kondy-
cjonowaniu niemieloablacyjnym, które jest największą nowością ostatnich lat [3, 4, 9],
a także zwiększania się znaczenia krwi pępowinowej [1, 13, 14], jako źródła komórek
krwiotwórczych, w tym przeszczepiania jednocześnie krwi od więcej niż jednego daw-
cy [2, 15].
EBMT [1, 10, 11] rozróżnia dla celów wskazań trzy rodzaje przeszczepień krwio-
twórczych (HT) zależnie od tego, kto jest dawcą. Są to:
1.
przeszczepienie autologiczne (AutoHT),
2.
przeszczepienie allogeniczne od rodzeństwa identycznego w HLA (ID-alloHT)
3.
przeszczepienie allogeniczne od dawcy niespokrewnionego (MUD-alloHT).
Z kolei w Polsce ze względów finansowych, zamiast tej trzeciej kategorii wyróż-
niamy przeszczepienie od dawcy alternatywnego (Alt-alloHT), którym jest albo dawca
niespokrewniony zgodny w co najmniej w 9 spośród 10 dobieranych antygenów HLA
albo dawca rodzinny częściowo niezgodny w HLA. Tak będzie to również omawiane
w obecnym opracowaniu i jest to jedynie niewielka modyfikacja dokumentu EBMT.
Jak wiadomo, w każdej z tych sytuacji komórki przeszczepiane mogą pochodzić ze
szpiku, krwi obwodowej i krwi pępowinowej. Istnieją tu więc różne standardowe wy-
mogi dotyczące zgodności.
1.
Dawca rodzinny szpiku lub krwi obwodowej: najlepiej zgodny w 6/6 antygenów
HLA (loci A, B, DR). Dopuszczalna niezgodność w 1 locus, czyli zgodność 5/6.
2.
Niespokrewniony dawca szpiku lub krwi obwodowej: najlepiej zgodny w 10/10
antygenów HLA w typowaniu wysokiej rozdzielczości (loci A, B, C, DR i DQ).
Dopuszczalna niezgodność w 1 locus, czyli zgodność w 9/10, wyjątkowo niezgod-
ność w 2 loci, czyli zgodność 8/10.
3.
Niespokrewniony dawca krwi pępowinowej: zgodność w zakresie 6/6-4/6 antyge-
nów HLA (loci A, B i DR), czyli standardowo dopuszczona niezgodność w 2 spo-
ś
ród 6 badanych loci. W tym zakresie zgodności nie ma większych różnic jeśli cho-
dzi o wyniki przeszczepiania, które zależą bardziej od liczby przeszczepionych ko-
mórek niż od ich zgodności.
Dla potrzeb obecnego opracowania wprowadzono jako oddzielną kategorię prze-
szczepienie allogeniczne po kondycjonowaniu niemieloablacyjnym, przy czym dla tej
kategorii nie rozdzielono tu dawców rodzinnych identycznych w HLA i pozostałych
identycznych w HLA i wskazania dotyczą tylko takich dawców. Warto tu podkreślić,
ż
e w związku z rozwojem metod typowania tkankowego, wprowadzeniem metod wy-
sokiej rozdzielczości i w związku z coraz lepszym doborem dawców wyniki prze-
Aktualne wskazania do przeszczepiania
307
szczepiania od dawców rodzinnych i dawców niespokrewnionych stają się coraz bar-
dziej zbliżone [1].
Wreszcie, ostatnio pojawiła się nowa forma przeszczepień allogenicznych wyko-
rzystywana u dorosłych. Jest to forma wcześniej wprowadzona u dzieci i polega na
wykorzystaniu megadawek komórek krwiotwórczych pochodzących od dawców ha-
ploidentycznych i poddanych zabiegowi pozaustrojowego usuwania komórek T [5].
Dla tej formy nie ma jeszcze ustalonych wskazań i zabiegi te dotyczą najczęściej cho-
rych, którzy nie mają innych opcji leczniczych tj. chorych na ostre białaczki bez remi-
sji. W związku z tym nie będzie ona dalej omawiana. Warto tu jeszcze zwrócić uwagę,
ż
e pewnym standardem stało się wybieranie do wstępnych prób klinicznych nowych
metod przeszczepiania komórek krwiotwórczych wspomnianej kategorii chorych na
oporne ostre białaczki (pod warunkiem, że są jeszcze w dobrym stanie ogólnym). Ro-
kowanie tych chorych jest bardzo złe, w związku z czym zaproponowanie im wypró-
bowania nowej metody stwarza choćby teoretyczne szanse przy minimalnym ryzyku.
Wiek jest podstawową kategorią rozważaną podczas decyzji o wykonaniu HT.
Standardowe limity wieku są następujące:
1. autoHT: 65 lat
2. ID-alloHT: 55 lat;
3. Alt-alloHT: 45 lat.
Jednakże, trzeba pamiętać, że w ciągu ostatnich 15 lat te limity przesunęły się w
górę o lat 20. Obecnie, większą wagę przykłada się do wieku biologicznego i stanu
ogólnego niż do wieku metrykalnego i dla osób w bardzo dobrym stanie ogólnym do
tych limitów można dodać około 5 lat. Co więcej, te limity dotyczą klasycznych form
zabiegów po kondycjonowaniu mieloablacyjnym. Przeszczepienia po kondycjonowa-
niu niemieloablacyjnym wykonuje się do 65 roku życia, przy czym dotyczy to zabie-
gów z wykorzystaniem dawców szpiku lub krwi obwodowej identycznych w HLA, bez
rozdzielenia na to, czy są to dawcy rodzinni, czy niespokrewnieni. Przed laty Gratwohl
i wsp. [7] zaproponowali też wskaźnik ryzyka przeszczepienia, który obecnie zwany
jest wskaźnikiem Gratwohla lub wskaźnikiem EBMT i lepiej niż sam wiek określa
szanse powodzenia zabiegu w konkretnej sytuacji klinicznej. Przydatność tego wskaź-
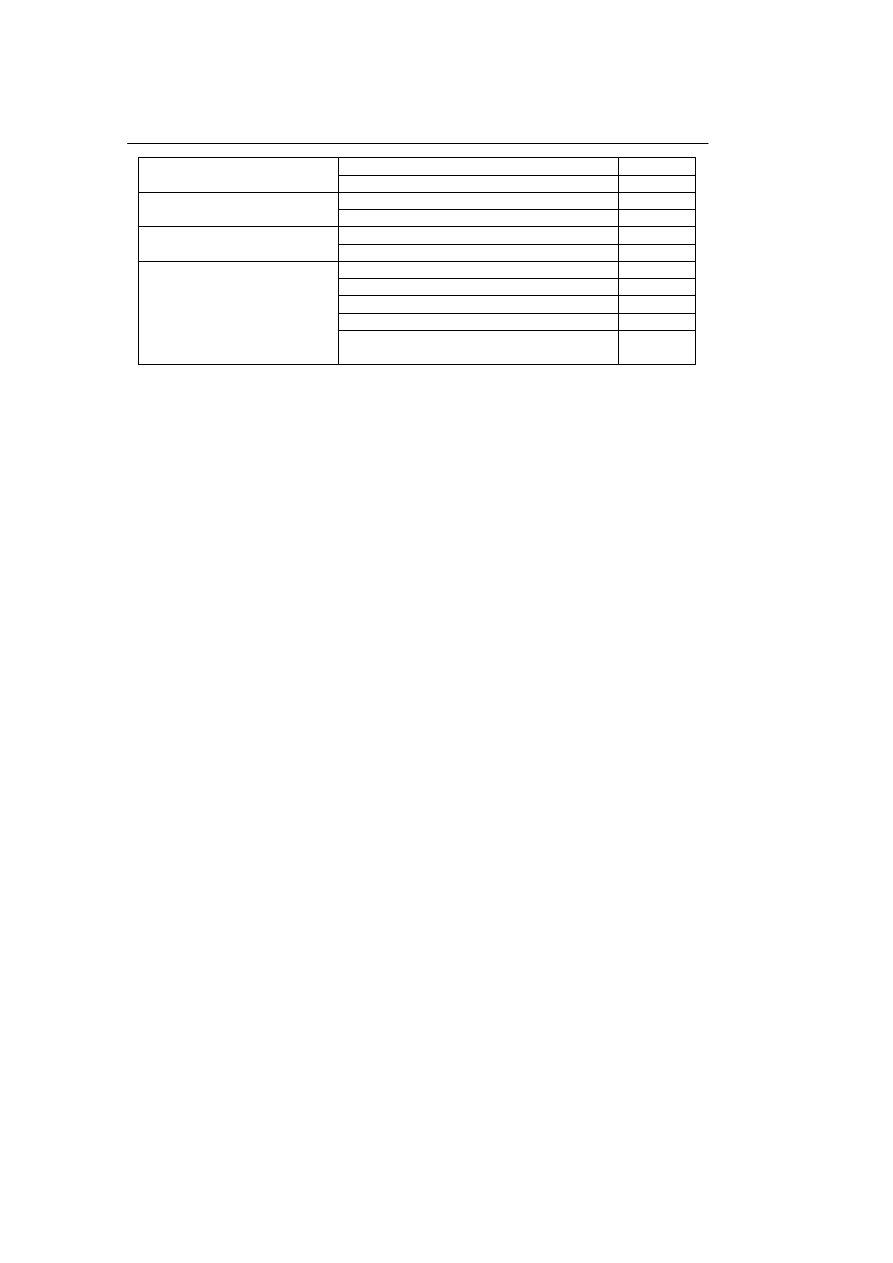
nika została niezależnie potwierdzona. Punktacja poszczególnych parametrów jest
podana w Tabeli 1. Chorzy, którzy mają 0–2 punktów mają niskie ryzyko przeszcze-
powe, chorzy z 3–4 punktami pośrednie ryzyko przeszczepowe, a chorzy, którzy uzy-
skają powyżej 4 punktów wysokie ryzyko przeszczepowe.
Tabela 1. Obliczanie wskaźnika ryzyka przeszczepienia wg Gratwohla i wsp.
Kryterium
Podgrupa
Punktacja
Wczesny
0
Pośredni
1
Stopień zaawansowania choroby
późny
2
<20 l
0
20-40 lat
1
Wiek chorego
>40 lat
2
W.W. JĘDRZEJCZAK
308
<12 mies.
0
Czas od rozpoznania do prze-
szczepienia
>12 mies.
1
Rodzeństwo identyczne w HLA
0
Zgodność tkankowa
Inny dawca
1
Inna niż poniżej
0
Płeć dawcy a płeć biorcy
Dawca kobieta dla mężczyzny
1
Karnofsky <80 lub schorzenia towarzyszące
+1
Dawca powyżej 50 lat
+1
Cytomegalia nie –/–
+1
Bliźnięta jednojajowe
-1
Inne parametry
Dawca niespokrewniony zgodny 10/10 w wyso-
kiej rozdzielczości
-1
Rodzaje wskazań:
EBMT wyróżnia cztery rodzaje wskazań do HT [1, 10, 11]:
1.
Rutynowe (R od „routine”) również określane jako standardowe (S od „standard of
care”): sytuacja, kiedy wykonanie przeszczepienia jest składową rutynowego postę-
powania leczniczego w danej sytuacji;
2.
Opcja kliniczna (CO: od „clinical option”): wskazania do przeszczepienia z nadzo-
rem badawczym: sytuacja, kiedy istnieją jeszcze pewne wątpliwości, czy przeszcze-
pienie jest z reguły najlepszym postępowaniem, ale jest postępowaniem co najmniej
równorzędnym. EBMT ma dla każdej z tych sytuacji protokół badań klinicznych i
chorzy leczeni w ośrodkach należących do EBMT powinni być zgłaszani i leczeni
zgodnie z tymi protokołami. Jest to jednak sytuacja, w której istnieje już wiele do-
wodów na to, że przeszczepienie jest w tej sytuacji leczeniem skutecznym.
3.
Rozwojowe (D od „developmental”): wskazania do przeszczepienia w warunkach
eksperymentu klinicznego: sytuacja, kiedy w grę wchodzi nowa jednostka chorobo-
wa lub nowa forma zabiegu, co do których istnieją poważne przesłanki, że będą sku-
teczne, ale dowody trzeba dopiero zgromadzić.
4.
Na ogół nierekomendowane (NR od „not generally recommended”): z reguły brak
wskazań: określa sytuacje, w których na ogół nie podejmuje się ryzyka zabiegu,
gdyż nie uzasadnia ono osiągalnych korzyści. Trzeba pamiętać, że dotyczy to tylko
zwykłych form zabiegów, gdyż możliwe jest zastosowanie innej formy zabiegu, któ-
ra okaże się skuteczna. I taka nowa forma znajdzie się wtedy kategorii rozwojowej,
czyli D.
Trzeba tu jeszcze dodać, że ostateczną decyzję o wykonaniu zabiegu zawsze po-
dejmuje kierownik ośrodka przeszczepiającego, gdyż on ponosi odpowiedzialność za
wynik zabiegu. On też decyduje o tym, czy kierowany przez niego zespół jest się w
stanie podjąć zabiegu w danej konkretnej sytuacji. I może zdyskwalifikować chorego,
który zgodnie z Tabelą mieści w kategorii ‘R”, a zakwalifikować chorego z kategorii
“NR”. W tej ostatniej sytuacji powinien jednak zgodnie z Ustawą o zawodzie lekarza
wykonywać zabieg w formule prawnej “eksperymentu leczniczego”, tj. eksperymentu
mającego na celu próbę ratowania chorego pozbawionego innej możliwości ratunku.
Aktualne wskazania do przeszczepiania
309
Ta formuła prawna wymaga uzyskania zgody odpowiedniej Komisji Bioetycznej na
wykonanie zabiegu u danego chorego.
Tabela 2. Wskazania do przeszczepienia allogenicznych komórek krwiotwórczych u chorych
dorosłych w 2009 roku według EBMT i innych źródeł
Choroba
Wiek
Stan zaawansowania
choroby
Zabieg
Auto-HT
Zabieg
ID-alloHT*
Zabieg
alt-alloHT
Zabieg
NST-HT
Ostra białaczka
szpikowa
(z wyj. M3,
inv16 i t8:21
Ogólne
zasady
CR1
CR2,3 zagraża-
jący nawrót,
Nawrót
CO
CO
NR
R
R
D
R
CO
D
Po 50. r.ż.
CO
CO
D
Ostra białaczka
szpikowa M3
Ogólne
zasady
Oporność na kwas
transretinowy i arszenik
CO
R
R
Po 50 r.ż
CO
Ostra białaczka
szpikowa z inv16
lub t8:21
Ogólne
zasady
CR2
CO
R
R
Po 50 r.ż.
CO
Ostra białaczka
limfoblastyczna
Dorośli
CR1 (wysokie ryzyko),
CR2, zagraża-
jący nawrót,
Ustalony nawrót
CO
NR
NR
R
R
D
R
R
D
Po 50 r.ż
CO
NR
Przewlekła
białaczka
szpikowa
ogólne
zasady
faza przewlekła oporna
na inhibitory kinaz
tyrozynowych
faza przyspieszona
kryza blastyczna
NR
NR
NR
R
R
D
R
CO
D
CO
CO
D
Osteomielo-
fibroza
Ogólne
zasady dla
NST-HT
Objawy kliniczne
D
CO
CO
CO
Inne choroby
mielopro-
liferacyjne
Ogólne
zasady
–
NR
NR
NR
NR
przewlekła
białaczka
limfocytowa
Ogólne
zasady
Oporna na analogi
puryn delecja p53
D
CO
CO
CO
Chłoniaki nieziar-
nicze:
limfoblastyczne
wysoka
złośliwość,
pośrednia
złośliwość,
niska
złośliwość
Ogólne
zasady
jak ostra b.
limfoblastyczna
CR1
CR2
CR1
Nawrót, CR2
CR1
nawrót, CR2
R
CO
R
CO
R
D
CO
CO
R
CO
CO
CO
D
CO
CO
CO
CO
CO
CO
D
CO
CO
(po 50 r.ż.)
CO
CO
CO
CO
D
CO
Chłoniak
ziarniczy
Ogólne
zasady
CR1
Nawrót, CR2,3
Oporna
NR
R
NR
NR
R/CO
D
NR
CO
D
NR
CO
D
Szpiczak mnogi
Ogólne
zasady
I stadium
pozostałe
R
R
NR
CO
NR
D
D
CO
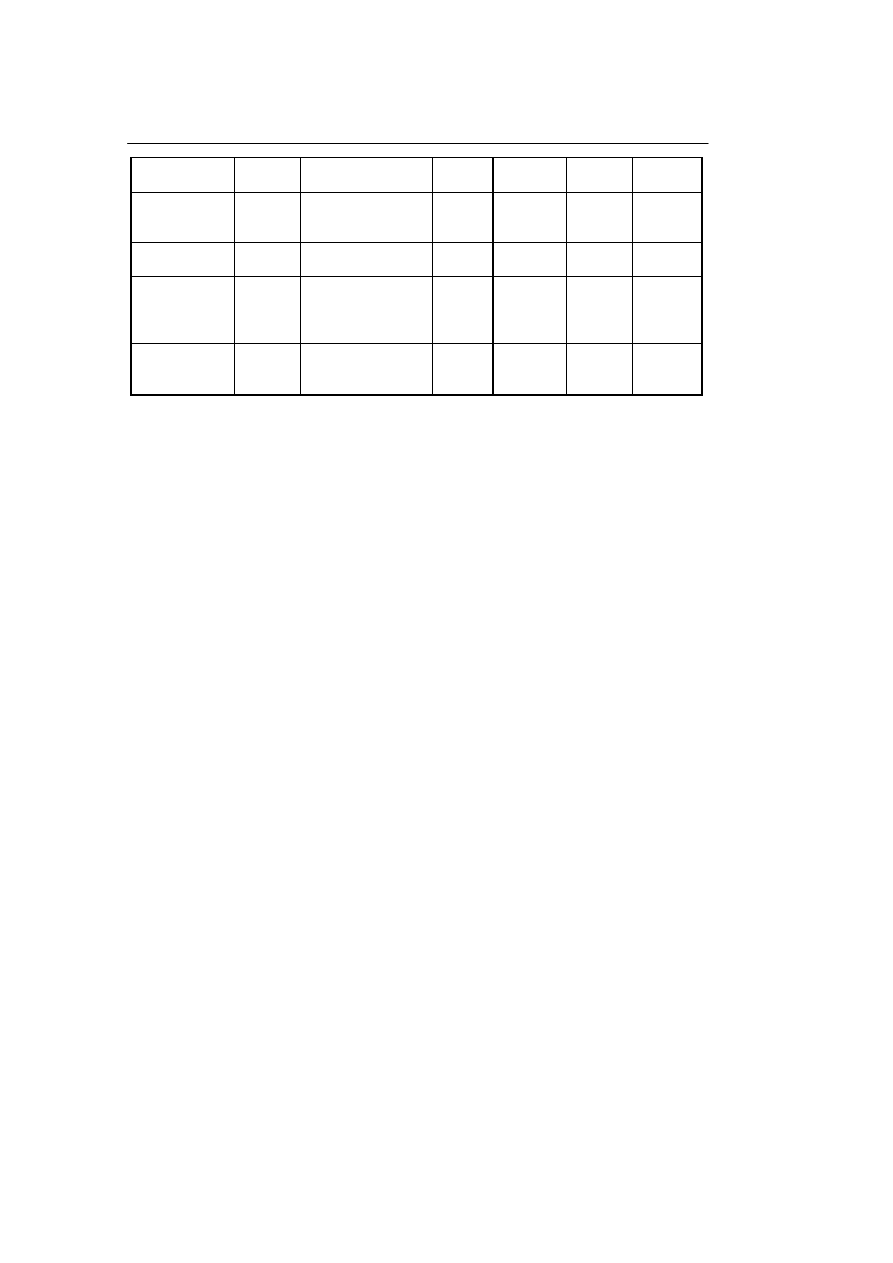
W.W. JĘDRZEJCZAK
310
Amyloidoza
Ogólne
zasady
Możliwie wcześnie po
rozpoznaniu
CO
D
D
D
MDS
Ogólne
zasady
5q- z progresją
RA, RC, RAEB
Inne
NR
NR
NR
R
R
R
R
CO
CO
CO
CO
CO
Aplazja szpiku
17-45 lat
45-60 lat
Oporna na ATG/CyA
NR
NR
R
CO
R
CO
CO
D
Choroby
autoimmuni-
zacyjne
Ogólne
zasady
Stwardnienie rozsiane,
toczeń trzewny,
twardzina uogólniona,
cukrzyca typu I
D
NR
NR
NR
Nowotwory lite
Ogólne
zasady
Rak piersi
Rak jajnika
Rak nerki
D
D
NR
NR
NR
NR
NR
NR
NR
NR
NR
D
*objaśnienia skrótów: ID-alloHT: przeszczepienie komórek krwiotwórczych od brata lub siostry identycz-
nego w HLA po kondycjonowaniu mieloablacyjnym; Alt-alloHT: przeszczepienie komórek krwiotwór-
czych od dawcy alternatywnego tj. dawcy spokrewnionego częściowo różnego w HLA lub dawcy niespo-
krewnionego identycznego w HLA po kondycjonowaniu mieloablacyjnym; NST-HT: przeszczepienie
allogenicznych komórek krwiotwórczych po kondycjonowaniu niemieloablacyjnym; CR: remisja całkowi-
ta i jej kolejny numer; R: rutynowe wskazanie do przeszczepienia; CO: wskazanie do przeszczepienia z
nadzorem badawczym; D: wskazanie do przeszczepienia w ramach eksperymentu klinicznego; NR: bez
wskazań: MDS: zespół mielodysplastyczny. RA: niedokrwistość oporna na leczenie; RC cytopenia oporna
na leczenie, RAEB: niedokrwistość oporna na leczenie z nadmiarem blastów
.
Trzeba się też zastrzec, że przedstawione w Tabeli 2 wskazania są z konieczności
uproszczone. Przykładowo: kategoria zabiegów po kondycjonowaniu niemieloablacyj-
nym jest bardzo zróżnicowana, gdyż istnieje co najmniej 30 różnych sposobów takiego
kondycjonowania różniących się zarówno rodzajem wykorzystywanych leków, jak i
ich dawkami [3, 4]. Pominięto także genetycznie uwarunkowane choroby rozpoznawa-
ne głównie u dzieci, które są wskazaniem do przeszczepień allogenicznych. Lista tych
schorzeń i innych wskazań pediatrycznych jest dostępna w innych opracowaniach [12].
PIŚMIENNICTWO
1.
Apperley JF, Carreras E, Gluckman E, Gratwohl A, Masszi T (red.): Hematopoietic Stem Cell Trans-
plantation. The EBMT Handbook. 5th Edition, EBMT-ESH, 2008
2.
Barker JN, Weisdorf DJ, DeFor TE, Blazar BR, McGlave PB, Miller JS, Verfaillie CM, Wagner JF:
Transplantation of 2 partially HLA-matched umbilical cord blood units to enhance engraftment in
adults with hematologic malignancy. Blood 2005; 105:1343-1347.
3.
Barrett AJ, Savani BN: Stem cell transplantation with reduced-intensity conditioning regimens: a
review of ten years experience with new transplant concepts and new therapeutic agents. Leukemia
2006; 20: 1661-1672.
4.
Bensinger WI: The current status of reduced-intensity allogeneic hematopoietic stem cell transplanta-
tation for multiple myeloma. Leukemia 2006; 20: 1683-2689.
5.
Dey BR, Spitzer TR: Current status of haploidentical stem cell transplantation. Br J Haematol 2006,
135: 423-37.

Aktualne wskazania do przeszczepiania
311
6.
Gratwohl A, Baldomero H, Schwendener A, Rocha V, Apperley JFrauendorfer K, Niederwieser D;
Joint Accreditation Committee of the International Society for Cellular Therapy; European Group for
Blood and Marrow Transplantation. The EBMT activity survey 2007 with focus on allogeneic HSCT
for AML and novel cellular therapies. Bone Marrow Transplant. 2009; 43: 275-91.
7.
Gratwohl A, Hermans J, Goldman JM i wsp.: Risk assessment for patients with chronic myeloid
leukemia before allogeneic blood or marrow transplantation. Chronic Leukemia Working Party of the
European Group for Blood and Marrow Transplantation. Lancet 1998; 352: 1087-109.
8.
Jędrzejczak WW: Wskazania do przeszczepiania komórek krwiotwórczych według zaleceń Europej-
skiej Grupy do Spraw Przeszczepiania Krwi i Szpiku. W: Standardy w hematologii (red. WW Ję-
drzejczak, M. Podolak-Dawidziak) Volumed, 2000, str. 165-168.
9.
Lazarus HM, Rowe JM: Reduced-intensity conditioning for acute myeloid leukemia: is this strategy
correct. Leukemia 2006; 20: 1673-1682.
10.
Ljungman P, Urbano-Ispizua A, Cavazzana-Calvo W i wsp.: Allogeneic and autologus transplanta-
tion for haematological dieseases, solid tumors, and immune disorders. Definitions and current prac-
tice in Europe. Bone Marrow Transplant 2006; 37: 439-449.
11.
Ljungman P, Gratwohl A for the European Group for Blood and Marrow Transplantation: Indications
and current practice for allogeneic and autologous HSCT for haematological diseases, solid tumors
and immune disorders. W Apperley J, Carreras E, Gluckman E, Gratwohl A, Masszi T: Haematopoi-
etic Stem Cell Transplantation. 2008 Revised 5
th
Edition. 2008, pp. 318-326
12.
Locatelli F, Giorgiani G, Di-Cesare-Merlone A, Merli P, Sparta V, Moretta F. The changing role of
stem cell transplantation in childhood. Bone Marrow Transplant 2008, 41 Suppl 2: S3-7.
13.
Rocha V, Gluckman E: Clinical use of umbilical cord blood hematopoietic stem cells. Biol Blood
Marrow Transplant. 2006; 12 Suppl 1: 34-41.
14.
Stanevsky A, Goldstein G, Nagler A. Umbilical cord blood transplantation: Pros, cons and be-
yond.Blood Rev. 2009 Mar 10. [Epub ahead of print]
15.
Wiktor-Jedrzejczak W, Rokicka M, Urbanowska E, Torosian T, Graczyk-Pol E, Tomaszewska A,
Krol M, Paluszewska M, Gronkowska A, Ziarkiewicz-Wróblewska B, Jolkowska J, Witt M: Simulta-
neous transplantation of two allogeneic units of cord blood in an adult patient with acute myeloblastic
leukemia: a case report. Arch Immunol Ther Exp 2005; 52: 364-8.
Praca wpłynęła do Redakcji 20.04.2009 r. i została zakwalifikowana do druku 30.04.2009 r.
Adres do korespondencji:
Klinika Hematologii, Onkologii i Chorób Wewnętrznych WUM w Warszawie
ul. Banacha 1a
02-097 Warszawa
Wyszukiwarka
Podobne podstrony:
Wskazań do masażu, MEDYCYNA
dr Mrowka Wskazania do usunięcia migdałków podniebiennych [06 WPK mrowka]
przeciwwskazania wskazania do zabiegów kosmetycznych, Kosmetyka
Carr Robyn Powrot do przeszlosci
WSKAZANIA DO KRIOTERAPII OGÓLNOUSTROJOWEJ
Powrót do przeszłości
Wskazania do masażu klasycznego, Masaż
wskazania do zimna, fizykoterapia
ONN I PNN, T:OSTRA NIEWYDOLNOŚĆ NEREK JAKO JEDNO ZE WSKAZAŃ DO DIALIZOTERAPII
DO TEL! Wskazania do skierowania pacjenta, genetyka
DO TEL! Wskazania do skierowania pacjenta genetyka
Wskazania do pracy z dzieckiem leworęcznym, Lewa ręka
POTOP-stosunek do przeszłści, Szkoła, Język polski, Wypracowania
Podstawowe wskazania do jonoforezy, Fizjoterapia, Fizyko
więcej podobnych podstron