
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
MINISTERSTWO EDUKACJI
NARODOWEJ
Kazimierz Olszewski
Wykonywanie podstawowych czynności laboratoryjnych
815[01].O2.01
Poradnik dla nauczyciela
Wydawca
Instytut Technologii Eksploatacji – Państwowy Instytut Badawczy
Radom 2007

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
1
Recenzenci:
dr. inż Sylwester Stawarz
mgr inż. Rafał Bator
Opracowanie redakcyjne:
mgr inż. Kazimierz Olszewski
Konsultacje:
mgr inż. Magdalena Rychlik
Poradnik stanowi obudowę dydaktyczną programu jednostki modułowej 815[01].O2.01
Wykonywanie podstawowych czynności laboratoryjnych, zawartego w modułowym
programie nauczania dla zawodu operator urządzeń przemysłu chemicznego.
Wydawca
Instytut Technologii Eksploatacji – Państwowy Instytut Badawczy, Radom 2007

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
2
SPIS TREŚCI
1.
Wprowadzenie
3
2.
Wymagania wstępne
5
3.
Cele kształcenia
6
4.
Przykładowe scenariusze zajęć
7
5.
Ćwiczenia
11
5.1.
Wyposażenie i zasady bezpiecznej pracy w laboratorium chemicznym
11
5.1.1.
Ć
wiczenia
11
5.2.
Podstawowe czynności laboratoryjne
14
5.2.1.
Ć
wiczenia
14
5.3.
Przygotowanie roztworów wodnych o określonych stężeniach
18
5.3.1.
Ć
wiczenia
18
5.4.
Rozdzielanie mieszanin jednorodnych i niejednorodnych
20
5.4.1.
Ć
wiczenia
20
6.
Ewaluacja osiągnięć ucznia
23
7.
Literatura
37

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
3
1. WPROWADZENIE
Przekazujemy Państwu Poradnik dla nauczyciela, który będzie pomocny w prowadzeniu
zajęć dydaktycznych w szkole kształcącej w zawodzie operator urządzeń przemysłu
chemicznego 815[01].
W poradniku zamieszczono:
−
wymagania wstępne,
−
wykaz umiejętności, jakie uczeń opanuje podczas zajęć,
−
przykładowe scenariusze zajęć,
−
propozycje ćwiczeń, które mają na celu ukształtowanie umiejętności praktycznych
uczniów,
−
wykaz literatury, z jakiej uczniowie mogą korzystać podczas nauki.
Wskazane jest, aby zajęcia dydaktyczne były prowadzone różnymi metodami ze
szczególnym uwzględnieniem:
−
pokazu z objaśnieniem,
−
tekstu przewodniego,
−
ć
wiczeń praktycznych.
Zajęcia powinny odbywać się w pracowni chemicznej z odpowiednim zapleczem; pokój
wagowy, podręczny magazyn odczynników chemicznych. Uczniowie powinni wykonywać
ć
wiczenia indywidualnie lub w zespołach dwuosobowych.
Z powodu obszernego materiału nauczania objętego programem jednostki modułowej
815[01].O2.01 w poradnikach zawarto tylko wybrane ćwiczenia zawarte w programie
jednostki jako najbardziej reprezentatywne dla specyfiki nauczania przedstawionych
w Materiale nauczania jednostki zagadnień.
W celu przeprowadzenia sprawdzianu wiadomości i umiejętności ucznia, nauczyciel
może posłużyć się zamieszczonym w rozdziale 6 zestawem zadań testowych. W tym
rozdziale podano również:
−
plan testu w formie tabelarycznej,
−
punktację zadań,
−
propozycje norm wymagań,
−
instrukcję dla nauczyciela,
−
instrukcję dla ucznia,
−
kartę odpowiedzi,
−
zestaw zadań testowych.
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
4
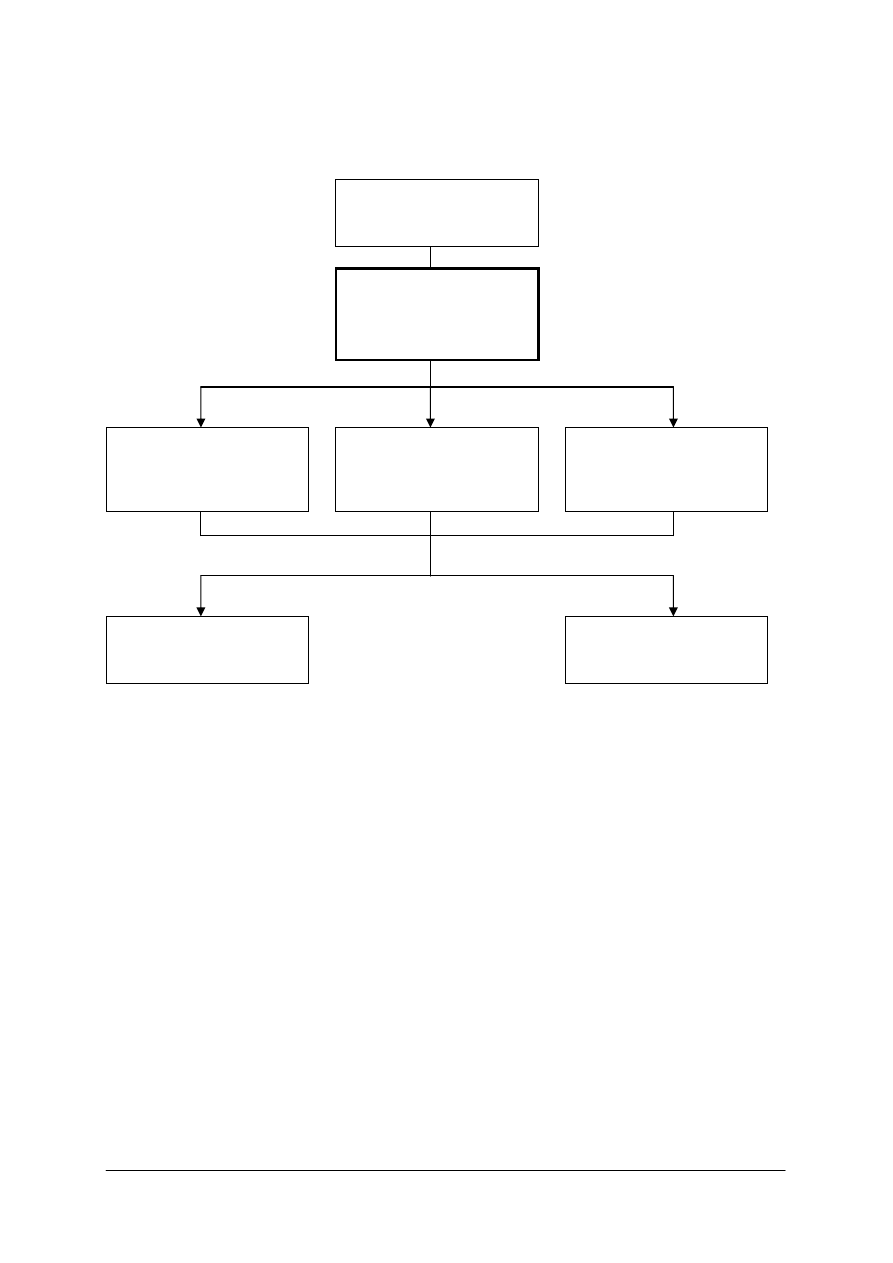
Schemat układu jednostek modułowych
815[01].O2
Technika laboratoryjna
815[01].O2.01
Wykonywanie
podstawowych czynności
laboratoryjnych
815[01].O2.05
Stosowanie fizycznych
procesów podstawowych
815[01].O2.06
Stosowanie chemicznych
procesów podstawowych
815[01].O2.02
Wykonywanie
podstawowych analiz
jakościowych
815[01].O2.04
Badanie właściwości
fizycznych substancji
815[01].O2.03
Wykonywanie
podstawowych analiz
ilościowych

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
5
2. WYMAGANIA WSTĘPNE
Przystępując do realizacji programu jednostki modułowej uczeń powinien umieć:
−
korzystać z różnych źródeł informacji,
−
wykonywać podstawowe obliczenia chemiczne,
−
czytać tekst ze zrozumieniem,
−
posługiwać się poprawną nomenklaturą i symboliką chemiczną,
−
wykonywać obliczenia związane ze stężeniem procentowym i stężeniem molowy
roztworu,
−
wskazywać najczęściej spotykane zagrożenia, przy których wymagane jest stosowanie
ś
rodków ochrony indywidualnej,
−
udzielać pierwszej pomocy w stanach zagrożenia życia lub zdrowia.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
6
3. CELE KSZTAŁCENIA
W wyniku realizacji programu jednostki modułowej uczeń powinien umieć:
−
zorganizować stanowisko pracy laboratoryjnej,
−
zinterpretować podstawowe pojęcia związane z bezpieczeństwem i higieną pracy
w laboratorium chemicznym,
−
dostrzec zagrożenia związane z wykonywaniem prac laboratoryjnych,
−
posłużyć się kartami charakterystyk substancji niebezpiecznych stosowanych w pracy
laboratoryjnej,
−
posłużyć się środkami ochrony indywidualnej i zbiorowej stosowanymi w laboratorium
chemicznym,
−
wykorzystać racjonalnie sprzęt i aparaturę laboratoryjną,
−
wykorzystać racjonalnie substancje i czynniki energetyczne,
−
przechować substancje chemiczne,
−
zakonserwować sprzęt laboratoryjny,
−
odmierzyć substancje ciekłe,
−
zważyć substancje stałe i ciekłe,
−
sporządzić roztwory wodne o określonym stężeniu,
−
oczyścić substancje nieorganiczne i organiczne,
−
przeprowadzić regenerację rozpuszczalników,
−
prowadzić dokumentację laboratoryjną,
−
zinterpretować wyniki pomiarów laboratoryjnych,
−
zastosować przepisy bezpieczeństwa i higieny pracy oraz przeciwpożarowe podczas
wykonywania prac laboratoryjnych.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
7
4. PRZYKŁADOWE SCENARIUSZE ZAJĘĆ
Scenariusz zajęć 1
Osoba prowadząca
………………………………….………………….
Modułowy program nauczania:
Operator urządzeń przemysłu chemicznego 815[01]
Moduł:
Technika laboratoryjna 815[01].O2
Jednostka modułowa:
Wykonywanie
podstawowych
czynności
laboratoryjnych 815[01].O2.01
Temat: Przygotowanie roztworów o określonym stężeniu procentowym z naważek.
Cel ogólny: Kształtowanie umiejętności przygotowania roztworów o określonym stężeniu
procentowym.
Po zakończeniu zajęć edukacyjnych uczeń powinien umieć:
−
obliczyć ilość substancji potrzebnej do przygotowania określonej ilości roztworu
o podanym stężeniu procentowym,
−
dobrać sprzęt laboratoryjny do przygotowania roztworu,
−
skorzystać z Karty charakterystyki substancji niebezpiecznej,
−
dobrać środki ochrony indywidualnej,
−
zorganizować stanowisko pracy,
−
przygotować roztwór.
Metody nauczania-uczenia się:
−
ć
wiczenie praktyczne.
Formy organizacyjne pracy uczniów:
−
grupowa jednolita.
Czas trwania zajęć: 3 godziny dydaktyczne.
Środki dydaktyczne:
−
wodorotlenek sodu,
−
woda destylowana,
−
cylindry miarowe,
−
naczyńka wagowe,
−
tryskawki,
−
lejki zwykłe,
−
waga techniczna,
−
karty charakterystyki substancji niebezpiecznych.
Zadanie dla ucznia
Sporządź 200 g roztworu wodnego wodorotlenku sodu o stężeniu 5%.
W tym celu:
−
sporządź wykaz niezbędnego sprzętu laboratoryjnego i odczynników,
−
oblicz ilość niezbędnej do sporządzenia roztworu substancji,
−
zaplanuj konieczne czynności laboratoryjne,
−
określ warunki bhp niezbędne do bezpiecznego wykonywania czynności laboratoryjnych,

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
8
−
pobierz od nauczyciela niezbędny sprzęt i odczynniki,
−
przeprowadź zaplanowane czynności laboratoryjne,
−
zapisz obserwacje w dzienniku laboratoryjnym.
Przebieg zajęć:
1.
Sprawy organizacyjne.
2.
Nawiązanie do tematu, omówienie celów zajęć.
3.
Realizacja zajęć:
−
nauczyciel omawia z uczniami zasady bezpiecznej pracy z substancjami wybranymi
do ćwiczenia, demonstruje sposób postępowania podczas wykonywania zadania,
−
uczniowie na podstawie instrukcji sporządzania roztworu o określonym stężeniu
procentowym obliczają ilość potrzebnej substancji do sporządzenia roztworu oraz
dobierają sprzęt do wykonania zadania, organizują stanowisko pracy,
−
nauczyciel ocenia wykonane obliczenia i przygotowane przez uczniów stanowiska
pracy,
−
uczniowie, odważają substancję na wagach technicznych i sporządzają roztwory,
postępując zgodnie z instrukcją.
4.
Nauczyciel ocenia dokładność wykonania zadania i technikę pracy uczniów, wskazuje
mocne i słabe strony uczniów.
5.
Uczniowie wskazują trudności, jakie napotkali przy wykonywaniu zadania.
Zakończenie zajęć
Praca domowa
Należy przygotować 500 g
roztworu kwasu siarkowego(VI) o stężeniu 20%
mając do
dyspozycji kwas siarkowy(VI) o stężeniu 98%, wodę destylowaną oraz dowolny sprzęt
laboratoryjny. Ustal zasady bezpiecznej pracy podczas sporządzania roztworu, wykonaj
obliczenia i zaproponuj kolejność czynności laboratoryjnych.
Sposób uzyskania informacji zwrotnej od ucznia po zakończonych zajęciach:
−
anonimowe ankiety ewaluacyjne dotyczące sposobu prowadzenia zajęć i zdobytych
umiejętności.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
9
Scenariusz zajęć 2
Osoba prowadząca
…………………………………….…………………
Modułowy program nauczania:
Operator urządzeń przemysłu chemicznego 815[01]
Moduł:
Technika laboratoryjna 815[01].O2
Jednostka modułowa:
Wykonywanie
podstawowych
czynności
laboratoryjnych 815[01].O2.01
Temat: Oczyszczanie substancji ciekłych przez destylację.
Cel ogólny: Kształtowanie umiejętności oczyszczania substancji ciekłych przez destylację.
Po zakończeniu zajęć edukacyjnych uczeń potrafi:
−
dobrać sprzęt laboratoryjny,
−
zaplanować kolejność czynności,
−
skorzystać z Karty charakterystyki substancji niebezpiecznej,
−
zorganizować stanowisko do przeprowadzenia destylacji prostej,
−
złożyć zestaw szlifowy do destylacji,
−
oczyścić substancję przez destylację.
Metody nauczania-uczenia się:
−
ć
wiczenie praktyczne.
Formy organizacyjne pracy uczniów:
−
grupowa jednolita.
Czas trwania zajęć: 4 godziny dydaktyczne.
Środki dydaktyczne:
−
zanieczyszczony etanol,
−
elementy zestawu do destylacji prostej,
−
sprzęt szklany: zlewki, cylindry,
−
elektryczny płaszcz grzewczy,
−
karty charakterystyki substancji niebezpiecznych.
Zadanie dla ucznia
Zastosuj destylację prostą do oczyszczenia 200 cm
3
zanieczyszczonego etanolu.
W tym celu:
−
sporządź wykaz niezbędnego sprzętu laboratoryjnego i odczynników,
−
zaplanuj konieczne czynności laboratoryjne,
−
określ warunki bhp niezbędne do bezpiecznego wykonywania czynności laboratoryjnych,
−
pobierz od nauczyciela niezbędny sprzęt i odczynniki,
−
przeprowadź zaplanowane czynności laboratoryjne,
−
zapisz obserwacje w dzienniku laboratoryjnym.
Przebieg zajęć:
1.
Sprawy organizacyjne.
2.
Nawiązanie do tematu, omówienie celów zajęć.
3.
Realizacja zajęć:

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
10
−
nauczyciel omawia z uczniami zasady bezpiecznej pracy z substancjami wybranymi
do ćwiczenia, demonstruje sposób postępowania podczas wykonywania zadania,
−
uczniowie na podstawie instrukcji oczyszczania substancji przez destylację dobierają
sprzęt do wykonania zadania, organizują stanowisko pracy,
−
nauczyciel ocenia przygotowane przez uczniów stanowiska pracy,
−
uczniowie oczyszczają substancje przez destylację postępując zgodnie z instrukcją.
4.
Nauczyciel ocenia dokładność wykonania zadania, technikę pracy uczniów oraz
przestrzeganie zasad bezpiecznej pracy.
5.
Uczniowie wskazują trudności, jakie napotkali przy wykonywaniu zadania.
Zakończenie zajęć
Praca domowa
Korzystając z dostępnych źródeł informacji, wskaż inne zastosowania procesu destylacji
w laboratorium chemicznym.
Sposób uzyskania informacji zwrotnej od ucznia po zakończonych zajęciach:
−
anonimowe ankiety ewaluacyjne dotyczące sposobu prowadzenia zajęć i zdobytych
umiejętności.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
11
5.
ĆWICZENIA
5.1. Wyposażenie i zasady bezpiecznej pracy w laboratorium
chemicznym
5.1.1. Ćwiczenia
Ćwiczenie 1
W czasie prac laboratoryjnych nastąpił zapłon rozlanego na stole rozpuszczalnika od
palącego się w pobliżu palnika. Zaproponuj sposób ugaszenia ognia.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać odpowiedni
fragment rozdziału Materiał nauczania dotyczący zabezpieczeń przeciwpożarowych
stosowanych w laboratorium chemicznym. Należy zwrócić szczególną uwagę na
zastosowania podstawowego sprzętu przeciwpożarowego.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
zaplanować właściwą kolejność czynności,
2)
dobrać odpowiedni sprzęt przeciwpożarowy,
3)
zapoznać się z obsługą podstawowego sprzętu przeciwpożarowego.
Zalecane metody nauczania–uczenia się:
−
pokaz z objaśnieniem,
−
ć
wiczenie praktyczne.
Ś
rodki dydaktyczne:
−
sprzęt gaśniczy,
−
instrukcje obsługi sprzętu gaśniczego.
Ćwiczenie 2
W pracach laboratoryjnych należy posługiwać się czystym i suchym szklanym sprzętem
laboratoryjnym. Przygotuj sprzęt laboratoryjny niezbędny do przeprowadzenia ekstrakcji typu
ciecz – ciecz. Do przeprowadzenia ekstrakcji niezbędne są dwie zlewki, rozdzielacz, cylinder
miarowy. Stosuj odpowiednią kolejność doboru środków myjących i zasady bezpiecznej
pracy.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać odpowiedni
fragment rozdziału Materiał nauczania dotyczący mycia szkła laboratoryjnego. Należy
zwrócić szczególną uwagę na zasady mycia i suszenia szkła laboratoryjnego. Nauczyciel
powinien omówić zakres ćwiczenia, sposób wykonania oraz warunki zachowania
bezpieczeństwa pracy. Ćwiczenie może być wykonywane indywidualnie lub w grupach
2–4-osobowych.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
12
Sposób wykonania ćwiczenia.
Uczeń powinien:
1)
zapoznać się z instrukcją mycia sprzętu szklanego,
2)
zorganizować stanowisko pracy do wykonania ćwiczenia,
3)
zastosować się do poleceń zawartych w instrukcji mycia szkła, suszenia,
4)
dobrać odpowiedni sposób suszenia szkła,
5)
wykonać ćwiczenie z uwzględnieniem przepisów bhp.
Zalecane metody nauczania–uczenia się:
−
pokaz z objaśnieniem,
−
ć
wiczenie laboratoryjne.
Ś
rodki dydaktyczne:
−
sprzęt szklany,
−
ś
rodki myjące,
−
szczotki do mycia naczyń,
−
deska do suszenia naczyń,
−
suszarka.
Ćwiczenie 3
Określ zastosowanie przedstawionego w tabeli sprzętu laboratoryjnego.
Tabela do ćwiczenia 3
Lp.
Sprzęt laboratoryjny
Zastosowanie sprzętu
1
2
3
4

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
13
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać odpowiedni
fragment rozdziału Materiał nauczania dotyczący podstawowego sprzętu laboratoryjnego.
Należy zwrócić szczególną uwagę na zastosowania sprzętu laboratoryjnego. Ćwiczenie
powinno być wykonywane indywidualnie.
Sposób wykonania ćwiczenia
Uczeń powinien:
1) zapoznać się przeznaczeniem podstawowego sprzętu laboratoryjnego korzystając
z literatury zaleconej przez nauczyciela,
2) określić zastosowanie podanego w tabeli sprzętu laboratoryjnego.
Zalecane metody nauczania–uczenia się:
−
pokaz z objaśnieniem,
−
ć
wiczenie praktyczne.
Ś
rodki dydaktyczne:
−
literatura zgodna z punktem 7 poradnika dla nauczyciela.
Ćwiczenie 4
Dobierz środki ochrony indywidualnej do pracy ze stężonym roztworem kwasu
siarkowego(VI).
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać odpowiedni
fragment rozdziału Materiał nauczania dotyczący zasad bezpiecznej pracy w laboratorium
chemicznym. Należy zwrócić szczególną uwagę na pracę z substancjami żrącymi lub
parzącymi. Przed przystąpieniem do realizacji ćwiczenia nauczyciel powinien omówić jego
zakres i sposób wykonania. Ćwiczenie może być wykonywane indywidualnie lub w grupach
2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
zapoznać się z kartą charakterystyki substancji niebezpiecznej dotyczącą stężonego
kwasu siarkowego(VI),
2)
dobrać niezbędne do zapewnienia bezpiecznej pracy środki ochrony indywidualnej.
Zalecane metody nauczania–uczenia się:
−
pokaz z objaśnieniem,
−
ć
wiczenie praktyczne.
Ś
rodki dydaktyczne:
−
ś
rodki ochrony indywidualnej,
−
karty charakterystyki substancji niebezpiecznej.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
14
5.2. Podstawowe czynności laboratoryjne
5.2.1. Ćwiczenia
Ćwiczenie 1
Zważ naczyńko wagowe stosując wagę techniczną.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać odpowiedni
fragment rozdziału Materiał nauczania dotyczący ważenia na wagach laboratoryjnych. Należy
zwrócić szczególną uwagę na ważenie na wagach technicznych oraz zasady prawidłowego
zapisu wyniku ważenia. Ćwiczenie może być wykonywane indywidualnie lub w grupach
2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
zapoznać się z instrukcją ważenia na wadze technicznej,
2)
zorganizować stanowisko pracy,
3)
zważyć naczyńko wagowe na wadze technicznej zgodnie z instrukcją,
4)
zapisać wynik ważenia.
Zalecane metody nauczania–uczenia się:
−
pokaz z objaśnieniem,
−
ć
wiczenie laboratoryjne.
Ś
rodki dydaktyczne:
−
waga techniczna z odważnikami,
−
naczyńko wagowe.
Ćwiczenie 2
Zważ próbkę soli kuchennej stosując wagę analityczną.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać odpowiedni
fragment rozdziału Materiał nauczania dotyczący ważenia na wagach laboratoryjnych. Należy
zwrócić szczególną uwagę na ważenie na wagach analitycznych oraz zasady prawidłowego
zapisu wyniku ważenia. Ćwiczenie może być wykonywane indywidualnie lub w grupach
2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
zapoznać się z instrukcją ważenia na wadze analitycznej,
2)
zważyć naczyńko wagowe z solą na wadze technicznej,
3)
zapisać wynik ważenia,
4)
zważyć naczyńko wagowe z solą na wadze analitycznej zgodnie z instrukcją,
5)
zapisać wyniki ważenia,
6)
zważyć puste naczyńko wagowe na wadze technicznej,

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
15
7)
zważyć puste naczyńko wagowe na wadze analitycznej,
8)
zapisać wynik ważenia,
9)
wyznaczyć masę próbki soli kuchennej.
Zalecane metody nauczania–uczenia się:
−
pokaz z objaśnieniem,
−
tekstu przewodniego.
Ś
rodki dydaktyczne:
−
waga techniczna i odważniki,
−
waga analityczna,
−
naczyńko wagowe z solą kuchenną.
Ćwiczenie 3
Odmierz 0,230 dm
3
wody mając do dyspozycji cylindry o pojemnościach: 1 dm
3
,
500 cm
3
, 250 cm
3
, 100 cm
3
i przelej odmierzoną wodę do kolby miarowej o objętości
250 cm
3
. Następnie uzupełnij wodą zawartość kolby, aż do osiągnięcia objętości 250 cm
3
.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać odpowiedni
fragment rozdziału Materiał nauczania dotyczący odmierzania objętości cieczy. Należy
zwrócić szczególną uwagę na odmierzanie cieczy cylindrami. Ćwiczenie może być
wykonywane indywidualnie lub w grupach 2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
dobrać cylinder o stosownej objętości,
2)
odmierzyć roztwór według górnej linii menisku,
3)
przelać roztwór do kolby miarowej,
4)
uzupełnić wodą zawartość kolby, aż do osiągnięcia objętości 250 cm
3
.
Zalecane metody nauczania–uczenia się:
−
pokaz z objaśnieniem,
−
ć
wiczenie laboratoryjne.
Ś
rodki dydaktyczne:
−
cylindry,
−
kolba miarowa,
−
woda.
Ćwiczenie 4
Wysusz w eksykatorze 5 g Na
2
CO
3
·10 H
2
O.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać odpowiedni
fragment rozdziału Materiał nauczania dotyczący suszenia substancji. Należy zwrócić
szczególną uwagę na suszenie substancji w eksykatorze. Ćwiczenie może być wykonywane
indywidualnie lub w grupach 2–4-osobowych.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
16
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
zaplanować sprzęt laboratoryjny,
2)
odważyć 5 g otrzymanej substancji na szkiełku zegarkowym,
3)
przygotować eksykator:
−
sprawdzić czystość eksykatora,
−
umieścić środek suszący na dnie eksykatora,
−
posmarować brzeg pokrywy wazeliną,
4)
umieścić odważoną substancję w eksykatorze,
5)
pozostawić w eksykatorze substancję na okres jednego tygodnia,
6)
ponownie zważyć substancję (wyjmować szkiełko, stosując szczypce),
7)
porównać wyniki ważeń i zapisać wnioski.
Zalecane metody nauczania–uczenia się:
−
pokaz z objaśnieniem,
−
ć
wiczenie laboratoryjne.
Ś
rodki dydaktyczne:
−
waga techniczna i odważniki,
−
szkiełko zegarkowe,
−
eksykator,
−
łyżeczka,
−
substancja higroskopijna pochłaniająca wilgoć,
−
substancja suszona.
Ćwiczenie 5
Wypraż 10,00 g węglanu wapnia w piecu.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać odpowiedni
fragment rozdziału Materiał nauczania dotyczący prażenia substancji. Nauczyciel powinien
omówić zakres ćwiczenia, sposób wykonania oraz warunki zachowania bezpieczeństwa
pracy. Ćwiczenie może być wykonywane indywidualnie lub w grupach 2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
dobrać sprzęt i urządzenie,
2)
odczytać z kalendarza chemicznego temperaturę rozkładu substancji,
3)
odważyć na wadze technicznej 10,00 g substancji,
4)
wstawić tygiel z substancją do pieca,
5)
poddać prażeniu substancję w temperaturze rozkładu przez 3 godziny,
6)
wystudzić substancję po prażeniu przez godzinę w eksykatorze,
7)
zważyć tygielek z substancją na wadze technicznej,
8)
obliczyć ubytek masy.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
17
Zalecane metody nauczania–uczenia się:
−
pokaz z objaśnieniem,
−
ć
wiczenie laboratoryjne.
Ś
rodki dydaktyczne:
−
piec elektryczny,
−
instrukcja obsługi pieca elektrycznego,
−
waga analityczna,
−
sprzęt laboratoryjny,
−
substancja prażona.
Ćwiczenie 6
Ochłodź roztwór glikolu do temperatury -3°C.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać odpowiedni
fragment rozdziału Materiał nauczania dotyczący chłodzenia. Należy zwrócić uwagę na skład
i zakres chłodzenia mieszanin oziębiających. Nauczyciel powinien omówić zakres ćwiczenia,
sposób wykonania oraz warunki zachowania bezpieczeństwa pracy. Ćwiczenie może być
wykonywane indywidualnie lub w grupach 2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
dobrać sprzęt, przyrządy pomiarowe i urządzenie,
2)
zapoznać się z kartami charakterystyki substancji niebezpiecznej stosowanych w czasie
wykonywania ćwiczenia,
3)
dobrać niezbędne do zapewnienia bezpiecznej pracy środki ochrony indywidualnej,
4)
zaplanować wykonywane czynności,
5)
zorganizować stanowisko pracy,
6)
zmontować zestaw laboratoryjny do oziębiania cieczy,
7)
dobrać składniki mieszaniny oziębiającej,
8)
przygotować mieszaninę oziębiającą,
9)
ochłodzić roztwór glikolu do podanej temperatury.
Zalecane metody nauczania–uczenia się:
−
pokaz z objaśnieniem,
−
metoda tekstu przewodniego,
−
ć
wiczenie praktyczne.
Ś
rodki dydaktyczne:
−
karty charakterystyk substancji niebezpiecznych,
−
ś
rodki ochrony indywidualnej,
−
waga techniczna z odważnikami,
−
sprzęt laboratoryjny,
−
termometry,
−
substancje chemiczne,
−
lód,
−
roztwór glikolu.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
18
5.3. Przygotowywanie roztworów wodnych o określonych
stężeniach
5.3.1. Ćwiczenia
Ćwiczenie 1
Przygotuj 200 g wodnego roztworu NaCl o stężeniu 2%.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać odpowiedni
fragment rozdziału Materiał nauczania dotyczący przygotowywania roztworów wodnych.
Należy zwrócić uwagę uczniom na wzory, z których będą musieli skorzystać przy obliczaniu
niezbędnej do sporządzenia roztworu masy NaCl. Ćwiczenie może być wykonywane
indywidualnie lub w grupach 2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
zapoznać się z instrukcją sporządzania roztworu o stężeniu procentowym,
2)
dobrać sprzęt niezbędny do wykonania ćwiczenia,
3)
obliczyć potrzebną masę chlorku sodu i objętość wody,
4)
sporządzić roztwór zgodnie z instrukcją.
Zalecane metody nauczania–uczenia się:
−
pokaz z objaśnieniem,
−
ć
wiczenie laboratoryjne.
Ś
rodki dydaktyczne:
−
instrukcja sporządzania roztworu,
−
waga techniczna i odważniki,
−
chlorek sodu,
−
sprzęt laboratoryjny: cylinder miarowy, szkiełko zegarkowe, zlewka, bagietka, butelka,
łyżeczka.
Ćwiczenie 2
Przygotuj 200 cm
3
wodnego roztworu NaCl o stężeniu 0,1 mol/dm
3
.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać odpowiedni
fragment rozdziału Materiał nauczania dotyczący przygotowywania roztworów wodnych.
Należy zwrócić uwagę uczniom na wzory, z których będą musieli skorzystać przy obliczaniu
niezbędnej do sporządzenia roztworu masy NaCl. Ćwiczenie może być wykonywane
indywidualnie lub w grupach 2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
zapoznać się z instrukcją sporządzania roztworu o stężeniu molowym,
2)
dobrać sprzęt niezbędny do wykonania ćwiczenia,

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
19
3)
obliczyć potrzebną masę chlorku sodu,
4)
sporządzić roztwór zgodnie z instrukcją.
Zalecane metody nauczania–uczenia się:
−
pokaz z objaśnieniem,
−
ć
wiczenie laboratoryjne.
Ś
rodki dydaktyczne:
−
instrukcja sporządzania roztworu,
−
waga techniczna i odważniki,
−
chlorek sodu,
−
sprzęt laboratoryjny: kolba miarowa, naczyńko wagowe, tryskawka, lejek zwykły,
łyżeczka.
Ćwiczenie 3
Sporządź 500 cm
3
roztworu kwasu siarkowego(VI) o stężeniu 1 mol/dm
3
przez
rozcieńczanie stężonego kwasu siarkowego(VI).
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać odpowiedni
fragment rozdziału Materiał nauczania dotyczący przygotowywania roztworów wodnych.
Należy zwrócić uwagę uczniom na wzory, z których będą musieli skorzystać przy obliczaniu
niezbędnej do sporządzenia roztworu masy lub objętości stężonego kwasu siarkowego(VI).
Nauczyciel powinien zwrócić szczególną uwagę na przygotowanie przez ucznia planu pracy,
zwłaszcza w części dotyczącej zachowania warunków bezpiecznej pracy ze stężonym
kwasem. Ćwiczenie może być wykonywane indywidualnie lub w grupach 2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
zapoznać się z zasadami bezpiecznej pracy ze stężonymi kwasem siarkowym(VI)
zgodnie z kartą charakterystyk dla tej substancji,
2)
dobrać odpowiedni sprzęt laboratoryjny i środki ochrony indywidualnej,
3)
zgromadzić niezbędne odczynniki, zwracając uwagę na ich stopień czystości, stężenie
i gęstość,
4)
zorganizować stanowisko pracy,
5)
zaplanować czynności,
6)
wykonać obliczenia,
7)
sporządzić roztwór kwasu,
8)
przelać sporządzony roztwór do butelki i oznakować ją zgodnie z zaleceniami zawartymi
w karcie charakterystyki.
Ś
rodki dydaktyczne:
−
podstawowy sprzęt laboratoryjny,
−
stężony kwas siarkowy(VI),
−
ś
rodki ochrony indywidualnej: rękawice odporne na chemikalia, okulary ochronne typu
gogle,
−
stół laboratoryjny z dostępem do wyciągu.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
20
5.4. Rozdzielanie mieszanin jednorodnych i niejednorodnych
5.4.1. Ćwiczenia
Ćwiczenie 1
Dokonaj rozdziału zawiesiny węglanu wapnia z zastosowaniem sączenia na sączku
karbowanym.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać odpowiedni
fragment rozdziału Materiał nauczania dotyczący sączenia. Należy zwrócić szczególną uwagę
na sączenie z zastosowaniem sączków karbowanych. Nauczyciel powinien omówić zakres
ć
wiczenia, sposób wykonania oraz warunki zachowania bezpieczeństwa pracy. Ćwiczenie
może być wykonywane indywidualnie lub w grupach 2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
dobrać odpowiedni sprzęt laboratoryjny i środki ochrony indywidualnej,
2)
przygotować z bibuły filtracyjnej sączek karbowany,
3)
zmontować zestaw do sączenia,
4)
umieścić sączek karbowany w lejku,
5)
przesączyć zawiesinę,
6)
zdemontować zestaw i umyć.
Zalecane metody nauczania–uczenia się:
−
pokaz z objaśnieniem,
−
ć
wiczenie laboratoryjne.
Ś
rodki dydaktyczne:
−
sprzęt laboratoryjny,
−
ś
rodki ochrony indywidualnej,
−
zestaw do sączenia,
−
sączek karbowany,
−
zawiesina węglanu wapnia.
Ćwiczenie 2
Przeprowadź rekrystalizację 5 g zanieczyszczonego kwasu benzoesowego.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać odpowiedni
fragment rozdziału Materiał nauczania dotyczący rekrystalizacji. Nauczyciel powinien
omówić zakres ćwiczenia, sposób wykonania oraz warunki zachowania bezpieczeństwa
pracy. Ćwiczenie może być wykonywane indywidualnie lub w grupach 2–4-osobowych.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
21
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
odczytać z kalendarza chemicznego rozpuszczalność kwasu benzoesowego w wodzie
zimnej i gorącej,
2)
obliczyć ilość wody potrzebnej do sporządzenia nasyconego roztworu kwasu w gorącej
wodzie,
3)
dobrać odpowiedni sprzęt laboratoryjny i środki ochrony indywidualnej,
4)
zaplanować czynności laboratoryjne,
5)
przygotować stanowisko pracy,
6)
przekrystalizować zanieczyszczony kwas,
7)
zastosować przepisy bhp.
Zalecane metody nauczania–uczenia się:
−
pokaz z objaśnieniem,
−
ć
wiczenie laboratoryjne.
Ś
rodki dydaktyczne:
−
sprzęt szklany,
−
waga techniczna i odważniki,
−
kalendarz chemiczny,
−
ź
ródło ciepła,
−
kwas benzoesowy,
−
węgiel aktywowany,
−
sączki.
Ćwiczenie 3
Przeprowadź proces ługowania olejku różanego z płatków róży stosując aparat Soxhleta.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać odpowiedni
fragment rozdziału Materiał nauczania dotyczący ekstrakcji typu ciało stałe – ciecz.
Nauczyciel powinien omówić zakres ćwiczenia, sposób wykonania oraz warunki zachowania
bezpieczeństwa pracy. Ćwiczenie może być wykonywane indywidualnie lub w grupach
2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien:
1)
dobrać odpowiedni sprzęt laboratoryjny i środki ochrony indywidualnej,
2)
zorganizować stanowisko pracy,
3)
zapoznać się z instrukcją prowadzenia procesu ługowania,
4)
zaplanować czynności laboratoryjne,
5)
wykonać ługowanie olejku różanego alkoholem etylowym,
6)
zastosować zasady bezpiecznej pracy.
Zalecane metody nauczania–uczenia się:
−
pokaz z objaśnieniem,
−
ć
wiczenie laboratoryjne.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
22
Ś
rodki dydaktyczne:
−
aparat Soxhleta,
−
sprzęt metalowy,
−
bibuła, wata,
−
waga techniczna z odważnikami,
−
płatki róż.
Ćwiczenie 4
Dokonaj rozdziału alkoholowego roztworu olejku różanego (uzyskanego w procesie
ługowania olejku różanego z płatków róży) z zastosowaniem destylacji prostej.
Wskazówki do realizacji
Przed przystąpieniem do realizacji ćwiczenia uczniowie powinni przeczytać odpowiedni
fragment rozdziału Materiał nauczania dotyczący destylacji. Nauczyciel powinien omówić
zakres ćwiczenia, sposób wykonania oraz warunki zachowania bezpieczeństwa pracy.
Ć
wiczenie może być wykonywane indywidualnie lub w grupach 2–4-osobowych.
Sposób wykonania ćwiczenia
Uczeń powinien
1)
zapoznać się z procesem destylacji prostej,
2)
dobrać sprzęt laboratoryjny do montażu zestawu,
3)
zorganizować stanowisko pracy,
4)
zapoznać się z instrukcją montażu zestawu do destylacji prostej,
5)
sprawdzić stan sprzętu do montażu,
6)
posmarować złącza szlifowe smarem,
7)
zmontować zestaw do destylacji prostej.
Zalecane metody nauczania–uczenia się:
−
pokaz z objaśnieniem,
−
ć
wiczenie laboratoryjne.
Ś
rodki dydaktyczne:
−
sprzęt szklany szlifowy,
−
sprzęt metalowy,
−
węże,
−
termometr,
−
smar do szlifów.
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
23
6. EWALUACJA OSIĄGNIĘĆ UCZNIA
Przykłady narzędzi pomiaru dydaktycznego
TEST 1
Test dwustopniowy do jednostki modułowej
„Wykonywanie podstawowych
czynności laboratoryjnych”
Test składa się z 20 zadań wielokrotnego wyboru, z których:
−
zadania 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 13, 16, 17, 19 są z poziomu podstawowego,
−
zadania 11, 14, 15, 18, 20 są z poziomu ponadpodstawowego.
Punktacja zadań: 0 lub 1 punkt
Za każdą prawidłową odpowiedź uczeń otrzymuje 1 punkt. Za złą odpowiedź lub jej brak
uczeń otrzymuje 0 punktów.
Proponuje się następujące normy wymagań – uczeń otrzyma następujące
oceny szkolne:
−
dopuszczający – za rozwiązanie co najmniej 9 zadań z poziomu podstawowego,
−
dostateczny – za rozwiązanie co najmniej 13 zadań z poziomu podstawowego,
−
dobry – za rozwiązanie 16 zadań, w tym co najmniej 2 z poziomu ponadpodstawowego,
−
bardzo dobry – za rozwiązanie 18 zadań, w tym co najmniej 4 z poziomu
ponadpodstawowego.
Klucz odpowiedzi: 1. b, 2. d, 3. a, 4. d, 5. b, 6. a, 7. d, 8. b, 9. b, 10. d, 11. b,
12. a, 13. a, 14. b, 15. a, 16. b, 17. d, 18. c, 19. a, 20. b.
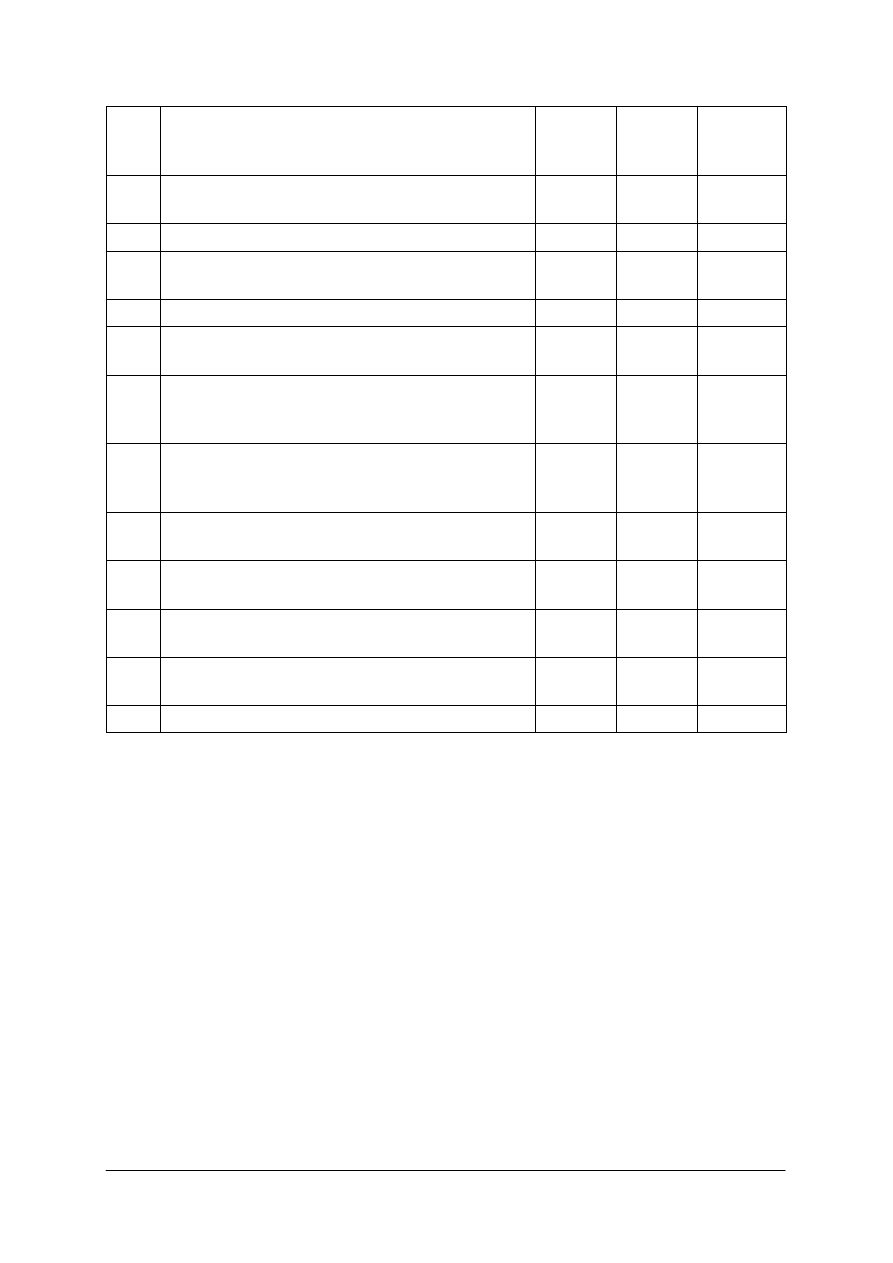
Plan testu
Nr
zad
Cel operacyjny
(mierzone osiągnięcia ucznia)
Kategoria
celu
Poziom
wymagań
Poprawna
odpowiedź
1.
Rozróżnić naczynie miarowe stosowane
w laboratorium chemicznym
B
P
b
2.
Dobrać środki myjące
B
P
d
3.
Dobrać cylinder miarowy do odmierzenia
określonej objętości cieczy
B
P
a
4.
Określić przeznaczenie zestawu laboratoryjnego
C
P
d
5.
Dobrać środek gaśniczy do gaszenia urządzenia
elektrycznego znajdującego się pod napięciem
B
P
b
6.
Wyjaśnić przeznaczenie sprzętu laboratoryjnego
B
P
a
7.
Wskazać źródła informacji o zagrożeniach
wynikających ze stosowania substancji
niebezpiecznych
B
P
d
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
24
8.
Wskazać znaczenie znaku ostrzegawczego
znajdującego się na opakowaniu z substancją
niebezpieczną
B
P
b
9.
Wskazać sytuację w laboratorium, w której należy
zastosować środki ochrony osobistej
B
P
b
10.
Dobrać sposób ogrzewania cieczy palnej
B
P
d
11.
Rozpoznać rozpuszczalnik do przeprowadzenia
procesu krystalizacji
C
PP
b
12.
Rozpoznać rodzaj palnika
C
P
a
13.
Dobrać warunki do prawidłowego przebiegu
procesu destylacji
B
P
a
14.
Obliczyć ilość substancji i rozpuszczalnika
niezbędną do przygotowania roztworu
o określonym stężeniu procentowym
C
PP
b
15.
Obliczyć ilość substancji niezbędnej do
sporządzenia roztworu o określonym stężeniu
molowym
C
PP
a
16.
Wskazać metodę rozdziału jednorodnej
mieszaniny ciekłej
B
P
b
17.
Wskazać dokładność, z jaką może być odważona
substancja na wadze technicznej
B
P
d
18.
Obliczyć masę substancji na podstawie ilości
i masy odważników ustawionych na szalce wagi
C
PP
c
19.
Dobrać zestaw laboratoryjny stosowany do
przeprowadzenia procesu ługowania
B
P
a
20.
Określić nazwę elementu zestawu destylacyjnego
C
PP
b

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
25
Przebieg testowania
Instrukcja dla nauczyciela
1.
Omów z uczniami sposób udzielania odpowiedzi.
2.
Zapewnij uczniom możliwość samodzielnej pracy.
3.
Rozdaj uczniom zestawy zadań testowych i karty odpowiedzi.
4.
Podaj czas przeznaczony na udzielanie odpowiedzi.
5.
Zbierz zestawy zadań testowych i sprawdź testy.
6.
Przeprowadź analizę uzyskanych wyników sprawdzianu i wybierz te zadania, które
sprawiły uczniom największe trudności.
7.
Ustal przyczyny trudności uczniów w opanowaniu wiadomości i umiejętności.
8.
Opracuj wnioski do dalszego postępowania, mającego na celu uniknięcie niepowodzeń
dydaktycznych.
Instrukcja dla ucznia
1.
Przeczytaj uważnie instrukcję.
2.
Podpisz imieniem i nazwiskiem kartę odpowiedzi.
3.
Zapoznaj się z zestawem zadań testowych.
4.
Test zawiera 20 zadań. Do każdego zadania dołączone są 4 możliwości odpowiedzi.
Tylko jedna jest prawidłowa.
5.
Udzielaj odpowiedzi na załączonej karcie odpowiedzi, stawiając w odpowiedniej rubryce
znak X. W przypadku pomyłki należy błędną odpowiedź zaznaczyć kółkiem, a następnie
ponownie zakreślić odpowiedź prawidłową.
6.
Pracuj samodzielnie, bo tylko wtedy będziesz miał satysfakcję z wykonanego zadania.
7.
Jeśli udzielenie odpowiedzi będzie Ci sprawiało trudność, wtedy odłóż jego rozwiązanie
na później i wróć do niego, gdy zostanie Ci wolny czas.
8.
Na rozwiązanie testu masz 40 minut.
Powodzenia!
Materiały dla ucznia:
-
instrukcja,
-
zestaw zadań testowych,
ZESTAW ZADAŃ TESTOWYCH
1.
Do sprzętu laboratoryjnego szklanego, miarowego zalicza się
a)
zlewkę.
b)
biuretę.
c)
kolbę stożkową.
d)
naczyńko wagowe.
2.
Gorącą wodą nie można myć
a)
zlewki.
b)
kolby płaskodennej.
c)
kolby stożkowej.
d)
kolby miarowej.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
26
3.
80 cm
3
wody należy odmierzyć w cylindrze o pojemności
a)
100 cm
3
.
b)
250 cm
3
.
c)
500 cm
3
.
d)
1000 cm
3
.
4.
Przedstawiony zestaw stosowany jest w laboratorium do przeprowadzenia procesu
a)
destylacji.
b)
sączenia.
c)
suszenia.
d)
prażenia.
5.
Płonącego urządzenia elektrycznego, znajdującego się pod napięciem nie wolno gasić
a)
piaskiem.
b)
wodą.
c)
kocem.
d)
gaśnicą proszkową.
6.
Przedstawiony sprzęt laboratoryjny to
a)
zaciskacze.
b)
łapy do biuret.
c)
łapy do probówek.
d)
szczypce metalowe.
7.
Przed przystąpieniem do pracy z substancją niebezpieczną należy zapoznać się z jej
właściwościami i zagrożeniami korzystając z
a)
kalendarza chemicznego.
b)
poradnika dla ucznia.
c)
poradnika chemicznego.
d)
karty charakterystyki substancji niebezpiecznej.
8.
Przedstawiony znak ostrzegawczy oznacza, że mamy do czynienia z substancją
a)
szkodliwą dla zdrowia.
b)
wybuchową.
c)
ż
rącą.
d)
łatwopalną.
9.
Ś
rodki ochrony indywidualnej należy stosować podczas pracy z
a)
rozcieńczonymi roztworami cukru.
b)
stężonymi kwasami.
c)
rozcieńczonymi roztworami soli kuchennej.
d)
wodą.
10.
Do ogrzewania cieczy palnych nie wolno używać
a)
elektrycznej płyty grzewczej.
b)
łaźni wodnej.
c)
elektrycznego garnka grzewczego.
d)
palnika.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
27
11.
Dobry rozpuszczalnik stosowany do krystalizacji substancji powinien
a)
reagować z substancją krystalizowaną.
b)
dobrze rozpuszczać substancję oczyszczaną na gorąco, a słabo na zimno.
c)
ulegać rozkładowi w wysokich temperaturach.
d)
dobrze rozpuszczać zanieczyszczenia.
12.
Przedstawiony sprzęt laboratoryjny to palnik
a)
Teclu.
b)
denaturatowy.
c)
Meckera.
d)
acetylenowy.
13.
Przed przystąpieniem do procesu destylacji do kolby destylacyjnej należy wrzucić
a)
kamyki wrzenne.
b)
katalizator.
c)
barwnik.
d)
koagulant.
14.
W celu sporządzenia 100 g roztworu NaCl o stężeniu 10% należy użyć
a)
1 g NaCl i 99 g wody.
b)
10 g NaCl i 90 cm
3
wody.
c)
90 g NaCl i 10 cm
3
wody.
d)
99 g NaCl i 1 g wody.
15.
Do sporządzenia 100 cm
3
roztworu wodorotlenku sodu o stężeniu 0,1 mol/dm
3
należy
rozpuścić w 100 cm
3
wody
a)
1 mol wodorotlenku sodu.
b)
10 moli wodorotlenku sodu.
c)
0,1 mola wodorotlenku sodu.
d)
0,01 mola wodorotlenku sodu.
16.
Jednorodną mieszaninę rozpuszczalników można rozdzielić stosując proces
a)
dekantacji.
b)
sączenia.
c)
sublimacji.
d)
krystalizacji.
17.
Na wadze technicznej można zważyć substancję z dokładnością
a)
0,0001 g.
b)
1 g.
c)
10 g.
d)
0,01 g.
18.
Na szalce wagi technicznej umieszczono odważniki: 10 g, 5 g, 500 mg, 100 mg, 2 g,
10 mg, masa wszystkich odważników wynosi
a)
15,610 g.
b)
17,510 g.
c)
17,610 g.
d)
15,600 g.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
28
19.
Proces ługowania w sposób ciągły prowadzi się w
a)
aparacie Soxhleta.
b)
rozdzielaczu z korkiem.
c)
biurecie.
d)
cylindrze.
20.
Opisany na rysunku cyfrą 2 element zestawu destylacyjnego to
a)
odbieralnik.
b)
kolba destylacyjna.
c)
kapilara.
d)
chłodnica.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
29
KARTA ODPOWIEDŹI
Imię i nazwisko...............................................................................................................
Wykonywanie podstawowych czynności laboratoryjnych
Zakreśl poprawną odpowiedź.
Nr
zadania
Odpowiedź
Punkty
1
a
b
c
d
2
a
b
c
d
3
a
b
c
d
4
a
b
c
d
5
a
b
c
d
6
a
b
c
d
7
a
b
c
d
8
a
b
c
d
9
a
b
c
d
10
a
b
c
d
11
a
b
c
d
12
a
b
c
d
13
a
b
c
d
14
a
b
c
d
15
a
b
c
d
16
a
b
c
d
17
a
b
c
d
18
a
b
c
d
19
a
b
c
d
20
a
b
c
d
Razem:
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
30
TEST 2
Test dwustopniowy do jednostki modułowej
„Wykonywanie podstawowych
czynności laboratoryjnych”
Test składa się z 20 zadań wielokrotnego wyboru, z których:
−
zadania 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 13, 16, 17 są z poziomu podstawowego,
−
zadania 11, 14, 15, 18, 19, 20 są z poziomu ponadpodstawowego.
Punktacja zadań: 0 lub 1 punkt
Za każdą prawidłową odpowiedź uczeń otrzymuje 1 punkt. Za złą odpowiedź lub jej brak
uczeń otrzymuje 0 punktów.
Proponuje się następujące normy wymagań – uczeń otrzyma następujące
oceny szkolne:
−
dopuszczający – za rozwiązanie co najmniej 9 zadań z poziomu podstawowego,
−
dostateczny – za rozwiązanie co najmniej 13 zadań z poziomu podstawowego,
−
dobry – za rozwiązanie 16 zadań, w tym co najmniej 3 z poziomu ponadpodstawowego,
−
bardzo dobry – za rozwiązanie 18 zadań, w tym co najmniej 5 z poziomu
ponadpodstawowego.
Klucz odpowiedzi: 1. b, 2. c, 3. b, 4. c, 5. c, 6. b, 7. d, 8. c, 9. a, 10. d, 11. b,
12. c, 13. a, 14. b, 15. c, 16. a, 17. a, 18. a, 19. d, 20. d.
Plan testu
Nr
zad
Cel operacyjny
(mierzone osiągnięcia ucznia)
Kategoria
celu
Poziom
wymagań
Poprawna
odpowiedź
1
Wskazać naczynie miarowe stosowane
w laboratorium chemicznym
A
P
b
2
Określić zastosowanie środka myjącego
B
P
c
3
Dobrać cylinder miarowy do odmierzenia
określonej objętości cieczy
B
P
b
4
Określić przeznaczenie zestawu laboratoryjnego
C
P
c
5
Dobrać środek gaśniczy do gaszenia urządzenia
elektrycznego znajdującego się pod napięciem
B
P
c
6
Określić przeznaczenie sprzętu laboratoryjnego
B
P
b
7
Wskazać źródła informacji o właściwościach
i zagrożeniach wynikających ze stosowania
substancji niebezpiecznych
B
P
d
8
Rozpoznać znak ostrzegawczy znajdujący się na
opakowaniu z substancją niebezpieczną
C
P
c
9
Dobrać środki ochrony osobistej
B
P
a
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
31
10
Dobrać sposób ogrzewania
B
P
d
11
Określić zakres stosowania procesu krystalizacji
C
PP
b
12
Wskazać zastosowanie sprzętu laboratoryjnego
B
P
c
13
Dobrać warunki do prawidłowego przebiegu
procesu destylacji
B
P
a
14
Obliczyć ilość substancji i rozpuszczalnika
niezbędną do przygotowania roztworu
o określonym stężeniu procentowym
C
PP
b
15
Obliczyć ilość substancji niezbędnej do
sporządzenia roztworu o określonym stężeniu
molowym
C
PP
c
16
Wskazać zastosowanie zestawu laboratoryjnego
B
P
a
17
Wskazać dokładność, z jaką może być odważona
substancja na wadze technicznej
B
P
a
18
Przeliczyć masę substancji na podstawie ilości
i masy odważników ustawionych na szalce wagi
C
PP
a
19
Określić nazwę elementu aparatu Soxhleta
C
PP
d
20
Określić nazwę elementu zestawu destylacyjnego
C
PP
d

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
32
Przebieg testowania
Instrukcja dla nauczyciela
1.
Omów z uczniami sposób udzielania odpowiedzi .
2.
Zapewnij uczniom możliwość samodzielnej pracy.
3.
Rozdaj uczniom zestawy zadań testowych i karty odpowiedzi.
4.
Podaj czas przeznaczony na udzielanie odpowiedzi.
5.
Zbierz zestawy zadań testowych i sprawdź testy.
6.
Przeprowadź analizę uzyskanych wyników sprawdzianu i wybierz te zadania, które
sprawiły uczniom największe trudności.
7.
Ustal przyczyny trudności uczniów w opanowaniu wiadomości i umiejętności.
8.
Opracuj wnioski do dalszego postępowania, mającego na celu uniknięcie niepowodzeń
dydaktycznych.
Instrukcja dla ucznia
1.
Przeczytaj uważnie instrukcję.
2.
Podpisz imieniem i nazwiskiem kartę odpowiedzi.
3.
Zapoznaj się z zestawem zadań testowych.
4.
Test zawiera 20 zadań. Do każdego zadania dołączone są 4 możliwości odpowiedzi.
Tylko jedna jest prawidłowa.
5.
Udzielaj odpowiedzi na załączonej karcie odpowiedzi, stawiając w odpowiedniej rubryce
znak X. W przypadku pomyłki należy błędną odpowiedź zaznaczyć kółkiem, a następnie
ponownie zakreślić odpowiedź prawidłową.
6.
Pracuj samodzielnie, bo tylko wtedy będziesz miał satysfakcję z wykonanego zadania.
7.
Jeśli udzielenie odpowiedzi będzie Ci sprawiało trudność, wtedy odłóż jego rozwiązanie
na później i wróć do niego, gdy zostanie Ci wolny czas.
8.
Na rozwiązanie testu masz 40 minut.
Powodzenia
Materiały dla ucznia:
-
instrukcja,
-
zestaw zadań testowych,
ZESTAW ZADAŃ TESTOWYCH
1.
Do sprzętu laboratoryjnego szklanego, miarowego zalicza się
a)
zlewkę.
b)
cylinder miarowy.
c)
kolbę stożkową.
d)
naczyńko wagowe.
2.
Alkoholowy roztwór wodorotlenku sodu służy do
a)
mycia wstępnego zatłuszczonych naczyń.
b)
mycia zanieczyszczeń tlenkowych.
c)
mycia końcowego zatłuszczonych naczyń.
d)
mycia zanieczyszczeń wodorotlenkowych.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
33
3.
180 cm
3
wody należy odmierzyć w cylindrze o pojemności
a)
100 cm
3
.
b)
250 cm
3
.
c)
500 cm
3
.
d)
1000 cm
3
.
4.
Przedstawiony zestaw stosowany jest w laboratorium do przeprowadzenia procesu
a)
destylacji.
b)
sączenia.
c)
ekstrakcji.
d)
prażenia.
5.
Płonącego urządzenia elektrycznego, znajdującego się pod napięciem nie wolno gasić
a)
piaskiem.
b)
gaśnicą śniegową.
c)
gaśnicą pianową.
d)
gaśnicą proszkową.
6.
Przedstawiony sprzęt laboratoryjny to
a)
zaciskacz.
b)
łapa do biuret.
c)
łapa do probówek.
d)
szczypce metalowe.
7.
Przed przystąpieniem do pracy z substancją niebezpieczną należy zapoznać się z jej
właściwościami i zagrożeniami korzystając z
a)
kalendarza chemicznego.
b)
poradnika dla ucznia.
c)
poradnika chemicznego.
d)
karty charakterystyki substancji niebezpiecznej.
8.
Przedstawiony znak ostrzegawczy oznacza, że mamy do czynienia z substancją
a)
szkodliwą dla zdrowia.
b)
wybuchową.
c)
ż
rącą.
d)
łatwopalną.
9.
Podczas pracy z substancjami żrącymi i parzącymi należy
a)
nałożyć okulary, rękawice i fartuch ochronny.
b)
nałożyć okulary i fartuch ochronny.
c)
nałożyć rękawice i fartuch ochronny.
d)
nałożyć okulary i rękawice.
10.
Łaźnie olejowe stosowane są do podgrzewania substancji do temperatury
a)
poniżej 50°C.
b)
poniżej 100°C.
c)
poniżej 0°C.
d)
powyżej 100°C.
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
34
11.
Krystalizacja nie jest stosowana do
a)
oczyszczania substancji stałych.
b)
rozdzielania mieszanin cieczy.
c)
rozdzielania mieszanin ciał stałych.
d)
wydzielania soli z roztworów wodnych.
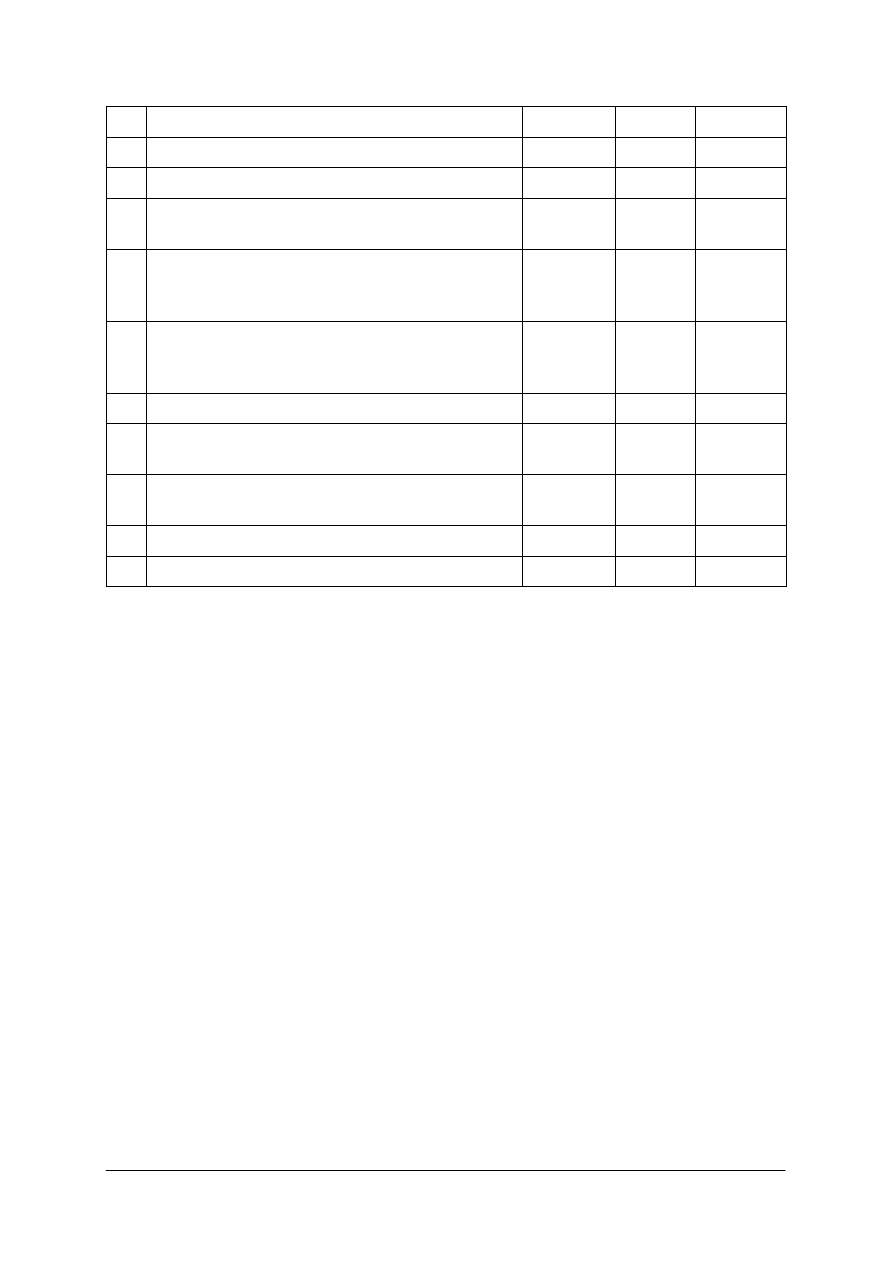
12.
Przedstawiony sprzęt laboratoryjny to
a)
palnik Teclu.
b)
palnik denaturatowy.
c)
palnik Meckera.
d)
palnik acetylenowy.
13.
Kolbę destylacyjną wypełniamy maksymalnie do
a)
2/3 pojemności.
b)
1/3 pojemności.
c)
1/2 pojemności.
d)
1/10 pojemności.
14.
Do sporządzenia 200 g roztworu NaCl o stężeniu 5% należy użyć
a)
1 g NaCl i 99 g wody.
b)
10 g NaCl i 90 cm
3
wody.
c)
90 g NaCl i 10 cm
3
wody.
d)
99 g NaCl i 1 g wody.
15.
Do sporządzenia 500 cm
3
roztworu wodorotlenku sodu o stężeniu 0,2 mol/dm
3
należy
rozpuścić w 500 cm
3
wody
a)
1 mol wodorotlenku sodu.
b)
10 moli wodorotlenku sodu.
c)
0,1 mola wodorotlenku sodu.
d)
0,01 mola wodorotlenku sodu.
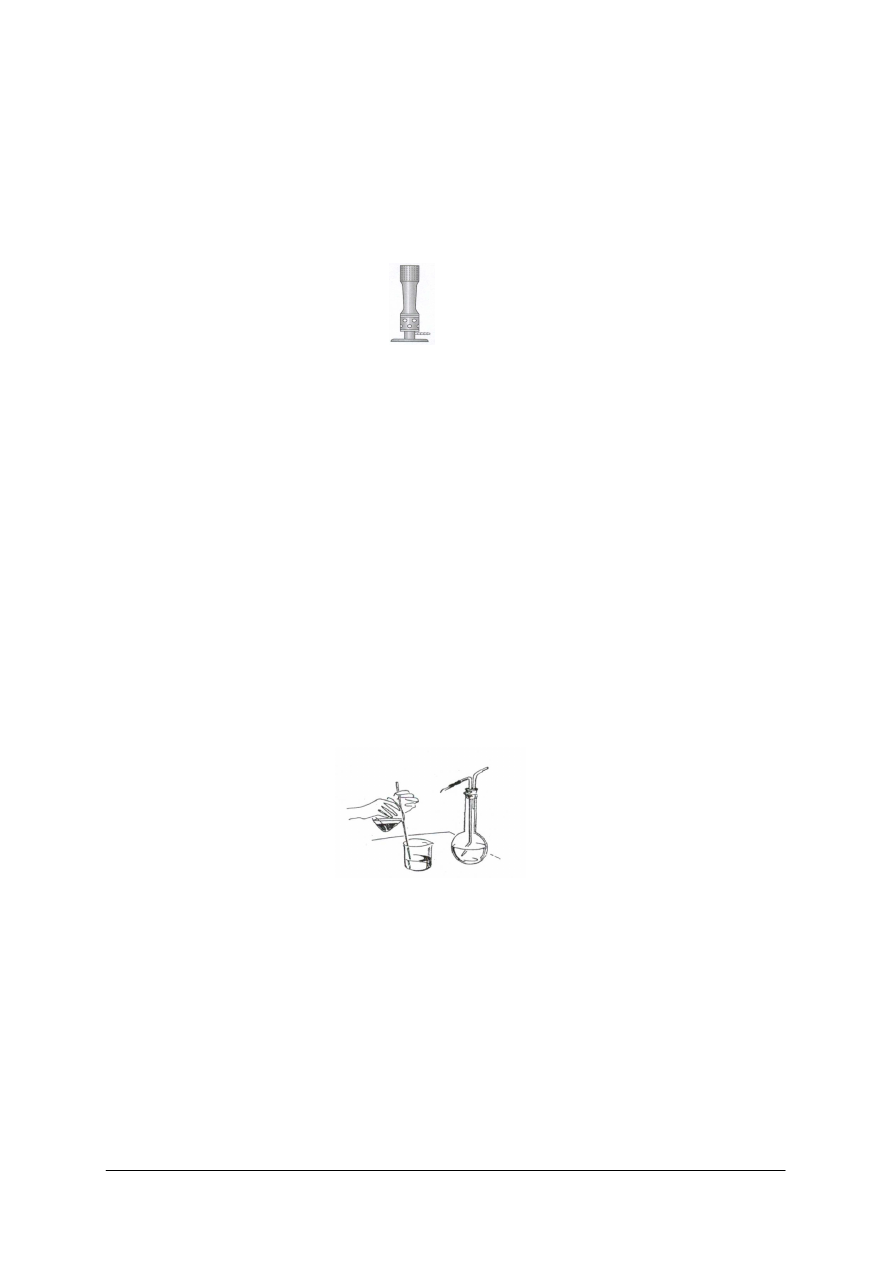
16.
Przedstawiony zestaw stosowany jest do
a)
dekantacji.
b)
destylacji.
c)
sublimacji.
d)
krystalizacji.
17.
Na wadze analitycznej można zważyć substancję z dokładnością
a)
0,0001 g.
b)
1 g.
c)
10 g.
d)
0,01 g.
18.
Na szalce wagi technicznej umieszczono odważniki: 10 g, 100 mg, 5 g, 500 mg, 10 mg,
masa wszystkich odważników wynosi:
a)
15,610 g.
b)
17,510 g.
c)
17,610 g.
d)
15,600 g.
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
35
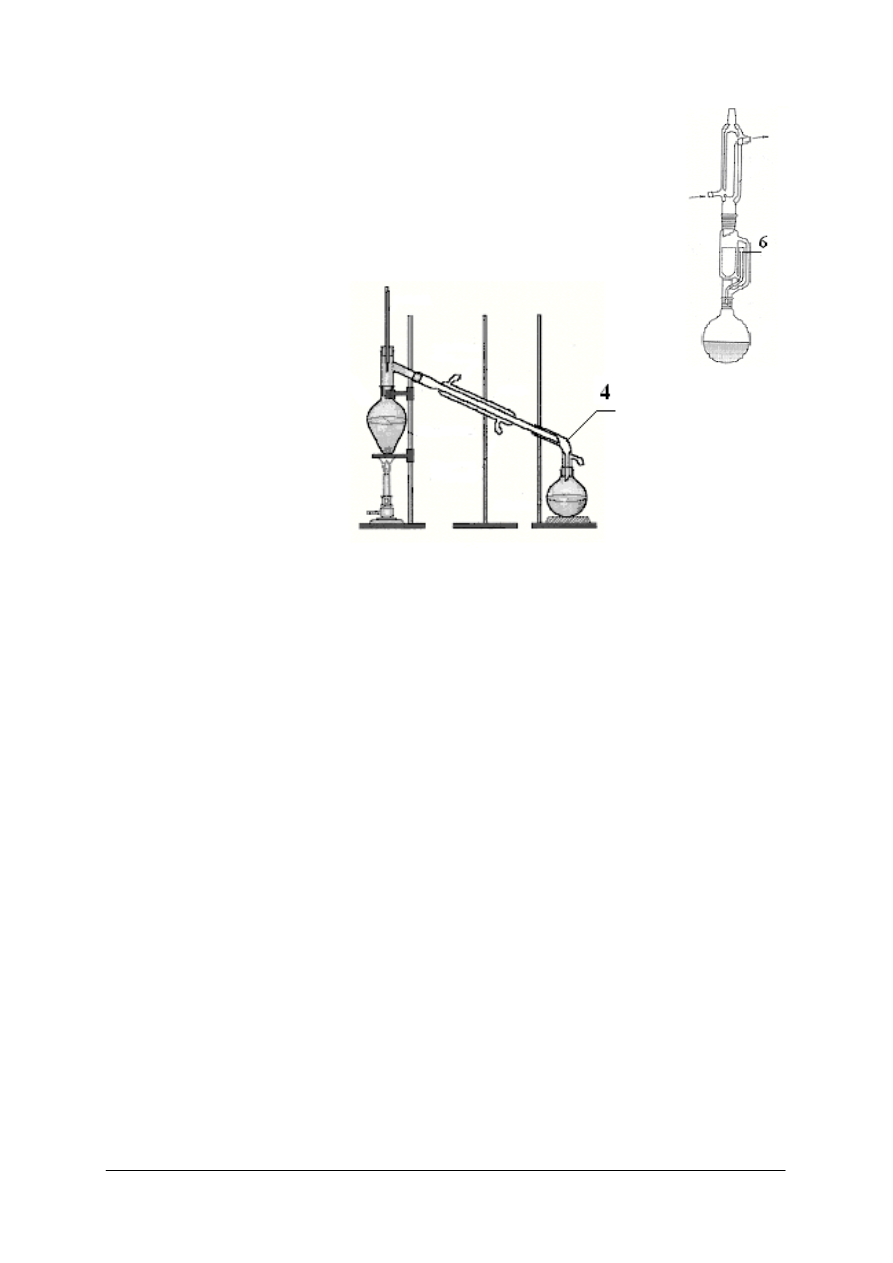
19.
Opisany na rysunku cyfrą 6 element aparatu Soxhleta to
a)
gilza.
b)
ekstraktor.
c)
rurka boczna.
d)
rurka przelewowa.
20.
Opisany na rysunku cyfrą 4 element zestawu destylacyjnego to
a)
kolba destylacyjna.
b)
nasadka Cleisena.
c)
kapilara.
d)
przedłużacz.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
36
KARTA ODPOWIEDZI
Imię i nazwisko...............................................................................................................
Wykonywanie podstawowych czynności laboratoryjnych
Zakreśl poprawną odpowiedź.
Nr
zadania
Odpowiedź
Punkty
1
a
b
c
d
2
a
b
c
d
3
a
b
c
d
4
a
b
c
d
5
a
b
c
d
6
a
b
c
d
7
a
b
c
d
8
a
b
c
d
9
a
b
c
d
10
a
b
c
d
11
a
b
c
d
12
a
b
c
d
13
a
b
c
d
14
a
b
c
d
15
a
b
c
d
16
a
b
c
d
17
a
b
c
d
18
a
b
c
d
19
a
b
c
d
20
a
b
c
d
Razem:

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
37
7. LITERATURA
1.
Jurgowska-Wernerowa M.: 500 zagadek chemicznych. Wiedza Powszechna, Warszawa
1983
2.
Klepaczko-Filipiak B., Jakubiak Z., Wulkiewicz U.: Badania chemiczne. Technika pracy
laboratoryjnej. WSiP, Warszawa 1998
3.
Klepaczko-Filipiak B.: Badania chemiczne. Analiza ilościowa substancji. WSiP,
Warszawa 1998
4.
Kupryszewski G.: Podstawowe zasady bezpiecznej pracy w laboratorium chemicznym.
Wydawnictwo Gdańskie, Gdańsk 1998
5.
Modzelewski M., Woliński J.: Pracownia chemiczna. Technika laboratoryjna. WSiP,
Warszawa 1996
6.
Rokosza A.: Ćwiczenia z chemii ogólnej i nieorganicznej. PWN, Warszawa 1974
7.
Rozporządzenie Ministra Zdrowia z dnia 2 września 2003 roku w sprawie kryteriów
i sposobu klasyfikacji substancji i preparatów chemicznych (Dz. U. z 2003 r. nr 171, poz.
1666 z późn. zm.)
Adresy internetowe
8.
www.zsrlututow.internetdsl.pl/zdjecia/chemia1.jpg
9.
www.p.lodz.pl/.../images/dest_zmn_cisnienie.jpg
10.
www.scholaris.pl
11.
www. moskit.uwm.edu.pl
12.
www.taniewagi.pl
Wyszukiwarka
Podobne podstrony:
01 Wykonywanie podstawowych czynności laboratoryjnych
Podstawowe czynności laboratoryjne, ~FARMACJA, I rok, chemia (ciul wie co), Semestr I
PODSTAWOWE CZYNNOŚCI LABORATORYJNE - ściąga, Pracownia Chemii kosmetycznej
04 Wykonywanie podstawowych for Nieznany (2)
01 Podstawowe czynności laboratoryjne instrukcja
Podstawowe czynności laboratoryjne
1 - Podstawowe czynności laboratoryjne, sprawko
PODSTAWOWE CZYNNOŚCI LABORATORYJNE, Pracownia Chemii kosmetycznej
04 Wykonywanie podstawowych robót tynkarskich
1 Podstawowe czynności laboratoryjne instrukcja
11 Wykonywanie podstawowych czynności higienicznych
1 Podstawowe czynności laboratoryjne sprawkoid 8789
04 Wykonywanie podstawowych robót tynkarskich
11 Wykonywanie podstawowych czynności higienicznychid 12677
1 Podstawowe czynności laboratoryjne instrukcja
Podstawowe czynności laboratoryjne, ~FARMACJA, I rok, chemia (ciul wie co), Semestr I
więcej podobnych podstron