Nr i tytuł ćwiczenia: Ćwiczenie 2-1 Wyznaczanie gęstości pary i masy molowej metodą Meyera
|
||||||
Imię i nazwisko osoby prowadzącej ćwiczenia: dr Ewa Więckowska-Bryłka |
||||||
Data wykonania ćwiczenia |
Godz: |
Nr grupy studenckiej |
Zespół |
Nazwiska osób wykonujących ćw |
Pkt za spr |
|
|
||||||
Uwagi prowadzącego |
|
|||||
1.CEL ĆWICZENIA
2.WSTĘP TEORETYCZNY
3.WYKONANIE ĆWICZENIA
4.OBLICZENIA I OPRACOWANIE WYNIKÓW
Próba 1
Masa pustej ampułki 2,2327 g
Masa ampułki z substancją 2,3849g
Ciśnienie atmosferyczne b= 101700Pa
Temperatura otoczenia T= 23oC = 296 K
Masa substancji ms=0,1522 g
Prężność pary wodnej w temp. 296K wynosi c= 2780,84 Pa
Objętość par po ustabilizowaniu się poziomu cieczy V= 20,2 cm3
Objętości:
20,2
19,3
18,7
19,0
18,9
18,5
18,6
18,3
18,7
18,2
17,7
17,3
16,7
16,4
16,7
17,2
Stała gazowa ![]()
![]()
Wzór na ciśnienie :
![]()
gdzie:
b - ciśnienie atmosferyczne
c - prężność pary wodnej w temperaturze pomiaru.
Wzór na masę molową M :
![]()
Wzór na gęstość pary badanej substancji :
![]()
Po podstawieniu do wzorów otrzymujemy :
p=101700Pa-2780,84Pa=98919,16Pa
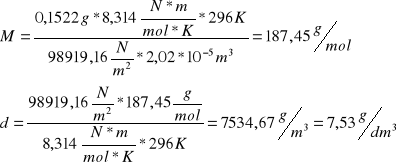
Próba 2
Masa pustej ampułki 2,2342 g
Masa ampułki z substancją 2,4000 g
Ciśnienie atmosferyczne b= 101700 Pa
Temperatura otoczenia T= 23oC = 296 K
Masa substancji ms=0,1658 g
Prężność pary wodnej w temp. 296K wynosi c= 2780,84Pa
Objętość par po ustabilizowaniu się poziomu cieczy V=18,2 cm3
Objętości:
17,9
18,0
18,3
18,1
18,0
18,1
18,0
17,8
17,7
17,6
17,2
16,8
16,7
Po podstawieniu do wzorów otrzymujemy :
p=101700Pa-2780,84Pa=98919,16Pa
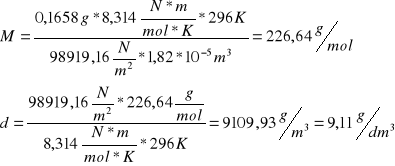
- 1 -
Wyszukiwarka
Podobne podstrony:
chemia fizyczna pytania, Technologia żywności UWM, chemia fizyczna (Dr Kalinowski)
Obliczenia91, SGGW - Technologia żywnosci, II semestr, SEMESTR 2, wyklady II rok, od kaski
Obliczenia91, SGGW - Technologia żywnosci, II semestr, SEMESTR 2, wyklady II rok, od kaski
pyt OTŻ, SGGW TECHNOLOGIA ŻYWNOŚCI I ŻYWIENIE CZŁOWIEKA, IV Semestr, OTŻ
Pytanka opisowe z dyspersji, SGGW TECHNOLOGIA ŻYWNOŚCI I ŻYWIENIE CZŁOWIEKA, IV Semestr, OTŻ
TH - przykladowe pytania egzaminacyjne KTZ-Technologii Zboz, SGGW - Technologia żywnosci, V semestr,
w3, SGGW - Technologia żywnosci, VII SEMESTR, zarzadzanie, Zarządzanie wd
Mięso - Pytania, SGGW - Technologia żywnosci, V semestr, 5 SEMESTR, semestr V, Mięso1
pytania z garw zaoczni!, SGGW - Technologia żywnosci, V semestr, 5 SEMESTR, semestr V, Gastronomia
Zadanie III, SGGW - Technologia żywnosci, VI SEEMSTR, Semestr VI, rachunkowość
Projektowanie - Różne, SGGW - Technologia żywnosci, VI SEEMSTR, Semestr VI, projektowanie
fiz 62 poprawione, SGGW - Technologia żywnosci, II semestr, SEMESTR 2, fizyka, sprawozdania, Sprawo
gospo dlugopisy 2, SGGW - Technologia żywnosci, IV semestr, SEMESTR 4, gospodarka
BERTHOLD, SGGW - Technologia żywnosci, VI SEEMSTR, Semestr VI, Bakterie mlekowe
więcej podobnych podstron