|
Data ćwiczenia: 17.12.2007 |
Imię i nazwisko studenta: Przemysław Machura |
Poprawa: |
|
Grupa ćwiczeniowa: VI |
Temat ćwiczenia: Oznaczenie zawartości miedzi w roztworze (próbka nr 6). |
Zaliczenie:
|
Cel ćwiczenia
Jodometryczne oznaczenie zawartości miedzi w próbce.
Opis wykonania
Mianowanie roztworu Na2S2O3
Odczynniki:
dwuchromian potasu 0.0167mol/dm3
kwas solny 10%
jodek potasu 10%
tiosiarczan sodu ok. 0.1mol/dm3
roztwór skrobi 0.5%
woda destylowana
Szkło i aparatura:
kolba stożkowa
pipeta Mohra na 10cm3
cylinder miarowy na 10cm3
biureta półautomatyczna
Wykonanie mianowania:
Do kolby stożkowej odpipetowano 10cm3 dwuchromianu potasu, następnie dodano 5cm3 kwasu solnego, oraz około 5cm3 KI. Tak przygotowaną próbkę natychmiast miareczkowano roztworem tiosiarczanu sodu, aż zmętnienie roztworu zaczęło znikać i pojawiło się żółtawe zabarwienie, następnie dodano kilka kropli roztworu skrobi i miareczkowano próbkę dalej do zmiany zabarwienia na zielony.
Mianowanie miedzi w roztworze
Odczynniki:
tiosiarczan sodu
badana próbka z miedzią
jodek potasu 10%
roztwór skrobi 0.5%
woda destylowana
Szkło i aparatura:
kolba stożkowa
cylinder miarowy na 10cm3
tryskawka
biureta półautomatyczna
Wykonanie oznaczenia:
Otrzymaną próbkę przeniesiono ilościowo do kolby stożkowej i dodano do niej około 15cm3 KI, oraz kilka kropli skrobi. Roztwór w kolbie zabarwił się na ciemnogranatowo. Próbkę miareczkowano tiosiarczanem sodu do całkowitego odbarwienia roztworu.
Obserwacje
Mianując tiosiarczan sodu na dwuchromian potasu obserwowano zanikanie zmętnienia próbki i roztwór powoli zmieniał kolor na żółty (po dodaniu 8.8cm3), wtedy dodano kilka kropli roztworu skrobi (ciemnogranatowa barwa roztworu) i podczas dalszego miareczkowania zabarwienie próbki zmieniło się na zielone (po dodaniu 0.7cm3). W sumie zużyto 9,5cm3 tiosiarczanu sodu.
Podczas oznaczenia zawartości miedzi w próbce w obecności wskaźnika skrobiowego obserwuje się odbarwienie ciemnogranatowego roztworu.
Równania przebiegających reakcji
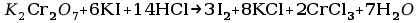
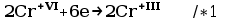

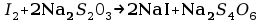
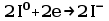
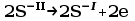
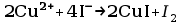
Wnioski wynikające z przeprowadzonych doświadczeń
Przy mianowaniu tiosiarczanu stosuje się dwuchromian potasu jako substancję podstawową (jest on utleniaczem) jednak jego właściwości utleniające są zbyt silne, aby miareczkować go bezpośrednio tiosiarczanem potasu dlatego dodaje się jodek potasu .W środowisku kwaśnym dwuchromian potasu reaguje z jodkiem potasu utleniając go do jodu. Dopiero wydzielony jod miareczkuje się tiosiarczanem sodu do zaniku barwy wskaźnika skrobiowego i zmiany barwy roztworu na zielony.
Przy oznaczeniu miedzi następuje również reakcja redukcji i utleniania. Miedź redukuje się do miedzi(I) utleniając jony jodkowe do jodu. Powstający wolny jod następnie miareczkuje się tiosiarczanem w obecności wskaźnika skrobiowego do momentu jego odbarwienia.
Wnioski ogólne dotyczące tematyki ćwiczenia
Przeprowadzane doświadczenia opierały się na reakcjach utleniania i redukcji. Przez zastosowanie odpowiedniego utleniacza czy reduktora dochodziło do wydzielenia się wolnego jodu który można było swobodnie miareczkować.
Obliczenia
obliczanie stężenia molowego tiosiarczanu
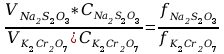
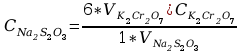
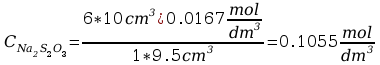
obliczanie masy miedzi w próbce
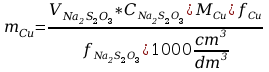
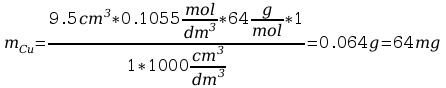
Wyszukiwarka
Podobne podstrony:
kryształy spr 3 bez filtra Cu
al -cu, Metalurgia i odlewnictwo metali nieżelaznych, nież - spr
kryształy spr 3 z filtrem Cu
Spr[1] adm i uznanie adm
08 03 KPGO Spr z realizacji
17 Rozp Min Zdr w spr szk czyn Nieznany
przetworka spr ostatnie
Informacje Cu
as spr 5 id 69978 Nieznany (2)
metr spr 5
belka spr podl
078c rozp zm rozp min gosp w spr szkolenia w dziedzinie bhp
99 SPOSOBÓW OKAZYWANIA DZIECIOM MIŁOŚCI, Różne Spr(1)(4)
Spr. 4-Techniki wytw, ZiIP, sem 1
klucz do age, Różne Spr(1)(4)
Wnioski do spr z elektry 3, PW SiMR, Inżynierskie, Semestr V, syf, laborki, Lab. Ukł. Napędowych
spr kl 5 dodaw ulamkow rozne mian2, Matematyka, kl 5
spr - koag pow, Sprawozdania, oczyszczanie wody
spr 2 - wizualizacja, ☆☆♠ Nauka dla Wszystkich Prawdziwych ∑ ξ ζ ω ∏ √¼½¾haslo nauka, mechanika płyn