AKADEMIA ROLNICZO - TECHNICZNA
W OLSZTYNIE
KATEDRA FIZYKI
ĆWICZENIA LABORATORYJNE Z FIZYKI
(CZĘŚĆ TEORETYCZNA)
ĆW. NR. 8:
Stany energetyczne w atomach. Doświadczenie Francka - Hertza
Krzysztof Dobosz
I MiBM gr 2 Zespół 3
Teoria Bohra przewiduje , że całkowita energia elektronu w atomie jest wielkością skwantowaną. Na energię elektronu w atomie składają się :
energia kinetyczna
energia potencjalna.
Energia kinetyczna , jaką ma elektron w atomie , jest określona wyrażeniem :
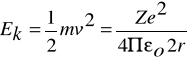
Gdzie:
Z - liczba atomowa pierwiastka
ρo -przenikalność elektryczna próżni
e - ładunek elektronu
r - promień orbity , po której krąży elektron
Wyrażenie na promień orbity wynika z warunku mechanicznej stabilności elektronu w atomie , który ma postać :
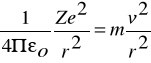
gdzie :
v - prędkość elektronu na danej orbicie
Prędkość elektronu na danej orbicie wyznacza się z pierwszego postulatu Bohra.
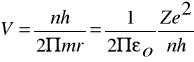
Gdzie:
n - główna liczba kwantowa
Wzór na promień dowolnej orbity , po której krąży elektron ma wyrażenie :
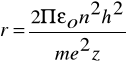
Energia potencjalna elektronu ma wyrażenie:
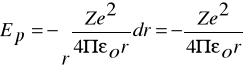
Tak więc energię całkowitą wyraża wzór:
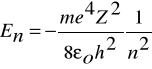
Doświadczenie Francka-hertza
W lampie znajdują się pary atomów rtęci. Ciśnienie pary dobiera się w ten sposób , aby na odcinku katoda siatka doszło co najmniej do jednego zderzenia elektronów z atomami rtęci. W celu utrzymania stałej temperatury pary należy lampę termostatować. Między anodą i siatką jest przyłożone ujemne napięcie rzędu 0,5v; ma ono zapobiegać emisji wtórnej elektronów z anody.
Pod wpływem energii dostarczonej katodzie z baterii żarzenia Bz emituje ona elektrony . Gęstość prądu emisyjnego w funkcji temperatury katody określa wzór Richardsana . Elektrony opuszczają katodę z prędkościami termicznymi , które można zaniedbać w porównaniu z prędkością uzyskaną w polu elektrycznym między katodą a siatką. Szybki elektron w zderzeniu z powolnymi atomami prawie nie zmienia swojej energii kinetycznej , a tylko zmienia kierunek, ze względu na dużą różnicę mas elektronu i atomu. Elektron odrzucony podczas zderzenia z powrotem w kierunku katody ulega zahamowaniu przez to pole , które go przed chwilą przyspieszyło. Jeżeli odbije się w bok , to samo można powiedzieć o składowej prędkości w kierunku pola. Wobec tego , w pewnej odległości od katody wszystkie elektrony mają jednakową energię kinetyczną , a tylko kierunki ruchu mogą być różne. Tak jest w przypadku zderzeń sprężystych elektronów z atomami .
W przypadku par rtęci odległość między elektronami wynosi zawsze 4,88eV, niezależnie od szczegółów konstrukcyjnych urządzenia. Przy małych napięciach prąd jest ograniczony przez ładunek przestrzenny. Obecność pary wpływa na ten ładunek w sposób mało istotny. W takim przypadku natężenie prądu anodowego zmienia się z prawem Ohma. W ten sposób wyjaśnia się początkowy wzrost natężenia prądu. Po osiągnięciu przez elektrony określonej energii kinetycznej , w tym przypadku 4,88eV , elektrony zderzają się niesprężyście z atomami rtęci , powodując ich wzbudzanie , same zaś zmniejszają energię kinetyczną o tę wartość. Nastąpiła zmiana energii kinetycznej elektronów na energię wzbudzenia atomów. Na skutek utraty energii przez elektrony oraz hamującego działania anody nie są one w stanie dotrzeć do anody w tym samym czasie co te , które się nie zderzyły z atomami , skutkiem czego natężenie prądu anodowego maleje.
Warstwa pary , w której zachodzi przekazywanie energii , przesuwa się w miarę wzrostu napięcia siatkowego w kierunku katody. Elektrony , które straciły energię , mogą ją odzyskać i dochodzą do siatki z energią wystarczającą , do pokonania napięcia hamującego. W ten sposób można wyjaśnić kolejny wzrost natężenia anodowego.
Z przebiegu doświadczenia Francka - Hertza wynika , że jeżeli energia , jaką mają w chwili zderzenia elektrony , jest mniejsza od energii wzbudzenia , to zachodzi zderzenie sprężste , a jeżeli energia ta jest równa energii wzbudzenia ,to zachodzi zderzenie niesprężyste.
Wyszukiwarka
Podobne podstrony:
F 40 KONTAKTOWA R NICA POT, Studia, Ogólne, Fiyzka, od romka, Fizyka lab
F 0X T, Studia, Ogólne, Fiyzka, od romka, Fizyka lab
F 55, Studia, Ogólne, Fiyzka, od romka, Fizyka lab
F 12, Studia, Ogólne, Fiyzka, od romka, Fizyka lab
F 44 WNIOSKI, Studia, Ogólne, Fiyzka, od romka, Fizyka lab
F 49FRANK HERTZA, Studia, Ogólne, Fiyzka, od romka, Fizyka lab
F 72, Studia, Ogólne, Fiyzka, od romka, Fizyka lab
F Q 24 P, Studia, Ogólne, Fiyzka, od romka, Fizyka lab
F 44 T, Studia, Ogólne, Fiyzka, od romka, Fizyka lab
F 7 P, Studia, Ogólne, Fiyzka, od romka, Fizyka lab
10fiz t, Studia, Ogólne, Fiyzka, od romka, Fizyka lab, Termopary
F 15 T, Studia, Ogólne, Fiyzka, od romka, Fizyka lab
F 92 T, Studia, Ogólne, Fiyzka, od romka, Fizyka lab
F 3 P, Studia, Ogólne, Fiyzka, od romka, Fizyka lab
F 15 P, Studia, Ogólne, Fiyzka, od romka, Fizyka lab
F 52 T, Studia, Ogólne, Fiyzka, od romka, Fizyka lab
FIZA PYT, Studia, Ogólne, Fiyzka, od romka, fizyka all, Fizyka lab, STARE, FU
więcej podobnych podstron