Czynniki zmniejszające ilość drgań.
Częstotliwości drgań podstawowych leżą poza obszarem IR i nie możemy ich obserwować
Pasma podstawowe są słabe i nie możemy ich obserwować
Częstotliwości podstawowe położone są blisko siebie i zlewają się w jedno pasmo
Występowanie pasm zdegenerowanych
Drganie podstawowe nie pojawia się w podczerwieni, bo nie wywołuje zmiany momentu dipolowego cząsteczki
Spektroskopia remanowska.
Polega na badaniu ruchu energii oscylacyjnej i rotacyjnej. Promieniowanie rozproszone zostaje rozszczepione i pada na detektor.
VRay - częst. Rayelowska
VSt - częst. Stockesowska
VAst - częst. Antystockesowska
∆V = VRay - VSt = VAst - VRay
Zastosowanie podczerwieni.
Identyfikacja związków - posługujemy się częstościami grupowymi - są to drgania związane z pewnym elementem związku. Stałość częstości grupowych stanowi podstawę analizy strukturalnej do identyfikacji wiązań wodorowych wewnątrz i międzycząsteczkowych.
Do określania stężeń w układzie statycznym i dynamicznym D = ε · l · c (w układzie statycznym c = const, a w dynamicznym zmienia się w czasie).
Spektrometria masowa (MS)
MS polega na wytwarzaniu się zw chem obojętnych cząst jonów i na badaniu zachodzącego następnie rozpadu tych jonów.
Spektrometr masowy - przyrząd który wytwarza i rozdziela naładowane cząstki.
ukł wprowadzania próbki
źródło jonów
analizator jonów
rejestrator
Jonizowanie próbki.
fotojonizacja PI => potencjał jonizacyjny zw org 5-13 eV, promieniowanie jon musi być >13 eV. Źródłem promieniowania są wyładowania elektryczne helu, które dostają fotony o energii 21;22 eV.
impakt elektronowy EI => bombardowanie elektronami. Wykorzystuje się elektrony emitowane przez rozżarzone włókno, przyspiesza się je różnicą potencjału.
pole elektryczne FI => zw. chem jest odparowywany w pobliżu elektrody o dużym dodatnim potencjale i małej krzywiźnie. Otrzymujemy duży gradient 107-???
jonizacja chemiczna => najrzadziej stosowana
Istota fizyczna.
W źródle jonów, jony o ład e- są przyspieszane potencjałem V. Ta energia przechodzi w en kinetyczną.
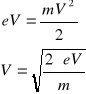
Jeśli dodatnio naładowany jon wpadnie w pole elektr to jony poruszają się po krzywych. Na jon działa siła dośrodkowa (eB) i odśrodkowa (mr2/re)
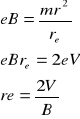
Magnetyczna siła dośrodkowa (siła Lorentza)
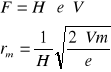
Reguły rozpadu.
związki w szeregu homologicznym ze ↑ ciężaru cz. wykazują zmniejszenie intensywności pasma macierzystego
względna intensywność jonu macierzystego ↓ wraz z rozgałęzieniem łańcucha
rozpad jonu jest uprzywilejowany w miejscu rozgałęzienia. Wiąże się to ze stabilnością
pasma macierzyste zw arom, heterocyklicznych alkenow, ukł cyklicznych posiadają dużą intensywność
w zw arom zaw podstawniki alkilowe najbardziej prawdopodobny jest rozpad wiązania β wzgl pierścienia arom.
cykliczne zw nasycone dążą do utraty bocznych łańcuchów poprzez rozerwanie wiązania α.
rozpadowi jonów często towarzyszy eliminacja trwałych, obojętnych cząst. (CO, CO2, H2O, H2S )
Istota fizyczna fragmentacji. (Krzywe Morse'a)
W stanie podst obojętna cząst jest na zerowym poziome en oscylacyjnej. Pod wpływem jonizacji wybicie elektr powoduje przejścia pionowe. Uzyskujemy jon o nadmiarze en wewnętrznej, ale niewystarczającej do rozpadu, jon będzie oscylował.
(Cząsteczki złożone) Powierzchnie M1+· i M2+· przecinają się we wspólnym punkcie X o takiej samej en oscylacyjnej.
Wyszukiwarka
Podobne podstrony:
Zmniejszona ilość zagadnień zP na5
Zmniejszona ilość zagadnień zP na5
chrysler grand cherokee zmieniona ilosc czynnika i oleju
czynniki zwiększające i zmniejszające efektywność
ilość czynnika klimatyzacji
Kurczliwość mięśnia sercowego, frakcja wyrzutu, czynniki zwiększające i zmniejszające kurczliwośćx
Czynnik środowiskowy, a czynnik ekologiczny
Analiza czynnikowa II
epidemiologia, czynniki ryzyka rola pielegniarki rak piersi szkola, nauczyciel
czynniki wpływające na zmeczenie psychiczne w pracy
Czynniki szkodliwe II(1)
CZYNNIKI ROZWOJU 2
Czynniki chemiczne w środowisku pracy prezentacja
więcej podobnych podstron