Wstęp teoretyczny
Równowagę dysocjacji słabego elektrolitu - kwasu octowego rozpuszczonego w wodzie można przedstawić za pomocą równania:
CH3COOH + H2O ↔ CH3COO- + H3O+
Stałą równowagi tego procesu zwaną termodynamiczną stałą dysocjacji Ka wyraża wzór:
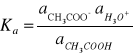
gdzie; ![]()
![]()
- równowagowe molowe aktywności jonów oraz niezdysocjowanych cząsteczek kwasu octowego
W roztworach rozcieńczonych wartości aktywności można zastąpić odpowiednimi stężeniami. Uzyskuje się wówczas stężeniową stała dysocjacji:
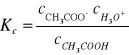
Stężenia jonów powstałych w procesie dysocjacji kwasu octowego są sobie równe i wynoszą: ![]()
, gdzie ![]()
oznacza stopień dysocjacji elektrolitu, natomiast c - całkowite stężenie roztworu. Stężenie niezdysocjowanego kwasu wynosi: ![]()
.Podstawienie powyższych wartości do wyrażenia na stałą dysocjacji prowadzi do wzoru zwanego prawem rozcieńczeń Ostwalda:
![]()
Zgonie z teorią Arrheniusa, stopień dysocjacji słabego elektrolitu ![]()
można wyrazić poprzez stosunek przewodnictw:
![]()
gdzie: ![]()
- przewodnictwo molowe słabego elektrolitu o stężeniu c, ![]()
- przewodnictwo molowe graniczne tego elektrolitu.
Jak wiadomo, przewodnictwo molowe roztworu elektrolitu ![]()
opisuje zależność:
![]()
gdzie: ![]()
- przewodnictwo właściwe, c- stężenie molowe
Przewodnictwo właściwe![]()
można opisać zależnością:
![]()
gdzie: ![]()
- przewodnictwo roztworu, l odległość między elektrodami, A - powierzchnia elektrod, Kn stała naczyńka
Stała dysocjacji kwasu octowego jest funkcją temperatury. Zgodnie ze statyką chemiczną , znajomość
Zależności Ka=f(T) pozwala wyznaczyć efekt energetyczny, czyli entalpię procesu ΔH opisanego przez daną stała równowagi. Rozważmy na wstępie dowolną równowagę chemiczną. W celu uzyskania temperaturowej zależności stałej równowagi reakcji, należy zróżniczkować względem temperatury T (przy stałym ciśnieniu) jedno z najważniejszych równania statyki chemicznej, przytoczone poniżej:
![]()
gdzie: ![]()
- standardowa entalpia swobodna reakcji, R- stała gazowa.
Zatem:
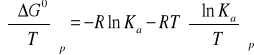
Z ogólnie słusznych zależności termodynamicznych wynikają następujące równania:
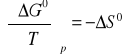
![]()
Przyrównanie stronami powyższych równań prowadzi do zależności zwanej izobarą vant`Hoffa:
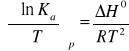
Z ostatniego równania wynika, że zmienność stałej równowagi reakcji wraz z temperatura jest ściśle związana ze standardową entalpia reakcji. Dogodniejsza w stosowaniu jest scałkowana postać tego równania:
![]()
Ostatnie równanie może być stosowane do wyznaczania entalpii reakcji, jeśli znane są wartości Ka w różnych temperaturach
Jak wcześniej wspomniano, dysocjacja elektrolityczna słabego kwasu jest procesem, któremu również towarzyszy efekt energetyczny - entalpia dysocjacji- ΔHdys. W roztworach rozcieńczonych termodynamiczna stała równowagi dysocjacji Ka jest w przybliżeniu równa stałej stężeniowej Kc Otrzymuje się wówczas:
![]()

Wyszukiwarka
Podobne podstrony:
Fizyczna27m, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna u
Sprawozdanie damiana nr 1, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i
poprawa II 25, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna
Chfizyczna5, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna u
moje 4, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna uł, Ch
wfizyczna9, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna uł
chemia fizyczna-ćwiczenie 22, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczn
fizyczna 20, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna u
fizyczna25, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna uł
Wstęp teoretyczny, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i anality
poprawa, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna uł, C
fIZYCZNA5, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna uł,
13 fiza word, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna
fizyczna nr 17 moja, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i anali
moje 18, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna uł, C
iza 25, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna uł, Ch
sprawozdanie 35 wstep, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i ana
więcej podobnych podstron