CZĘŚĆ TEORETYCZNA
Fotometria.
Fotometria to dział optyki zajmujący się pomiarem wielkości charakteryzujących promieniowanie świetlne (podczerwień, widzialne, ultrafiolet) i źródła tego promieniowania.
Rozróżniamy fotometrię:
Selektywna- badającą zależność wielkości fotometrycznych od długości fali
Nieselektywna - badającą moc promieniowania
Wielkości fotometryczne
światłość (kandela)
natężenie oświetlenia (luks)
strumień świetlny (lumen)
napromieniowanie (J/m²)
natężenie napromieniowania (W/m²)
gęstość kątowa strumienia energii (W/sr)
luminacja energetyczna ( W m²sr¹- ilość światła (ms)
naświetlenie (lxs)
Rodzaje widm i ich powstawanie
Ze względu na sposób powstania
widmo emisyjne - powstaje w wyniku emisji promieniowania przez ciało
absorpcyjne - powstaje w wyniku oddziaływania (przejścia lub odbicia) fali o widmie zazwyczaj ciągłym z substancją.
Widmo emisyjne - powstaje zwykle na skutek wzbudzenia elektromagentycznego elektronów atomów tworzących dane ciało i następnie powrót tych elektronów do stanu podstawowego. Po przejściu elektronu do stanu podstawowego następuje emisja kwantu promieniowania elektromagnetycznego równego różnicy energii poziomu wzbudzonego i podstawowego.
Ma postać jasnych, barwnych prążków(widmo liniowe) lub pasm (widmo pasmowe) w obszarze widzialnym na ciemnym tle albo zespołu barw przechodzących płynnie (od czerwieni do fioletu) jedna w drugą (widmo ciągłe).
Widma absorpcyjne powstają w wyniku pochłaniania przez ciało, przez które przechodzi promieniowanie o widmie ciągłym, fal o określonych długościach i w obszarze widzialnym, ma postać ciemnych prążków (lub pasm) na tle ciągłego widma emisyjnego. Dla atomów i prostych cząsteczek lokalizacja linii absorpcyjnych pokrywa się z odpowiednimi liniami emisyjnymi. Przykładem widma absorpcyjnego jest widmo Słońca (Fraunhofera linie).
Absorcjometria
Jest podstawową metodą identyfikacji związków chemicznych ich ilościowego oznaczania w zakresie widzialnym służy do określania stężenia barwnika w roztworach.
Prawo Lamberta-Beera
Prawo Lamberta określa ilościowo zależność między natężeniem I0 światła padającego na ciało a natężeniem I światła wychodzącego po drugiej stronie tego ciała:
I = I0. e-k*d
k - współczynnik absorpcji charakterystyczny dla danej substancji,
d - grubość warstwy, przez którą przeszło światło.
Dla roztworów (szczególnie dla roztworów barwnych)można zastosować prawo Beera, zgodnie z którym współczynnik absorpcji k jest proporcjonalny do stężenia roztworu c, czyli :
k = a.c
gdzie a oznacza współczynnik proporcjonalności zwany molowym współczynnikiem absorpcji.
Otrzymamy w ten sposób prawo Lamberta-Beera w postaci:
I = I0.e-a*c*d
Ekstynkcja i transmisja
Ekstynkcja- osłabienie natężenia wiązki światła przechodzącej przez ośrodek (np. powietrze, szkło) wskutek rozpraszania i pochłaniania. Ekstynkcje, definiujemy następująco:
Czasami potrzebna jest informacja o tym, jaką ilość światła przepuściła dana substancja. Informację tę daje nam wielkość zwana transmisją (lub przepuszczalnością). Definiujemy ją następująco:
Łatwo sprawdzić, że między ekstynkcją a transmisją zachodzi związek:
E=a*c
Gdzie a- współczynnik proporcjonalności obliczany ze wzoru
a=ln(1/T)
Zarówno ekstynkcja jak i transmisja dla danej substancji zależy od długości fali padającego na nią światła. Dlatego pomiarów dokonujemy za pomocą tak zwanych kolorymetrów, które oświetlają badaną substancję monochromatyczną (jednobarwną) wiązką światła i porównują jej natężenie przed i po przejściu przez substancję.
Barwy ciał
Proces widzenia barw jest zjawiskiem fizjologicznym związanym z budową siatkówki oka. Barwa ciała nie jest jego cechą stałą, zależy od rodzaju światła, przez które dane ciało jest oświetlone oraz od tego, czy światło odbija się od ciała czy przez nie przechodzi.
Barwę charakteryzują: odcień, natężenie (jasność), nasycenie i czystość.
Odcień (ton, chromatyczność) daje barwie jej nazwę (np. czerwony, żółty, niebieski), a określa go odpowiadająca mu długość fali elektromagnetycznej w zakresie od 400 nm do 700 nm.
Barwa prosta(widmową, spektralną, monochromatyczną) -barwa wywołana promieniowaniem o ściśle określonej długości fali (np. kolejne barwy tęczy).
Barwy zasadnicze - wszystkie barwy proste z barwami purpurowymi (powstałymi ze zmieszania barwami fioletowych z czerwonymi).
Nasycenie barw maleje wraz z domieszką światła białego (np. barwa czerwona, różowa, biała),
Czystość barwy maleje wraz ze zbliżaniem się do czerni (np. czerwona, czerwonobrązowa, czerń).
Chromatyczność- jakościowa cechą barwy obejmującą jej odcień i nasycenie
Barwy achromatyczne (niekolorowe) obejmują różne odcienie szarości od bieli do czerni. Mieszanie różnych barw chromatycznych prowadzi do innej barwy — tzw. addytywne mieszanie barw.
Barwy dopełniające- barwy, których mieszanie daje barwę achromatyczną (biel), (np. fioletowa 400 nm i żółta 570 nm; czerwona 650 nm i niebieskozielona 490 nm);
Barwy podstawowe 3 barwy proste wybrane tak, że po zmieszaniu dowolnych 2 spośród nich nie jest możliwe uzyskanie trzeciej. Przez dodanie w różnych proporcjach 3 barw podstawowych można uzyskać barwy chromatyczne lub biel (a zatem tę samą barwę można uzyskać przez zmieszanie różnych barw podstawowych).
Przyczyną zabarwienia ciał jest selektywna (występująca intensywnie tylko dla pewnych długości fal) absorpcja, odbicie lub transmisja światła. Zabarwienie ciał w wyniku interferencji światła powstaje głównie przy odbiciu światła od przedniej i tylnej powierzchni cienkich przezroczystych warstw (np. baniek mydlanych).
Barwne ciała oświetlone światłem białym odbijają tylko jeden lub dwa ze składników światła białego, a pozostałe pochłaniają.
Ciało nieprzezroczyste ma taką barwę w świetle odbitym, jaka powstaje ze zmieszania wszystkich barw odbijanych przez to ciało. Każdy barwnik rozprasza właściwie sobie składnik światła białego; odpowiada mu określone miejsce w widmie światła białego tzn. określony zakres długości fal.
Filtry ciała przezroczyste, które przepuszczają tylko jedną barwę tzn. pochłaniają prawie wszystkie rodzaje światła z wyjątkiem jednego.
CZĘŚĆ PRAKTYCZNA
1. Tabela wyników pomiarów.
filtr [nm] |
390 |
430 |
480 |
535 |
590 |
610 |
680 |
Transmisja T cieczy [%] |
91 |
92 |
88 |
71 |
41 |
27 |
4 |
stężenie c [%] |
2 |
4 |
6 |
8 |
10 |
x |
Ekstynkcja E [%] |
0,33 |
0,57 |
0,85 |
1,1 |
1,4 |
0,78 |
Transmisja T [%] |
|
|
|
8 |
4 |
|
2. Obliczenia.
W celu obliczenia ekstynkcji na podstawie transmisji korzystamy ze wzoru:
![]()
celem ćwiczenia jest narysowanie wykresu funkcji:
![]()
, gdzie:
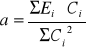
Nieznane stężenie roztworu odczytujemy z wykresu T(c):
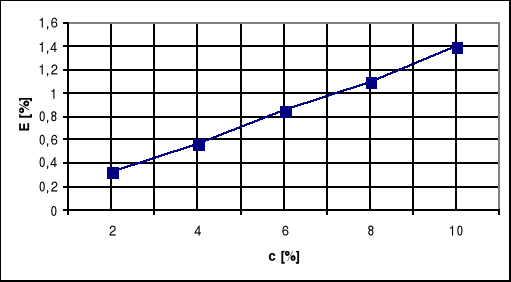
3. Spostrzeżenia i wnioski.
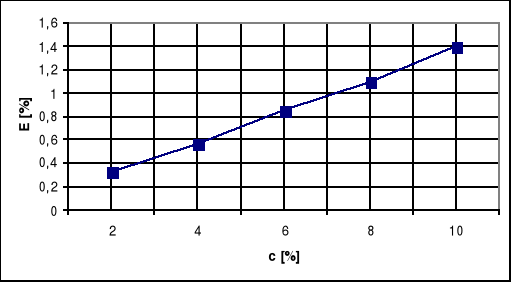
Widzimy, że wraz ze wzrostem długości fali świetlnej zmniejsza się przepuszczalność fali świetlnej dla kuwety z 10% roztworem CuSo4. Jednak wniosek jaki nasuwa się po wykonaniu ćwiczenia polega na stwierdzeniu, że wraz ze wzrostem stężenia roztworu wzrasta wartość ekstynkcji. Nieznane stężenie roztworu wynosi ok. 5,3%.
Wyszukiwarka
Podobne podstrony:
Powtorzenie mechanika, Wojskowo-lekarski lekarski umed łódź giełdy i materiały I rok, Biofizyka I ro
Test 2012 z psychologii, Wojskowo-lekarski lekarski umed łódź giełdy i materiały I rok, Psychologia
Ocena-rozwoju-psychoruchowego, wojskowo-lekarski umed łódź giełdy i materiały III rok, pediatria
BIO z forum odp , Wojskowo-lekarski lekarski umed łódź giełdy i materiały I rok, Biologia medyczna,
M3 - Badanie progu czucia wibracji, Wojskowo-lekarski lekarski umed łódź giełdy i materiały I rok, B
giełda histologia 2012 - II koło, Wojskowo-lekarski lekarski umed łódź giełdy i materiały I rok, His
Parazytologia III wejściówka, Wojskowo-lekarski lekarski umed łódź giełdy i materiały I rok, Biologi
strzelectwo opracowane pytania, Wojskowo-lekarski lekarski umed łódź giełdy i materiały I rok, Strze
formy inwazyjna - ćw. 1, Wojskowo-lekarski lekarski umed łódź giełdy i materiały I rok, Biologia med
mechanika notatki, Wojskowo-lekarski lekarski umed łódź giełdy i materiały I rok, Biofizyka I rok
Układ pokarmowy, Wojskowo-lekarski lekarski umed łódź giełdy i materiały I rok, Anatomia I rok
Sprawozdanie E3, Wojskowo-lekarski lekarski umed łódź giełdy i materiały I rok, Biofizyka I rok
POPRAWIONE - strzelectwo opracowane pytania, Wojskowo-lekarski lekarski umed łódź giełdy i materiały
Kopia O2 - Badanie dyfrakcji światła laserowego, Wojskowo-lekarski lekarski umed łódź giełdy i mater
biofizyka pytania częściowo opracowane, Wojskowo-lekarski lekarski umed łódź giełdy i materiały I ro
Histologia. Notatki ćw. 18(1), Wojskowo-lekarski lekarski umed łódź giełdy i materiały I rok, Histol
mechanika giełda, Wojskowo-lekarski lekarski umed łódź giełdy i materiały I rok, Biofizyka I rok
więcej podobnych podstron