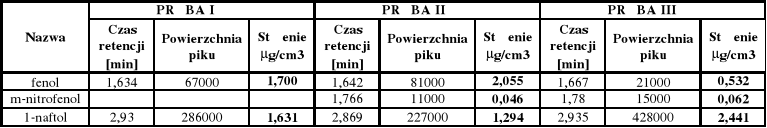
Mieszanina fenoli: pompa: faza ruchoma: 60% MeOH / 40% H2O
CHROMATOGRAFIA CIECZOWA
Ćwiczenie CH - 1 i CH - 2
Oznaczanie fenoli w mieszaninie: (fenol, 2-amino-4,6-dinitrofenol, p-nitrofenol, m-nitrofenol, o-nitrofenol, 1-naftol) oraz oznaczanie w mieszaninie benzenu i pochodnych (benzen, toluen, chlorobenzen, jodobenzen, nitrobenzen, o-ksylen).
Chromatografia jest grupą metod analizy, w których podstawowym elementem jest rozdzielenie mieszanin jednorodnych substancji na składniki. Odbywa się to na podstawie podziału mieszaniny między fazę nieruchomą (stacjonarną) i ruchomą układu chromatograficznego. Rozdzielenie to następuje w skutek różnej dla poszczególnych składników dynamiki wymiany masy pomiędzy fazami: ruchomą i nieruchomą. Warunkiem analizowania próbek jest ich rozpuszczalność w odpowiednich rozpuszczalnikach.
Celem ćwiczenia jest ilościowe oznaczenie składników mieszaniny. Metoda opiera się na fakcie, że wielkość powierzchni piku jest proporcjonalna do stężenia odpowiedniego składnika w mieszaninie.
Aparatura i odczynniki:
chromatograf cieczowy Hewlett Packard Model 1050 z dekoderem absorpcji UV
mikrostrzykawka
roztwory wzorcowe fenoli w alkoholu metylowym
roztwory benzenu i pochodnych w alkoholu metylowym
roztwór (zadanie) zawierające fenole o nieznanym składzie
roztwór (zadanie) zawierające benzen i jego pochodne o nieznanym składzie
kolbki miarowe, pipety, metanol, woda.
Wykonanie ćwiczenia
Wykonanie ćwiczenia sprowadzało się do wykonania roztworów analizowanych próbek. W tym celu odmierzono pipetą 0,5 cm3 badanej mieszaniny fenoli i dopełniono w 3 kolbach miarowych o pojemności 10 cm3 do kreski roztworem składającym się z 60% metanolu i 40% wody. Do wykonania roztworów benzenu i jego pochodnych wzięto 0,7 cm3 badanego roztworu i dopełniono w 3 kolbach miarowych o pojemności 10 cm3 do kreski mieszaniną 75% metanolu i 25% wody. Następnie wykonano chromatogramy mieszanin wstrzykując po 20 μl każdego z roztworów do chromatografu. Z chromatogramu odczytano na podstawie czasu retencji nazwy poszczególnych składników mieszanin a na podstawie liczby impulsów każdej substancji odczytano z wykresu (lub z równania) stężenia poszczególnych składników mieszaniny.
Wyniki pomiarów:

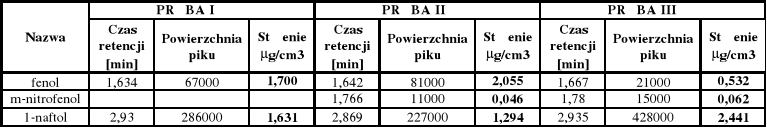
Mieszanina fenoli: pompa: faza ruchoma: 60% MeOH / 40% H2O
przepływ: 1 cm3 / min ciśnienie ok. 130 bar
Czasy retencji [min] : stężenie [μg/cm3] :
fenol - (1,6 - 1,8) y = 39,4 ⋅ x + 0,5
m-nitrofenol - (1,8 - 2,0) y = 238,1 ⋅ x +14,9
o-nitrofenol - (2,1 - 2,3)
1-naftol -(2,8 - 3,1) y = 175,3 ⋅ x + 17,5
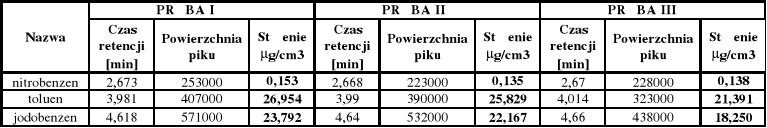
Mieszanina benzenu: pompa: faza ruchoma: 75% MeOH / 25% H2O
przepływ: 0,6 cm3/min ciśnienie: ok. 75 bar
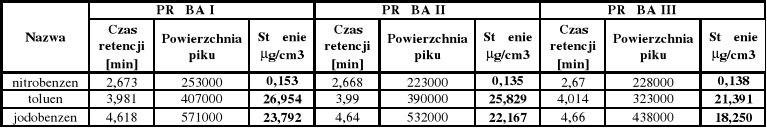
Czasy retencji [min] : Stężenie [μg/cm3] :
nitrobenzen - (2,5 - 2,7) y = 1644,2 ⋅ x +7,2
benzen - (3,1 - 3,3)
toluen - (3,8 - 4,0) y = 15,1 ⋅ x - 18,6
jodobenzen - (4,5 - 4,7) y = 24,0 ⋅ x - 18,6
o-ksylen - (5,0 - 5,2)
Analiza wyników
Średnia arytmetyczna zbiorowości próbnej:
![]()
Odchylenie standardowe pojedynczego wyniku
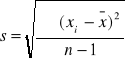
Odchylenie standardowe średniej arytmetycznej
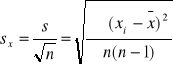
Przedział ufności:
95% dla k = 2 tstudenta = 4,303
![]()
[ ]
fenol:
x = (1,7 + 2,055 + 0,532) / 3 = 1,429
S = (1,27 / 2)1/2 = 0,7968
Sx = 0,7968 / √3 = 0,46
X = 1,429 ± 4,303 ⋅ 0,46 =1,429 ± 1,98 μg cm3 Cfenol = 1,429 ± 1,98 μg/cm3
m-nitrofenol:
x = (0,46 + 0,62) / 2 = 0,54
S = (0,013 / 1)1/2 = 0,114
Sx = 0,114 / √2 = 0,081
X = 0,54 ± 4,303 ⋅ 0,081 = 0,54 ± 0,35 Cm-nitrofenol = 0,54 ± 0,35 μg/cm3
1-naftol:
x = (1,631 + 1,294 + 2,441) / 3 = 1,786
S = (0,695 / 2)1/2 = 0,589
Sx = 0,589 / √3 = 0,34
X = 1,786 ± 4,303 ⋅ 0,34 = 1,786 ± 1,463 C1-naftol = 1,786 ± 1,463 μg/cm3
Mieszanina benzenu
nitrobenzen:
x = (0,153 + 0,135 + 0,138) / 3 = 0,142
S = (0,0002/2)1/2 = 0,01
Sx = 0,01 / √3 = 0,006
X = 0,142 ± 4,303 ⋅ 0,006 = 0,142 ± 0,026 Cnitrobenzen = 0,142 ± 0,026 μg/cm3
toluen:
x = (26,954 + 25,829 + 21,391) / 3 = 24,725
S = (17.303 / 2)1/2 = 2,941
Sx = 2,941 / √3 = 1,698
X = 24,725 ± 4,303 ⋅ 1,698 = 24,725 ± 7,306 Ctoluen = 24,725 ± 7,306 μg/cm3
jodobenzen:
x = (23,792 + 22,167 + 18,250) / 3 = 21,403
S = (16,232 / 2)1/2 = 2,849
Sx = 2,849 / √3 = 1,645
X = 21,403 ± 4,303 ⋅ 1,645 = 21,403 ± 7,078 Cjodobenzen = 21,403 ± 7,078 μg/cm3
Wnioski:
Różnice w odczytach różnych próbek tych samych roztworów wynikały prawdopodobnie z niedokładnego odmierzenia mieszaniny fenoli do kolbek, oraz z niedokładnego dopełnienia kolb miarowych do kreski roztworem metanolu. Podczas badania mieszaniny fenoli w chromatografie było ustawione zbyt duże ciśnienie (powyżej 130 bar) co spowodowało niedokładne rozdzielenie składników (przesunięty czas retencji m-nitrofenolu). Na końcowy wynik miało wpływ również stosunkowo niskie stężenie poszczególnych składników, oraz czystość kolb użytych do analizy.
Wzory strukturalne:
OH - fenol
NO2 - nitrobenzen
CH3 - toluen
J - jodobenzen