Jolanta Lipowska Kraków, dn.08.04.2008
Gr. 14C2
Wtorek godz.1700
Wyznaczanie ciepła topnienia lodu
1. Wstęp
Ciepło to energia przekazywana przez kontakt termiczny. Ciepło właściwe, to ilość ciepła potrzebna do ogrzania jednostkowej masy danej substancji o jeden K lub o 1oC.
Przepływ ciepła najczęściej wiąże się ze zmianą temperatury, jednak nie zawsze tak jest.
Jeżeli ciało stałe, krystaliczne ogrzewamy, to jego temperatura początkowa wzrasta, aż do temperatury topnienia Tt. Dalsze ogrzewanie ciała nie zmienia jego temperatury, a jedynie powoduje stopniowe topnienie. Całe ciepło dostarczane do ciała jest zużywane na zmianę rodzaju oddziaływań międzycząsteczkowych, czyli na zmianę energii potencjalnej. Energia kinetyczna cząsteczek, a więc również temperatura, nie zmienia się. Jeżeli całe ciało przejdzie w stan ciekły, to przy dalszym dostarczaniu ciepła temperatura znowu zaczyna wzrastać.
Przebieg zmian temperatury przy procesie ogrzewania lodu:
T
lód lód + woda woda
Krzywa ogrzewania substancji krystalicznej ΔQ
W układzie odizolowanym termicznie od otoczenia, na którym nie jest wykonywana żadna praca makroskopowa, całe ciepło oddane przez część układu musi zostać pobrane przez pozostałe części układu. Kalorymetr jest naczyniem zbudowanym w taki sposób, aby zminimalizować kontakt termiczny z otoczeniem. Gdy przygotujemy kalorymetr z wodą o znanej masie mw w temperaturze Tp i wrzucimy do niego masę ml topniejącego lodu, lód roztopi się i ustali się temperatura końcowa Tk. Z jednej strony woda i kalorymetr oddają ciepło aż do ustalenia się temperatury końcowej Tk, z drugiej strony ciepło to zostaje wydatkowane najpierw na roztopnienie się lodu, a następnie podgrzanie wody powstałej z roztopionego już lodu do temperatury Tk.
2. Plan pracy - wyznaczanie ciepła topnienia lodu
Sprawdzono czy waga jest wypoziomowana
Zważono pusty kalorymetr razem z mieszadełkiemM
Napełniono kalorymetr do połowy objętości letnią wodą i ponownie zważono
Po ustabilizowaniu temperatury wody w kalorymetrze - zanotowano ją
Wrzucono kilka kawałków osuszonego lodu do kalorymetru i mieszano wodę do momentu gdy kawałki lodu całkowicie roztopiły się
Zanotowano temperaturę po ustabilizowaniu
Zważono kalorymetr w celu ustalenia masy roztopionego lodu
Pomiary powtórzono kilka razy
3. Plan pracy - wyznaczanie ciepła właściwego kalorymetru
Zważono ponownie pusty kalorymetr z mieszadełkiem
Napełniono kalorymetr zimną wodą i ponownie zważono
Po ustabilizowaniu temperatury wody w kalorymetrze - zanotowaną ją
Dolano gorącej wody
Zamieszano i zważono kalorymetr
Zanotowano temperaturę po ustabilizowaniu
4. Wyniki pomiarów do ciepła topnienia lodu
M kalorymetru [kg] ± 0,0001 kg |
M kalorymetru z wodą [kg] ± 0,0001 kg |
M kalorymetru z wodą po dodaniu lodu [kg] ± 0,0001 kg |
M wody [kg] ± 0,0001 kg |
M lodu [kg] ± 0,0001 kg |
T początkowa [°C] ± 0,2°C |
T końcowa [°C] ± 0,2°C |
Δ T [°C] ± 0,2°C |
0,4082 |
1,0097 |
1,0301 |
0,6015 |
0,0204 |
24,8 |
21,6 |
3,2 |
0,4082 |
1,0301 |
1,0765 |
0,6219 |
0,0464 |
21,6 |
15,4 |
6,2 |
0,4082 |
1,0765 |
1,1395 |
0,6683 |
0,0630 |
15,4 |
8,2 |
7,2 |
0,4082 |
1,1395 |
1,2076 |
0,7313 |
0,0681 |
8,2 |
2,2 |
6,0 |
0,4082 |
1,0654 |
1,0995 |
0,6572 |
0,0341 |
22,6 |
18,2 |
4,4 |
5. Opracowanie wyników
ciepło topnienia lodu - qt - wyznaczono po przekształceniu wzoru na bilans cieplny:
( mwCw + mkCk )(Tp - Tk) = ml [ qt + Cw( Tk - 0°C )]
( mwCw + mkCk )(Tp - Tk)
qt = - CwTk
ml
cw - ciepło właściwe wody - 4187,0 J⋅ kg-1⋅K-1
mw - masa wody
ck - ciepło właściwe kalorymetru (wartość tablicowa dla aluminium)- 880,0 J⋅ kg-1⋅K-1
mk - masa kalorymetru
ml - masa lodu
⇒ wyznaczenie ciepła topnienia lodu dla pierwszego pomiaru
( 4187,0 ⋅ 0,6015 + 880,0 ⋅ 0,4082)( 24,8 - 21,6)
qt1 = - ( 4187,0 ⋅ 21,6 ) = 360964,2 [J/kg]
0,0204
⇒ obliczenia dla pozostałych pomiarów wykonano w analogiczny sposób
wyniki umieszczono w tabelce:
Nr. pomiaru |
qt - ciepło topnienia lodu [J/kg] |
Średnie qt |
1 |
360964,2 |
327269,2 |
2 |
331453,2 |
|
3 |
326510,9 |
|
4 |
292213,2 |
|
5 |
325204,7 |
|
⇒ Wyznaczenie niepewności pomiarowych otrzymanych wyników metodą różniczki zupełnej (błąd bezwzględny).
dokładność wagi - 0,0001 kg
dokładność termometru - 0,2°C
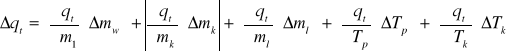
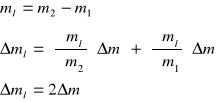
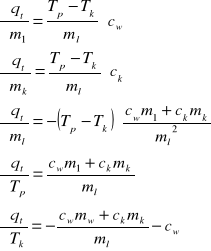
∆mw = 0,1g = 0,0001kg
∆mk = 0,1g = 0,0001 kg
∆ml = 0,1 g = 0,0001 kg
∆Tp = 0,2°C
∆Tk = 0,2°C
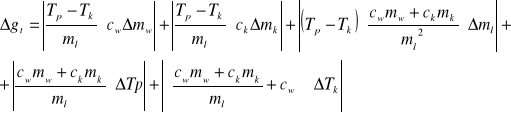
3,2 3,2 4187 ⋅ 0,6015 + 880⋅ 0,4082
Δqt = ⋅ 4187 ⋅ 0,0001 + ⋅ 880 ⋅ 0,0001 + 3,2⋅ ⋅ 0,0001
0,0204 0,0204 ( 0,0204)2
4187 ⋅ 0,6015 + 880⋅ 0,4082 4187 ⋅ 0,6015 + 880⋅ 0,4082
+ ⋅ 0,2 + + 4187 ⋅ 0,2 =
0,0204 0,0204
= 59555,1 [J/kg]
⇒ Obliczenia dla pozostałych pomiarów wykonano w analogiczny sposób
Nr. pomiaru |
∆qt [J/kg] |
1 |
59555,1 |
2 |
27302,5 |
3 |
21541,9 |
4 |
21419,6 |
5 |
38571,6 |
qt = 360964,2 ± 59555,1
qt = 331453,2 ± 27302,5
qt = 326510,9 ± 21541,9
qt = 292213,2 ± 21419,6
qt = 325204,7 ± 38571,6
⇒ wyznaczenie niepewności wartości średniej ( x ).
Wykorzystano wzór na odchylenie standardowe średniej arytmetycznej S![]()
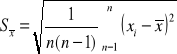
![]()
- wartości ciepła topnienia obliczone z kolejnych pomiarów
![]()
- średnie ciepło topnienia
|
|
|
|
360964,2 |
327269,2
|
1135353025 |
2386619196 |
331453,2 |
|
17505856 |
|
326510,9 |
|
575018,89 |
|
292213,2 |
|
1228923136 |
|
325204,7 |
|
4262160,25 |
|
![]()
= 48853,04
⇒ wyznaczenie procentowej wielkości błędu:
Δqt 48853,04
= ⋅ 100% = 14,9%
qt 327269,2
6. Wnioski
Wartość tablicowa ciepła topnienia lodu wynosi: 332000 [J/kg]
Wyznaczona przez nas wartość średnia ciepła topnienia qt= ( 327269 ± 48853 ) [J/kg]
Odbiega od wartości tablicowej. Ta różnica może wynikać z niedokładności przyrządów, niedokładnego osuszania kawałków lodu lub niedokładnego odczytywania wyników przez obserwatora.
7. Wyniki pomiarów do ciepła właściwego kalorymetru
waga kalorymetru - 407,7g = 0,4077 kg
waga kalorymetru z zimną wodą - 850,3g = 0,8503kg
temperatura zimnej wody 24,4°C
waga kalorymetru z zimną wodą + ciepłą wodą - 993,0g = 0,9930kg
temperatura końcowa 36,8°C
8. Opracowanie wyników
m1 ( masa zimnej wody) = 0,8503 - 0,4077 = 0,4426kg
m2 ( masa ciepłej wody) = 0,9930 - 0,8503 = 0,1427kg
T1 (temperatura zimnej wody) = 24,4°C
T (temperatura końcowa) = 36,8°C
⇒ obliczono temperaturę wody ciepłej ze wzoru:
( cwm1 + ckmk )(T - T1) = cwm2( T2 - T)
( cwm1 + ckmk )(T - T1)
T2 = + T
cwm2
1
Wyszukiwarka
Podobne podstrony:
spr od diany wyznaczanie ciepla topnienia lodu, biologia uj, biologia II, fizyka
Sprawko M21, biologia uj, biologia II, fizyka, jakies sprawozdania i inne
m16, biologia uj, biologia II, fizyka
sprawozdanie wlasne, biologia uj, biologia II, fizyka
e3, biologia uj, biologia II, fizyka
aneks, biologia uj, biologia II, fizyka
Terenowka 2 od Kozy[1], Biologia II, Terenówki- zwierzęta i rośliny
fizyka o7, biologia uj, biologia II, fizyka
wyznaczanie ciep-a topnienia lodu, Studia PWr W-10 MBM, Semestr II, Fizyka, Fizyka - laborki, Fizyka
EKOLOGIA, biologia uj, biologia II, eko
BIOL.KOM pytania chyba Witaliński, biologia uj, biologia II, biologia komorki, egz
eko sprawozdanie zuk, biologia uj, biologia II, eko
Western blot - TEORIA, BIOLOGIA UJ, ROK II, Semestr 1, Biologia Komórki
wyklady z bioetyki 2012, biologia i geografia - UJ, I rok II stopnia, bioetyka
ZADANIA BIOCHEMIAIIROK (1), biologia uj, biologia II, biochemia
więcej podobnych podstron