ZAGADNIENIA TEORETYCZNE
Budowa wszystkich ciał makroskopowych jest cząsteczkowa, przy czym owe cząsteczki są w ciągłym ruchu i oddziaływają między sobą pewnymi siłami. Siły oddziaływania międzyatomowego są odpowiedzialne za powstawanie cząsteczek. Siły oddziaływania miedzy cząsteczkami prowadzą do tworzenia się struktur wielomolekularnych, w szczególności do powstania ciał stałych i cieczy. Zbliżanie do siebie atomów powoduje pojawienie się sił przyciągających, które najpierw wzrastają w miarę zmniejszania odległości miedzy jądrami atomów, a potem zmniejszają się aż w końcu przechodzą w siły odpychające. Gdy siła oddziaływania jest zerowa dla pewnej odległości r oraz energia potencjalna osiąga minimalną wartość cząstka jest w stanie równowagi trwałej. Ową odległość r nazywamy długością wiązania atomowego. Ze względu na strukturę wiązań możemy wyróżnić wiązania jonowe (powstają w wyniku przyciągania się elektrostatycznego) oraz kowalencyjne (powstaje dzięki 2 elektronom - po jednym z każdego atomu - ale jako para należą jednocześnie do jednego jak i drugiego atomu).
W przypadku cząsteczki wody atomy wodoru połączone są z atomem tlenu wiązaniem kowalencyjnym. W cząsteczce wody ładunek ujemny jest przesunięty w kierunku atomu tlenu (większa zdolność przyciągania elektronów przez atomy tlenu), a co za tym idzie - ładunek dodatni jest przesunięty w kierunku atomów wodoru. W rezultacie cząsteczka wody ma charakter dipolowy (o określonym momencie dipolowym).
W cieczach odległości między cząsteczkami są porównywalne z ich wymiarami, dlatego ważne są też oddziaływania między cząsteczkowe. W wodzie występują tzw. siły van der Wallsa. Są to siły międzycząsteczkowe w krysztale, mające tę samą naturę co siły przyciągania się cząsteczek w gazach.
W przypadku wody, elektrycznie spolaryzowane cząsteczki łączą się z sąsiednimi cząsteczkami wiązaniami wodorowymi (słabe wiązanie tworzące mostek wodorowy). Przyjmuje się, że struktura wody ma charakter kwazikrystaliczny (zmienny w czasie), o uporządkowaniu bliskim względem najbliższych sąsiadów. Woda zawiera cząsteczki swobodne, ale również grupy cząsteczek powiązanych ze sobą wiązaniami wodorowymi. Te właśnie wiązania wodorowe są odpowiedzialne za oddziaływania cząsteczek i za szczególne właściwości wody i lodu. Większość cieczy zwiększa swoją objętość wraz ze wzrostem temperatury. Woda jest jednak wyjątkiem. Powyżej 4![]()
zachowuje się „normalnie” jednak w zakresie temperatur od 0![]()
do 4![]()
kurczy się aby w temperaturze 4![]()
mieć najmniejszą objętość (największą gęstość). Wynika z tego, że obniżając temperaturę woda rozszerza się. Jest to skutkiem asocjacji (łączenia się) cząsteczek wody, w wyniku czego w temperaturze 0![]()
tworzy się heksagonalna struktura lodu z dużymi otwartymi przestrzeniami między ściankami kryształu. Konsekwencją takich procesów jest zwiększenie objętości wody o około 10%. W czasie topnienia wiązania wodorowe pękają a kryształki przechodzą w stan ciekłej wody.
OPIS DOŚWIADCZENIA
Aby zaobserwować rozszerzalność wody w zależności od temperatury posłużyliśmy się specjalnym naczyńkiem z kapilarą. Dzięki mieszaninie chłodzącej (lód i sól) mogliśmy obniżyć temperaturę wody do 0![]()
. Do ogrzania posłużyło nam otaczające powietrze.
Jak można było się spodziewać i jak wynika z wykresu woda w czasie ochładzania zmniejszała swoją objętość, tak długo, aż osiągnęła temperaturę 4![]()
. W czasie dalszego ochładzania poziom wody w kapilarze zaczął się podnosić. Warto przy tej okazji zauważyć, iż wykres ma charakter paraboliczny. Oznacza to, iż w miarę jak temperatura spadała ku 4![]()
objętość wody malała coraz wolniej natomiast po przekroczeniu tej temperatury i zbliżaniu się ku 0![]()
poziom wody rósł szybciej.
Odwrotna sytuacja miała miejsce, gdy naczyńko wyjęliśmy z mieszaniny chłodzącej (ogrzewanie). Wraz ze wzrostem temperatury woda „kurczyła” się do temperatury 4![]()
, w której ponownie osiągnęła minimum swojej objętości. W trakcie dalszego podnoszenia temperatury poziom wody również zaczął wzrastać. Podobnie jak w przypadku ochładzania wykres także przypomina parabolę.
Maksymalny przyrost wysokości słupa wody w doświadczeniu wniósł 30 milimetrów dla temperatury 11![]()
- przy czym 0 milimetrów przyjmujemy dla 4![]()
. Wysokość słupa wody dla 0![]()
wyniosła 12 milimetrów.
Wiemy, że gęstość jest to ilość masy przypadającej na daną objętość. Biorąc pod uwagę, że masa wody w doświadczeniu nie zmieniała się, łatwo wywnioskować, iż największa gęstość była w momencie najmniejszej osiągniętej objętości - czyli w temperaturze 4![]()
.
Aby obliczyć maksymalną gęstość skorzystamy z danych tablicowych. Otóż gęstość wody dla temperatury 10°C wynosi δ=0,9997*103 [kg*m-3]. Masa wody jest stała.
Czyli:
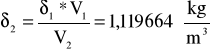
Przyjąłem, że wysokość kapilarki w temperaturze 10°C jest równa 0,25m+0,03m, natomiast w temperaturze 4°C (największa gęstość była w momencie najmniejszej osiągniętej objętości - czyli w temperaturze 4![]()
). jest równa 0,25m
WNIOSKI
Doświadczenie to pokazało, iż woda zachowuje się inaczej niż inne ciecze. Dodatkowo można zauważyć, że objętość wody nie zależy od temperatury w sposób liniowy. Można się domyślać, iż przy dalszym podnoszeniu temperatury powyżej 11![]()
(ochładzaniu poniżej 0![]()
- przejście wody w stan stały skupienia) woda rozszerza się bardzo szybko. Ciekawe jest też to, że wykres nie jest symetryczny względem prostej przechodzącej przez punkt 4![]()
. Ćwiczenie tłumaczy też zjawisko unoszenia się lodu na powierzchni wody. Lód ma o wiele mniejszą gęstość niż woda i właśnie dlatego może w niej pływać.
Dokładność pomiaru temperatury wynosi 0,1°C. Odczyt temperatury wydaje mi się, iż był prawidłowy, ponieważ temperatura wody w całym naczyńku była równomierna (dzięki mieszadełku).
Natomiast dokładność pomiaru wysokości słupa w kapilarze wynosi 1mm.
Wyszukiwarka
Podobne podstrony:
Anomalna rozszerzalność wody, Studia, Pracownie, I pracownia, 29 Anomalia rozszerzalności cieplnej w
25, Studia, Pracownie, I pracownia, 25 Wyznaczanie współczynnika rozszerzalności cieplnej metali za
cw25, Studia, Pracownie, I pracownia, 25 Wyznaczanie współczynnika rozszerzalności cieplnej metali z
Numer pomiaru, Studia, Pracownie, I pracownia, 28 Wyznaczanie współczynnika rozszeżalności liniowej
ROZSZERZALNOŚĆ TEMPERATUROWA, Studia, Pracownie, I pracownia
28 - NAPISAĆ, Studia, Pracownie, I pracownia, 28 Wyznaczanie współczynnika rozszeżalności liniowej d
Badanie wahadła skrętnego, Studia, Pracownie, I pracownia, 7 Badanie drgań wahadła skrętnego {torsyj
24 - oddane 21.04.2010, Studia, Pracownie, I pracownia, 24 Wyznaczenie mechanicznego równoważnika ci
Wstęp 59, Studia, Pracownie, I pracownia, 59 Rezonans elektromagnetyczny, Waldek
m5 NP, Studia, Pracownie, I pracownia
OSCYLOSK, Studia, Pracownie, I pracownia, 51 Pomiary oscyloskopowe, Ludwikowski
Wstęp teoretyczny 32, Studia, Pracownie, I pracownia
Sprawozdanie M7w, Studia, Pracownie, I pracownia
INSTRUKCJE, cw29 wstep, ANOMALNA ROZSZERZALNOŚĆ WODY 29
76, Studia, Pracownie, I pracownia, 76 Rozpady promieniotwórcze
teor 76, Studia, Pracownie, I pracownia
ZAGADN1, Studia, Pracownie, I pracownia, 1 Dokładność pomiaru długości, Marek
cw30, Studia, Pracownie, I pracownia, 30 Wyznaczanie względnej gęstości cieczy i ciał stałych, Ludwi
więcej podobnych podstron