0208; 22.04.2009, wykład nr 8., - Apoptoza; Paul Esz
Fizjologiczna śmierć komórki (śmierć programowana) synonim apoptoza (apoptosis, od greckiego słowa - opadania liści, płatków kwiatu - Kerr w 1972 roku) Jest konsekwencją samobójczego programu genetycznego, uruchomianego w odpowiedzi na złożone oddziaływanie z innymi komórkami.
Najczęściej następuje naruszenie integralności 1 z 4 systemów wewnątrzkomórkowych
oddychania tlenowego
funkcjonowania błon komórkowych
enzymów i białek strukturalnych
naprawy aparatu genetycznego
Apoptoza Caenorhabditis elegans
Dorosły osobnik jest hermafrodytą i składa się z 959 komórek somatycznych.
Liczba komórek powstających - 1090.
W wyniku apoptozy ginie 131
131 umiera podczas embriogenezy
18 podczas dorosłego życia
Geny proapoptotyczne
ced-3 (ICE)
ced-4 (Apaf-1)
Feny antyapoptotyczne → brak apoptozy
ced-9 (bcl-2)
Genetyczne kontrola apoptozy
„ced” (cell death) geny śmierci są dobrze zachowane w procesie ewolucji
ekspresja genów ced-3 i ced-4 odpowiada za molekularne procesy apoptozy
„ced-9” (u ludzi bcl-2) - ekspresja w komórkach stymulowanych do proliferacji (między innymi limfocyty prawidłowe, komórki nowotworowe)
Różnice morfologiczne pomiędzy apoptozą, a martwicą
Apotoza |
Martwica |
|
|
Zmiany biochemiczne
Materiał genetyczny |
Apoptoza |
Martwica |
|
aktywacja specyficznych endonukleaz, fragmentacja, utworzenie odcinków o długości 200-300kb, 20-50 kb, 200-300 bp |
aktywacja niespecyficznych nukleaz, fragmentacja na odcinki o przypadkowej długości |
Rozdział elektroforetyczny |
Obraz drabinki Dna |
Obraz smugi (smear) |
Aktywacja enzymów |
kinaz białkowych (np. kinazy MAP) i fosfataz, nukleaz, kaspaz, kalpain |
niespecyficzna degradacja |
Białka regulacyjne |
Apoptoza;; białka rodziny Bel-2 (pro- i anty- apoptotyczne), inhibitory apoptozy (białka IAP), inhibitory kaspaz |
W niektórych przypadkach ekspresja Bel-2 |
Wymagania energetyczne |
Proces aktywny, zależny od ATP |
Proces bierny, niezależny od ATP |
Substraty |
Białka enzymatyczne o strukturalne |
Przypadkowe białka |
Inne |
Synteza poli(ADP-rybozy), synteza de novo mRNA i białek |
Brak syntezy białek |
Czynniki wywołujące apoptozę
hormony i cytokiny
deficyt czynników wzrostowych i troficznych
czynniki cytotoksyczne
czynniki fizyczne
Szlaki sygnałowe apoptozy
W zależności od rodzaju komórki i czynnika indukującego proces apoptozy może przebiega, rożnymi ścieżkami
Do najlepiej poznanych należą
szlak związany z błoną komórkową tzw. zewnętrzny
szlak wewnętrzny zwany mitochondrialnym
szlak angażujący perforyny i granzym B, czyli pseudoreceptorowy
Apoptoza może również odbywać się z udziałem szlaku sfingomielinowo-ceramidowego oraz indukowanego stresem.
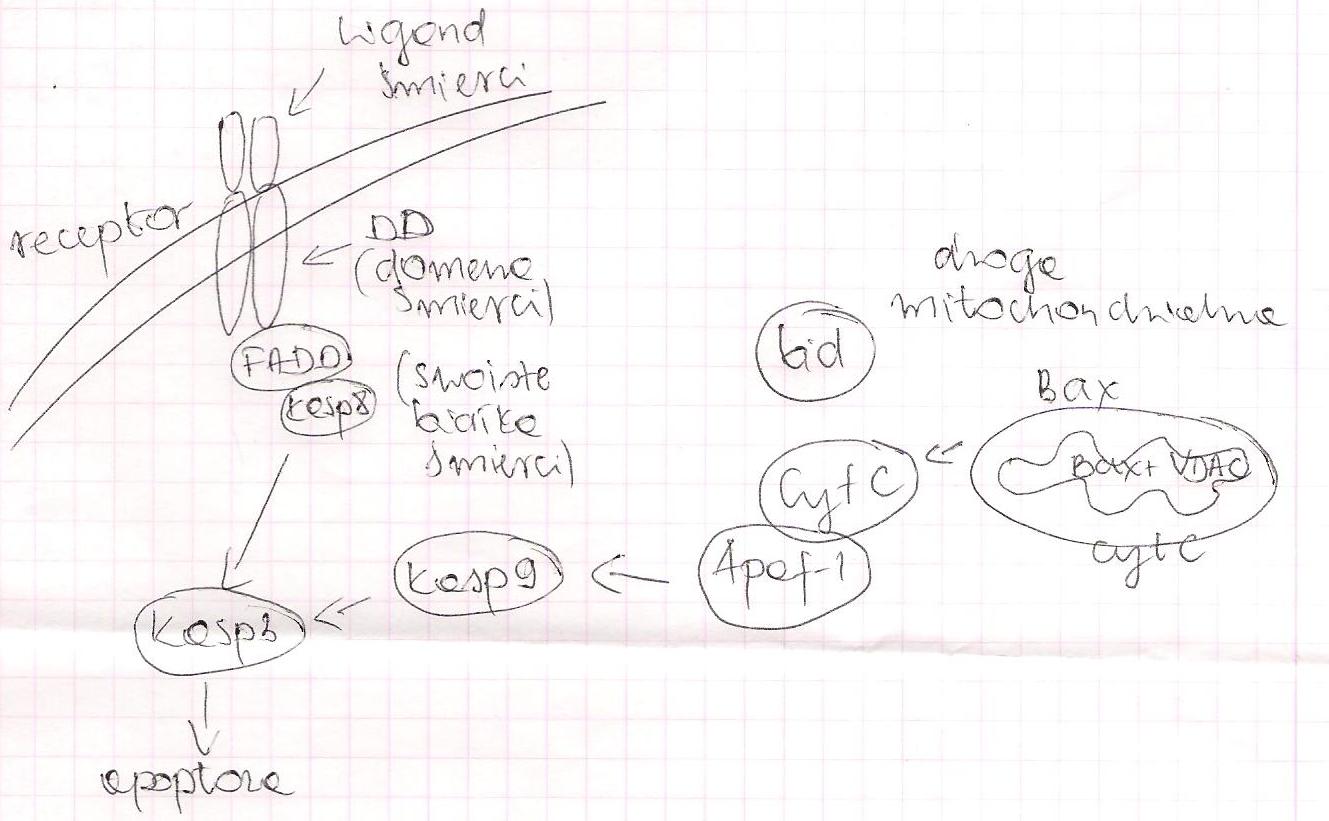
Szlak zewnętrznych
pobudzenie receptorów śmierci należących do nadrodziny receptorów TNF np. Fas/CD95/Apol, TRAIL-R1 i R2/Apo2
receptory śmierci posiadają wewnątrzkomórkową domenę śmierci DD
po związaniu się odpowiedniego liganda z receptorem błonowym (TNF-alfa, FasL, TRAIL/Apo2L) dochodzi do oligomeryzacji receptora, a następnie powstaje kompleks DISC (death inducin singnaling caomplex)
kompleks ten powstaje poprzez połączenie domen śmierci z białkiem adaptorowym FADD oraz z prokaspazą 8
następuje aktywacja prokaspazy 8 (powstaje kaspaza 8), która jest bezpośrednim aktywatorem kaspazy 3 (kaspazy wykonawczej)
Szlak wewnętrzny
inicjowany poprzez
zmiany potencjału mitochondrialnego
mutacje DNA
inne zaburzenia metabolizmu komórkowego
Szlak ten może łączy się ze ścieżką receptorową zewnętrzną poprzez białko Bid, które ulega proteolizie - powstaje tBid (truncated Bid) - posta ta wpływa na uwalnianie cytochromu c - aktywacja szlaku mitochondrialnego
istotnym etapem jest uwolnienie cytochromu c z przestrzeni międzybłonowej poprzez specjalne kanały
kanały te tworzone są poprzez białka z rodziny Bel-2 (bax, bak) z bialekiem VDAC (voltage Dependent Anion Channel)
przez kanały mitochondrium do cytoplazmy dostaje się cytochrom c
wypływ cytochromu c jest sygnałem do tworzenia kompleksu zwanego apoptosomem
apoptosom skalda się z cytochromu c, prokaspazy 9, bialka Apaf-1 (ATP)
kompleks ten potrzebny jest do autoproteolizy kaspazy 9 , która następnie aktywuje kaspazę 3
podczas apoptozy z mitochondrium uwalniane są także białka Smac/Diablo o Omi/HTR A2 są one antagonistami inhibitorów apoptozy (IAP)
Szlak pseudoreceptorowy - indukowany przez cytotoksyczne limfocyty T oraz komorki NK - będzie jeszcze potem
Właściwości kaspaz - (będzie na ćwiczeniach jeszcze)
są to proteazy cysteinowe, substraty ich zawierają kwas asparaginowy w pozycji P1 (proteoliza w miejscu reszty Asp)
syntetyzowane są jako nieaktywne zymogeny
dotychczas zidentyfikowano 14 kaspaz
kaspozy inicjatorowe 2,8,9,10
kaspazy wykonawcze 3,6,7
kaspazy inicjatorowe posiadają „domeny śmierci” CARD i DED
kaspazy wykonawcze aktywują enzymy prowadzące do destrukcji komórek
Białka trawione przez kaspazy
większość tych białek uczestniczy w procesach molekularnych związanych z cyklem komórkowym i apoptozą
do proteolizy białek dochodzi przy udziale tylko kaspaz 3,6,7
Śmierć komórki niezależna od kaspaz
proteaza aktywowana wapniem kalpaina (kapalina), prawdopodobnie pełni autonomiczną rolę w apoptozie
ostatnie doniesienia wskazują na jej rolę w procesie aktywacji i unieczynnienia kaspaz 3,7,9, i ostatnio 12
Apoptoza w stanach patologicznych
Ograniczenie apoptozy prowadzi do powstania nowotworów i autoagresji komórek układu odpornościowego. Wzrost apoptozy jest charakterystyczny dla chorób zwyrodnieniowych: choroby Alzheimera, Parkinsona, AIDS, zawału serca czy udaru mózgu
Schemat
Wyszukiwarka
Podobne podstrony:
0108 20[1].04.2009, II rok, II rok CM UMK, Histologia i cytofizjologia, histologia, Histologia, His
nabłonek, II rok, II rok CM UMK, Histologia i cytofizjologia, histologia, Histologia, Histologia2
Apoptoza, II rok, II rok CM UMK, Histologia i cytofizjologia, histologia, Histologia, Histologia2
Cytoszkielet, II rok, II rok CM UMK, Histologia i cytofizjologia, histologia, Histologia, Histologia
Układ moczowy, II rok, II rok CM UMK, Histologia i cytofizjologia, wykłady II semestr
0208 22 04 2009, wykład nr 8 , Apoptoza Paul Esz(1)
fizjo - egz.lek.2009, II rok, II rok CM UMK, Giełdy, 2 rok, II rok, giełdy od Nura, fizjo, egzamin,
egzamin z fizjo 2009, II rok, II rok CM UMK, Giełdy, 2 rok, II rok, giełdy od Nura, fizjo, egzamin,
PYTANIA FIZJO 2009 od bartka(1), II rok, II rok CM UMK, Giełdy, 2 rok, II rok, giełdy od Nura, fizjo
NEUROFIZJOLOGIA I. Colloquium 04, II rok, II rok CM UMK, Giełdy, od Joe, FIZJOLOGIA, KOLOKWIA, NEURO
egz fizjo 2009, II rok, II rok CM UMK, Giełdy, od Joe, FIZJOLOGIA, EGZAMIN, Fizjologia giełdy exam,
więcej podobnych podstron