1. RÓWNIANIE KALORYCZNE GAZÓW DOSKONAŁYCH
Równania kaloryczne gazów doskonałych określają zależność pomiędzy energią wewnętrzną, entalpią, entropią - termodynamicznymi funkcjami stanu.
Mają one postać :
di = CP dT
du = CV dT
![]()
CP i CV - stałe, nie zależą od temperatury dla gazów doskonałych.
2. EGZERGIA - DEFINICJA I PODZIAŁ
W celu określenia przydatności energii do wykonania pracy wprowadzono tzw. egzergię.
Jest to maksymalna zdolność do wykonywania pracy mechanicznej energii danej materii przy wykorzystaniu otoczenia jako źródła bezwartościowego ciepła i bezwartościowej substancji przy założeniu, że parametry końcowe czynnika termodynamicznego po procesie równe będą parametrom otoczenia.
Rozróżnia się straty zewnętrzne i wewnętrzne egzercji, polegające na nieodwracalności (straty wewnętrzne) oraz nieuzyskaniu stanu równowagi parametrów czynnika i otoczenia (straty zewnętrzne).
Egzergia chemiczna wynika z różnicy koncentracji chemicznej czynnika i otoczenia.
Egzergia fizyczna wynika z różnicy parametrów termicznych czynnika i otoczenia.
3. III ZASADA TERMODYNAMIKI
W reakcji pomiędzy doskonałymi kryształami (mającymi jednakową strukturę w całej objętości) w temp. 0K suma entropii substratów jest równa sumie entropii produktów.
Wnioski :
![]()
- pojemność cieplna właściwa doskonałych kryształów zmierza do zera przy temp. obniżającej się do zera bezwzględnego
- temp. 0K jest nieosiągalna zarówno w zakresie dodatnich jak też ujemnych temp. bezwzględnych
4. WŁASNOŚCI POWIETRZA WILGOTNEGO
![]()
- wilgotność bezwzględna objętościowa - stosunek masy pary mP [g]do objętości [m3] powietrza wilgotnego.
![]()
- wilgotność bezwzględna wagowa - x - ilość masy wilgoci w granicach przypadającej na jednostkę masy [kg] gazu suchego.
- wilgotność względna - stosunek masy wilgoci zawartej w jednostce objętości gazu do masy wilgoci w stanie nasycenia w danej temp.
![]()
- wilgotność względna powietrz wilgotnego - ϕ jest stosunkiem wilgotności bezwzględnej ϕbezw do maks. wilgotności bezwzględnej ϕ''bezw dla tej temp. lub stosunek ciśnienia składnikowego pary pP do jej ciśnienia maks. pP'' w tej temp.
![]()
- stan nasycenia - równowaga pomiędzy wilgocią w postaci pary i wilgocią w postaci mgły w powietrzu
5. RÓWNANIE CIĄGŁOŚCI STRUGI
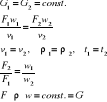
Dla przepływów ciągłych masowe natężenie przepływów jest wielkością stałą więc :
- masowe równanie ciągłości strugi
Ogólnie można zdefiniować, że dla płynów nieściśliwych, przy przemieszczaniu się bez tarcia w dwu dowolnych miejscach przewodu, prędkości są odwrotnie proporcjonalne do przekrojów. Przez każdy przekrój rurociągu płynie ta sama ilość czynnika. Jeżeli przekrój maleje, prędkość rośnie.
- różniczkowe równ. ciągłości 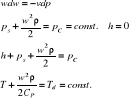
strugi
- równanie Bernouliego
- równanie energetyczne
ciągłości strugi
6. OPRY PRZEPŁYWU W RUROCIĄGU, OPORY TARCIA , MIEJSCOWE, HYDROSTATYCZNE
Opory, czyli straty ciśnienia na drodze przepływu spowodowane są:
1) tarciem gazów o ścianki kanałów - opory tarcia
2) straty ciśnienia na skutek zmian kształtu i wymiarów - opory miejscowe (lokalne)
3) różnicą ciśnień w układzie i otoczeniu - opory hydrostatyczne
![]()
Opory tarcia występują na ściankach rurociągu i zależą od stanu powierzchni i parametrów fizycznych medium.
![]()
Dla rurociągów krótkich :
λ - współczynnik tarcia, zależy od v
![]()
Dla rurociągów długich :
κ - współczynnik chropowatości
![]()
Opory miejscowe wyznaczane będą dla każdego układu empirycznie
ξ - współczynnik oporów miejscowych
Opory hydrostatyczne
![]()
7. PRZEWODZENIE CIEPŁA, WSPÓŁCZYNNIK PRZEWODZENIA
Przewodzenie ciepła jest to wymiana ciepła w obrębie tego samego ciała przy różnicy temperatur. Wymiana ciepła jest to sposób wymiany energii między układami lub w jednym układzie.
![]()
Gradient temp. jest to zmiana tej temp. w kierunku osi x :
Ilość ciepła :
Występuje tutaj minus ponieważ kierunek przepływu ciepła jest odwrotnie proporcjonalny do gradientu temp.
![]()
Równanie Fouriera :
λ - współczynnik przewodzenia ciepła, tj. ilość ciepła jaka przejdzie przez ścianę o grubości 1m w ciągu 1s przy zmianie temp. o 1°. Jednostką tego współczynnika
![]()
jest .
λ = a . c V . η, gdzie:
a - współczynnik charakteryzujący rodzaj gazu
c V - ciepło właściwe
η - lepkość dynamiczna
Dla gazów λ jest funkcją temp. i ciśnienia λ = f (T, p).
8. WYMIANA CIEPŁA PRZEZ PROMIENIOWANIE POMIĘDZY ŚCIANAMI PŁASKIMI
![]()
a) przegroda płaska
s - grubość przegrody
λ - współczynnik przewodzenia ciepła
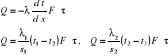
b) wielowarstwowa ściana płaska
![]()
R - opór cieplny
9. ZMIANA PUNKTU PRACY WENTYLATORA
Zmianę punktu pracy poprzez zmianę charakterystyk wentylatora możliwe jest poprzez zmianę jego obrotów spowodowaną zmianą obrotów silnika lub przez zmianę parametrów geometrycznych wirnika wentylatora.
Podstawowe sposoby regulacji to :
- Regulacja za pomocą zmiany prędkości obrotowej wirnika. Związana jest ona z napędem o zmiennej prędkości, np. przekładnią zmieniająca w sposób ciągły prędkość obrotową. Zapewnia możliwość regulacji wentylatora bez potrzeby zmiany jego konstrukcji i budowy dodatkowego systemu rozrządu.
Wydajność wentylatora jest wówczas proporcjonalna do zmiany obrotów.
- Regulacja za pomocą nastawnych kierownic wstępnych. Polega na zmianie ustawienia kąta łopatek kierownicy wstępnej znajdującej się przed wirnikiem. Powoduje to zmianę kąta napływu czynnika na wirnik, przez co ulega zmianie kinematyka przepływu. Wpływa to na energię przekazywaną przepływającemu czynnikowi, a więc możliwość zmiany przyrostu ciśnienia całkowitego.
- Regulacja za pomocą nastawianych w ruchu łopatek wirnika. Zmiana kąta ustawienia łopatek wirnika wpływa na kinematykę przepływu czynnika, na skutek czego następuje zmiana warunków pracy, przede wszystkim zmiana przyrostu ciśnienia całkowitego. Regulacja ta jest bardzo czuła, nawet niewielka zmiana kąta ustawienia
powoduje szybką zmianę ciśnienia. Stosowana jest praktycznie w wentylatorach osiowych.
10. PRAWA PROMIENIOWANIA
1) Prawo Plancka określa zależność pomiędzy energią wypromieniowaną przez dane ciało a jego temperaturą T i długością fali promieniowania λ.
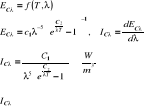
- natężenie promieniowania
2) Prawo przesunięć Wiena
Wraz ze wzrostem temperatury maksimum ![]()
promieniowania przesuwa się w kierunku krótszych fal.
Można tez powiedzieć, że ze wzrostem temperatury ciała długość fali odpowiadająca maksymalnej wartości widmowego natężenia promieniowania zmniejsza się.
3) Prawo Stefana Boltzmana
Całkowita energia wypromieniowana przez powierzchnię ciała doskonale czarnego jest proporcjonalna do 4 potęgi temp. bezwzględnej.
![]()
4) Prawo Kirchhoffa podaje zależność pomiędzy zdolnością emisji danego ciała a zdolnością absorbcji danego ciała.
Zdolność emisji i absorbcji danego ciała jest jednakowa,
czyli ciało szare w danej temperaturze emituje tyle energii ile energii zaabsorbowało przy wysyłaniu jej przez ciało czarne w tej samej temperaturze.
ε = A przy T = const.
5) Prawo Lamberta - określa ilość energii wysyłanej przez ciało w danym kierunku.
Energia wysyłana przez dane ciało we wszystkich kierunkach równa się : E = -π E n
Wymiana ciepła pomiędzy ciałami stałymi w zależności od powierzchni emitowanej i absorbowanej ciepło :
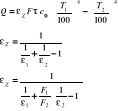
- emisyjność zastępcza dla
powierzchni otwartej
- emisyjność zastępcza dla
powierzchni zamkniętej
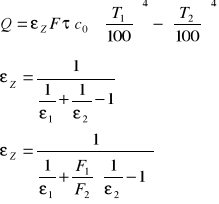
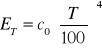
![]()
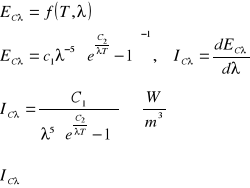
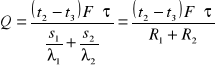
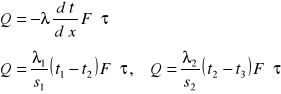
![]()
![]()
![]()
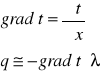
![]()
![]()
![]()
![]()
![]()
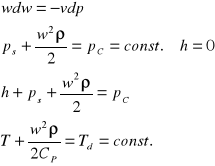
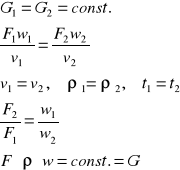
![]()
![]()
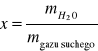
![]()
![]()
![]()
Wyszukiwarka
Podobne podstrony:
Egzamin grupa 2b, Chemia fizyczna AGH laborki, !egzamin
Egzamin grupa 1b, Chemia fizyczna AGH laborki, !egzamin
Egzamin grupa 4b, Chemia fizyczna AGH laborki, !egzamin
CHEMIA 12, Chemia fizyczna AGH laborki, lab 12
SPRAWOZ4, Chemia fizyczna AGH laborki, lab 12
napiecie pow nr 2, Chemia fizyczna AGH laborki, lab 2
LABORKA UKASZ 3, Chemia fizyczna AGH laborki, lab 3,4
CHEMIA 12, Chemia fizyczna AGH laborki, lab 12
korozja dla justyny, Chemia fizyczna AGH laborki, lab 21
Wyniki pomiarów ciepła rozpuszczania, Chemia fizyczna AGH laborki, lab 3,4
SPRAWOZ6, Chemia fizyczna AGH laborki, lab 18
Chemia fizyczna (3, Chemia fizyczna AGH laborki, lab 3,4
lab. 05 - baron, Chemia fizyczna AGH laborki, lab 5
Wykresy do 3, Chemia fizyczna AGH laborki, lab 3,4
tekst 7, Chemia fizyczna AGH laborki, lab 6
Chem 1, Chemia fizyczna AGH laborki, lab 1
skoootaaa, Chemia fizyczna AGH laborki, lab 20
więcej podobnych podstron