POLITECHNIKA LUBELSKA w LUBLINIE |
Laboratorium fizyki |
|||
|
Ćwiczenie EM 7.1 |
|||
Nazwisko i imię: Smołka Jakub |
Semestr
Trzeci |
Grupa
ED 3.7 |
Rok akademicki
99/ 00 |
|
Temat ćwiczenia Wyznaczanie równoważników elektrochemicznych metali, stałej Faraday'a i ładunku elementarnego. |
Data wykonania 1999. XI. 30.
|
Ocena |
||
1. Opis metody.
Rys.1. Schemat układu pomiarowego.
Pomiary przeprowadza się w woltametrze miedziowym, który włączony jest do obwodu prądu stałego. Układ pomiarowy jest przedstawiony na rysunku. Elektrody wykonane są z miedzi. Elektrolit stanowi wodny roztwór CuSO4. Podczas przepływu prądu na katodzie zachodzi reakcja redukcji, w wyniku, czego zredukowane jony miedzi odkładają się na tej elektrodzie. Na anodzie zachodzi reakcja utleniania miedzi, co prowadzi do pojawiania się w roztworze nowych jonów tego pierwiastka. Dzięki temu procesowi stężenie elektrolitu pozostaje stałe w trakcie elektrolizy.
Korzystając z pierwszego prawa Faraday'a, które mówi, że masa substancji wydzielonej na elektrodzie jest wprost proporcjonalna do ładunku, jaki przepłynął przez elektrolit, można wyznaczyć równoważnik elektrochemiczny wyrażający się wzorem: ![]()
, gdzie: ![]()
- ładunek, który przepłynął przez elektrodę, I-natężenie prądu (jeżeli natężenie prądu zmienia się w trakcie elektrolizy należy obliczyć wartość średnią wartości odczytywanych w równych odstępach czasu), t- czas trwania elektrolizy, m- masa wydzielona na elektrodzie.
Równoważnik elektrochemiczny jest równy liczbowo masie substancji wydzielonej w procesie elektrolizy na jednej z elektrod podczas przepływu ładunku jednostkowego.
Z drugiego prawa Faraday'a, które mówi, że masy substancji wydzielonych podczas przepływu takiego samego ładunku elektrycznego przez różne elektrolity są wprost proporcjonalne do odpowiednich współczynników elektrochemicznych, wynika, że dla danego pierwiastka:
![]()
, gdzie: F- stała Faraday'a, k- równoważnik elektrochemiczny, ![]()
- równoważnik chemiczny, A- masa atomowa, z- wartościowość.
Stała Faraday'a jest liczbowo równa ładunkowi, który przepływając przez elektrolit powoduje wydzielenie na elektrodzie masy równej równoważnikowi chemicznemu danej substancji.
Równoważnik chemiczny jonów jednowartościowych jest równy jego masie molowej, a więc przepłynięcie przez elektrodę ładunku równego stałej Faraday'a spowoduje wydzielenie jednego mola substancji, a więc: ![]()
, gdzie: e- ładunek elementarny, F- stała Faraday'a, NA- liczba jonów w jednym molu substancji (liczba Avogadra).
2. Tabela pomiarów i obliczeń.
Lp. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,28816 |
0,28882 |
1,0364 |
1799,97 |
3,54·10-7 |
89798 |
1,49·10-19 |
|
0,28882 |
0,28969 |
2,1236 |
1200,20 |
3,41·10-7 |
93073 |
1,55·10-19 |
![]()
; ![]()
; ![]()
3. Przykładowe obliczenia.
![]()
![]()
![]()
![]()
gdzie: k- równoważnik elektrochemiczny, I- natężenie prądu, t- czas trwania elektrolizy, R- równoważnik chemiczny, F- stała Faraday'a, e- ładunek elementarny
4. Dyskusja błędu (dla pomiaru nr 2).
Do pomiaru prądu użyto miernika o klasie dokładności 1. Zakres miernika wynosił 3 [A] natomiast liczba działek 75. Do pomiaru czasu wykorzystano sekundomierz o dokładności 0,01 [s], czas potrzebny na włączenie i zatrzymanie pomiaru czasu przyjęto po 0,1 [s]. Niedokładność pomiaru masy jest równa masie najmniejszego odważnika.
![]()
; ![]()
; ![]()
Błąd względny maksymalny wyraża się wzorem:
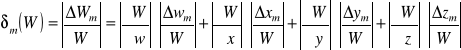
4.1. Obliczanie błędu względnego maksymalnego dla równoważnika elektrochemicznego.
Uwzględniając, że: ![]()
; ![]()
; ![]()
; ![]()
; ![]()
i podstawiając wartości otrzymujemy wartość błędu maksymalnego względnego:

Błąd bezwzględny maksymalny wynosi:
![]()
Natomiast błąd względny popełniony wynosi:
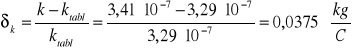
i jest mniejszy od błędu maksymalnego.
4.2. Obliczanie błędu względnego maksymalnego dla stałej Faraday'a.
Przyjmując wartość równoważnika chemicznego za dokładną, i uwzględniając, że:
![]()
; ![]()
; ![]()
; ![]()
; ![]()
można otrzymać wyrażenie na błąd względny maksymalny:
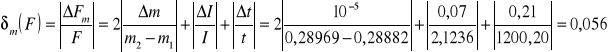
Błąd bezwzględny maksymalny wynosi:
![]()
4.3. Obliczanie błędu względnego maksymalnego dla ładunku elementarnego.
Błędy względne ![]()
i ![]()
są sobie równe ponieważ: ![]()
; ![]()
![]()
wobec czego błąd bezwzględny maksymalny wynosi:
![]()
4.4. Wnioski.
Z analogiczne przeprowadzonych obliczeń dla pomiaru nr 1 wynika, że błąd względny popełniony jest większy niż błąd względny maksymalny. Oznacza to, że pierwszy pomiar był nieudany.
1
Wyszukiwarka
Podobne podstrony:
2.2 b, Studia Fizyka sprawozdania, Elektryczność i magnetyzm, 2.2
11.1 b, Politechnika Lubelska, Studia, Studia, materiały na studia, Fizyka - Sprawozdania poukładane
Spektrometr-76, Studia, Fizyka, Sprawozdania, 76a
Wahadlo matematyczne, Studia, pomoc studialna, Fizyka- sprawozdania
Sprawozdanie E-9 stary word, Studia, Fizyka, Sprawozdania
Fizyka test 1, Studia, pomoc studialna, Fizyka- sprawozdania
Zadania fizyka 1, Studia, pomoc studialna, Fizyka- sprawozdania
Promieniowanie gamma, Studia, pomoc studialna, Fizyka- sprawozdania
Rezonator kwarcowy, Studia, pomoc studialna, Fizyka- sprawozdania
Wyznaczanie predkosci dzwieku w powietrzu, Studia, pomoc studialna, Fizyka- sprawozdania
Rezonator-Wnioski, Studia, pomoc studialna, Fizyka- sprawozdania
76 - WYZNACZANIE WSPÓŁCZYNNIKA ZAŁAMANIA SZKŁA ZA POMOCĄ SPEKTROMETRU, Materiały na studia, Fizyka
więcej podobnych podstron