Politechnika Krakowska |
|
rok: 1998/99 |
nr ćwiczenia |
Fizyka Techniczna |
MARCIN |
semestr: I |
20 |
Grupa: C |
KUK |
Ocena: |
Podpis: |
Zespół: 8 |
|
|
|
Wyznaczanie równoważnika elektrochemicznego wodoru.
Teoria.
Prąd elektryczny, przepływając przez elektrolit, wydziela na elektrodach produkty dyspozycji elektrolitycznej.
Prawo Faraday'a: Masa jonów wydzielana na elektrodzie jest proporcjonalna do natężenia prądu oraz czasu jego przepływu.
m=kIT
k-współczynnik proporcjonalności zwany równoważnikiem elektrochemicznym.
![]()
Dyspozycja elektrolityczna - jet to zachodzący w roztworach proces rozpadu cząstek elektroliów na kationy i aniony.
Elektroliza - proces zachodzący na elektronach podczas przepływu stałego prądu elektrycznego przez elektrolit. Pod wpływem pola elektrycznego między elektrodami, kationy dążą do katody, gdzie pobierają elektrony i w postaci zredukowanej wydzielają się, natomiast aniony oddają elektrony na anodzie i wydzielają się w postaci utlenionej.
Drugie prawo Faradaya:
![]()
μ - masa molowa atomu (jonów)
ω - elektrowartościowość jonów
Ilości różnych substancji ulegające reakcji na elektrodach przy przepływie równych ilości elektryczności są proporcjonalne do ich równoważników chemicznych.
Stała Faraday'a: współczynnik, przez który należy pomnożyc liczbę równoważników chemicznych jonów, aby otrzymać ładunek przenoszony przez te jony.
Elektrolity: substancje, które po rozpuszczeniu w odpowiednim rozpuszczaliku ulegają dysocjacji elektrolitycznej i w skutek tego w stanie ciekłym lub roztworze przewodzą prąd elektryczny.
Pomiary przewodnictwa muszą być wykonywae dokładnym zachowaniem stałości temperatury, ponieważ zmiana tempertury o 1oC zmienia przewodnictwo elektrolitów średnio o 2-2,5%..
Prawo Ohma.
![]()
R - opór przewodnika
U - napięcie
I - natężenie
Prędkości jonów są proporcjonalne do natężenia pola. Prędkości jonów przy jednostkowym natężeniu pola nazywamy ich ruchliwościami bezwzględnymi. Najruchliwszym jonem jest jon wodoru (prędkość około 0,003 cm/s).
Prawo gazów doskonałych.
Prawo Avokadra: jednakowe objętości różnych gazów, znajdujących się pod tym samym ciśnieniem i w tej samej temperaturze, zawierają jednakową liczbę cząstek . Obj. Molowa: V=22,415 l
Prawo Boyle'a: iloczyn ciśnienia i objętości jest wielkością stałą w stałj temperaturze pV=const.
Prawo Gay - Luccasa: wszystkie gazy ogrzewane pod stałym ciśnieniem rozszerzają się zgodnie z zależnością p=Vo(1+αt).
Vo - objętość danej masy gazu pod danym ciśnieniem w temperaturze równej 0oC
α - współczynnik rozszerzalności równy 1/237,16.
Doświadczenie.
Obliczenia do pomiaru pierwszego.
po = 1008 [hPa] = 100800 [Pa] - ciśnienie normalne.
p1 =( 98800±50 )[Pa] = 98800 [Pa] - ciśnienie atmosferyczne.
p 3 = 26,38 [hPa] = 2638 [Pa] - prężność nasyconej pary wodnej dla 22oC.
ρ = 1066,9 [kg/m3] - gęstość 10% H2SO4
ρo = 0,08987 [kg/m3] - gęstość normalna wodoru.
Ciśnienie hydrostatyczne słupa roztworu
p2 = hρg h = 0,225 [m]
p2 = 0,225⋅1066,9⋅9,8105
p2 = 2355,035 [Pa]
Ciśnienie suchego wodoru.
p = p1 + p2 - p3
p = 98800+2355,035-2638
p = 98517,03 [Pa]
Objętość normalna Vo.
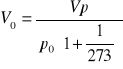
V = 0,0000165 m3
![]()
![]()
Masa wydzielanego wodoru.
m = Voρ
m = 0,000016⋅0,08987 To = 273 [K]
m = 0,0000014 [kg] = 1,4 [mg] T = 295 [K]
p = 98800 [Pa]
po = 100800 [Pa]
ρo = 0,08987
![]()
ρ = 0,08987
Obliczanie równoważnika elektrochemicznego.
![]()
I = 0,25 [A]
τ = 497,1 [s]
![]()
k = 0,01126 [mg/As]
Obliczanie stałej Faraday'a:
F=R/k R=1,008⋅10-3
F=95100[C/mol]
Obliczanie błędu pomiaru.
![]()
![]()
![]()
ρ=1066,9[kg/m3]
![]()
[Pa]
Δp=70,93[Pa]
![]()
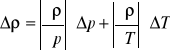
![]()
Δρ=(2,3⋅10-4)[kg/m3]
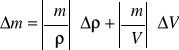
![]()
ΔV=0,5⋅10-6[m]
![]()
![]()
ΔI=0,01[A] Δt=0,2[s]
![]()
![]()
![]()
![]()
![]()
Zestawienie wyników.
p =( 98517,03±70,93) [Pa] Δp/p=0,07%
m =(1,4±0,04) [mg] Δm/m=2,8%
k = (0,01126±0,0006) [mg/As] Δk/k=4,9%
F=(95100±5300)[C/mol] ΔF/F=5,2%
Obliczenia dla pomiaru drugiego.
p 3 = 31,58 [hPa] = 3158 [Pa] - prężność nasyconej pary wodnej dla 25oC.
Ciśnienie hydrostatyczne słupa roztworu
p2 = hρg h = 0,23 [m]
p2 = 0,23⋅1066,9⋅9,8105
p2 = 2407 [Pa]
Ciśnienie suchego wodoru.
p = p1 + p2 - p3
p = 98800+2407-3158
p = 98049,36 [Pa]
Objętość normalna Vo.
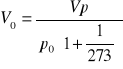
V = 0,000017 m3
![]()
![]()
Masa wydzielanego wodoru.
m = Voρ
m = 0,0000164⋅0,08786 ρ = 0,08786
m = 0,0000014 [kg] = 1,4 [mg]
Obliczanie równoważnika elektrochemicznego.
![]()
I = 0,34 [A]
τ = 351,09 [s]
![]()
k = 0,011728 [mg/As]
Obliczanie stałej Faraday'a:
F=R/k R=1,008⋅10-3
F=96300[C/mol]
Δp=71,24[Pa]
![]()
Δρ=(2,1⋅10-4)[kg/m3]
![]()
![]()
![]()
Zestawienie wyników.
p =( 98049,36±71,24) [Pa] Δp/p=0,07%
m =(1,4±0,04) [mg] Δm/m=2,9%
k = (0,011728±0,0006) [mg/As] Δk/k=4,8%
F=(96300±6200)[C/mol] ΔF/F=6,2%
Obliczenia dla pomiaru trzeciego
p 3 = 33,50 [hPa] = 3350 [Pa] - prężność nasyconej pary wodnej dla 26oC.
Ciśnienie hydrostatyczne słupa roztworu
p2 = hρg h = 0,245 [m]
p2 = 0,245⋅1066,9⋅9,8105
p2 = 2564,3 [Pa]
Ciśnienie suchego wodoru.
p = p1 + p2 - p3
p = 98800+2564,3-3350
p = 98014,3 [Pa]
Objętość normalna Vo.
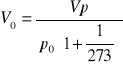
V = 0,000018 m3
![]()
![]()
Masa wydzielanego wodoru.
m = Voρ
m = 0,0000174⋅0,08384 ρ = 0,08384
m = 0,0000015 [kg] = 1,5 [mg]
Obliczanie równoważnika elektrochemicznego.
![]()
I = 0,42 [A]
τ = 312,4 [s]
![]()
k = 0,01143 [mg/As]
F=95900[C/mol]
Δp=70,35[Pa]
![]()
Δρ=(2,6⋅10-4)[kg/m3]
![]()
![]()
![]()
Zestawienie wyników.
p =( 98014,3±70,35) [Pa] Δp/p=0,07%
m =(1,5±0,04) [mg] Δm/m=2,9%
k = (0,01143±0,0006) [mg/As] Δk/k=5%
F=(95900±6300)[C/mol] ΔF/F=5,1%
Wnioski:
Duży błąd procentowy wynika w znacznej mierze z braku możliwości dokładnego pomiaru czasu oraz pozostałych wielkości m.in. objętości wodoru znajdującego się w biurecie.
Wyszukiwarka
Podobne podstrony:
elektrycznych tensometrow oporowych, Inżynieria Środowiska PK, Semestr 1, Fizyka, Fizyka Laboratoria
pomiar oporu elektrycznego i wyznaczanie oporu wlasciewgo metali, Inżynieria Środowiska PK, Semestr
20. Wyznaczanie stałej siatki dyfrakcyjnej, Inżynieria Środowiska PK, Semestr 1, Fizyka, Fizyka Labo
cw12, Inżynieria Środowiska PK, Semestr 1, Fizyka, Fizyka Laboratoria
cw13, Inżynieria Środowiska PK, Semestr 1, Fizyka, Fizyka Laboratoria
cw7, Inżynieria Środowiska PK, Semestr 1, Fizyka, Fizyka Laboratoria
Wyznaczanie równoważnika elektro-chemicznego miedzi i stałej Faraday'a, LABORATORIUM Z PRZETWORNI
ćw 11 Wyznaczanie równoważnika elektrochemicznego wodoru
Sprawozdanie bla bla, Inżynieria Środowiska PK, Semestr 1, Chemia
kolokwium2 pyt&odp Lemek, Inżynieria Środowiska PK, Semestr 1, Biologia i ekologia
Sprawozdanie nr 4, Inżynieria Środowiska PK, Semestr 1, Chemia
O6, Inżynieria Środowiska PŚk, Semestr 2, Fizyka, Labo
więcej podobnych podstron