2. STĘŻENIA
Przy omawianiu zagadnień związanych z ochroną atmosfery, w tym przy określaniu właściwości powietrza lub gazów odlotowych niezbędna jest znajomość składu ilościowego, czyli stężeń poszczególnych składników. Jest to także niezbędne do określenia wielkości ładunku zanieczyszczeń unoszonych z gazami odlotowymi, a także poziomu stężenia zanieczyszczeń w powietrzu.
2.1. SPOSOBY WYRAŻANIA STĘŻEŃ GAZÓW
Niżej przedstawiono najczęściej stosowane sposoby wyrażania stężeń gazów.
Ułamek molowy - yi jest wielkością bezwymiarową, określającą stosunek liczby moli rozpatrywanego składnika ni do sumy moli wszystkich składników mieszaniny n (łącznie z rozpatrywanym składnikiem „i”).
![]()
(2.1)
Korzystając z zależności (1.9) oraz (1.11) możemy ułamek molowy wyrazić jako stosunek ciśnienia parcjalnego pi oraz ciśnienia całkowitego mieszaniny p.
![]()
(2.2)
Ułamek molowy jest wielkością bezwymiarową i przyjmuje wartości 0< yi <1.
Procent objętościowy - Si(%obj.)
![]()
(2.3)
gdzie:
V - objętość mieszaniny gazów,
Vi - objętość jaką przyjąłby rozpatrywany składnik „i” w warunkach (temperatury i ciśnienia) w jakich znajduje się mieszanina.
Ten sposób wyrażania stężenia jest zbliżony do poprzedniego - ułamka molowego. Stężenie wyrażone w Si(%obj.) ma wartość stukrotnie większą od ułamka molowego. W powszechnym odbiorze jest to sposób bardziej komunikatywny. W obliczeniach inżynierskich natomiast mniej praktyczny.
Tak wyrażane stężenie przyjmuje wartości 0< Si(%obj.) <100%.
Stężenie wyrażone w ppm - Si(ppm) wyraża ilość cząstek rozpatrywanego składnika „i” przypadającą na 1 milion cząstek mieszaniny (łącznie z rozpatrywanym składnikiem) lub ilość moli składnika „i” przypadająca na 1 milion moli mieszaniny. Tak wyrażane stężenie przyjmuje wartości w zakresie 0< Si(ppm) <106.
Zależność między Si(ppm) a dwoma wcześniej przedstawionymi sposobami wyrażania stężenia ujmuje wzór:
![]()
![]()
(2.4)
Stężenie masowe - Si(mg/m3) wyraża stosunek masy rozpatrywanego składnika „i” do objętości
![]()
(2.5)
gdzie:
mi - masa składnika „i” w mieszaninie, mg,
V - objętość mieszaniny, m3.
Podstawową jednostką stężenia masowego w układzie SI jest [kg/m3]. Przy omawianiu zagadnień ochrony atmosfery, ze względów praktycznych, najczęściej stosuje się wymiar [mg/m3]. Stężenie masowe można również wyrażać w [μg/m3] lub [g/m3].
Stężenie molowe - Si(kmol/m3) wyraża stosunek ilości kilomoli rozpatrywanego składnika „i” do objętości gazu.
![]()
(2.6)
gdzie:
ni - ilość rozpatrywanego składnika „i” w mieszaninie wyrażona w kilomolach (lub jednostkach pochodnych)
Jednostką stężenia jest [kmol/m3]. Ten sposób wyrażania stężenia bardzo rzadko jest stosowany przy omawianiu zagadnień ochrony atmosfery.
Ciśnienie parcjalne - pi chociaż nie jest bezpośrednio miarą stężenia, to jednak pośrednio świadczy o zawartości rozpatrywanego składnika w jednostce objętości. Zależność ciśnienia parcjalnego pi od zawartości rozpatrywanego składnika w określonej objętości (ni, mi) wynika bezpośrednio z równania Clapeyrona (1.11).
![]()
(2.7)
gdzie:
mi - masa rozpatrywanego składnika, [kg]
ni - liczba kilomoli rozpatrywanego składnika, [kmol]
Jak widać z zaprezentowanego wzoru, wartość ciśnienia parcjalnego pi jest proporcjonalna do ![]()
, wyrażającego stężenie molowe oraz ![]()
, wyrażającego stężenie masowe, czyli traktowanie ciśnienia parcjalnego jako formę wyrażania stężenia rozpatrywanego składnika w mieszanie gazowej jest całkowicie uzasadnione.
Uwagi ogólne. Przedstawione wyżej sposoby wyrażania stężenia gazów można podzielić na dwie grupy. W trzech przypadkach (yi, Si(%obj.), Si(ppm)), określanych niekiedy jako stężenia objętościowe, wartość stężenia jest informacją o tym jaką część mieszaniny stanowi rozpatrywany składnik. Jeśli gaz zmieni swoją objętość (np. zwiększy wskutek podgrzania pod stałym ciśnieniem) to wzajemny stosunek składników i tak nie ulegnie zmianie, a tym samym nie zmieni się wartość tak zdefiniowanego stężenia. Ten sposób wyrażania stężenia nie daje jednak informacji o tym jakie jest zagęszczenie rozpatrywanego składnika w jednostce objętości. Inaczej jest w pozostałych trzech wypadkach, stężenia masowego - Si(mg/m3), stężenia molowego Si(kmol/m3) oraz ciśnienia parcjalnego - pi. Tutaj przez określenie stężenia uzyskujemy bezpośrednią informację o zagęszczeniu rozpatrywanego składnika w jednostce objętości (Si(mg/m3), Si(kmol/m3) lub pośrednią przez określenie ciśnienia parcjalnego (pi). Nie wiadomo natomiast jaki jest udział rozpatrywanego składnika w mieszaninie względem pozostałych składników. We wszystkich przytoczonych przypadkach dopełnieniem informacji jest znajomość temperatury T oraz ciśnienia całkowitego p. Jest to szczególnie ważne w wypadku stężenia masowego - Si(mg/m3) i molowego Si(kmol/m3), których wartości ulegają zmianom wraz ze zmianami parametrów. Wywołują je zmiany objętości gazu wskutek zmiany parametrów. Dlatego przy wyrażaniu stężenia w tej postaci, dla jednoznacznego podania pełnej informacji, niezbędne jest podanie również parametrów, temperatury i ciśnienia , których ta wartość dotyczy - Si(mg/m3)T,p, Si(kmol/m3)T,p.(dolny indeks za nawiasem dotyczczy oznaczenia parametrów) Dla stężenia masowego zobrazowano to na rysunku 2.1.
Tutaj rysunek
Na rysunku przedstawiono zamknięte naczynie zawierające określoną ilość gazu. Wynosi ona n kilomoli. W niej zawarte jest ni kilomoli rozpatrywanego składnika „i”, co odpowiada masie mi. Gaz poddano przemianom izotermicznym. Zmiany ciśnienia powodują zmiany objętości, a tym samym zmiany jego zagęszczenia. Wskutek tego odpowiednim zmianom ulega również stężenia masowe - ![]()
. Natomiast stężenie objętościowe - ![]()
, obrazujące wzajemny stosunek składników w mieszaninie, pozostaje niezmienne.
Ciśnienie parcjalne pi ulega zmianom proporcjonalnie do zmian ciśnienia całkowitego, a zatem i tutaj też należy uwzględnić te zależność w zapisie -(pi)p.
Trzy wymienione na początku postacie stężeń (yi, Si(%obj.), Si(ppm)) są postaciami równoważnymi i wzajemne ich przeliczanie nie stanowi problemu (wzór 2.4). Pewne trudności mogą natomiast nastręczać pozostałe przekształcenia.
Niezależnie od przyjętego sposobu wyrażania stężenia, konkretna wartość dotyczy rozpatrywanego, pojedynczego składnika mieszaniny. W wypadku stężenia masowego możliwe jest jednak określanie sumarycznego stężenia wielu składników. Nie jest to jednak zwykle prosta suma stężeń wybranych składników. Sumuje się zawartość wybranego, wspólnego dla rozpatrywanej grupy zanieczyszczeń pierwiastka, np. siarki na stopniu utlenienia ![]()
(do określenia sumy stężeń siarkowodoru i tioli). Z tego sposobu korzysta się najczęściej przy określaniu sumy związków organicznych poprzez podanie stężenia węgla organicznego, ![]()
. Stosując zasadę stechiometrii, stężenie każdego z zanieczyszczeń organicznych przelicza się na stężenie węgla zawartego w cząsteczce i następnie oblicza się sumę.
Zależność między Si(ppm) a Si(mg/m3)T,p przedstawia się następująco:
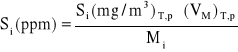
(2.8)
Uwzględniając, że objętość molowa ![]()
przyjmuje wartości zależne od parametrów (wzory (1.4) oraz (1.7)):
![]()
(2.9)
![]()
(2.10)
otrzymujemy:
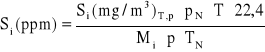
(2.11)
lub
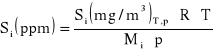
(2.12)
Zależność między Si(mg/m3)T,p oraz pi można wyprowadzić korzystając z równania (2.7).
![]()
(2.13)
W większości wypadków, przy korzystaniu z podanych w tym rozdziale wzorów, musimy pamiętać, żeby podstawić dane do wzorów w odpowiednich jednostkach oraz znać wymiar wielkości obliczanej.
Przeliczanie wartości stężenia masowego. Oprócz przedstawionych wyżej przeliczań stężeń niekiedy zachodzi potrzeba przeliczanie wartości stężenia masowego z jednych warunków (![]()
) na inne (![]()
), np. z wartości określonej w warunkach pomiaru na wartość w warunkach normalnych. Można to wykonać w następującym ciągu, na który składają się dwa kolejne przeliczenia:
![]()
(2.14)
W myśl powyższego równania, korzystając ze wzoru (2.12) może napisać:
![]()
![]()
(2.15)
oraz:
![]()
(2.16)
Porównując obie zależności otrzymamy;
![]()
(2.17)
a po uproszczeniu i przekształceniu:
![]()
![]()
(2.18)
2.2. WPŁYW ZMIAN STĘŻENIA JEDNEGO SKŁADNIKA MIESZANINY GAZÓW NA STĘŻENIA POZOSTAŁYCH SKŁADNIKÓW
W mieszaninie gazów i par zmiana stężenia jednego składnika powoduje proporcjonalną zmianę pozostałych wartości stężeń. Wprowadzenie dodatkowego składnika do mieszaniny gazów (np. pary wodnej) powoduje zmniejszenie stężeń składników pozostałych. W przypadku usunięcia jednego ze składników dzieje się odwrotnie. Z takimi sytuacjami mamy do czynienia zarówno w rzeczywistości jak i w rozważaniach teoretycznych. Przykładami mogą być:
nawilżanie powietrza suchego, gdy do mieszaniny o niezmiennym wzajemnym stosunku ilościowym składników wprowadzana jest para wodna,
przeliczanie stężeń składników spalin wilgotnych (zawierających niekiedy znaczne ilości pary wodnej) na hipotetyczne wartości, jakie mogłyby wystąpić w spalinach pozbawionych wilgoci,
W wypadku zmiany zawartości pary wodnej rozważamy sytuacje, gdy para wodna występuje w gazach wilgotnych w określonym, znanym stężeniu lub gdy jej nie ma, tzn. że mamy do czynienia z gazami suchymi. Przeliczanie najłatwiej wykonać posługując się stężeniami wyrażonymi w ułamkach molowych. Dla odróżnienia gazów suchych i wilgotnych wprowadzamy, przy oznaczaniu stężeń poszczególnych składników, indeksy górne „s” oraz „w”.
![]()
stężenie rozpatrywanego składnika i w gazach suchych,
![]()
stężenie rozpatrywanego składnika w gazach wilgotnych.
Rozpatrzmy zagadnienie przeliczania stężeń składników gazu suchego na stężenia gazu wilgotnego (lub odwrotnie) na przykładzie mieszaniny, która w stanie suchym zawiera składniki A, B, C a w stanie wilgotnym jeszcze ![]()
(w postaci pary). Dla gazu suchego możemy napisać:
![]()
![]()
(2.19)
a dla gazu wilgotnego:
![]()
(2.20)
W gazie wilgotnym stężenia składników A, B i C zostają pomniejszone proporcjonalnie o udział pary wodnej, ![]()
. Suma ich stężeń jest zatem mniejsza od 1 i wynosi:
![]()
(2.21)
Na podstawie równań (2.19) oraz (2.21) można ułożyć proporcję:
![]()
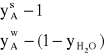
(2.22)
a stąd uzyskamy wzór na przeliczenie stężenia rozpatrywanego składnika w gazie suchym na stężenie w gazie wilgotnym:
![]()
![]()
(2.23)
oraz wartości stężenia w gazie wilgotnym na wartość stężenia w gazie suchym:
![]()
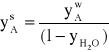
(2.24)
Dla wszystkich pozostałych składników można wyprowadzić takie same wzory. Zależność obowiązuje zatem dla każdego dowolnego składnika „i” dowolnie złożonej mieszaniny (oprócz pary wodnej). Możemy zatem napisać:
![]()
![]()
(2.25)
![]()
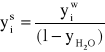
(2.26)
Podobne przekształcenia możemy wykonać dla innych sposobów wyrażania stężeń. Dla stężeń wyrażanych w ![]()
otrzymamy:
![]()
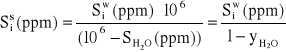
(2.27)
lub:
![]()
![]()
(2.28)
oraz dla stężeń wyrażonych w ![]()
:
![]()
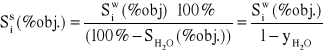
(2.29)
lub:
![]()
![]()
(2.30)
W podobny sposób możemy również przeliczać wartości stężenia masowego, ![]()
. Odpowiedni wzór uzyskamy z przekształcenia zależności (2.27) oraz (2.13). Jeśli założymy, że wraz ze zmianą stężenia pary wodnej zmianie ulegają również parametry gazów to z połączenia obu wzorów otrzymamy:
![]()
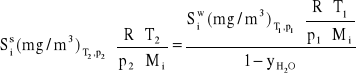
(2.31)
a po uproszczeniu i przekształceniu:
![]()
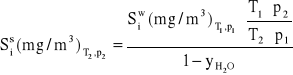
(2.32)
Jeśli parametry gazów nie ulegają zmianie to zależność przyjmuje jeszcze prostszą postać:
![]()
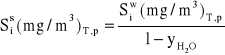
(2.33)
2.3. PRZELICZANIE STĘŻEŃ ZANIECZYSZCZEŃ W GAZACH ODLOTOWYCH
Drugim obszarem, w którym występuje potrzeba przeliczania wartości stężeń są obliczenia dotyczące tzw. standardów emisyjnych z instalacji [Rozporządzenie Ministra Środowiska z dnia 20 grudnia 2005 r. w sprawie standardów emisyjnych z instalacji, Dz. U. Nr 260 poz. 2181] . Jest to inne zagadnienie niż omawiane w poprzednim rozdziale. Standardy emisyjne są to maksymalne dopuszczalne masowe stężenia zanieczyszczeń w emitowanych do atmosfery gazach, odniesione do tzw. warunków umownych. Pod tym pojęciem należy rozumieć:
ciśnienie normalne,
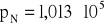
Pa,temperatura normalna, T = 273 K,
gaz suchy (nie zawierający pary wodnej).
W największym stopniu sprawa standardów emisyjnych została uregulowana dla instalacji kotłowych. Są to szczególne obiekty emisji bowiem tutaj istotnym czynnikiem wpływającym na wartości stężeń zanieczyszczeń jest wielkość strumienia spalin, który można regulować przez doprowadzanie większej lub mniejszej ilości powietrza do paleniska.. Daje to możliwość rozrzedzania spalin. Wielkością wskazującą na ilość doprowadzonego do paleniska powietrza jest stężenie tlenu w spalinach. Im większy strumień powietrza tym większe stężenie tlenu. Dlatego dla tych obiektów narzucono dodatkowy warunek, jakim jest:
standardowa zawartość tlenu w spalinach,
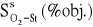
.
Przyjęte zostały różne wartości standardowe, w zależności od rodzaju kotła i rodzaju paliwa.
W tej sytuacji, aby orzec czy w danej instalacji kotłowej są dotrzymane standardy emisyjne, należy pomierzone rzeczywiste wartości stężeń ![]()
, występujące przy stężeniu tlenu w spalinach odniesionym do gazów suchych, ![]()
kolejno przeliczyć na:
stężenia zanieczyszczenia odniesione do gazów suchych,
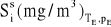
,
stężenia zanieczyszczenia w gazach suchych w warunkach umownych (normalnych),
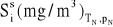
,stężenie zanieczyszczenia w gazach suchych, w przeliczeniu na warunki normalne i odniesione do standardowej zawartości tlenu,
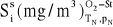
.
Dwa pierwsze kroki przeliczenia zostały już opisane wcześniej. Ostatnie przeliczenie możemy wykonać przy zastosowaniu następującego wzoru;
![]()
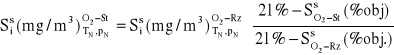
(2.34)
Zastosowany sposób oznaczeń, z indeksami dolnymi i górnymi przed oraz za nawiasem, może wydawać się nieco skomplikowany, dlatego niżej objaśniono szczegółowo zastosowany zapis.
![]()
- stężenie składnika „i” w gazach suchych (górny indeks „s” przed nawiasem), odniesione do warunków normalnych (dolny indeks „![]()
” za nawiasem), w przeliczeniu na standardową zawartość w spalinach (górny indeks „![]()
” za nawiasem),
![]()
- stężenie składnika „i” w gazach suchych (górny indeks przed nawiasem), odniesione do warunków normalnych (dolny indeks „![]()
” za nawiasem), odniesione do stężenia tlenu w spalinach zmierzonego i przeliczonego na gazy suche (górny indeks „![]()
” za nawiasem),
![]()
- stężenie tlenu w spalinach zmierzone (dolny indeks „![]()
” i przeliczone na gazy suche (górny indeks „s”),
![]()
- standardowe stężenie tlenu w spalinach (dolny indeks „![]()
”) odniesione do spalin suchych (górny indeks „s”), wartości dla odpowiednich przypadków są zawarte w Rozporządzeniu Ministra.
Rys. 3.1. Ilustracja zmian stężenia wybranego składnika „i” podczas izotermicznej przemiany próbki gazu (n - ilość kilomoli gazu, ni = ilość kilomoli składnika „i” w gazie, mi = masa składnika „i”.
T1, p1, V1
T1, p2, V2
T1, p3, V3
1)
2)
3)
Warunki 1: T1, p1, V1.
Stężenia:
![]()
![]()
Warunki 2: T1, ![]()
, ![]()
,
Stężenia:
![]()
(bez zmiany)
![]()
(dwukrotnie zmalało)
Warunki 3: T1, ![]()
, ![]()
,
Stężenia:
![]()
(bez zmiany)
![]()
(dwukrotnie wzrosło)
Wyszukiwarka
Podobne podstrony:
7164
7164
7164
7164
7164
7164
077 Gatunki filmu fabularnego IVid 7164
7164
7164
więcej podobnych podstron