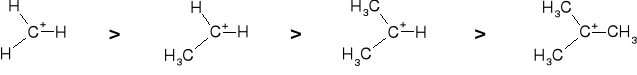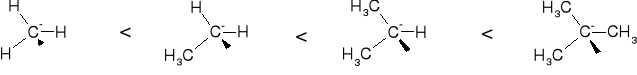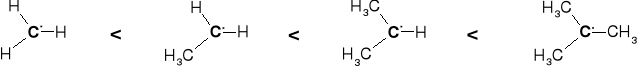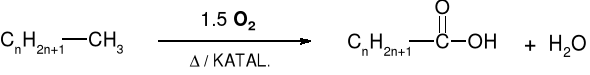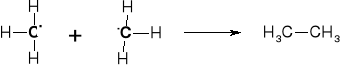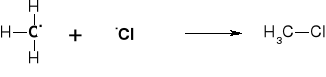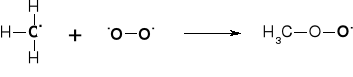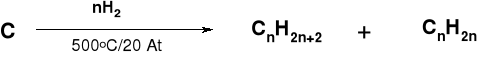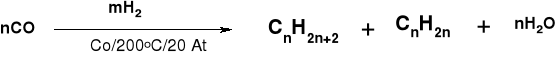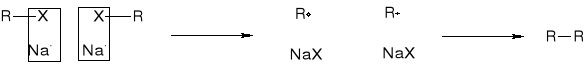WYKŁADY Z CHEMII ORGANICZNEJ |
||||
|
||||
Nr |
data |
h |
|
|
1 |
|
2 |
Podstawy (konfiguracja elektronowa, hybrydyzacja) |
|
2 |
|
3 |
Alkany, reakcje wolnorodnikowe, cykloalkany |
|
3 |
|
2 |
Alkeny i alkiny |
|
4 |
|
2 |
Związki monofunkcyjne: halogenki alkilu |
|
5 |
|
2 |
Alkohole i fenole |
|
6 |
|
3 |
Dieny, rezonans |
|
7 |
|
3 |
Związki aromatyczne |
|
8 |
|
2 |
|
|
9 |
|
3 |
Związki karbonylowe: aldehydy i ketony |
|
10 |
|
3 |
Kwasy karboksylowe |
|
11 |
|
2 |
Pochodne kwasów karboksylowych: chlorki, bezwodniki i estry |
|
12 |
|
3 |
Aminy |
|
|
|
|
|
|
Nr |
data |
h |
|
1 |
|
2 |
Podstawy |
|
|
|
[konfiguracja elektronowa (od H do Ne oraz Si, P, S, Cl, Ar), hybrydyzacja (sp3, sp2, sp)] |
2 |
|
3 |
Alkany, reakcje wolnorodnikowe, cykloalkany |
|
|
|
|
3 |
|
2 |
Alkeny i alkiny |
|
|
|
|
4 |
|
2 |
Związki monofunkcyjne: halogenki alkilu |
|
|
|
|
5 |
|
2 |
Alkohole i fenole |
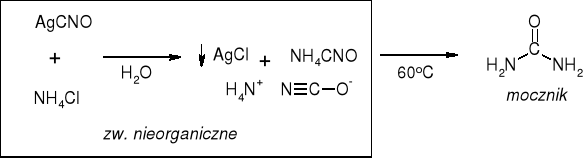
CHEMIA ORGANICZNA |
|
BERGMAN [1784] |
|
ZW. ORGANICZNE |
ZW. NIEORGANICZNE |
VIS VITALIS ≡ SIŁA ŻYCIOWA |
|
|
|
BERZELIUS [1818] WPROWADZIŁ TERMIN CHEMIA ORGANICZNA |
|
WOHLER [1828] |
|
|
|
BERTHELOT [1856-1863]: |
KOLBE [1848] |
CH4, HC≡CH, etc. |
SYNTEZA AcOH |
|
|
GMELIN [1848]: |
|
CHEMIA ORGANICZNA ≡ CHEMIA ZWIĄZKÓW WĘGLA O WODORU |
|
|
|
FARKLAND [1853]: WARTOŚCIOWOŚĆ |
|
|
|
COUPER, KEKULE, BUTLEROW: |
|
PODSTAWY TEORII STRUKTURALNEJ |
|
|
|
OBECNIE
|
|
15 MLN ZIAZKÓW ORGANICZNYCH |
200-300.000 NOWYCH ZWIAZKÓW ROCZNIE |
UKŁAD OKRESOWY |
|||||||||||||
OK. ↓ |
GRUPY: → |
||||||||||||
|
I |
II |
III |
IV |
V |
VI |
VII |
VIII |
|||||
1 |
1H |
|
|
|
|
|
|
He |
|||||
|
1s1 |
|
|
|
|
|
|
1s2 |
|||||
2 |
3Li |
4Be |
5B |
6C |
7N |
8O |
9F |
10Ne |
|||||
|
1s2 2s1 |
|
|
|
|
|
|
1s2 2s2p6 |
|||||
3 |
11Na |
12Mg |
13Al |
14Si |
15P |
16S |
17Cl |
18Ar |
|||||
|
1s2 2s2p6 3s1 |
|
|
|
|
|
|
1s2 2s2p6 3s2p6 |
|||||
4 |
|
|
|
|
|
|
|
|
|||||
5 |
|
|
|
|
|
|
|
|
|||||
6 |
|
|
|
|
|
|
|
|
|||||
7 |
|
|
|
|
|
|
|
|
|||||
1. ALKANY |
|
1.1. BUDOWA |
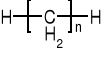
1.1.1. SZEREG HOMOLOGICZNY |
CnH2n+2
|
1.1.2. IZOMERIA |
1.1.2.1. IZOMERIA STRUKTURALNA |
1.1.2.2. IZOMERIA KONFORMACYJNA |
1.1.3. NAZEWNICTWO |
1.1.4. KARBO-JONY & KARBO-RODNIKI |
|
TRWAŁOŚĆ KARBO-JONÓW & KARBO-RODNIKÓW |
|
|
|
TRWAŁOŚĆ KARBOKATIONÓW |
|
|
|
WZROST ŁADUNKU
SPADEK TRWAŁOŚCI |
|
|
|
SPADEK ŁADUNKU
WZROST TRWAŁOŚCI |
|
TRWAŁOŚĆ KARBO-ANIONÓW |
|
SPADEK ŁADUNKU
WZROST TRWAŁOŚCI |
|
|
|
WZROST ŁADUNKU
SPADEK TRWAŁOŚCI |
|
|
|
TRWAŁOŚĆ KARBO-RODNIKÓW |
|
SPADEK TRWAŁOŚCI
|
|
|
|
WZROST TRWAŁOŚCI
|
|
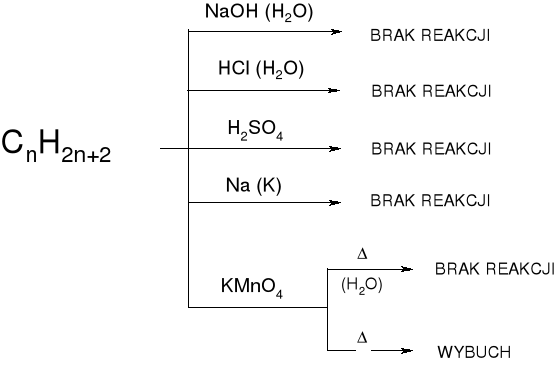
1.2. REAKTYWNOŚĆ |
|
PARAFINY (PARA AFFINI) ≡ MAŁO AKTYWNE |
1.2.1. REAKCJE ALKANÓW - REAKCJE WOLNORODNIKOWE |
|
|
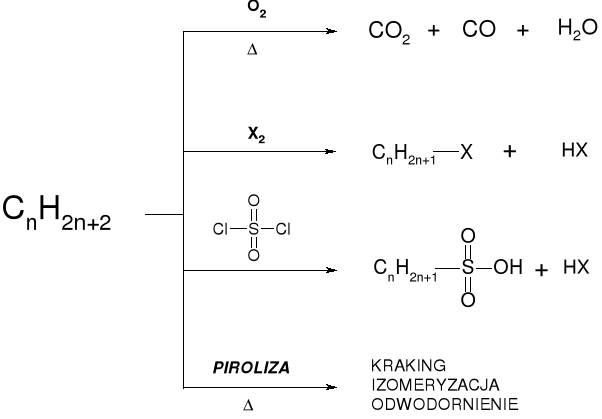
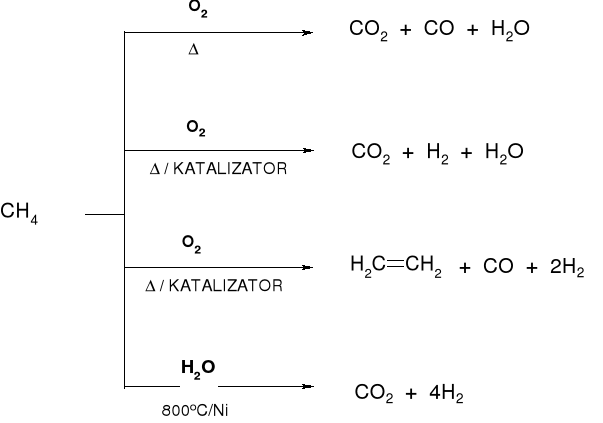
1.2.1.1. REAKCJE ALKANÓW Z TLENEM |
|
|
|
|
|
|
|
UTLENIANIE SELEKTYWNE |
|
|
|
|
|
n = 1 |
kwas octowy |
n=2 |
kwas propionowy |
n=16 |
kwas stearynowy |
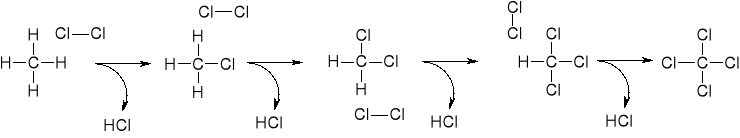
1.1.1.2. CHLOROWCOWANIE ALKANÓW |
|
|
|
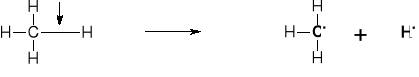
1. INICJOWANIE R. WOLNORODNIKOWEJ |
|
|
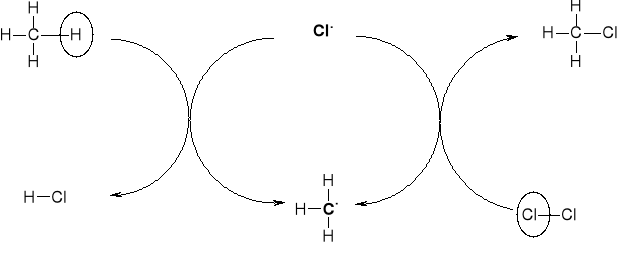
2. KONTYNUACJA R. ŁAŃCUCHOWEJ |
|
3. TERMINACJA (PRZERWANIE) R. ŁAŃCUCHOWEJ |
|
|
|
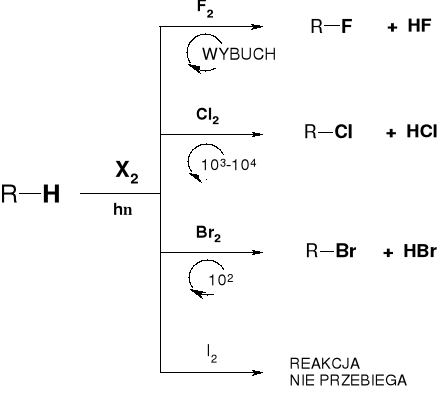
1.1.1.2. CHLOROWCOWANIE ALKANÓW |
|
|
|
|
|
|
|
|
ILOŚĆ OBROTÓW (n) REAKCJI PRZYPADAJĄCYCH NA 1 FOTON |
|
|
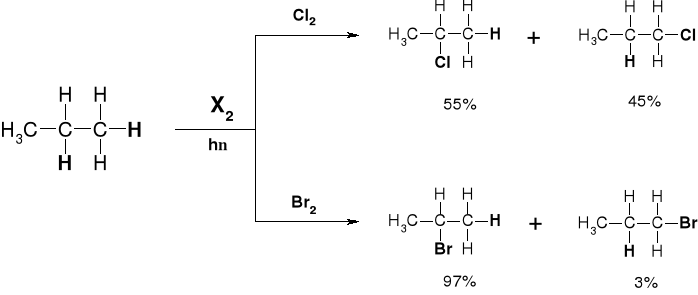
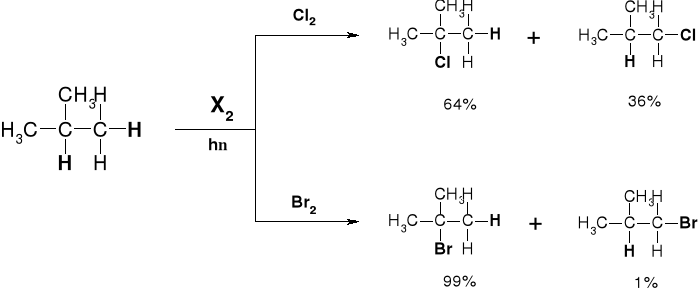
1.1.1.2. CHLOROWCOWANIE ALKANÓW |
1.1.1.2.1. KIERUNEK CHLOROWCOWANIA |
|
|
|
|
|
1.2. METODY PRZEMYSŁOWE OTRZYMYWANIA ALKANÓW |
1. METODA BERGIUSA |
|
|
2. METODA FISCHERA-TROPSCHA |
|
|
|
|
1.3. METODY CHEMICZNE OTRZYMYWANIA ALKANÓW |
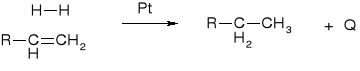
1. REDUKCJA ALKENÓW |
|
|
2. R. WURTZA |
|
|
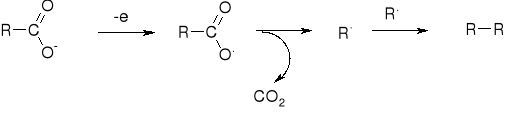
3. R. KOLBEGO |
|
|
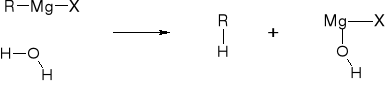
4. HYDROLIZA ZWIĄZKÓW GRIGNARDA |
|
|
2. CYKLOALKANY |
|||
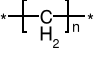
CnH2n
|
|||
2.1. BUDOWA |
|||
|
|
|
|
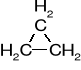
Cyklopropan |
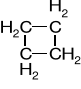
Cyklobutan |
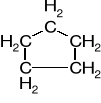
Cyklopentan |
Cyklohehsan |
KĄTY WIĄZAŃ C-C |
|||
60o |
90o |
?o |
?o |
2.1.1. KONFORMACJE CYKLOALKANÓW |
|||
2.2. REAKTYWNOŚĆ |
|||
SILNY WPŁYW WIELKOŚCI PIERŚCIENIA NA REAKTYWNOŚĆ: WIĘKSZY KĄT MNIEJSZE NAPRĘŻENIE WIĄZAŃ |
|||
CYKLOPENTAN & WYŻSZE CYKLOALKANY POSIADAJĄ REAKTYWNOŚĆ ALKANÓW |
|||
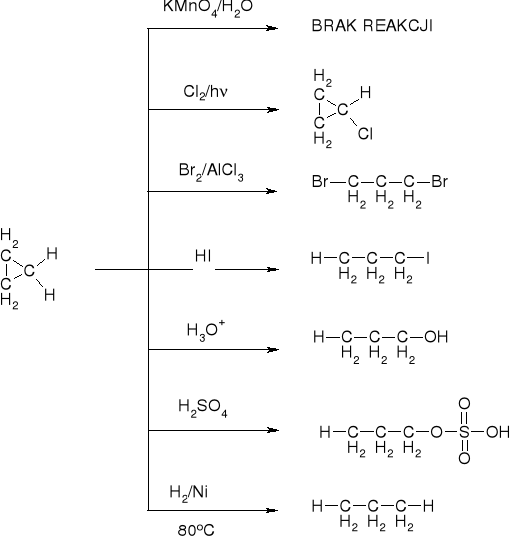
2.2.1. REAKTYWNOŚĆ CYKLOPROPANU |
|
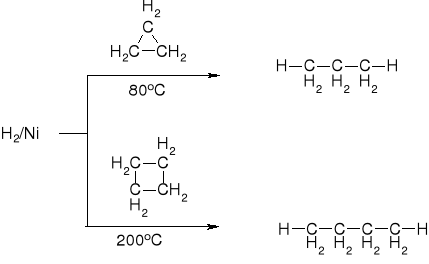
2.2.2. REAKTYWNOŚĆ CYKLOPROPANU I CYKLOBUTANU |
|
|
2.3. SYNTEZA |
|
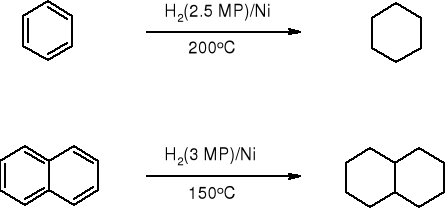
1. UWODORNIENIE WĘGLOWODORÓW AROMATYCZNYCH |
|
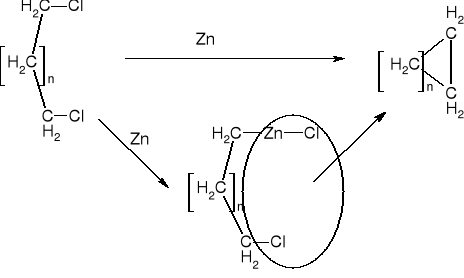
2. CYKLIZACJE |
|
n= 1,2 |
Wyszukiwarka
Podobne podstrony:
257 266 id 31221 Nieznany (2)
Lekki pojazd gasienicowy id 266 Nieznany
J 266
266
1 (266)
Mazowieckie Studia Humanistyczne r2002 t8 n2 s257 266
KD6 266 303
266
266
BANK 266 2015 01 08
266 267
266
266 i 267, Uczelnia, Administracja publiczna, Jan Boć 'Administracja publiczna'
MPLP 266 31.10.2009, lp
266 gotowy wykroj asymetryczna spodnica z zakadkami
Lektury 5 Lektury 2010 id 266 Nieznany
BANK 266 2015 01 24
266
więcej podobnych podstron