LICZBA MASOWA I ATOMOWA. IZOTOPY.
TEST
Podaj liczbę protonów, neutronów i nukleonów znajdujących się w jądrze atomu
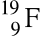
.
l. p: ..............................
l. n: ..............................
l. nukl.: ........................
3 p
Podaj liczbę protonów, neutronów i nukleonów znajdujących się w jądrze atomu
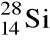
.
l. p: ..............................
l. n: ..............................
l. nukl.: ........................
3 p
Podaj liczbę protonów, neutronów i nukleonów znajdujących się w jądrze atomu
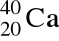
.
l. p: ..............................
l. n: ..............................
l. nukl.: ........................
3 p
Liczba masowa izotopu pierwiastka E wynosi 196. Neutrony w tym izotopie stanowią 60,2% nukleonów.
Na podstawie powyższych danych uzupełnij tabelę, dotyczącą budowy tego izotopu.
liczba neutronów |
|
liczba protonów |
|
2 p
Dla którego pierwiastka prawidłowo podano liczby elektronów, nukleonów, protonów i neutronów:
|
|
l. elektronów |
l. nukleonów |
l. protonów |
l. neutronów |
A. |
|
34 |
74 |
34 |
40 |
B. |
|
32 |
37 |
37 |
37 |
C. |
|
54 |
24 |
54 |
24 |
D. |
|
16 |
34 |
16 |
16 |
1 p
Liczba cząstek elementarnych w atomie
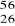
E wynosi:
|
liczba elektronów |
liczba neutronów |
liczba protonów |
A. |
30 |
26 |
26 |
B. |
26 |
26 |
30 |
C. |
30 |
30 |
26 |
D. |
26 |
30 |
26 |
1 p
Dla atomu
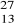
Al. Wskaż poprawną odpowiedź.
|
liczba elektronów |
liczba neutronów |
ładunek jądra |
A. |
27 |
14 |
+ 27 |
B. |
14 |
27 |
+ 13 |
C. |
13 |
27 |
+ 14 |
D. |
13 |
14 |
+ 13 |
1 p
Spośród podanych nuklidów:
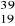
K,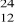
Mg,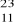
Na,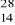
Si wybierz te, których atomy w jądrze posiadają 12 neutronów.
..........................................................................................................
1 p
Które z poniższych stwierdzeń jest prawdziwe?
w jądrze liczba protonów jest zawsze równa liczbie neutronów;
jądro każdego pierwiastka zbudowane jest z protonów i neutronów;
jądro ma zawsze ładunek dodatni;
liczba neutronów w jądrze jest zawsze taka sama jak liczba elektronów.
1 p
Pojęciom z kolumny 1 przyporządkuj odpowiednie określenia z kolumny 2:
1 |
2 |
I. elektron |
a) określa liczbę protonów w jądrze atomu |
II. proton |
b) określa sumę protonów i neutronów w jądrze atomu i oznaczamy ją symbolem A |
III. neutron |
c) elektrycznie obojętny składnik atomu |
IV. liczba atomowa |
d) cząstka elementarna o ładunku ujemnym |
V. liczba masowa |
e) cząstka o masie około 1 u i elementarnym ładunku dodatnim |
1 |
2 |
I. |
|
II. |
|
III. |
|
IV. |
|
V. |
|
5 p
Atom radonu
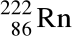
zawiera w jądrze:
222 protony i 86 neutronów;
86 protonów i 136 neutronów;
86 protonów i 222 neutrony;
86 protonów, 136 neutronów i 86 elektronów.
1 p
Jądro atomu pewnego pierwiastka zawiera 16 protonów i 16 neutronów. Podaj jego symbol, liczbę atomową i masową.
symbol pierwiastka: ..............
liczba atomowa: ...............
liczba masowa: .................
3 p
Informacja do zadań: 10 i 11.
Najbardziej rozpowszechnionym izotopem polonu, pierwiastka odkrytego przez małżonków Curie w 1898 roku, jest izotop ![]()
.
Liczbę protonów i elektronów znajdujących się w atomie izotopu
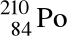
prawidłowo podano w punkcie:
|
p+ |
e- |
A. |
210 |
84 |
B. |
84 |
84 |
C. |
210 |
210 |
D. |
84 |
210 |
1 p
Liczba neutronów w jądrze atomu izotopu
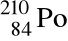
wynosi:
420;
168;
126;
294.
1 p
Wskaż wyjątek od stwierdzenia dotyczącego budowy atomów:
Jądra wszystkich pierwiastków składają się z protonów i neutronów.
............................
1 p
Podaj liczby atomowe Z dla atomów zawierających:
11 protonów: ....................
20 elektronów: ....................
2 p
O dwóch izotopach pierwiastka
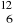
A1 i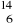
A2 wiadomo, że:
|
liczba protonów w atomach A1 i A2 jest |
liczba neutronów w atomach A1 i A2 jest |
A. |
różna |
taka sama |
B. |
różna |
różna |
C. |
taka sama |
taka sama |
D. |
taka sama |
różna |
1 p
Które z podanych nuklidów:
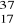
E,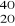
E,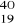
E,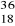
E,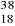
E są izotopami?
..............................................................................................................
Odpowiedź uzasadnij:
.......................................................................................................................................................
.......................................................................................................................................................
2 p
Przyporządkuj terminom w kolumnie I odpowiednie objaśnienia z kolumny II.
Kolumna I |
Kolumna II |
1. nuklid |
A. zbiór atomów o tej samej wartości liczby atomowej |
2. pierwiastek |
B. nazwa elektrycznie obojętnej cząstki składowej jądra o masie ok. 1 u |
3. nukleon |
C. zbiór atomów o tej samej wartości liczby atomowej i masowej |
4. neutron |
D. nazwa cząstki składowej jądra o masie ok. 1 u i jednostkowym ładunku dodatnim |
5. proton |
|
Kolumna I |
Kolumna II |
1. |
|
2. |
|
3. |
|
4. |
|
5. |
|
5 p
Podaj liczbę ładunków dodatnich i ujemnych zawartych w atomach o następującej liczbie atomowej: Z = 14
liczba ładunków dodatnich: ....................
liczba ładunków ujemnych: ....................
2 p
Podaj liczby: elektronów, nukleonów, protonów i neutronów zawartych w następującym atomie:
![]()
liczba elektronów: ..................
liczba nukleonów: ..................
liczba protonów: ..................
liczba neutronów: ..................
4 p
Posługując się zapisem
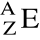
podaj zapisy atomów o następującym składzie jądra atomowego:
liczba protonów: 20
liczba neutronów: 20
...........................
1 p
Zapisz dane
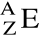
dla atomu, którego:
liczba masowa równa jest sumie liczby protonów w atomie
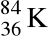
i liczby neutronów w atomie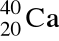
;liczba neutronów równa jest iloczynowi liczby elektronów w atomie
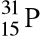
i liczby neutronów w atomie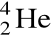
.
........................................................
2 p
Uzupełnij luki w poniższym tekście:
Atom polonu -
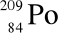
składa się z ............................... protonów, ............................... neutronów, ............................... elektronów, ............................... nukleonów.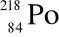
i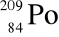
stanowią parę ......................................., która ma taką sama liczbę ....................................... i różną liczbę ....................................... . Nuklidy te zawierają w jądrze ....................................... liczbę neutronów.
8 p
Spośród nuklidów:
![]()
![]()
![]()
![]()
![]()
![]()
wybierz i wpisz w odpowiednie rubryki te, które spełniają podane warunki:
są izotopami |
|
mają jednakową liczbę elektronów |
|
mają jednakową liczbę neutronów |
|
mają jednakowa liczbę nukleonów |
|
4 p
Dany jest pierwiastek
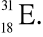
Podaj:jego miejsce w układzie okresowym pierwiastków:
..........................................................................................................................
liczbę poszczególnych cząstek elementarnych:
..........................................................................................................................
2 p
Uzupełnij tabelę:
cząstka |
protony |
elektrony |
nukleony |
neutrony |
|
|
|
|
|
4 p
Uzupełnij tabelę:
cząstka |
protony |
elektrony |
nukleony |
neutrony |
|
|
|
|
|
4 p
Liczba cząstek elementarnych w atomie
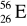
wynosi:
|
liczba elektronów |
liczba neutronów |
liczba protonów |
A. |
30 |
26 |
26 |
B. |
26 |
26 |
30 |
C. |
30 |
30 |
26 |
D. |
26 |
30 |
26 |
1 p
O dwóch izotopach pierwiastka E wiadomo, że mają następujące liczby masowe: A1 i A2. Wybierz odpowiedź określającą liczby cząstek elementarnych w jądrach tych atomów:
|
liczba protonów w atomach A1 i A2 jest: |
liczba neutronów w atomach A1 i A2 jest: |
A. |
różna |
taka sama |
B. |
różna |
różna |
C. |
taka sama |
taka sama |
D. |
taka sama |
różna |
1 p
Zapis:
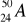
,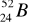
,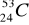
dotyczy trzech różnych nuklidów. Są nimi kolejno:
cyna, tellur, jod;
wanad, chrom, mangan;
cyna;
chrom.
liczby atomowe: cyna - 50, tellur - 52, jod - 53, chrom - 24.
1 p
W podanych niżej zdaniach uzupełnij brakujące słowa:
Izotopy są to odmiany tego samego ............................... złożone z atomów o tych samych liczbach ....................................., a różnych liczbach ............................... . Różnią się więc liczbą ................................. w jądrze. Prot, ........................... i tryt są izotopami ........................... .
6 p
Pierwiastek jest to zbiór atomów o tej samej:
liczbie atomowej;
liczbie masowej;
liczbie protonów w jądrze atomowym;
liczbie neutronów;
poprawne są odpowiedzi A i C.
1 p
O neutronach można powiedzieć, że:
równoważą masę protonów;
nadają dodatni ładunek jądru;
tworzą chmurę ładunku wokół jądra;
ich liczba jest różna w nuklidach izotopów danego pierwiastka;
mają masę równą 1/1836 u.
1 p
Podany zbiór atomów podziel na zbiory izotopów i podaj ich nazwy:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
I zbiór: ................................................................. nazwa zbioru: ...............................
II zbiór: ................................................................. nazwa zbioru: ...............................
III zbiór: ................................................................. nazwa zbioru: ...............................
3 p
Podkreśl cechy, którymi różnią się dwa atomy zapisane w następujący sposób:
![]()
i ![]()
liczba neutronów, liczba nukleonów, liczba atomowa, liczba masowa, liczba elektronów, ładunek jądra.
3 p
Z podanych zdań wybierz zdanie fałszywe:
proton jest trwałą cząstką elementarną;
proton ma dodatni ładunek elektryczny;
masa protonu jest około 1836 razy mniejsza od masy elektronu;
proton wchodzi w skład jądra atomowego.
1 p
Proton jest to:
trwała cząstka o ujemnym ładunku elektrycznym i masie równej w przybliżeniu 1 u;
cząstka o ujemnym ładunku elektrycznym i masie 1/1836 u;
trwała cząstka o dodatnim ładunku elektrycznym i masie równej w przybliżeniu 1/1836 u;
cząstka elektrycznie obojętna o masie równej w przybliżeniu 1 u;
trwała cząstka elementarna o dodatnim ładunku elektrycznym i masie równej w przybliżeniu jednostce mas atomowych.
1 p
Która z informacji, odnoszących się do elektronu jest nieprawdziwa?
masa elektronu jest niewielka w porównaniu z masą jądra i wynosi 0,0005434 u;
wartość ładunku zgromadzonego na elektronie zwana jest ładunkiem elementarnym;
łączny ładunek elektronów w atomie jest równy co do wartości ładunkowi jądra;
atom przekształcony w jon jednoujemny posiada jeden elektron.
1 p
O masie atomu decyduje liczba:
neutronów;
protonów;
elektronów;
nukleonów.
1 p
Prawie cała masa atomu skupiona jest:
w chmurze elektronowej;
w jądrze atomowym;
w całym atomie;
tylko w protonach atomów wieloelektronowych;
tylko w neutronach.
1 p
Elektron jest to:
najmniejsza cząstka o ujemnym elementarnym ładunku elektrycznym i masie 1836 razy mniejszej od masy protonu;
cząstka elementarna, elektrycznie obojętna, o masie w przybliżeniu równej masie protonu;
cząstka o dodatnim ładunku elementarnym i masie 1836 razy mniejszej od masy protonu;
trwała cząstka o ujemnym ładunku elementarnym i masie 1836 razy większej od masy protonu;
negaton o ładunku elementarnym i masie równej jednostce mas atomowych.
1 p
O neutronach można powiedzieć, że:
równoważą masę protonów;
nadają dodatni ładunek jądru;
tworzą chmurę ładunku wokół jądra;
ich liczba jest różna w nuklidach izotopów danego pierwiastka;
mają masę równą 1/1836 u.
1 p
Przy każdej z podanych informacji dopisz odpowiednią nazwę cząstek składowych jądra atomowego:
a) mają masę równą 1 u i ładunek „+” ........................................
b) mają masę równą 1 u i nie mają ładunku elektrycznego ........................................
2 p
Pozyton to cząstka o masie równej masie elektronu i ładunku równym ładunkowi protonu. Podaj masę i ładunek pozytonu.
masa: ........................................
ładunek: ........................................
2 p
Do opisu budowy atomu używane są pojęcia: cząstki elementarne, proton, neutron, elektron, nukleon, liczba atomowa, liczba masowa. Niektóre z nich związane są bezpośrednio z jądrem atomowym.
Z podanych powyżej określeń wybierz trzy bezpośrednio związane z jądrem atomowym.
........................................
........................................
........................................
3 p
Wyszukiwarka
Podobne podstrony:
Liczba atomowa a liczba masowa
3Liczba atomowa i liczba masowa zadania do lekcji nr 2
2Liczba atomowa i liczba masowa zadania do lekcji nr 1
WODOROTLENKI, Liceum, testy
Nazewnictwo i podział tlenków, Liceum, testy
MODEL ATOMU BOHRA, Liceum, testy
Typy reakcji chemicznych, Liceum, testy
UKŁAD OKRESOWY PIERWIASTKÓW, Liceum, testy
Nazewnictwo i podział kwasów, Liceum, testy
OBLICZENIA CHEMICZNE, Liceum, testy
Właściwosci tlenków kwasowych i zasadowych, Liceum, testy
PROMIENIOTWÓRCZOŚĆ, Liceum, testy
Chemia - wiązania atomowe, Liceum Matura, Chemia, Chemia(1)
METODY OTRZYMYWANIA SOLI, Liceum, testy
ekologia2k, Nauka, Szkoła, Matura, Biologia - testy liceum, Testy
ROZTWORY, Liceum, testy
więcej podobnych podstron