ODDZIAŁYWANIA MIĘDZYCZĄSTECZKOWE
Gazy nawet typu He lub H2 można skroplić i nawet zestalić. Woda
H2O (m. cz. = 18) jest cieczą, H2S (m. cz. = 34) jest gazem.
n-pentan C5H12 CH3-CH2-CH2-CH2-CH3 t. w. = 36 o C
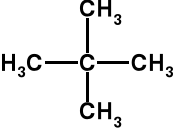
2,2-dimetylopropan C5H12 t. w. = 10 o C
ta sama masa cząsteczkowa co n-pentan
Jakie oddziaływania mają miejsce między cząsteczkami i co z nich wynika?
Typy oddziaływań międzycząsteczkowych
Siły dyspersyjne Londona
Typowa energia ~ 2 KJ · mol-1 dla H2, He, Ne.
Nawet całkowicie niepolarne cząsteczki (N2, H2) i pojedyncze atomy (He, Ne) dają się skroplić lub zestalić. Kiedy mówimy, że jakaś cząsteczka jest niepolarna, to rozumiemy, że uśredniony moment dipolowy wynosi 0. Ale on się zmienia w czasie. Przyczyna - fluktuacje chmur elektronowych. Dwa chwilowe dipole się przyciągają. Ulegają temu oddziaływaniu wszystkie cząsteczki.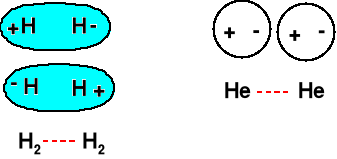
Oddziaływania najsłabsze, ale addytywne. Dla długich łańcuchów dość duże. Im więcej elektronów w cząsteczce tym tego typu oddziaływania silniejsze.
F2 - gaz, Cl2 - gaz, Br2 - ciecz, I2 - ciało stałe.
n-pentan C5H12 ruchliwa ciecz, n-pentadekan C15H32 - olej,
n-oktadekan C18H38 - woskowate ciało stałe.
Kształt cząsteczki - im bardziej „kulista” cząsteczka tym oddziaływania słabsze.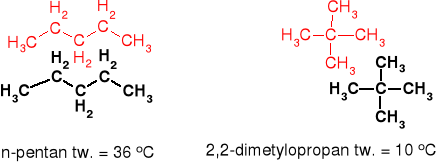
Oddziaływania dipol-dipol, dla substancji polarnych, trwałe ładunki cząstkowe sąsiednich cząsteczek oddziaływają między sobą.
Typowa energia ~ 2 KJ · mol-1. Jeżeli cząsteczki rotują (faza gazowa) to tylko ~ 0,3 KJ · mol-1. Skraplanie i zestalanie gazów polarnych jest częściowo spowodowane tym oddziaływaniem
Oddziaływania dipol-dipol indukowany, oddziaływania raczej słabe, ale np. „ luźne związki CH4 z wodą ”, hydraty gazów szlachetnych (stosunkowo trwałe). Często substancje są utrzymywane w stanie ciekłym lub stałym przez te wszystkie siły razem.
Oddziaływania 1, 2, 3 nazywa się często oddziaływaniami van der Waals'a.
Wiązania wodorowe. Jest utworzone przez atom wodoru między dwoma małymi elektroujemnymi atomami (N, O i F)
Typowa energia ~ 20 KJ · mol-1. Najsilniejsze z oddziaływań międzycząsteczkowych. Ale entalpia wiązania H2 = 436 KJ · mol-1.
Temp. wrzenia (o C) - w przybliżeniu miara oddziaływań międzycząsteczkowych
HF (19,5), HCl (-84,2), HBr (-67,1), HI (-35,1)
H2O (100), H2S (-60,1), H2Se (-41,3), H2Te (-4,1).
NH3 (-34,5), PH3 (-87,7), AsH3 (-62,4), SbH3 (-18,4).
CH4 (-161,5), SiH4 (-118,8), GeH4 (-88,1), SnH4 (-52,5).
Woda - skomplikowany układ wiązań wodorowych
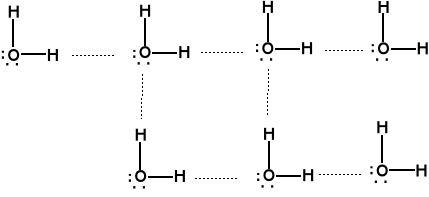
Podobnie amoniak
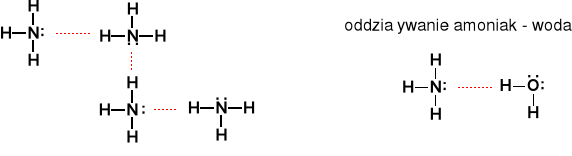
dobra rozpuszczalność HF we wodzie i alkoholu we wodzie.

Alk. etylowy (M.cz. 46) tw.=78,3 oC eter metyl. (M.cz. 46) tw.=-24 oC
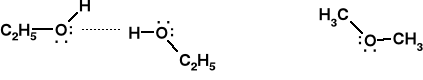
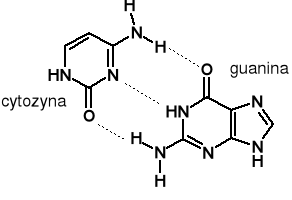
Przykłady biologiczne: drewno, białka, łańcuch DNA
Ciecze i CIAŁA STAŁE
Ciecze; atomy jony lub cząsteczki są blisko siebie, ściśliwość cieczy jest niewielka, ale oddziaływania międzycząsteczkowe pozwalają na niezależny ruch cząsteczek, jonów lub atomów wobec siebie.
Lepkość cieczy - wynik oddziaływań międzycząsteczkowych.
Rtęć, kwas siarkowy, gliceryna, pentadekan, woda, eter etylowy
Napięcie powierzchniowe wynika z niezrównoważenia sił międzycząsteczkowych przy powierzchni cieczy. Stąd wynikają siły kapilarne i menisk.
Siły adhezji: oddziaływanie powierzchnia naczynia - cząsteczki w cieczy.
Siły kohezji: oddziaływanie cząsteczki w cieczy - cząsteczki w cieczy.

Ciała stałe; atomy jony lub cząsteczki są blisko siebie, oddziaływania międzycząsteczkowe nie pozwalają na niezależny ruch cząsteczek, jonów lub atomów wobec siebie. Ciała stałe dzielą się na:
bezpostaciowe (amorficzne) np. szkło, kauczuk, smalec, szkło kwarcowe. Atomy, jony lub cząsteczki są rozmieszczone bezładnie.
krystaliczne np. chlorek sodu, metale, siarka rombowa, fosfor czarny, naftalen, kwarc. Atomy, jony lub cząsteczki są rozmieszczone w sposób uporządkowany tworząc sieć krystaliczną. Wykazują płaskie powierzchnie zwane ścianami kryształu.
ciekłe kryształy, właściwości pośrednie między cieczą a ciałem krystalicznym.
Ciała krystaliczne; podział ze względu na oddziaływania międzycząsteczkowe scalające kryształ.
Metale, scalone przez wiązanie metaliczne, pierwiastki bloków s, p i d. K, Ba, Au, Al, Fe, Pt. Kowalne, ciągliwe, przewodniki ciepła i prądu elektrycznego.
Jonowe, scalone przez przyciąganie się anionów i kationów. Sole, tlenki, wodorotlenki. NaCl, BaO, KOH, Twarde, sztywne, kruche, wysokie temperatury topnienia i wrzenia. Stopione oraz rozpuszczone we wodzie przewodzą prąd elektryczny.
Kowalencyjne, usieciowane przez oddziaływania kowalencyjne w całej objętości kryształu. Diament, kwarc, bor. Twarde, sztywne, kruche, wysokie temperatury topnienia i wrzenia, nierozpuszczalne we wodzie. W stanie stopionym nie przewodzą prądu elektrycznego
Molekularne, usieciowane przez oddziaływania międzycząsteczkowe typu dyspersyjne, dipol - dipol lub wiązanie wodorowe. P4, I2, lód, naftalen. Stosunkowo niskie temperatury topnienia i wrzenia, kruche.
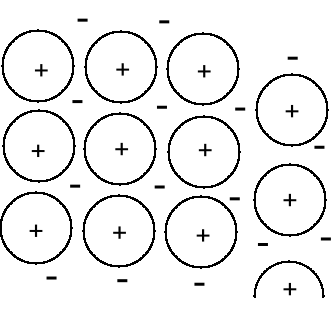
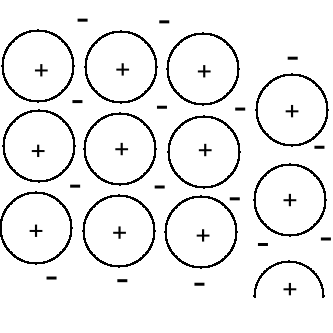
Metale.
Sieć przestrzenna zbudowana jest z jonów metalu otoczonych morzem elektronów, stąd połysk, kowalność, przewodnictwo elektronowe.
Pasmowa teoria ciała stałego.
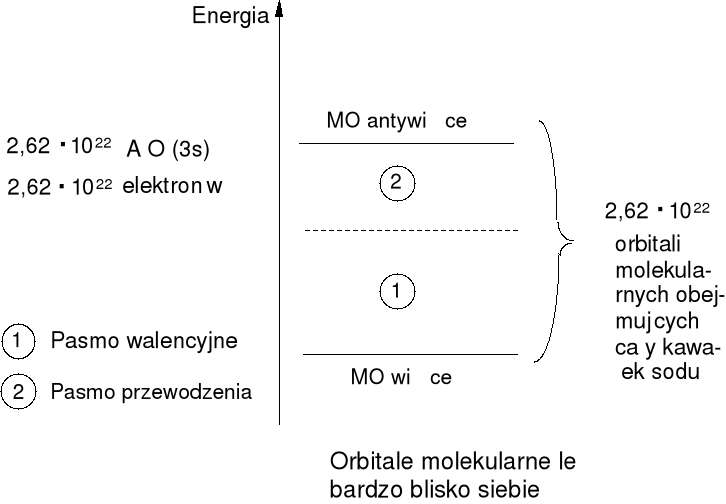
Jest to zastosowanie teorii orbitali molekularnych do makrocząsteczek. Rozpatrzmy ”cząsteczkę” składającą się z 1g sodu (1 mol Na = 23g) - 2,62 · 1022 atomów sodu co daje 2,62 · 1022 orbitali atomowych 3s z obsadzeniem 2,62 · 1022 elektronów. Tworzymy 2,62 · 1022 orbitale
molekularne, około połowa obsadzona jest przez pary elektronowe.
![]()
Przewodniki, izolatory, półprzewodniki
CB - pasmo przewodzenia
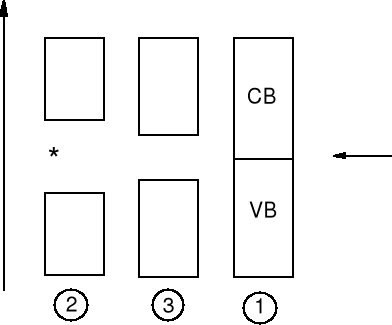
(conductivity band)
poziom Fermiego
(najwyższy poziom
obsadzony)
![]()
VB - pasmo walencyjne
(valence band)
Domieszkowanie półprzewodników, n arsen, p bor.
8
![]()
Wyszukiwarka
Podobne podstrony:
04-Wodór TECH, Materiały PG, Nieorgana
12-helowceTECH, Materiały PG, Nieorgana
13-fluorowceTECH, Materiały PG, Nieorgana
08-tlen, Materiały PG, Nieorgana
TCh1-stud1, Materiały PG, Nieorgana
11-dysocjacjaTECH, Materiały PG, Nieorgana
IR, Materiały PG, Nieorgana
05-OrbitalemolekTECH, Materiały PG, Nieorgana
Egzamin pisemny TChem 2010-tematy-1, Materiały PG, Nieorgana
7-makroukłady TECH, Technologia chemiczna PG, Chemia, I ROK, WYKŁADY, WYKŁADY
Akustyka materiały pg gda
MATERIAŁY IZOLACYJNE NIEORGANICNE, MATERIAŁY IZOLACYJNE NIEORGANICNE
L 07 F2 Fale materii
2006-07 Czarna procesja, materiały, Z PRASY
07 - Kompomery, Stomatologia, Materiałoznawstwo stomatologiczne
opracowanie pyt z tech chem cz nieorg
więcej podobnych podstron