5. SPALANIE
5.1. WPROWADZENIE, POJĘCIA PODSTAWOWE
Spalanie jest procesem fizyko-chemicznym, którego podstawę stanowi reakcja gwałtownego utleniania palnych składników paliwa przez tlen zawarty w powietrzu. W niskiej temperaturze (np. temperatura otoczenia) paliwo nie ulega spalaniu pomimo dostępu odpowiedniej ilości tlenu. Do zapoczątkowania procesu należy układ (paliwo - powietrze) doprowadzić do odpowiednio wysokiej temperatury, tak oby został osiągnięty poziom energii aktywacji reakcji utleniania. W rozpatrywanym wypadku odpowiada to temperaturze zapłonu. Wystarczy, że wystąpi ona tylko lokalnie. Zapoczątkowany lokalnie proces przebiega dalej z dużą szybkością samoistnie (autotermicznie), bowiem jego efektem jest wyzwalanie się dużej ilości ciepła.
Zagadnienie spalania zostanie tutaj omówione wybiórczo, jedynie pod kątem obliczania ilości oraz składu powstających w procesie spalin. W opisie rachunkowym symbole dotyczące stężeń oraz ilości poszczególnych składników substratów będą oznaczane indeksem górnym ![]()
(prim) a dotyczące stężeń oraz ilości składników produktów ![]()
(bis).
Jeśli pominiemy obecność w spalinach zanieczyszczeń powstających w procesach ubocznych (takich jak ![]()
lub ![]()
), a głównymi produktami spalania są ![]()
oraz ![]()
to proces spalania jest całkowity i zupełny. Jeśli w spalinach występują gazowe składniki palne (![]()
, ![]()
, ![]()
, itp.) to wtedy spalanie jest niezupełne. Natomiast jeśli w spalinach są obecne stałe składniki palne (sadza, koksik) to wtedy spalanie jest niecałkowite.
Prowadzone dalej rozważania będą dotyczyć procesu spalania przebiegającego całkowicie i zupełnie. W ten sposób idealizuję się omawiany proces, bowiem zwykłe w gazach spalinowych występują jakieś (choćby niewielkie, a nawet śladowe) ilości ![]()
oraz sadzy.
Dla właściwego przebiegu procesu spalania niezbędne jest:
dobre wymieszanie paliwa powietrzem, tak aby wszystkie cząstki palne znalazły w swoim otoczeniu dostateczną ilość tlenu (do całkowitego i zupełnego spalenia),
dostateczne podgrzanie mieszaniny do temperatury odpowiadającej (co najmniej) temperaturze zapłonu.
Paliwo i powietrze są substratami procesu spalania. W powietrzu to tlen jest składnikiem aktywnym, biorącym udział w reakcji. Pozostałe składniki nie biorą udziału w procesie i stanowią nieaktywny balast. Przy obliczaniu składu i ilości spalin, a także zapotrzebowania powietrza zakładamy jego uproszczony skład. Przyjmujemy, że stężenie tlenu wynosi ![]()
21% a resztę stanowi azot ![]()
79%. Dla uproszczenia pomija się także obecność w powietrzu pary wodnej.
Ze względu na niedoskonałość wymieszania substratów spalania, dla zapewnienia dostatecznej ilości tlenu w każdym miejscu komory spalania, stosujemy odpowiedni nadmiar powietrza. Celem tego jest zagwarantowanie odpowiedniego nadmiaru tlenu, w stosunku do ilości wynikającej ze stechiometrii reakcji spalania. Nadmiar powinien być tym większy im trudniej jest wymieszać substraty. Stosunek rzeczywistej ilości powietrza do ilości teoretycznej (wynikającej ze stechiometrii) nazywamy współczynnikiem nadmiaru powietrza λ.
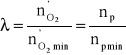
(5.1)
gdzie:
![]()
- rzeczywiste zapotrzebowanie na tlen,
![]()
- teoretyczne (minimalne) zapotrzebowanie na tlen,
![]()
- rzeczywiste zapotrzebowanie na powietrze,
![]()
- teoretyczne (minimalne) zapotrzebowanie na powietrze.
Rzeczywista ilość powietrza będzie zatem zależna od niezbędnego nadmiaru powietrza λ.
![]()
(5.2)
Relację między ilością powietrza oraz zawartą w nim ilością tlenu, wyrażoną w kilomolach, można wyliczyć z proporcji.
1 kmol powietrza - 0,21 kmol O2
n kmol powietrza - 1 kmol O2
stąd: n kmol powietrza = ![]()
4,76kmol (5.3)
4,76 kilomoli powietrza zawiera 1 kilomol O2 oraz 3,76 kilomoli N2
Spalanie 1 kilomola węgla C, z zastosowaniem stechiometrycznej ilości powietrza (tlenu), można opisać następującym równaniem:
1 kmol C + 1 kmol O2 + 3,76 kmol N2 = 1 kmol CO2 + 3,76 kmol N2 (5.4)
Spalanie 1 kilomola węgla C, z zastosowaniem nadmiaru powietrza (określonym współczynnikiem nadmiaru λ), można opisać równaniem:
1 kmol C + λ kmol O2 + 3,76·λ kmol N2 = 1 kmol CO2 + (λ - 1) kmol O2 + λ·3,76 kmol N2 (5.5)
Z faktu, iż spalanie prowadzimy z nadmiarem powietrza wynika, że w spalinach występuje tlen. Będzie go tym więcej, im większy nadmiar powietrza zastosujemy. Jego stężenie w spalinach, wyrażone ułamkiem molowym ![]()
, możemy wyliczyć na podstawie składu spalin, wyrażonego liczbą kilomoli składników, który przedstawia prawa strona równania (5.5).
![]()
(5.6)
Z powyższej zależności możemy wywieść równanie, pozwalające określić współczynnik nadmiaru powietrza λ, w funkcji stężenia tlenu w spalinach ![]()
.
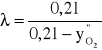
(5.7)
Dla rozpatrywanego, wyidealizowanego przypadku spalania czystego węgla stężenia ![]()
oraz ![]()
w spalinach są ze sobą ściśle powiązane.
![]()
(5.8)
Stąd wyrażenie (5.7) może przyjąć postać:
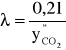
(5.9)
Pomimo, że wzór (5.7) został wyprowadzony dla przypadku spalania paliwa zawierającego czysty węgiel, to można go stosować, uzyskując zadawalającą dokładność, do obliczeń dla wszystkich paliw energetycznych. Możemy zatem poprzez oznaczanie składu spalin kontrolować rzeczywistą wartość współczynnika nadmiaru powietrza λ. Jest to bardzo ważny parametr decydujący o jakości procesu spalania. Zbyt mały nadmiar powietrza jest przyczyną niedokładnego spalania i powstawania dużych ilości produktów niecałkowitego i niezupełnego spalania (CO, sadza). Zbyt duży nadmiar powietrza prowadzi do nieefektywnego wykorzystania wyzwalanego w kotle ciepła. Powstaje bowiem wtedy większa ilość spalin i tym samym większa ilość ciepła jest wraz z nimi wyprowadzana bezużytecznie do otoczenia. Odpowiednie wartości współczynnika nadmiaru powietrza dla różnego typu kotłów są z znane z praktyki.
Tabela 5.1
Wartości współczynników nadmiaru powietrza λ dla różnych typów kotłów
Typ kotła |
Paliwo |
λ |
z rusztem zasilanym ręcznie |
węgiel kamienny węgiel brunatny drewno |
1,4 ÷ 1,7 1,5 ÷ 1,8 1,35 |
z rusztem mechanicznym |
węgiel kamienny węgiel brunatny |
1,25 ÷ 1,6 1,3 ÷ 1,5 |
pyłowy |
węgiel kamienny lub brunatny w formie pyłu |
1,25 |
olejowy |
olej opałowy |
1,2 ÷ 1,5 |
gazowy |
gaz ziemny |
1,05 ÷ 1,15 |
Zestawione w tabeli wartości λ zostały zebrane z różnych pozycji literatury dotyczącej omawianego zagadnienia. Mają one jedynie charakter orientacyjny. Właściwy nadmiar powietrza zależy od wielu czynników, w tym znacznie od szczegółów konstrukcyjnych kotła oraz urządzeń wspomagających jego pracę.
5.2. SPALANIE PALIW GAZOWYCH
5.2.1. Stechiometria spalania -obliczanie zapotrzebowania na powietrze
W przypadku spalania paliw gazowych, o znanym składzie molowym, zapotrzebowanie na powietrze, ilość powstających spalin oraz ich skład możemy wyliczyć na podstawie zależności teoretycznych.
Skład gazu suchego można opisać następującym równaniem:
![]()
![]()
(5.10)
W skład gazu wchodzą składniki palne (H2, CO, CH4, węglowodory - CmHn), niepalne (N2, CO2) oraz tlen (tylko w nieznacznych, bezpiecznych ilościach). Teoretyczne zapotrzebowanie na tlen do spalania można wyliczyć z równań stechiometrycznych.
Spalanie wodoru
1 kmol H2 + 0,5 kmol O2 = 1 kmol H2O (5.11)
Do spalenia 1 kilomola wodoru potrzeba 0,5 kilomola tlenu, zatem do spalenia ![]()
kilomola wodoru potrzeba (![]()
) kilomola tlenu.
Spalanie tlenku węgla
1 kmol CO + 0,5 kmol O2 =1 kmol CO2 (5.12)
Do spalenia 1 kilomola tlenku węgla potrzeba 0,5 kilomola tlenu, zatem do spalenia ![]()
kilomola tlenku węgla potrzeba (![]()
) kilomola tlenu.
Spalanie metanu
1 kmol CH4 +2 kmol O2 = 1 kmol CO2 +2 kmol H2O (5.13)
Do spalenia 1 kilomola metanu potrzeba 2 kilomoli tlenu, zatem do spalenia ![]()
kilomola wodoru potrzeba (![]()
) kilomola tlenu.
Spalanie węglowodorów o ogólnym wzorze CmHn
1 kmol CmHn +![]()
kmol O2 = m kmol CO2 +![]()
kmol H2O (5.14)
Powyższe równanie dotyczy każdego węglowodoru, zawartego w spalanym gazie, o liczbie atomów węgla w cząsteczce większej niż jeden. Dla każdego z nich zapotrzebowanie na tlen do spalenia liczymy osobno. Przykładowo, dla spalenia 1 kilomola propanu C3H8 zapotrzebowanie na tlen wynosi (3 + 8/4) = 5, zatem dla spalenia ![]()
kilomola propanu potrzeba ![]()
kilomola tlenu.
Teoretyczne (stechiometryczne, minimalne) zapotrzebowanie na tlen do spalenia 1 kilomola gazu ![]()
wyniesie zatem:
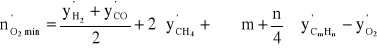
(5.15)
Wymiarem ![]()
jest 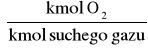
Teoretyczne (minimalne) zapotrzebowanie na powietrze ![]()
będzie odpowiednio większe - stosownie do równości (5.3) - i wyniesie:
![]()
(5.16)
A w zapisie rozszerzonym, z wykorzystaniem wzoru (5.15):
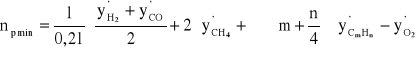
(5.17)
Wymiarem ![]()
jest 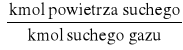
Rzeczywiste zapotrzebowanie na powietrze obliczamy z wzoru (5. 2). W tym wypadku współczynnik nadmiaru powietrza λ przyjmujemy z zakresu 1,05 ÷ 1,15. Nadmiar powietrza jest tutaj mniejszy niż wypadku spalania węgla. Wynika to z tego, że paliwo gazowe łatwiej wymieszać powietrzem niż paliwo stałe, jakim jest węgiel.
5.2.2. Ilość i skład spalin
Podczas spalania całkowitego i zupełnego spaliny będą zawierać :
ditlenek węgla (z węgla w paliwie),
azot (z azotu w powietrzu oraz w paliwie),
tlen (z nadmiaru tlenu w powietrzu),
parę wodną (ze spalenia wodoru zawartego w paliwie).
Przedstawiony niżej sposób obliczania odnosi się do 1 kilomola gazu. Do obliczeń potrzebna jest znajomość składu ilościowego gazu.
Ilość ditlenku węgla w spalinach.
![]()
(5.18)
gdzie: ![]()
- ilość kmoli węgla (jako składnika elementarnego) w paliwie, którą obliczamy z następującego wzoru:
![]()
(5.19)
Ilość azotu w spalinach
![]()
(5.20)
gdzie: ![]()
- ilość kmoli azotu zawartego w paliwie,
![]()
- ilość azotu dostarczonego z powietrzem.
Ilość tlenu w spalinach
![]()
(5.21)
![]()
(5.21a)
Ilość pary wodnej w spalinach
![]()
(5.22)
gdzie: ![]()
- ilość wodoru (jako składnika elementarnego) w paliwie, którą obliczamy z następującego wzoru:
![]()
(5.23)
Całkowita ilość spalin wilgotnych ![]()
będzie równa:
![]()
(5.24)
Całkowita ilość spalin suchych ![]()
wyniesie:
![]()
(5.25)
Objętość spalin obliczamy mnożąc obliczone ilości kilomoli przez objętość molową.
5.2.3. Współczynnik nadmiaru powietrza
Współczynnik nadmiaru powietrza można opisać, w sposób zbliżony do tego, który opisano wzorem (5.7).
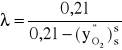
(5.26)
Przedstawiony wyżej wzór uzyskano przez stosowne przekształcenie wzoru (5.7), w którym uwzględniono specyfikę spalania gazu. Występujące w nim stężenie tlenu odniesione do spalin suchych, ![]()
, obliczymy w następujący sposób:
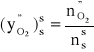
(5.27)
Inną formułę na obliczenie λ uzyskano z przekształcenia wzoru (5.9)
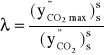
(5.28)
Maksymalne stężenie dwutlenku węgla w spalinach ![]()
jest jego stężeniem dla hipotetycznej sytuacji spalania gazu bez nadmiaru powietrza (λ = 1). Można go wyrazić wzorem:
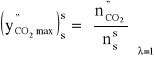
(5.29)
5.2.4. Obliczanie ilości spalin z wzorów empirycznych
Ilość spalin powstającą przy spalaniu paliw gazowych możemy obliczać także w sposób przybliżony przy użyciu wzorów empirycznych.
Przy spalaniu gazu o niskiej wartości opałowej (H<12,5 MJ/![]()
) korzystamy z wzorów:
![]()
(5.30)
![]()
(5.31)
Przy spalaniu gazu o średniej oraz wysokiej wartości opałowej (H≥12,5 MJ/![]()
) stosujemy inną parę wzorów:
![]()
(5.32)
![]()
(5.33)
Przedstawione wyżej wzory odnoszą się do spalania jednostkowej ilości gazu, czyli objętości 1 metra sześciennego (odniesionego do warunków normalnych), natomiast wyliczane wartości to:
![]()
- minimalne (teoretyczne) jednostkowe zapotrzebowanie powietrza, odniesione do warunków normalnych, ![]()
(metrów sześciennych powietrza na metr sześcienny gazu suchego)
![]()
- minimalna (teoretyczna) jednostkowa ilość spalin wilgotnych, odniesiona do warunków normalnych, ![]()
(metrów sześciennych spalin wilgotnych na metr sześcienny gazu suchego),
Rzeczywista jednostkowa ilość powietrza odniesiona do warunków normalnych ![]()
potrzebna do spalenia jednostkowej ilości gazu (objętości metra sześciennego odniesionego do warunków normalnych) będzie równa:
![]()
(5.34)
Rzeczywistą jednostkową ilość powietrza możemy podzielić na ilość teoretyczną ![]()
oraz nadmiar ![]()
. W palenisku teoretyczna ilość powietrza przekształca się w teoretyczną ilość spalin, natomiast nadmiar powietrza przechodzi przez palenisko bez zmian. Stąd rzeczywista jednostkowa ilość spalin będzie równa:
![]()
(5.35)
Rzeczywista ilość spalin wyzwalana w kotle (strumień objętościowy) zależy od strumienia objętościowego spalanego gazu.
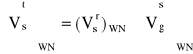
(5.36)
gdzie:
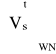
- strumień objętościowy spalin ulatujących z kotła odniesiony do warunków normalnych, ![]()
,
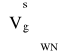
- strumień objętościowy spalanego w kotle gazu suchego odniesiony do warunków normalnych, ![]()
.
W celu przeliczenia wielkości strumienia objętościowego na warunki emisji 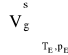
skorzystamy z wzoru (1.18).
5.3. SPALANIE WĘGLA
Węgle, tak kamienny jak i brunatny, są materiałami o bardzo złożonym składzie. Zawierają palną materie organiczną oraz skałę, z której podczas spalania powstaje popiół. Pierwiastkami, które wchodzą w skład węgli, a mającymi znaczenie dla składu spalin (pomijając pył) są: węgiel, wodór, tlen, siarka. Przykładowy skład pierwiastkowy palnej materii węgla energetycznego przedstawia się w przybliżeniu następująco: C135H96O9NS. Znając dokładny skład węgla możemy obliczać teoretyczne jednostkowe zapotrzebowanie powietrza z wzoru wyprowadzone na podstawie stechiometrii spalania.
![]()
(5.37)
gdzie:
![]()
- ułamek masowy węgla w paliwie,
![]()
- ułamek masowy wodoru,
![]()
- ułamek masowy siarki,
![]()
- ułamek masowy tlenu.
Skład paliwa najczęściej jest podawany w procentach masowych, ![]()
. Ułamek masowy jest jego jednostką pochodną, mniejszą stukrotnie.
![]()
(5.38)
Oznaczanie dokładnego składu pierwiastkowego węgli jest pracochłonne i nie jest powszechnie stosowane przy określaniu ich charakterystyki. Dlatego wzór (5.38) nie znajduje zastosowanie (z braku odpowiednich danych). Najczęściej charakteryzuje się węgle przez podanie ich wartości opałowej, zawartości popiołu, siarki oraz wody. Charakterystyki węgli wydobywanych w Polsce przestawiono w tabeli 5.2.
Tabela 5.2
Charakterystyka węgli wydobywanych w Polsce
Rodzaj węgla |
Wartość opałowa |
Zawartość popiołu |
Zawartość siarki |
Zawartość wody |
|
|
MJ/kg |
% masowy |
% masowy |
% masowy |
|
Kamienny energetyczny wg. Głównego Instytutu Górnictwa |
jaworznicki mikołowski dąbrowsko-siemianowicki katowicko-chorzowski rybnicki lubelski |
18,4 20,1 21,8 23,5 20,1 18,85 |
20 ÷ 24 20 20 20 20 ÷ 27 25 |
1,25 ÷ 1,5 1,5 0,6 0,8 0,7 ÷ 1,3 1,2 |
16 ÷ 20 12 8 5 9 9 |
Brunatny wg. Energopomiaru |
Turowski koniński adamowski bełchatowski |
8,4 9,2 8,0 8,0 |
12,2 ÷ 20 5,8 ÷ 6,3 9,8 10,6 |
0,6 0,25 ÷ 0,35 0,25 0,60 |
42 ÷ 50 50 ÷ 54 50 50 |
[Za: Kucowski J., Laudyn D., Przekwas M., Energetyka a Ochrona Środowiska, WNT, Warszawa 1997]
Do celów praktycznych zarówno jednostkowe zapotrzebowanie powietrza ![]()
jak i jednostkową ilość powstających spalin ![]()
odniesione do 1 kilograma węgla (brunatnego lub kamiennego) możemy określić z wzorów empirycznych opracowanych przez Rosina [za: Orłowski P., Dobrzański W.: Kotły parowe w energetyce przemysłowej. WNT, Warszawa 1991]:
![]()
(5.39)
![]()
(5.40)
gdzie:
H - wartość opałowa węgla, MJ/kg
Opracowano więcej podobnych wzorów. Przykładem mogą być te, w których uwzględniono to, że węgle zawierają popiół [za: Laudyn D., Pawlik W., Strzelczyk F.: Elektrownie. WNT warszawa 1995].
![]()
(5.41)
![]()
(6.42)
gdzie:
![]()
- ułamek masowy popiołu w węglu.
Cztery ostatnie wzory służą do obliczania teoretycznej jednostkowej ilości powietrza oraz spalin. Jednostkowe wartości rzeczywiste możemy obliczyć podobnie jak w wypadku spalania gazu z wzorów (5.34) oraz (5.35). Przy obliczaniu strumienia spalin uwzględniamy masowe zużycie paliwa:
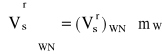
(5.43)
gdzie:
![]()
- zużycie węgla (strumień masowy), kg/s.
W celu przeliczenia wielkości strumienia objętościowego na warunki emisji 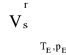
skorzystamy z wzoru (1.18).
5.4. SPALANIE PALIW CIEKŁYCH
Do obliczania zapotrzebowania powietrza oraz ilości powstających spalin przy spalaniu paliw ciekłych korzystamy z wzorów empirycznych:
![]()
(5.44)
![]()
(5.45)
gdzie:
H - wartość opałowa paliwa, MJ/kg.
Pozostałe obliczenia wykonujemy podobnie jak w wypadku spalania węgla lub gazu.
5.5. ZUŻYCIE PALIWA
Ciepło powstające w kotle w procesie spalania dzieli się na ciepło użyteczne oraz ciepło tracone. Ciepło tracone jest sumą ciepła oddawanego do otoczenia wskutek wymiany oraz wskutek ucieczki do atmosfery wraz ze spalinami. Im większe straty tym mniejsza sprawność kotła η wyrażona w procentach Strumień ciepła użytecznego określamy jako wydajność cieplną kotła ![]()
(wyrażaną w J/s, lub jednostkach większych kJ/s, MJ/s). Zużycie paliwa wyrażamy wzorem (5.46)
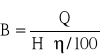
(5.46)
gdzie:
![]()
- zużycie paliwa, kg/s,
H - wartość opałowa paliwa, MJ/kg,
![]()
- wydajność cieplna (moc) kotła, MJ/s
η - sprawność cieplna kotła, %.
W jednostkach energetycznych produktem jest energia elektryczna. Wtedy wzór określający zużycie paliwa przyjmie postać:
![]()
(5.47)
gdzie:
![]()
- moc energetyczna jednostki, MW.
Wyszukiwarka
Podobne podstrony:
Przedsiebi, inżynieria ochrony środowiska kalisz, z mix inżynieria środowiska moje z ioś pwsz kalis
pwsz ioś kalisz Ćw. 6 POLARYMETRIA, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, analiza
pwsz kalisz rozporzadz, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, VI odzysk ciepla ob
W-14, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, Meteorologia materialy
W-10, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, Meteorologia materialy
OCHRONA POWIETRZA, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, IV ochrona powietrza
pwsz ioś kalisz Ćw 4 Spektrofotometria, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, ana
pwsz kalisz Metody oznaczania mikroorganizmów w powietrzu, inżynieria ochrony środowiska kalisz, a p
Wentylatory 2003, inżynieria ochrony środowiska kalisz, z mix inżynieria środowiska moje z ioś pwsz
pwsz ioś kalisz moje sprawozdanie PEHAMETRIA, inżynieria ochrony środowiska kalisz, a pwsz kalisz io
pwsz ioś kalisz Analiza-Pehametria, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, analiza
GRUPA C, inżynieria ochrony środowiska kalisz, z mix inżynieria środowiska moje z ioś pwsz kalisz
pwsz ioś kalisz polarymetria, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, analiza chemi
tab rozbiorów najnowsza, inżynieria ochrony środowiska kalisz, z mix inżynieria środowiska moje z i
pwsz kalisz Tabela nie ociepl, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, V Budownictw
Tosik wzory, inżynieria ochrony środowiska kalisz, z mix inżynieria środowiska moje z ioś pwsz kali
pwsz ioś kalisz Tabela Ćw.4, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, analiza chemic
pwsz kalisz BHp, inżynieria ochrony środowiska kalisz, Rok 1 IOS
więcej podobnych podstron