Inżynieria Ochrony Środowiska
PWSZ w Kaliszu
Laboratorium z Analizy Instrumentalnej
Ćwiczenie nr 4
SPEKTROFOTOMETRIA
Cel ćwiczenia : Spektrofotometryczne oznaczanie nadmanganianu potasu KMnO4 metodą krzywej wzorcowej.
Grupa laboratoryjna I A
Wykonali :
Piotr Grzesiak
Michał Ciesielski
Kalisz, 27.11.2003
Zarys teoretyczny :
W technikach absorpcyjnych wykorzystuje się fakt, że niektóre substancje
(barwne) zdolne są pochłaniania światła. Chcąc wykorzystać ten fakt, należy wiedzieć : jakie długości fal są pochłaniane i z jaką intensywnością.
W procesie pochłaniania biorą udział 2 czynniki : czynnik pochłaniający (np. ciecz) oraz czynnik pochłaniany (gaz, fale elektromagnetyczne). Pochłanianie może się odbywać na powierzchni czynnika pochłaniającego - tego typu pochłanianie to adsorpcja. Czynnik pochłaniany może gromadzić się w całej objętości czynnika pochłaniającego-jest to absorpcja.
![]()
Do pomiaru intensywności pochłaniania światła służy absorbancja-A (inaczej ekstynkcja). Jeżeli wiązkę światła o natężeniu Io przepuścimy przez warstwę roztworu substancji pochłaniającej światło, to po przejściu natężenie wiązki spadnie do I1. Absorbancję definiujemy jako :
Wartość A jest bezwymiarowa, zawsze dodatnia, jest ona tym większa im mniejsza jest I1, czyli im silniej jest pochłaniana wiązka - I.
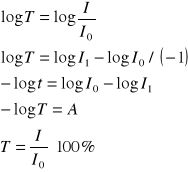
Drugą wielkością pozwalającą ocenić spadek natężenia wiązki światła po przejściu przez warstwę roztworu substancji pochłaniającej światło jest transmitancja. Definiuje się ją jako :
![]()
po zlogarytmowaniu stronami :
Pod pojęciem transmitancji często rozumie się wartość wyrażoną ostatnim wzorem, czyli procentową przepuszczalność światła dla danej substancji, przez
którą przechodzi wiązka światła. Może ona przyjmować wartości od 0 do 100.
W celu stwierdzenia, czy dana substancja pochłania promienie w określonym zakresie (np. w zakresie długości fal odpowiadających światłu widzialnemu) należy przeprowadzić pomiar absorbancji lub transmitancji dla każdej długości fali z tego zakresu. Z uzyskanych danych sporządza się wykres zależności A od długości fali. Wykres to charakterystyczne dla danej substancji (o stałym stężeniu) widmo absorpcyjne.
Długość fali, której odpowiada największa wartość absorbancji to analityczna długość fali ( λmax). Pomiary wykonany przy λmax odznaczają się dokładnością i czułością.
Najczęściej do wykonywania ilościowych oznaczeń spektrofotometrycznych jest stosowana metoda krzywej wzorcowej. Krzywa wzorcowa przedstawia graficzną zależność absorbancji od stężenia substancji wzorcowej. Prostoliniowy przebieg tej zależności w badanym zakresie stężeń świadczy o spełnieniu przez układ prawa Beera.
W celu wykreślenia krzywej wzorcowej przygotowuje się 5-8 roztworów wzorcowych tej samej substancji różniące się coraz większym stężeniem oznaczonym.
Doświadczenie.
Cel ćwiczenia
Celem ćwiczenia jest oznaczenie ilościowe nadmanganianu potasu KMnO4 spektrofotometrycznie metodą krzywej wzorcowej. Wykorzystywana jest prostoliniowa zależność badanego zakresu stężeń zgodnie z prawe Lamberta-Beera.
2. Przebieg doświadczenia.
W doświadczeniu wykorzystywaliśmy roztwory wzorcowe nadmanganianu potasu (KMnO4) o określonych stężeniach (µg / cm3) : 0,04 ; 0,08 ; 0,12 ; 0,16 ; 0,2 ; 0,24 ; 0,32 ; 0,4.
Za pomocą spektrofotometru dokonywaliśmy pomiaru absorbancji (A) dla każdego z roztworu KMnO4 w kolejności od najmniejszego stężenia do największego. Dla KMnO4 analityczna długość fali wynosi : λmax = 530 nm
Po każdorazowym pomiarze dla danego stężenia roztworu wyzerowywaliśmy długość fali światła na pokrętne spektrofotometru dla precyzyjnego pomiaru
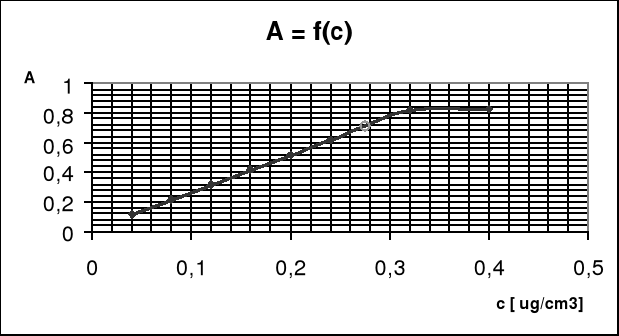
Jako ostatni do analizy otrzymaliśmy roztwór o nieznanym stężeniu, którego wartość mieliśmy odczytać z wykresu krzywej wzorcowej : A = f(c) powstałej na bazie wartości absorbancji odczytanych na spektrofotometrze dla poszczególnych roztworów o znanym stężeniu.
Zestawienie wyników w tabeli.
Spektrofotometr
Roztwory nadmanganianu potasu (KMnO4) o określonych stężeniach (µg / cm3) : 0,04 ; 0,08 ; 0,12 ; 0,16 ; 0,2 ; 0,24 ; 0,32 ; 0,4.
Badany roztwór nadmanganianu potasu (KMnO4) o nieznanym stężeniu
błąd bezwzględny pomiaru :
błąd względny pomiaru:
L. p. |
Stężenie - c [µg / cm3] |
Absorbancja (ekstynkcja) - A |
1. |
0,04 |
0,115 |
2. |
0,08 |
0,215 |
3. |
0,12 |
0,315 |
4. |
0,16 |
0,420 |
5. |
0,2 |
0,515 |
6. |
0,24 |
0,622 |
7. |
0,32 |
0,818 |
8. |
0,4 |
0,830 |
9. |
X |
0,710 |
Odczynniki, sprzęt laboratoryjny i aparatura :
Obliczenia :
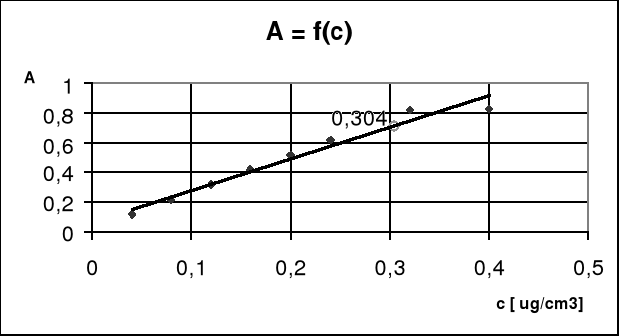
Z wykresu krzywej wzorcowej odczytaliśmy stężenie badanego roztworu KMnO4, którego absorbancja wyniosła na spektrofotometrze 0,710 :
cx = 0,304
Obliczanie błędów pomiarowych :
BB = | WT - WD |
gdzie : WT - wartość teoretyczna (podana przez prowadzącego)
WD - wartość doświadczalna (odczytana z wykresu krzywej
kalibracyjnej)
WT = 0,3 μg/cm3 , a WD = 0,304 μg/cm3 ; stąd
BB = | 0,3 - 0,304 | = 0,004 μg/cm3
BW =| (BB / WT) ۰ 100% |
BW =| (0,004 / 0,3) ۰ 100% | = 1,34 %
Wnioski :
W ćwiczeniu stosowaliśmy metodę krzywej wzorcowej do oznaczenia stężenia badanego roztworu.
Zaobserwowaliśmy, że wraz ze wzrostem stężenia roztworów nadmanganianu potasu KMnO4 wzrastała absorbancja. Linia trendu tego wzrostu miała charakter prostoliniowy co jest zgodne z prawem Lambert'a-Berr'a.
Jedynie pomiar dla 8 roztworu tj. o stężeniu 0,4 μg/cm3 nie spełniał założenia prawa Lambet'a-Berr'a - nie znajdował się w obrębie zakresu prostoliniowego wykresu A = f(c). Mogło to być spowodowane niedokładnym odczytem absorbancji na wskaźniku spektrofotometru lub nieprawidłowym działaniem urządzenia. Mimo tego problemu dzięki temu pomiarowi, gdy rozpatrywaliśmy linie trendu krzywej wzorcowej, wynik był obarczony mniejszym błędem (różnica między wartością podaną przez prowadzącego a wart. odczytaną z wykresu) - 1,34 %, niż w przypadku gdybyśmy nie rozpatrywali tego punktu.
Jednak każdy z pomiarów absorbancji dla roztworów o podanych stężeniach odbiegał od linii trendu wykresu krzywej wzorcowej co można tłumaczyć niedokładnością odczytu absorbancji z wskaźnika spektrofotometru jak również rozkalibrowaniem się przyrządu w trakcie pomiaru.
![]()
![]()
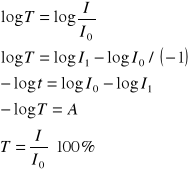
Wyszukiwarka
Podobne podstrony:
pwsz ioś kalisz Ćw. 6 POLARYMETRIA, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, analiza
pwsz ioś kalisz Ćw 5 Refraktometria, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, anali
pwsz ioś kalisz Analiza- ćw.5 Refraktometria, inżynieria ochrony środowiska kalisz, a pwsz kalisz io
pwsz ioś kalisz Ćw 3 Chromatografia, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, analiz
pwsz ioś kalisz Ćw 1 Potencjonometria, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, anal
pwsz ioś kalisz Ćw. 6 POLARYMETRIA, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, analiza
pwsz ioś kalisz Tabela Ćw.4, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, analiza chemic
pwsz ioś kalisz zadania cw, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, IV ochrona pow
Przedsiebi, inżynieria ochrony środowiska kalisz, z mix inżynieria środowiska moje z ioś pwsz kalis
pwsz kalisz rozporzadz, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, VI odzysk ciepla ob
W-14, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, Meteorologia materialy
W-10, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, Meteorologia materialy
OCHRONA POWIETRZA, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, IV ochrona powietrza
pwsz kalisz Metody oznaczania mikroorganizmów w powietrzu, inżynieria ochrony środowiska kalisz, a p
Wentylatory 2003, inżynieria ochrony środowiska kalisz, z mix inżynieria środowiska moje z ioś pwsz
pwsz ioś kalisz moje sprawozdanie PEHAMETRIA, inżynieria ochrony środowiska kalisz, a pwsz kalisz io
pwsz ioś kalisz Analiza-Pehametria, inżynieria ochrony środowiska kalisz, a pwsz kalisz ioś, analiza
więcej podobnych podstron