NAZWISKO: CHILIŃSKI
IMIE: BARTŁOMIEJ
KIERUNEK: FIZ-INF
ROK STUDIÓW : II
GRUPA LABORATORYJNA: VI |
WYŻSZA SZKOŁA PEDAGOGICZNA W RZESZOWIE I PRACOWNIA FIZYCZNA |
||||
|
WYKONANO |
ODDANO
|
|||
|
DATA
|
PODPIS |
DATA
|
PODPIS |
|
Ćwiczenie Nr:
|
Temat:
.
|
||||
Część teoretyczna
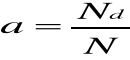
Wodne roztwory kwasów, zasad i soli ulegają dysocjacji elektrolitycznej polegającej na rozpadzie drobin na jony : dodatnie zwane katodami oraz ujemne zwane anionami . Dodatnimi jonami są metale i wodór, a ujemnymi reszta kwasowa lub grupa wodorotlenowa. Dysocjacja nie jest całkowita; stąd wprowadzamy pojęcie stopnia dysocjacji a będącego stosunkiem liczby drobin zdysocjowanych Nd do ogólnej liczby drobin zawartych w roztworze N,
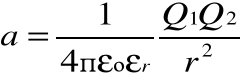
Stopień dysocjacji zależy od wielu czynników (temp. stężenia itp.) , z których najważniejszą rolę odgrywa względna przenikalność dielektryczna εr rozpószczalnika. Cęści drobin substancji dysocjujących są jonami i związane są siłami columbowskimi:
A więc proporcjonalnymi do odwrotności względnej stałej dielektryzcnej εo rozpószczalnika. Im większe εr , tym wyższy stopień dysocjacji. W roztwoże następuje również rekombinacja drobin a stopień dysocjacji jest wynikiem równowagi dynamicznej między dysocjacją i rekombinacją.
Jony pochodzące z dysocjowanych drobin mogą przewodzic prąd elektryczny . Prąd taki różni się od prądu przewodzonego w metalach, ponieważ nie jest to przepływ elektronów lecz dużych jonów , czyli prąd konwekcyjny. Stąd też opór lektrolitu jest duży. Poza tym elektrolity zachowują się jak przewodniki tzn. Stosują się do prawa Ohma i ich opór zależy od temperatury w taki sam sposób jak dla metali. Czułość zjawisk zachodzących przy prepływie prądu elektrycznego przez elektrolity nazywamy elektrolizą. Ponieważ w elektrolitach występują prądy konwekcyjne, toważyszy im transport masy. Jony oddaja swój ładunek elektrodie, ulegają zobojętnieniu i wydzielają się na elektrodze lub reagują natychmiast z elektrodą bądz z roztworem. Ilość ![]()
![]()
wydzielonej masy jest proporcjonalny do ładunku Q, który przepływa przez elektrolit:
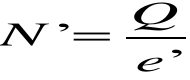
![]()
Współczynnik proporcjonalności k nazywamy równoważnikiem elektrochemicznym. Równanie powyższe nazywamy Iprawem Faradaya. Oznaczając masę pojedynczego jonu przez m΄, jego ładunek przez e', a ilość wydzielonych jonów przez N' otrzymamy:
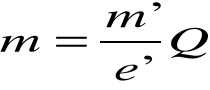
Skąd:
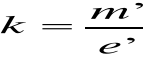
I porównując powyższy wzór otrzymamy interpretację równoważnika elektrochemicznego
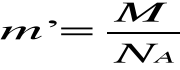
Ładunek jonu e'=We jest równy iloczynowi wartościowości i ładunku elementarnego, a masa m' jonu jest równa stosunkowi masy atomowej do liczby Avogadra NA , czyli :
Podstawiając te wartości otrzymamy:
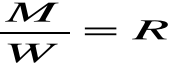
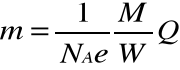
Gdzie wielkość :
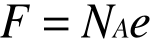
Nazywamy równoważnikiem chemicznym, a iloczyn :
STAŁĄ FARADAYA.
Tak więc ostatmi wzór przsyjmuje postać:
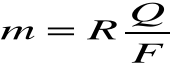
Wynika stąd że ładunek Q=F równy stałej Faradaya wydziela masę równą jednemu równoważnikowi chemicznemu m=R dowolnej substancji.
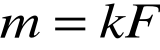
Jest to treść II prawa Faradaya. Stała Faradaya = 96519,3 C · równoważnikˉ¹. Podstawiając otrzymamy:
POMIARY:
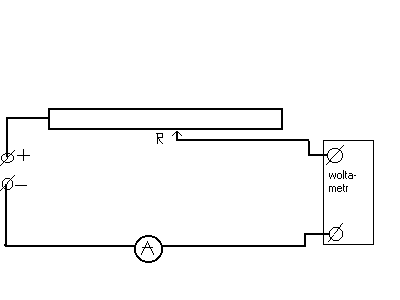
Elektrolizę badamy w naczyniu zwanym woltomieżem zawierającym elektrolit , może to być wodny roztwór CuSO4 i miedziane elektrody. Elektrody posiadają kształt płaskich blaszek o powieszchni ok. 10cm² . W woltometrze umieszczamy je w odległości kilku centymetrów. Układ łączymy wedłóg schematu
Przed przystąpieniem do pomiarów elektrody czyścimy papierem ściernym, obmywamy wodą destylowaną i suszymy za pomocą fenu w strómieniu ciepłego powietrza. Elektrodę która będzie katodą, ważymy na wadze analitycznej ( m1 ). Po osuszeniu, elektrod nie wolno dotykać palcami, gdyż grozi to zatłuszczeniem. Przed rozpoczęciem właściwego pomiaru włączamy katodę zapasową (nie oczyszczoną). Włączamy prąd i dobieramy warunki pracy. Stosunek natężenia prądu nie może przekroczyć 1 A/dm² . Natężenie dobieramy w zależności od powieszchni czynnej elektrod (powieszchni zanurzonej w roztworze). Następnie włączamy prąd i zakładamy właściwą elektrodę. Włączamy równocześnie sekundomierz i prąd, który musi płynąć przez 30 minut. W tym czasie ciągle obserwujemy wskazania amperomierza i wachania prądu natychmiast kompensujemy.Po upływie 30 minut wyłączamy prąd, suszymy elektrodę i ważymy( m2 ). Analizujemy otrzymane wyniki i pomiary powtarzamy w warunkach zapewniających optymalny wynik.
OBLICZENIA:
1
4
Wyszukiwarka
Podobne podstrony:
pierwsza strona sprawozdania, fff, dużo
FIZYKA 47, fff, dużo
76bmoje, fff, dużo
Indukcyjność cewki, fff, dużo
Lab fiz 01, fff, dużo
Pomiar predkosci dzieku w powietrzu, fff, dużo
FIZ43'' 222222222, fff, dużo
Wyznaczanie temperatury Curie dla ferrytow, fff, dużo
fotometr Bunsena 75, fff, dużo
Lab fiz 05, fff, dużo
Lab fiz 24, fff, dużo
Lab fiz 04, fff, dużo
przenikalność, fff, dużo
Stala siatka dyfrakcji2, fff, dużo
wahadlo maxela 4422, fff, dużo
Fiz24 teoria, fff, dużo
więcej podobnych podstron