Ćwiczenie 9
Analiza jakościowa cukrów
Identyfikacja nieznanego cukru
Ćw. 1 Działanie stężonych kwasów na cukry - Próba Molischa
Wykonanie: Do 1 ml badanego roztworu dodać 2-3 krople świeżo sporządzonego 20% roztworu etanolowego -naftolu. Po dokładnym zmieszaniu, bardzo ostrożnie po ściankach skośnie ustawionej probówki wprowadzić około 1ml stężonego H2SO4, tak aby nie zmieszać obydwu roztworów. Powstający na granicy warstw czerwonofioletowy pierścień świadczy
o obecności cukru.
Uwaga! Wystąpienie zielonego zabarwienia może pochodzić od zanieczyszczeń odczynników i nie jest swoiste dla tej reakcji.
Ćw. 2 Wykrywanie ketoz - Próba Seliwanowa
Wykonanie: Do 1 ml badanego roztworu dodać 1ml rozcieńczonego HCl i 2-3 krople etanolowego roztworu rezorcyny. Po zmieszaniu wstawić do wrzącej łaźni wodnej i gotować przez około 30-60 sekund.
W obecności ketoz powstaje czerwono-łososiowe zabarwienie. W przypadku aldoz barwa pojawia się po dłuższym czasie.
Ćw. 3 Wykrywanie pentoz
a) Próba Tollensa z floroglucyną
Wykonanie: Do 1ml badanego roztworu dodać 2 ml stężonego HCl i 5 kropel etanolowego roztworu floroglucyny. Ogrzewać na łaźni wodnej.
W obecności pentoz powstaje związek o wiśniowofioletowej barwie, a heksoz - żółtej lub brązowej.
b) Próba Biala
Wykonanie: Do 0,5 ml badanego roztworu dodać ok. 1 ml 0,2% roztworu orcyny w 20% HCl oraz kroplę 1% roztworu FeCl3 i wymieszać. Wstawić probówkę do wrzącej łaźni wodnej.
W obecności pentoz powstaje zielononiebieskie zabarwienie produktu kondensacji furfuralu z orcyną.
Ćw. 4 Odczyny redukcyjne
Ćw.4a Próba Fehlinga
Wykonanie: 2 ml mieszaniny roztworów Fehlinga I i Fehlinga II (1:1, v:v) zagotować na łaźni wodnej,
a następnie dodać 1 ml badanego roztworu i ogrzewać do wrzenia.
Pojawienie się ceglastoczerwonego osadu tlenku miedzi (I) świadczy o obecności w próbie cukru redukującego.
Odczynnik Fehlinga I: 34,65 g CuSO4 x 5 H2O / 500 ml wodnego roztworu
Odczynnik Fehlinga II: 173 g winianu sodowo-potasowego i 15 g NaOH / 500 ml wodnego roztworu
Ćw. 4b Próba Benedicta
Wykonanie: Do 1 ml odczynnika Benedicta dodać 3-8 kropli badanego roztworu i wstawić na 3 minuty do wrzącej łaźni wodnej.
W zależności od stężenia cukrów rozwór może przybierać różne odcienie zieleni lub kolor pomarańczowy.
Odczynnik Benedicta: 173 g cytrynianu sodu i 90 g bezwodnego węglanu sodu rozpuścić
w 60 ml gorącej wody. Po przesączeniu roztworu, do przesączu dodać 100 ml 17,3% roztworu CuSO4 x 5 H2O. Mieszaninę uzupełnić w kolbie miarowej do 1000 ml.
Ćw. 4c Reakcja z kwasem pikrynowym
Wykonanie: Do 1 ml badanego roztworu dodać 1 ml nasyconego roztworu kwasu pikrynowego i 0,5 ml 10% roztworu NaOH i wstawić na wrzącą łaźnię wodną.
Powstające czerwone zabarwienie pochodzące od pikraminianu sodu potwierdza obecność w próbie cukru redukującego.
Ćw. 5 Próba Barfoeda w modyfikacji Tauber-Kleinera
Wykonanie: Do 0,5 ml badanego roztworu dodać 1 ml odczynnika Barfoeda i ogrzewać we wrzącej łaźni wodnej przez 3 minuty. Jeżeli po tym czasie nie wytrącił się osad probówkę ponownie umieścić na łaźni wodnej i ogrzewać kolejnych 10 minut.
Pojawienie się czerwonego osadu Cu2O w próbie po 3 min. ogrzewania potwierdza obecność monosacharydu, a gdy powstaje on po kilkunastu minutach dowodzi obecności disacharydu.
Odczynnik Barfoeda: 24 g octanu miedzi (II) rozpuścić w 450 ml gorącej wody. Dodać 25 ml 8,5% roztworu kwasu mlekowego. Po rozpuszczeniu soli odczynnik oziębić
i uzupełnić w kolbie miarowej wodą do objętości 500 ml. W razie potrzeby przesączyć.
Ćw. 6 Próba Wöhlkego
Wykonanie: Do 1 ml badanego roztworu dodać 1 ml stężonego roztworu amoniaku i 3 krople 3% KOH. Wstawić do wrzącej łaźni wodnej na kilka minut.
W obecności laktozy lub maltozy powstaje czerwone zabarwienie.
Ćw. 7 Reakcja skrobi z jodem
Wykonanie: Do 1 ml badanego roztworu dodać 3 krople J2 w KJ. W obecności skrobi powstaje ciemnoniebieskie zabarwienie.
Schemat analizy cukrów
5
+
Fruktoza
-
Glukoza
Galaktoza
PRÓBA
SELIWANOWA
Ksyloza
Glukoza
Galaktoza
Fruktoza
Laktoza
Maltoza
+
+
-
-
PRÓBA WOHLKEGO
PRÓBA TOLLENSA Z FLOROGLUCYNĄ
Sacharoza
+
-
+
-
PRÓBA BARFOEDA
+
PRÓBA
SELIWANOWA
Skrobia
-
PRÓBA BENEDICTA
+
-
PRÓBA Z JODEM
-
+
PRÓBA MOLISHA
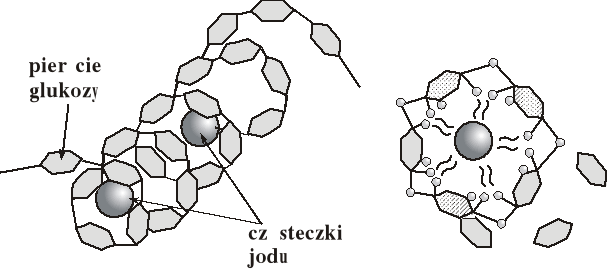
Reakcja skrobi lub glikogenu z jodem polega na adsorpcji jodu, który wnika do „kanału” utworzonego przez spiralnie skręcone łańcuchy polisacharydowe i jest „przytrzymywane” przez tlen przy pierwszym i czwartym atomie węgla każdej cząsteczki glukozy. Wytwarza się więc łańcuch drobin jodu, wzdłuż którego mogą przemieszczać się elektrony, co powoduje pochłanianie światła przez układ. Skrobia po adsorpcji cząsteczek jodu barwi się na kolor ciemnoniebieski. Obserwowana barwa zależy od budowy
i stopnia rozgałęzienia łańcucha polisacharydu, a więc reakcja jodu z amylozą powoduje powstanie niebieskiego produktu, a z amylopektyną - fioletowego. Glikogen barwi się z jodem na czerwono. Ogrzewanie skrobi z rozcieńczonymi kwasami prowadzi do hydrolizy wiązań glikozydowych i powstania wraz z czasem trwania tego procesu odpowiednio: amylodekstryny barwiącej się z jodem na fioletowo, erytrodekstryny - czerwono i achrodekstryny nie barwiącej się z jodem. Końcowymi produktami hydrolizy kwaśnej tych wielocukrów są maltoza i glukoza.
Ogrzewając roztwór laktozy lub maltozy z amoniakiem w obecności KOH powstaje czerwone zabarwienie. Natomiast glukoza lub fruktoza tworzą żółtobrązowy produkt.
Wzrost stężenia jonów wodorowych powoduje zmniejszenie zdolności redukcyjnych węglowodanów, co pozwala na odróżnienie cukrów prostych od disacharydów redukujących. Reakcję tę prowadzi się w środowisku kwaśnym, stosując niskie stężenia cukrów i krótki czas ogrzewania, który zapewnia pozytywny wynik jedynie dla monosacharydów, natomiast przy dłuższym ogrzewaniu disacharydy ulegają hydrolizie dając także wynik dodatni.
W tej reakcji jony miedzi zmieniają stopień utlenienia z +2 na +1. analogicznie jak w próbie Fehlinga. Odczyn Benedicta jest jednak od niej bardziej swoisty i czuły, dlatego stosuje się go do wykrywania cukrów w moczu.
W środowisku alkalicznym w obecności cukru redukującego jony Cu2+ redukowane są do Cu+
i wytrąca się ceglastoczerwony osad Cu2O.
Cukry w środowisku zasadowym mogą redukować nie tylko jony metali ciężkich, ale również inne związki, np. kwas pikrynowy (pikrynian sodu), który w tych warunkach tworzy czerwony pikraminian sodu.
Dodatni wynik próby na właściwości redukujące nie zawsze świadczy o obecności cukru w roztworze, ponieważ posiadają je także inne związki, np. chloroform, kreatynina.
Wolne grupy aldehydowe i ketonowe cukrów wykazują w środowisku alkalicznym właściwości redukujące. Aktywna w tych warunkach forma aldehydowa (lub ketonowa po enolizacji do formy aldehydowej) redukuje jony metali ciężkich - jony miedzi z +2 na +1 (próba Benedicta i Fehlinga), jony bizmutu z +3 na 0 (próba Nylandera), a jony srebra z +1 na 0 stopień utlenienia (próba Tollensa). Podczas redukcji jonów metali aldozy utleniają się do odpowiednich kwasów aldonowych.
Utlenianie ketoz, jest procesem bardziej złożonym, bowiem jego produktem jest mieszanina kwasów.
Dla przeprowadzenia prób redukcyjnych przygotowuje się odpowiednią mieszaninę reakcją.
W tym celu w próbie Fehlinga do siarczanu (VI) miedzi (II) dodaje się roztworu NaOH, a w próbie Benedicta węglanu sodu. Powstający w środowisku zasadowym wodorotlenek miedzi (I) może wytrącić się w postaci koloidalnej zawiesiny, aby temu zapobiec dodaje się związków kompleksujących jony Cu2+ (w próbie Fehlinga - winian sodowo potasowy, a w próbie Benedicta - cytrynian trójsodowy).
Pentozy ogrzewane ze stężonym kwasem solnym odwadniają się do furfuralu, który z orcyną
i jonami Fe3+ barwi się na zielono. Próbę tę wykorzystuje się do ilościowego oznaczania rybozy
w kwasach nukleinowych.
W reakcji kwasu solnego z pentozami powstaje furfural, który tworzy z floroglucyną związek
o barwie wiśniowofiołkowej. Natomiast z 5-hydroksymetylenofurfuralem powstaje żółty lub brunatny produkt kondensacji. Analogiczny wynik otrzymuje się również z kwasami uronowymi, ulegającymi
w tych warunkach dekarboksylacji.
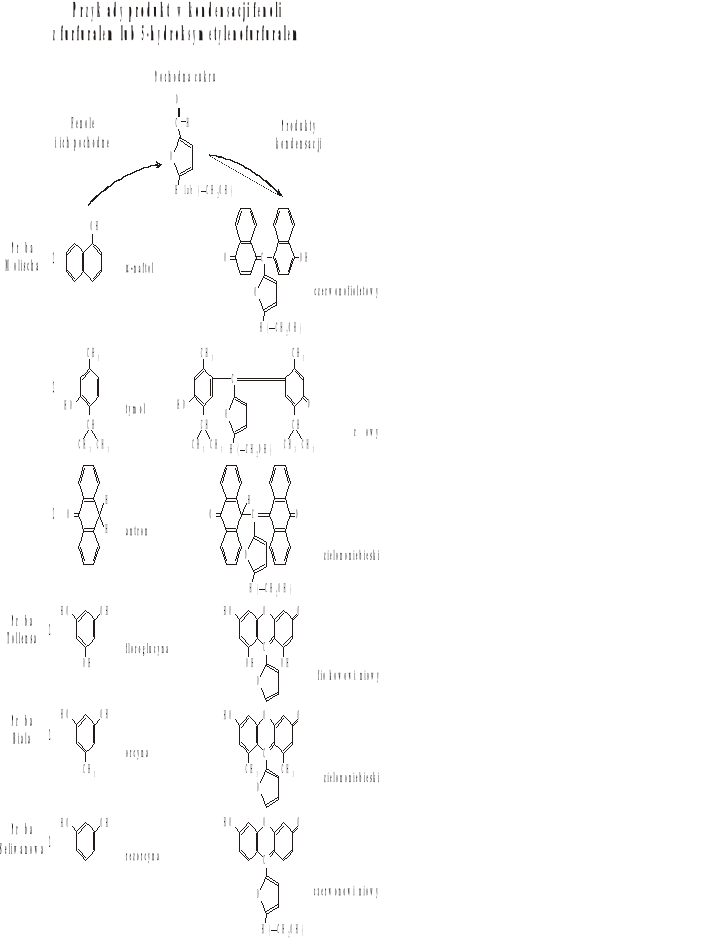
Reakcja ta pozwala na odróżnienie ketoz od aldoz i opiera się na różnej szybkości odwadniania tych cukrów. Podczas 1 minutowego ogrzewania we wrzącej łaźni wodnej roztworów cukrów z 12% HCl ketozy ulegają odwodnieniu i powstaje hydroksymetylenofurfural. W tych warunkach czasowo-środowiskowych aldozy nie ulegają odwodnieniu. Próba ta daje również wynik pozytywny dla wielocukrów zawierających ketozy.
|
Ogrzewanie monosacharydów ze stężonymi kwasami (siarkowym, solnym) powoduje ich odwodnienie. Pentozy przekształcają się w furfural, a heksozy Reakcje ze stężonymi kwasami należą do ogólnych reakcji na węglowodany, ponieważ umożliwiają wykrycie cukru, natomiast nie pozwalają na jego identyfikację. Reakcja Molischa jest mało specyficzna, ponieważ dodatni wynik reakcji otrzymujemy także w obecności aldehydów, acetonu i kwasów - mrówkowego, szczawiowego lub cytrynowego. |
Wyszukiwarka
Podobne podstrony:
MELATONINA, II rok, II rok CM UMK, Giełdy, od Joe, biochemia, BIOCHEMIA, GIEŁDY - EGZAMIN, Dodatkowe
homocysteina, II rok, II rok CM UMK, Giełdy, od Joe, biochemia, BIOCHEMIA, GIEŁDY - EGZAMIN, Dodatko
MELATONINA, II rok, II rok CM UMK, Giełdy, od Joe, biochemia, BIOCHEMIA, GIEŁDY - EGZAMIN, Dodatkowe
integracja 1(1), II rok, II rok CM UMK, Giełdy, od Joe, biochemia, BIOCHEMIA, GIEŁDY - KOLOKWIA, Gie
Feromony wytwarzane są przez ciało każdego człowieka, II rok, II rok CM UMK, Giełdy, od Joe, biochem
Integracja kolo 2008 rozwiazane, II rok, II rok CM UMK, Giełdy, od Joe, biochemia, BIOCHEMIA, GIEŁDY
lab(1), II rok, II rok CM UMK, Giełdy, od Joe, biochemia, BIOCHEMIA, GIEŁDY - KOLOKWIA, Giełdy - PRA
Laboratorium 18, II rok, II rok CM UMK, Giełdy, od Joe, biochemia
integracja[1](1), II rok, II rok CM UMK, Giełdy, od Joe, biochemia, BIOCHEMIA, GIEŁDY - KOLOKWIA, Gi
Biochemia 2011 egzamin 100 opyta, II rok, II rok CM UMK, Giełdy, od Joe, biochemia, BIOCHEMIA, GIEŁD
Laboratorium 19, II rok, II rok CM UMK, Giełdy, od Joe, biochemia, BIOCHEMIA, GIEŁDY - KOLOKWIA, Gie
Laboratorium 11 OKSYDOREDUKTAZY, II rok, II rok CM UMK, Giełdy, od Joe, biochemia
więcej podobnych podstron