CCF20111021�002

■mi /.mieszano parami mzlwory następujących soli: l‘h( N(),)2, K .S, Z11SO4 i NaMr 6 możliwych kombinacjach). W których mieszaninach zajdą reakcje? Ułożyć równa-jonowe tych reakcji.
Bffll Do roztworu zawierającego 2 mole AgN03 dodano roztwór zawierający 4 mole •1. Osad odsączono, a do przesączu dodano 3 mole Ba(OH)2 oraz kilka kropli lakom-Jakie zabarwienie miał roztwór, i dlaczego?
Kii Do roztworu zawierającego 0,5 mola wodorowęglanu sodu dodano 1 mol kwa-iolnego, a następnie 0,25 mola wodorotlenku baru. Jaki odczyn miał roztwór?
na Do roztworu zawierającego 2,5 mola krzemianu sodu dodano roztwór zawie-icy 5,5 mola kwasu solnego. Osad odsączono, a do przesączu dodano 0,75 mola wo-otlenku potasu. Jaki odczyn miał otrzymany roztwór?
Kil W probówkach znajdują się roztwory chlorku sodu i chlorku baru. Jak je rozróż-wykonując jedną reakcję chemiczną?
Ba W probówkach znajdują się roztwory węglanu sodu i siarczanu sodu. Jak je roz-ńć?
m W jednej probówce znajduje się wodny roztwór azotanu sodu, a w drugiej la. Jak rozróżnić zawartość probówek?
W trzech probówkach znajdują się roztwory: AgN03, Pb(N03)2, Zn(N03)2. Jak óżnić zawartość probówek?
;n W trzech probówkach znajdują się roztwory: Na2S04, KC1, NH4N03. Jak roz-lić zawartość probówek?
331 W trzech probówkach znajdują się rozcieńczone roztwory: HC1, H2S04, HN03. rozróżnić zawartość probówek?
331 W pięciu probówkach znajdują się roztwory: CuS04, AgN03, ZnCl2, HC1, •H. Jak je rozróżnić bez użycia wskaźników pH i innych odczynników?
m Do roztworu zawierającego 1 mol azotanu srebra dodano roztwór zawierający mola chlorku magnezu. Obliczyć masę wytrąconego osadu. Co pozostało w roz-
ze?
H! Do roztworu zawierającego 0,22 g chlorku wapnia dodano roztwór zawierający 5 azotanu srebra. Obliczyć masę wytrąconego osadu. Co pozostało w roztworze?
m Do roztworu zawierającego 5 g FeCl3 dodano roztwór zawierający 3,4 g NaOH. czyć masę wytrąconego osadu.
Na węglan dwuwartościcwe-go metalu działano kwasem azotowym. Wykres na rysunku 9.2 ilustruje zależność objętości otrzymanego gazu od masy użytego węglanu. Obliczyć masę cząsteczkową węglanu i ustalić jego wzór.
9.129.
a
T3
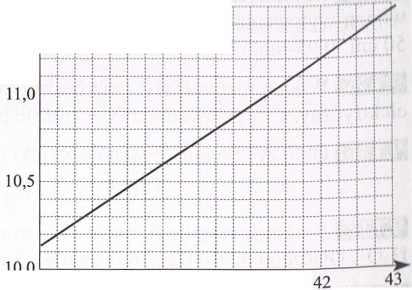
węglan [g]
Rys. 9.2
9.130.
CU
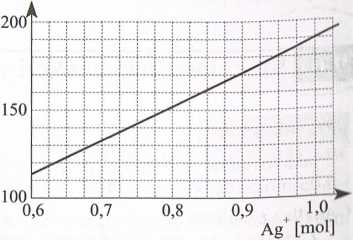
|Do wodnego roztworu pewnej soli typu MX (gdzie: M - metal jednowartościo-wy, X - fluorowiec) wkraplano roztwór azotanu srebra i obserwowano wytrącanie się osadu. Wykres na rysunku 9.3 przedstawia zależność masy wytrąconego osadu od liczby moli dodawanych jonów srebra. Ustalić wzór substancji, która wytrąciła się w formie osadu. Rys 9 3
| Do wodnego roztworu trójhydronowego kwasu wkraplano 0,3-molowy roztwór jedno wodorotlenkowej zasady, aż do uzyskania obojętnego odczynu. Wykres na rysunku 9.4 ilustruje zależność objętości roztworu zasady od objętości zobojętnionego roztworu kwasu. Obliczyć stężenie molowe kwasu.
9.131.
40
30
10 20 30 40
Rys. 9.4
3,
roztwór kwasu [cm J
9.132.
| Do 100 cm3 0,2-molowego roztworu azotanu srebra dodano 100 cm3 0,1-molowego roztworu kwasu siarkowego. Obliczyć masę wytrąconego osadu, jeżeli rozpuszczalność siarczanu srebra wynosi 0,8 g (w temperaturze, w której wykonano doświadczenie).
* KKiflEMI Ile gramów chlorku baru należy dodać do roztworu, w którym rozpuszczono 1,5 g mieszaniny siarczanu sodu i siarczanu żelaza(III), aby mieć pewność, że użyto nadmiaru chlorku baru, niezbędnego do całkowitego wytrącenia osadu?
Wyszukiwarka
Podobne podstrony:
CCF20111021�002 ■im /.iiiics/ano parami roztwory następujących soli: l’b(NOj)2, K..>S, ZnS04 i Na
CCF20111022�004 I Zmieszano parami roztwory następujących soli: Pb(N03)2, K2S, ZnS04 i NaL (w 6 możl
CCF20111022�004 I Zmieszano parami roztwory następujących soli: Pb(N03)2, K2S, ZnS04 i NaL (w 6 możl
CCF20111122�009 BELKA WYMIAN OWA - e B&UcA IAIWMiAHOIMA -KOt-O KO Mi NA i.p OpC,IA2&NIA St
CCF20120531�002 Pieczywo mieszane produkowane jest z mąki pszennej, żytniej soli i innych dodatków,
IMG#16 *8- 1 mi Mod> i zobojętniając roasrwor. a następnie <k*>cłiuajac d
IMGF35 (3) 6. Napisać nazwy następujących soli z uwzględnieniem systemu Stocka, Ew
HPIM5126 Projektując sprzęgło łubkowe, należy przestrzegać następujących zaleceń L» 3rf + 40mm,
DSC00109 (21) ZAt/10/1 I. Napisać reakcje hydrolizy ( równania jonowe) następujących soli: ńarczaa(V
P1013881 Przechodząc do równań skalarnych otrzymamy trzy następujące równania: x+M -O r!} +/£ * =0
więcej podobnych podstron