Chemia0001

Praca semestralna II semestr, chemia
Praca semestralna II semestr, chemia
Zad 6 (lp)
Miarą dysocjacji słabych kwasów jest ich stała dysocjacji. Uszereguj kwasy od najsłabszego do najsilniejszego: HC104 (2,82-10'2), HC10 (2,95-10'8), HCN (6,03-10‘10), HN02 (5,13-10'4).
Zad 7 (2p)
Zapisz równanie reakcji chemicznej przebiegającej między dowolnym triglicerydem i wodorotlenkiem sodu:
Zad 8 (lp)
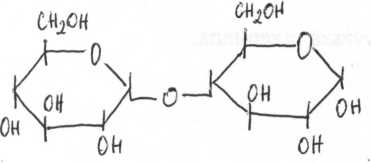
Podczas hydrolizy dwucukru maltozy o wzorze.
otrzymamy:
a) 1 cząsteczkę glukozy i 1 cząsteczkę fruktozy c) 2 cząsteczki glukozy
b) 1 cząsteczkę sacharozy d) 2 cząsteczki fruktozy
Zad 9 (3p)
Tlenek manganu (IV) powstaje w wyniku reakcji:
2KMn04 + 3K2S03 + H20 2Mn02 + 3K2S04 + 2KOH
Określ stopnie utlenienia manganu i siarki przed i po reakcji oraz wskaż utleniacz i reduktor.
|
stopnie utlenienia |
przed reakcją |
po reakcji |
|
Mn | ||
|
S |
|
utleniacz | |
|
reduktor |
Zad 10 (lp)
Wybierz roztwór, w którym stężenie jonów wodorowych jest największe: a) [OH"] = 10'2 b) [OIT] = KT4 c) [OK] = IV6 d) [OH] = 10'8
Zad 11 (2p)
Wskaż równania reakcji, w których, zgodnie z teorią Bronsteda - Lowryego woda zachowuje się jak kwas, a w których jak zasada.
a) H20 + NH3 o NH4 4 OH ........................................................
b) H20 + HC1 H30+ + Cl' ........................................................
c) C032' + H20 o HC03' 4- oh- ........................................................
d) HS04' 4- H20 o h3o+ 4- S042' ....................!..................................
e) OK + H30+ o 2H20 .......................................................
Wyszukiwarka
Podobne podstrony:
81380 Rozdział II Funkcje trygonometryczne Zad ? 93 4. Miara łukowa kąta nieskie
2ba0d06cc2f62fd43bfdea72b7b480a9 PRACA KONTROLNA KASA 1 (semestr drugi) Zad. 1 Wiedząc że łF(x) = 3x
ROK IV Semestr VII - zimowy Lp. Nazwa kursu Wymiar Punkty Realizator Kod kursu 1. Praca
2ba0d06cc2f62fd43bfdea72b7b480a9 PRACA KONTROLNA KASA 1 (semestr drugi) Zad. 1 Wiedząc że łF(x) = 3x
Praca kontrolna nr 2 semestr III Zad 1. Dana jest funkcja kwadratowa/(x) = —2x2 + 12x — 10: a)
NAUKI O RODZINIE II rok, III semestrrok 2010/11 Lp. Nazwa przedmiotu 1. godz. C 1.
ROK II Semestr III - zimowy Lp. Nazwa kursu Wymiar Punkty Realizator Kod kursu 1. Równania
ROK II SEMESTR III IZR Lp. Przedmiot Kod Godzin w sem. Godziny za eć w
Rok II, semestr III (zimowy) Lp. Nazwa przedmiotu Forma
Rok II, semestr IV (letni) Lp. Nazwa przedmiotu Forma
ROK II SEMESTR III EIP Lp. Przedmiot Kod Godzin w sem. Godziny za eć w
ROK II SEMESTR III EIP Lp. Przedmiot Kod Godzin w sem. Godziny za eć w
II Semestr: I ROK STUDIÓW LP RODZĄ) NAZWA MODUŁU KSZTAŁCENIA ZAjĘĆ O/F
Rok IV SEMESTR VII /ESOiO/ Lp. Przedmiot Kod Godzin w sem. Godziny zajęć
SEMESTR IBIOCHEMIA I BIOFIZYKA Lp. TEMATY Główne czynniki odpowiedzialne za powstawanie chorób
więcej podobnych podstron