img084 4

Piśmiennictwo
1. Allen J.W. i wsp. 2002. Engincering livcr therapies tor the futurę. Tiss. Engin., 8, 725.
2. Ellis A J. i wsp. 1996. Pilot- Controlled trial of extracorporeal Iiver assist tlcvice in acute livi'i failurc. Hepatology, 24, 1446.
3. Fisher R.A. i wsp. 2006. Humań hepatocyte transplantation worldwide rcsults. Transplanlation 82.441.
4. Habibullah C.M. i wsp. 1994. Humań fetal hepatocyte transplantation in patients with fulminal hepatic failure. Transplant.58, 951.
5. Mi to M. i wsp. 1992. Hepatocyte transplantation in nian. Transplant. Proc. 24, 3052.
6. Morsiani E. i wsp. 2001. Long- term expression of highly differentiated functions by isolatei porcine hepatocytes perfused in a radial- flow bioreactor. Artif. Org. 25,740.
7. Morsiani E. i wsp. 2002. Early cxperiences with a porcine hepatocyte-based bioartificial liver in acute hepatic failure patients. Int. J. Artif. Organs. 25, 192.
8. Ohashi K. i wsp. 2001. Hepatocyte transplantation: clinical and experimential application. .1 Mol. Mcd., 79, 617.
9. Rubik J. i wsp. 2004. Dializa albuminowa jako nowa metoda pozaustrojowej eliminacji toksyn, Stand. Mcd., 3, 346.
10. Sauer I.M. 2003. Clinical extracorporcal hybrid livcr support- phase 1 study with primary porcine livcr cells. Xenotransplant., 10,460.
ll.Stangc J. 1999. Molecular absorbent recycling system (MARS): clinical results of a ncw membrano bascd blood purification system for bioartyficial liver support. Int. J. Artif. Organs., 23,319.
12. Stockmann H.B. i wsp. 2002. Prospect fort he lemporary treatment of acute livcr failure. Eur. .1 Gaslroentcrol. Hepatol., 14, 195.
13. Stront S.C. i wsp. 1999. Hepatocyte transplantation for the treatment of human disease. Scmin Liver Dis.. 19, 39.
14. Watanabc F.D. i wsp. 1997. Clinical cxpericncc with a bioartificial liver in the treatment ol severc livcr failure. A phase I clinical trial. Ann. Surg., 225, 484.
Uo/dzial 11.
WSPOMAGANIE REGENERACJI MIĘŚNIA SERCOWEGO
Arkadiusz JundzM, Maciej Dąbrowski
1. Wstęp
Układ sercowo-naczyniowy zaopatruje tkanki całego organizmu w tlen i I mibstancje odżywcze. Centralną pozycję tego układu zajmuje serce, które w I warunkach fizjologicznych swoją ciągłą pracą gwarantuje przepływ krwi przez ■naczynia krwionośne.
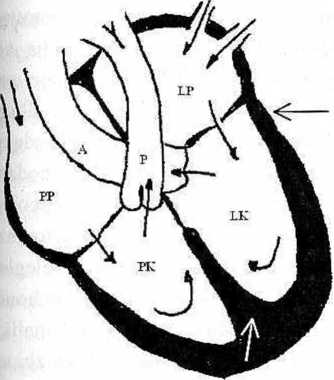
Ryc. 11.1. Schemat budowy serca. PI’ prawy przedsionek, PK - prawa komora, P — pień płucny, A - aorta, LP - lewy przedsionek, LK - lewa komora. Strzałki wskazują docelowe miejsce przeszczepu komórek w obrębie mięśnia sercowego (czarna - mięsień lewej komory, biała -przegroda międzykomorowa)
Mięsień sercowy zaopatrywany jest w krew przez tętnice wieńcowe. Do niedokrwienia lub martwicy części mięśnia sercowego
może dojść w wyniku istotnego zwężenia lub zamknięcia tętnicy wieńcowej.
Serce kurczy się około 70 razy/min w spoczynku, przyspieszając nawet do 200 skurczów/min w czasie wysiłku. Ilość pompowanej krwi wzrasta z 5 1/min do 20 1/min przy wysiłku. Każdy skurcz przedsionków, a potem komór jest inicjowany w węźle zatokowo-przedsionkowym, zlokalizowanym w mięśniu
I
Wyszukiwarka
Podobne podstrony:
Slajd51 (65) Modyfikacja intensywności dawki (IMRT) Hurkmans i wsp. 2002, Cho i wsp.
skanowanie0019(1) II,Klanie ukończone w 2002 roku w Danii [Larsen i wsp. 2002) poświęcone było oceni
DESIGNED FOOD [2011] (0,41% i 0,43%) oraz Abhayawicka i wsp. [2002] (0,4-0,58%). Procesy termiczne z
81101 Slajd51 (65) Modyfikacja intensywności dawki (IMRT) Hurkmans i wsp. 2002, Cho i wsp.
Piśmiennictwo: 1. Szubert P. i wsp.: Analiza czynników predysponujących do powikła
POLECANE PIŚMIENNICTWO 1. Allen B. G.. Wdlsh Af. Pr The biocbcmicaJ basis of ihe r
81101 Slajd51 (65) Modyfikacja intensywności dawki (IMRT) Hurkmans i wsp. 2002, Cho i wsp.
VII. PIŚMIENNICTWO Ahlborg G. L. P. Felig. Lactate and glucose exchange across the forearm, egs, and
56 (314) 3.3.6. Therapy for the extensor indicis. Starting Position: P: Supine; forearm flexed and f
57 (309) 3.3.7. Therapy for the extensor digitorum communis. (Middle finger only). Starting Position
58 (288) 3.3.8. Therapy for the extensor digiti minimi. Starting Position: P: Supine; arm flexed app
59 (281) 3.3.9. Therapy for the supinator. Starting Position: P: Supine; arm flexed approx-imately 9
60 (279) 3.3.10. Therapy for the extensor carpi ulnaris. Starting Position: P: Supine; arm flexed ap
61 (266) 3.3.11. Therapy for the flexor carpi ulnaris. Starting Position: P: Supine; arm flexed appr
62 (264) 3.3.12. Therapy for the flexor carpi radialis. Starting Position: P: Supine; arm flexed app
64 (249) 3.3.14. Therapy for the pronator teres, humerał head. Starting Position: P: Supine; arm fle
65 (244) 3.3.15. Therapy for the pronator teres, ulnar head and the pronator quadratus. Starting Pos
66 (236) 3.3.16. Therapy for the palmaris longus. Starting Position: P: Supine; shoulder abducted an
69 (223) 4.2.1. Therapy for the extensor pollicis longus. Starting Position: P: Supine; upper arm an
więcej podobnych podstron