P1183093
RACKMtn HYDUOCHWWHMIM
H OH
JL X CH»
H CM,
ęjgcwo
(lso-nj)
"** WNN ObM; po m-
■*•.!%* da wyłamania
U1UD0ŚĆ
ftflMŚdć 0»150g mśtmrncp badanej w 50 mL mmudm (9t%) <X> t itśat ljt mL tmwm tthmg» (B,Qj mm. WykamŁ mm-
ndamM fM^ataycae (2JL20) roztworem wtoraMu mduRklmil) RM Odczytać ntojĘcIi dadaaąpoaMĘdiy 2 punk -
I mL mmmm wodorotlenku sodu (0.1 moUl) RM odpowiada 20.17 ag uMurowodorku efedryny (C^H^CTNO)
HZBCHOWYWANIE
zanieczyszczenia Mmmayrnaum* indywidualnie określane: A. im wykrywalne zanieczyszczenia (następujące substancje, je-fcfi a obecne w wystarczającej ilości, mogą być wykryte w jed-■ya z badmk podaiyd) w monografii Są ograniczone przez ogólne taylaaa akceptacji <fla ornych tub meokreśianych indywidualnie ■Moyocad i/łd> przez monografię ogólną Camom ad mtm phamocewticum (2034). Nie jest więc konieczne identyfikowanie ijiI i—i ijih nil nr rrhi wykazania zgodności substancji Patrz tafcie 5.1A Kontrola zanieczyszczeń w substancjach do celów far-macm*vczMvch\ B
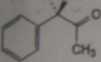
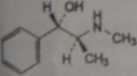
fc, (l£2S)r2-(raelytoammo)-1 -fenylopropan-1 -ol
Ffpewdwfcdryna).
01/2010:0715 zad—tana (OJ)
CPHEDRINIRACEMICI HYDROCHLORIDUM
Efedryny chlorowodorek racemiczny
Kpktśim hydroddoride, rocemlc; Śphśdrine (chlorhydrate d) mdadąae i anancjomef. HCf
BUŁ 201,7
DOTMCJA
Ifcdryayrfcśmouiidurta lUtsu ■) zawiera nie mniej nti 99,0% tmsTyiml IfllflH iśdran u intratni (Iftllff) 2 (metyloamino) •Mtaąśapropaa-l-otu, w pnsbUczcntu na wysuszoną substancję
WŁAŚCIWOŚCI
Bidy łub prawie bidy, krystaliczny proszek tato bezbarwne kryfdy, tam rozpuszczalne w wodzie, rozpuszczalne w etanolu (9ó%).
Substancje topi się w temperatura ok. 1ITC
TOŻSAMOŚĆ Thżmumć pierwsza B. E Tożsamość druga A. C.D.E K Skręcałność optyczna (patrz „Badania”).
B. Wykonać badanie metodą absorpcyjnej spektrofotometrii w podczerwieni (2.2.24), porównując z widmem nscuadgufo ehlo-rowodorku efedryny CSP. Substancje do badania przygotować w postaci pastylek.
C. Obejrzeć chromatogramy otrzymane w badaniu substancji pokrewnych. Plama główna na chromatogramie roztworu badane-go (b) wykazuje pollenie, zabarwienie i wielkość zgodną z plamą główną na chrotnatogramie roztworu porównawczego (a).
D. Do 0,1 mL roztworu S (patrz Jadania") dodać 1 mL mufy OD, <L2 mL noęfwon rinmia wadi OD i 1 ml rtpnwpi roatwo-nt -wodorotlenku soda OD. Powstaje fioletowe zabarwienie. Dodać 2 mL eteru etylowego OD i wytrząsnąć Warstwa etatowa jęta purpurowa, a warstwa wodna niebieska.
E. Do 5 mL roztworu S dodać S mL wody OD. Roztwór wykazuje reakcję (a) aa chlorki (2.5.1)
BADANIA
Roztwór S. Rozpuścić 5,00 g substancji badanej w wodh* de-styknmmj OD i uzupełnić takim samym rozpuszczalnikiem do 50,0 mL.
Wygląd roztworu. Roztwór S jest przezroczysty (121) i bez-burwny (2.2.2. metoda U).
Kwasowość łub zasadowość Do 10 mL roztworu S dodać 0,1 mL mątwom czerwieni metylowej OD i 0,1 mL mątwom wo-Jororienku sodu (0,01 mol/L) RM. roztwór jeat Żółty Dodać 0.2 ml kwam solnego (0,01 moi/L) RM, roztwór jest czerwony.
Skręcało ość optyczna (2.2.7): +0.2* do -0,2°; do wykonania bartanśa utyć roatworu &.
Substancje pokrewne. Wykonać badanie metodą c la omatografii cienkowarstwowej (2.2.27), używając płytki pokrytej idem krzemionkowym G OD.
Roztwór badany (a). Rozpuścić 0,20 g substancji badanej w metanolu OD i uzupełnić takim samym rozpuszczalnikiem do 10 mL.
Roztwór badany (b). Uzupełnić 1 mL roztworu badanego (a) metanolem OD do 10 mL.
Roztwór porównawczy (a). Rozpuścić 20 mg rocemicznega chlorowodorku efedryny CSP w metanolu OD i uzupełnić takim samym rozpuszczalnikiem do 10 mL.
Roztwór porównawczy (b). Uzupełnić I mL roztworu badanego (a) metanolem OD do 200 mL Nanieść oddzielnie na płytkę po 10 pL każdego roztworu. Chro-matogrum rozwinąć na odległość 15 cm używając mieszaniny 5 objętości chloroformu OD, 15 objętości stężonego wodorotlenku amonowego OD i 80 objętości 2 propanolu OD. Pozostawić płytkę do wysuszenia na powietrzu. Spryskać roztworem mnkydryny OD i ogrzewać 5 min w temp. 110“C. Żadna plama na chromatogramie roztworu porównawczego (a), poza plamą główną, nic jata intensywniejsza niż plama na chromatogramie roztworu porównawczego (b) (0,5%). Pominąć każdą plamę o jaśniejszym zabarwieniu niż tło.
Siarczany (2.4.13). IS mL roztworu S spełnia wymagania oznaczenia granicznego zanieczyszczenia siarczanami (100 pg/g).
Strata masy po suszeniu (2.2.32). Nic więcej niż 0,5%, po suszeniu 1,000 g substancji badanej w suszarce w temp. 105°C.
Popiół siarczanowy (2 4.14) Nie więcej niż 0,1%; do wykonania badania użyć 1,0 g subtaancji badanej.
ZAWARTOŚĆ
Rozpuścić 0,170 g substancji badanej w 30 mL etanolu (96%) OD Dodać 5,0 mL kwasu solnego (0,01 mol/L) RM. Wykonaćmia-irirtirąmńa potencjosoetrycztie (2 2 20) i kywając roztworu wodo-
2201
Strona 15 z 19
Wyszukiwarka
Podobne podstrony:
36774 Obraz39 (5) ♦ Ca (OH) 3 2 M,0 CaCl. Ł ąig^CH-CM, fcovy i 5<>n wodorowy tworząca chlorowo
page0223 TABLICA XXVIII6. Wykaz oh winiony ch i skazanych przez sądy pokoju w Guberniach Zachodnich
HOCH— CHOH—CH,OH H,C=C—C=CH- C(CH,OH), 2
Kolokwium CHj-OH CHrOKOj
Scan0026 (4) Krew Cytozol Rumi
UNIWERSYTET OTWARTY SGGW SERDECZNIE ZAPRASZA NA SKUTECZNE biologia chemia . o . sCV ,OH ■c ch CH, he
JPj 7 kw/jl&ĄUtAsi cM*j & ;u
DSC04532 (3) ch2-c nh2 p OH Gly O CH,—CH-Cf Ala CH3 J> CH—CH—cr CHs^ nh2 OH ValAMINOKWASY
73121 skanuj0003 A, Sc Je an OH OH OH N B, Jon wodorkowy; h h CM© ‘
ho- CH ~CH - COOht I (5cr) CM JCH-CH - CM - CoOff (Ją / i, i ItUUjnCt ( Cm,
więcej podobnych podstron