319
64. DESTYLACJA OKRESOWA ROZTWORÓW WIELOSKŁADNIKOWYCH 319
Dzielimy przez siebie obie strony równania i uwzględniając, zależność [X-21b], całkujemy w granicach od Ap do Ah i Bp do Bk.
Stosując takie postępowanie również dla innych par składników, ostatecznie otrzymamy związki
D
Dl
n+l
*AB
irAC
N,
n+l
lAN
„ , [X-23]
>p / w \ *-*p / w \ /w \ -Np
Z równania powyższego, znając zawartości składników w surowcu Ap, Bp, Cp... oraz założywszy ilość składnika wybranego, np. Ah w cieczy końcowej, znajdujemy zawartości wszystkich pozostałych składników Bfc, Cfc,... Następnie obliczamy ilości oddestylowane Aa = Ap—Ah itd. Stąd znajdujemy ilości cieczy wyczerpanej i destylatu
B
[X-24]
[X-25]
W — ... +Nfc
D = S-W = AO+BO+CD+ ... +Nd oraz udziały składników w obu produktach.
b. Powrót li skończony
Zasadnicze równanie, podane przez Gillilanda3, jest analogiczne do równania [X-23]; różne są tylko wykładniki potęgowe. Równanie ma postać
Ak
A
w
B,
B
aŚT
AB
c
(**-]
{fiśr)
Hi \»+ł AC
£
[X-26]
W
W
gdzie: aśr
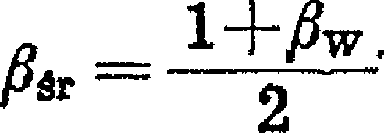
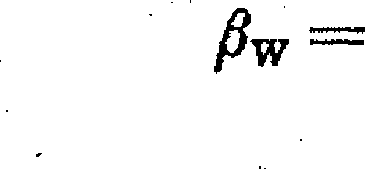
Dxp
Lxw
Dxnd
Lxnw
[X“27]
[X-28]
[X-29]
Współczynniki a§r, /?źr i /3W obliczamy kolejno dla każdego składnika, odnosząc je dó składnika porównawczego, np. najmniej lotnego N. Występujące w równaniu [X-29] udziały w destylacie poszczególnych składników określa wyrażenie
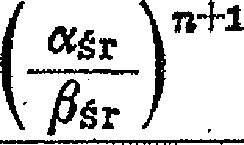
Xy?
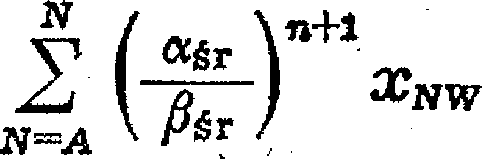
[X-30]
4
Wyszukiwarka
Podobne podstrony:
242 VII, DESTYLACJA FRAKCYJNA ROZTWORÓW WIELOSKŁADNIKOWYCH 11. Holland C. D.:
+Q + V FF= Jeżeli teraz obie strony równania podzielimy przez q, otrzymamy nową wi
12 - Mnożymy obie strony równania 9 i 10 przez odległość biegunową planu sił /H= EJ /,należącego do
Układ nieliniowy SC zCn "J* I Rys. 10 Fig. 10 Ozislęc obie strony równania przez Cp oraz uwzglę
Wreszcie dzieląc obie strony równania przez (1+ r) uzyskujemy standardowy postać międzyokresowego
W tyin celu rozdzielimy zmienne dzieląc obie strony równania najpierw przez 2x2, x * 0 co daje nam —
/ 322 X. DESTYLACJA FRAKCYJNA OKRESOWA udziałów na półkach. Dla roztworów wieloskładnikowych można
/64 II. PODSTAWY FIZYKOCHEMICZNE DESTYLACJI ( • t t Entalpia roztworu ciekłego wynosi zatem (bez
skanuj0025 (29) Dobry dla partii środka. Zamiast przez kolejne liczby naturalne, dzielimy przez: 1,4
img032 (64) zani na wypijanie ilitra tranu dziennie przez okres trzech lat, co jak wiadomo, nie nale
więcej podobnych podstron