skanuj0008

|
b) |
213 | ||
|
R |
I IOI \ |
i |
V§ i |
|
i R |
i R |
i R |
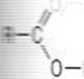
Rys. 3.19. Wiązania wadoro--we między cząsteczkami kwasów karboksylowych; a} z udziałem dwóch cząsteczek kwasu, b) z udziatem wielu cząsteczek kwasu


Rys. 3.20. Modele cząsteczek kwasów: a) octowego (etanowego), b) stearynowego (oktadekanowego)

Fot. 3.4. Wyniki reakcji kwasu octowego z tlenkiem miedzi(ll)
Doświadczenie 3.19. Badanie właściwości kwasu octowego ' Zbadaj za pom.Gcą papierka wskaźnikowego odczyn wodnego rozporu kv/asu octowego. O czym on świadczy?
I Do probówki zawierającej 5 cm3 50-procentowego roztworu kwasu octowego -wrzuć kilka opiłków magnezowych. Cc obserwujesz? Napisz ■ównanie zachodzącej reakcji.
3. Do probówki zawierającej 5 cm3 50-procentowego roztworu kwasu octowego dodaj szczyptę tlenku miedzi(ll) i ogrzewaj przez parę minut w promieniu palnika (fot. 3.4). Co obserwujesz? Napisz równanie zachodzącej reakcji.
4. Do 2 cm3 roztworu wodorotlenku sodu 0 stężeniu ok. 1 moi.‘dm3 dodaj kilka kropli fenotoftaieiny i wkraplaj powoli 10-procentowy roztwór kwasu octowego. Zaobserwuj zmianę barwy wskaźnika. Jaka reakcja zaszta w tym doświadczeniu? Napisz je) równanie w formie cząsteczkowej i jonowej.
5. Do 10-procentowego roztworu kwasu octowego dodaj szczyptę starego wodorowęglanu sodu. Co obserwujesz? Co można powiedzieć na tej podstawie o mocy kwasu octowego? Napisz równanie zachodzącej reakcji.
6. Zbadaj odczyn i zapach wodnego roztworu octanu sodu. O czym świadczą otrzymane wyniki? Spróbuj wyjaśnić je za pomocą równania odpowiedniej -reakcji.
Doświadczenie 3.20. Badanie właściwości kwasu stearynowego
1. Zbadaj właściwości fizyczne kwasu stearynowego: stan skupienia, barwę, zapach i rozpuszczalność w wodzie i w benzynie.
2. Do 2 cm3 5-prccentowego roztworu wodorotlenku sodu dodaj kilka kropli fenotoftaieiny i ok. 0,5 g kwasu stearynowego, po czym ogrzewaj ostrożnie w płomieniu palnika. Zanotuj obserwacje i napisz równanie zachodzącej reakcji.
Wyszukiwarka
Podobne podstrony:
skanuj0078 2 Pomiary twardości 79 Rys. 5.19. Młotek Poldiego Rys. 5.20. Zasada pomiaru metodą Poldie
Rozprężanie swobodne Rys. 19.16. Otwarcie zaworu między dwiema komorami powoduje
skanuj0014 (213) Rys.17-28. Ruch dyHeiny^powod uje . wyginanie się wici.JelRfztwnętrzną parę m
skanuj0131 (13) *) Rys. 6.19. Schemat połączenia śrubowego w zbiorniku ciśnieniowym;
skanuj0413 padania wiązki (kąt ugięcia) można napisać (zgodnie z rys. 4.19) oraz 2sin0 h = -jt 4.I.I
skanuj0411 Rys. 19. Schemat blokowy formułowania strategii typu OT-»SW Zasadnicze znaczenie dla powo
skanuj0009 resize J/O 19.6.3. NAKRĘTKI a) b) Ryś. 19.6.8. Nakrętki sześciokątne: a) przedstawienie z
skanuj0024 2 Statyczna próba rozciągania 23 Rys. 1.19. Maszyna wytrzymałościowa ZD-40 6.
46657 skanuj0138 (12) 256 B. Cieślar 256 B. Cieślar 6.19. Dane: rys. 6.19.1. Rozwiązanie Jx# = 78a4;
3tom301 9. INSTALACJE ELEKTRYCZNE 604w _2 ® vO A® vO v® ®I] II UOOT[]o Vo Ao & Rys. 9.19.
więcej podobnych podstron