Image6 (50)

16 Rozwiązania zadań ze zbioru "MENDLA"


Odp.: Średnia prędkość cząsteczek gazu równa się 501—.
s
Zadanie 544 str.108
Dane:
V = Ofibrr?
Szukane:
Ekśr=?
n = 0,12kmol= 120 moli p = 6-106 Pa Na = 6,023-1023
Z podstawowego wzoru teorii kinetyczno-molekularnej ciśnienie wywierane przez cząsteczki przedstawimy w postaci:
2 N
P = 3-V'Ekśr /3'V
3 • p • V = 2 • N • Ekśr /: (2 • N) 3PV 2 • N kśr
Liczba N cząsteczek gazu jest równa iloczynowi liczby moli substancji n i ilości cząsteczek w jednym molu N = n Na, więc po podstawieniu:
Pamiętamy, że Pa = —r
rrr
Jednostki

3 6- 106 • 0,05 _ 0,015 • 106
2 • 120 • 6,23 • 1023 ” 241 • 1023
Ekśr = 0,0006224-10'17 = 6,224-10"21 J
Odp.: Średnia energia kinetyczna ruch wynosi 6,224 10 21J.
i
Zadanie 545 str.108
Dane: Szukane:
p _ 10~5Pa d = ? - średnia odległość między cząsteczkami gazu
Objętość średnia przypadająca na jedną cząsteczkę wynosi: V
V0 = — , gdzie N - liczba cząsteczek.
pierwiastkiem

Zakładając, że każda cząsteczka zajmuje sześcian o krawędzi d można napisać:
V0 = d3
V
Po podstawieniu V0 = ^ mamy: ° N
Pierwiastkując obie strony trzeciego stopnia otrzymamy:
N
Z równania gazu doskonałego otrzymamy:
/: k
n = łv k-T
Po podstawieniu będzie:
dśr =

ale T = t + 273K
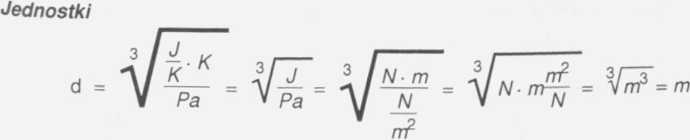
* - Zeszyt 5
Wyszukiwarka
Podobne podstrony:
54330 Image2 (75) 8 Rozwiązania zadań ze zbioru "MENDLA Odp.: Średnia prędkość cząsteczek wynos
Image6 (49) 66 _Rozwiązania zadań ze zbioru "MENDLA"_ Za pi i P2 oraz objętość podstawiamy
69485 Image43 (19) 173 Rozwiązania zadań ze zbioru "MENDLA " k = n • R • T n- R T-W Odp.:
Image43 (19) 173 Rozwiązania zadań ze zbioru "MENDLA " k = n • R • T n- R T-W Odp.: Szukan
Image11 (42) 76 Rozwiązania zadań ze zbioru "MENDLA" Zgodnie z przemianą izotermiczną dla
Image43 (19) 173 Rozwiązania zadań ze zbioru "MENDLA " k = n • R • T n- R T-W Odp.: Szukan
Image46 (16) 179 Rozwiązania zadań ze zbioru "MENDLA —Zadanie 684 str.136Dane: Q = 100 kJ W = 6
więcej podobnych podstron