IMGX08 (4)
5 Kuwety są prostopadłościennymi naczynkami ze szkła lub kwarcu. Materiały tg I są bardzo odporne na działanie chemikaliów i ich stosowanie jest niewspółmiernie I mniej kłopotliwe niż materiałów używanych w spektroskopii podczerwieni. Kuwety mają stałą, znaną grubość warstwy.
Wiele przyrządów ma oprócz skali transmisji również skalę logarytmiczny log (1/T) = D. Wielkość D nazywa się gęstością optyczną.
5.4.2. Metodyka spektroskopu obszaru widzialnego i nadfioletu
Spektrofotometr rejestruje widmo jako funkcję T = f(v), D - f(v) lub T=f(A). Cechowanie skali częstości (długości fali) odbywa się na podstawie rejestracji widma substancji o dokładnie znanych położeniach pasm absorpcyjnych. Przykładowo podano na rys. 5.14 widmo jako funkcję T = f(v).
350Atnml
200
250
300
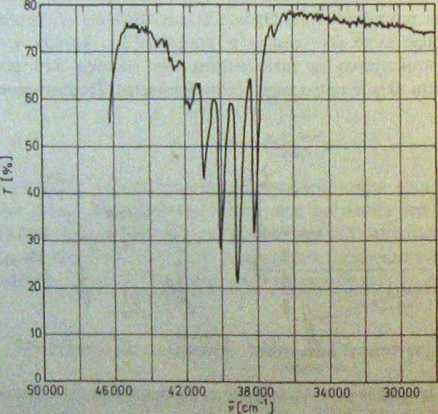
Rys. 5.14. Pasmo elektronowej absorpcji benzenu rozcieńczonego n-helcsanem w stosunku objętołdowys j: 1000, grubość warstwy 2 mm. Widmo uzyskano względem n-heksanu w wiązce porównawczej. Z»na ; u-.-agę struktura oscylacyjna pasma elektronowego, w której odległości składowych około 970 as'1 odzwierciedlają odstępy energetycznych poziomów oscylacyjnych pulsacyjnego drgania pieródcoi* benzenu we wzbudzonym stanie elektronowym (por. rys. 5.23 i 5.24) (widmo uzyskane dzięki uprzejmota I dr Jadwigi Rzeszotattkiej z Wydziału Chemii Uniwersytetu Warszawskiego)
Widma UV -V1S uzyskuje się przeważnie dla substancji w roztworach, określą# : T względem czystego rozpuszczalnika jako wzorca. Jako rozpuszczalniki stosowani! j są cykloheksan, n-heksan, izooktan, metanol, etanol, woda, acetonitryl, chloroform j dioksan r inne. Nie używa się benzenu i jego pochodnych, ponieważ absorbują ow w obszarze k < 280 nm, trzeba też uważać, by nie stanowiły one zanieczyszcza, w używanych rozpuszczalnikach.
Intensywność pasm określa się po odpowiednim przeliczeniu opartym na prawie 6.4 Lamberta-Beera, a opisanym w punkcie 3.5.2. Po określeniu molowej integralnej intensywności pasma oblicza się moc oscylatora / według wzoru (5.24).
Ze względu na znaczną szerokość i nieforemność pasm absorpcji elektronowej bardzo rozpowszechniony jest pomiar tylko różniczkowej intensywności, czyli współczynnika absorpcji c w maksimum lub nawet na zboczu pasma.
Jednostkami molowej intensywności są jednostki podane w tabl. 3.25.
5.5. Zastosowania spektroskopii elektronowej
Widmo elektronowe odzwierciedla najpełniej strukturę molekuły. W swej naturze jest widmem elektronowo-oscylacyjno-rotacyjnym, przekazuje więc informacje zawarte w widmie rotacyjnym i oscylacyjnym, a ponadto informacje o stanach elektronowych. Można by pomyśleć, że widma rotacyjne i oscylacyjne są niepotrzebne, jeżeli dysponujemy widmem elektronowym. W rzeczywistości jednak widma elektronowe są tak zagmatwane i nieczytelne, że bez informacji o stałych rotacyjnych, o częstościach i anharmoniczności oscylacji trudno byłoby je rozszyfrować.
Pełna struktura pasm elektronowo-oscylacyjno-rotacyjnych może się przejawić tylko wtedy, gdy badana substancja znajduje się w stanie gazowym pod zmniejszonym ciśnieniem. W fazie skondensowanej rotacje są zahamowane, a składowe oscylacyjne pasm są tak rozszerzone, że zlewają się ze sobą. Pasma elektronowe są bardzo szerokie i rozmyte. Ich szerokości połówkowe są rzędu 1000 cm-1.
55.1. Proste molekuły w stanie gazowym
Schemat poziomów energetycznych energii wewnętrznej molekuły dwuato-mowej przedstawiono na rys. 5.15. Przejścia spektralne mogą następować między różnymi poziomami. Ich prawdopodobieństwo uzależnione jest od obsadzenia poziomów wyjściowych i od momentu przejścia. W temperaturze pokojowej przejścia następują z zerowego poziomu elektronowego i jego zerowego poziomu oscylacyjnego (£„, v" = 0), ale z licznych poziomów rotacyjnych, w tej temperaturze bowiem najsilniej obsadzony jest któryś z wyższych poziomów rotacyjnych (por. rya.
2.3), wyższe natomiast poziomy oscylacyjne są obsadzone bardzo słabo (patrz punkt 3.2.1), Przejścia sięgają któregoś z poziomów rotacyjnych któregokolwiek poziomu oscylacyjnego na wzbudzonym poziomie elektronowym Można więc sobie wyobrazić, jak wiele fotonów nieznacznie różniących się wielkością będzie pasowało do różnicy poziomów energetycznych zgodnie z warunkiem hv = AE. Wprawdzie reguły wyboru dotyczące zmian kwantowych liczb v i J ograniczą liczbę przejść, ale nie zmieni to zasadniczo bogactwa możliwości. Reguły wyboru dla molekuł liniowych są następujące:
jpg. i 1, £2, ±X —
AJ = £1 dla pasm równoległych AJ * 0, ±1 dla pasm prostopadłych
(5.25)
185
Wyszukiwarka
Podobne podstrony:
CCF20081202�016 p£>imy przetrwalni ko we są bardzo odporne na niekor/y wpływy otoczenia, np. na d
0000064 2 miast w nieobecności tlenu są bardzo odporne na wysoką temperaturę, dochodzącą nawet do 20
0000064 2 miast w nieobecności tlenu są bardzo odporne na wysoką temperaturę, dochodzącą nawet do 20
IMAG0091 (10) zatem powinny być wykonane ze szkła lub sz-kła orgameznego. hóoch gęstości niewiele si
43jasf14(1) ca titerlcowa1 UI iŁł SE W domu pani Łucji można znaleźć wszędzie ze szkła lub z porcela
strona!4 (2) Oferujemy najwyższej jakości akwaria » dowolnych kształtach wykonane ze szkła lub akryl
Plusy i minusy Wadą ogniw cynkowo-węglowych jest, że są mało odporne na długie przechowywanie a
bardziej, panuje obecnie przekonanie, że to kobiety są bardziej odporne na ból, współczesny mężczyzn
IMG?61 trudnym do wykazania jest fakt, że pozytywna lub negatywna ocena programu reformy ma wpływ na
SL275420 Kolagen Włókna są giętkie, odporne na czynniki mechaniczne Rozpuszczają się w gorącej wodzi
n FORBUILD Podkładki wykonane z tworzywa sztucznego przeznaczone na budowę są również bardzo odporne
więcej podobnych podstron