skan0053
100 A. TRAMER
widma; w środowisku węglowodorowym najniższym stanem wzbudzonym jest rn>n,, podczas gdy w roztworach alkoholowych emisja następuje z poziomu rW(R* [50].
Odwrócenie poziomów może być skutkiem oddziaływań między-cząsteczkowych nie angażujących bezpośrednio grupy czynnej (w tym przypadku karbonylowej). Porter [51] np. wyjaśnia reaktywność 4-hydroksy-benzofenonu odwróceniem poziomów («, n*) i (n, n*), zachodzącym pod wpływem przejścia protonu w wiązaniu wodorowym między grupą hydroksylową badanej substancji i aktywnym rozpuszczalnikiem.
Bardzo charakterystyczny i szczegółowo zbadany jest wpływ wiązań wodorowych na własności stanów wzbudzonych N-heterocykli, w których stan singletowy S„iK, leży nieznacznie poniżej stanu SniK, [52 — 56]. Na przykład chinolina w zamrożonych roztworach węglowodorowych lub eterowych nie wykazuje fluorescencji, a jedynie fosforescencję: z poziomu singletowego S„iK* zachodzi z wysokim prawdopodobieństwem dezaktywacja bezpromienista do stanu trypletowego TntnDodatek niewielkiej ilości alkoholu (ok. 1 %) powoduje silny wzrost wydajności fluorescencji, Qfosfl <2fl = 0,55, nazywany efektem aktywacji fluorescencji [53], W niektórych przypadkach wiązanie wodorowe powoduje niewątpliwie odwrócenie poziomów, w innych mechanizm procesów może być bardziej złożony [57],
Odwróceniu mogą ulec również dwa stany (n, n*), jeżeli w tych dwu stanach energie wiązań wodorowych znacznie się różnią. Naftol-1 jest znacznie mocniejszym kwasem w stanie S2 (La) niż wstanie SX(Lb) lub »S0(A), dlatego też pod wpływem wiązania wodorowego pasmo La przesuwa się znacznie silniej w stronę fal długich, niż pasmo Lb (rys. 12). Z wielkości przesunięć można oszacować energie wiązań wodorowych w stanie podstawowym i przy konfiguracji FC w stanach wzbudzonych; dla kompleksu z dioksanem energie te wynoszą: AHSo = -5,4, AHSl = —5,8 i AHS2= —7,5 kcal/mol, co nie wystarcza na odwrócenie poziomów. Również fluores-cencja kompleksu z dioksanem następuje z poziomu Lb. W trwalszym kompleksie z trójetyloaminą przesunięcie absorpcji jest nieco większe, a widmo fluorescencji całkowicie zmienia charakter: pojawia się silnie przesunięte i rozmyte pasmo odpowiadające zapewne emisji ze stanu La. W roztworach alkoholowych naftolu-1 emisja w temperaturach pokojowych odpowiada przejściu La-+A, natomiast przy r=77°K pojawia się
a) b)
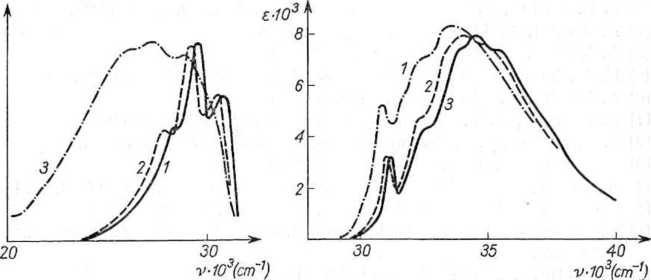
Rys. 12. Widmo absorpcji (a) i fluorescencji (b) naftolu-1 w następujących rozpuszczalnikach: 1 — heksanie, 2 — heksanie + 2% mol. dioksanu, 3 — heksanie + 2%
mol. trójetyloaminy
ponownie przejście A. Efekt ten jest związany zapewne ze stabilizacją silniej polarnego kompleksu w stanie La przez polarny rozpuszczalnik w niskiej temperaturze, gdzie reorientacja cząsteczek rozpuszczalnika zostaje zahamowana, *s2 > ESl. Hipoteza o odwróceniu poziomów została w tym przypadku potwierdzona przez pomiar polaryzacji fluorescencji [59].
Podobny efekt odwrócenia poziomów występuje także, jak się zdaje, w przypadku kompleksów indolu [34] i 1-naftyloaminy [60], przy czym w tym ostatnim przypadku odstęp energetyczny między poziomami S2 i jest na tyle mały, że efekt może nastąpić bez udziału wiązań wodorowych pod wpływem polarnego rozpuszczalnika.
Zjawisko odwrócenia poziomów, a przez to zmiany czasu życia cząsteczki wzbudzonej, ma zasadnicze znaczenie dla foto- i radiochemii układów zdolnych do tworzenia wiązań wodorowych.
LITERATURA *
[1] G. J. Brealy, M. Kasha, J. Am. Chem. Soc., 77, 4462 (1955).
[2] G. C. Pimentel, J. Am. Chem. Soc. 79, 3323 (1957).
[3] K. Nishimoto, J. Phys. Chem., 67, 1443 61963).
Wyszukiwarka
Podobne podstrony:
skan0051 (2) 96 A. TRAMER Znając różnicę energii form (2*) i (4*) w stanie wzbudzonym AE* można, z r
skan0051 (2) 96 A. TRAMER Znając różnicę energii form (2*) i (4*) w stanie wzbudzonym AE* można, z r
skan0051 (2) 96 A. TRAMER Znając różnicę energii form (2*) i (4*) w stanie wzbudzonym AE* można, z r
Układy równań liniowych�5 100 Układy równań liniowych Oznacza to, że rząd macierzy A układu jest rów
31029 srodowisko 27 Najniższa śmiertelna dawka promieniowania jiomzmącegw ,u wuro Odpowiedź: r a 10
P2060239 5 Błędy środowiskowe, związane ze stanem warunków otoczenia w czasie wykonywania pomiaru Wa
skan0049 (2) 92 A. TRAMER Przykładem mogą tu być aromatyczne o-hydroksykwasy, ich estry i amidy [36,
43955 skan0039 (2) Rys. 19. Widma absorpcji onitroacetanilidu (krzywe 1—4) oraz N-metylo-o-nitro-ace
więcej podobnych podstron