I rok INFORMATYKA |
Ryszard Szyłak |
95.03.31 |
Nr 17 |
Temat : Wyznaczanie ciepła właściwego ciał stałych . |
|
1. Opis ćwiczenia.
Do wyznaczania ciepła właściwego używano kalorymetru aluminiowego , zbudowanego z dwu koncentrycznie osadzonych naczyń . Wymiana ciepła zachodziła w naczyniu wewnętrznym . Do kalorymetru należało wprowadzić wodę o temperaturze nieco niższej od temperatury otoczenia .Układ ten
pobierał ciepło , którego źródłem było badane ciało ogrzane do temperatury bliskiej temperaturze wrzenia wody . Z prawa bilansu cieplnego wyliczamy ciepło właściwe badanego ciała .
2. Przebieg ćwiczenia.
1) ważenie części wewnętrznej kalorymetru ,
2) ważenie części wewnętrznej kalorymetru napełnionego do połowy wodą
3) ogrzewanie badanego ciała parą wodną ,
4) włożenie ogrzanego ciała do kalorymetru .
3. Tabela pomiarów.
Badane ciało |
Masa wody i kalorymetru [g] |
Masa badanego ciała [g] |
Aluminium |
213,6 |
36,05 |
Miedź |
190,3 |
118,0 |
Żelazo |
202,3 |
111,0 |
Aluminium :
.
Czas[min] |
0' |
5' |
15' |
25' |
25'43” |
26'13” |
30'13” |
33'13” |
Temp.[oC] |
21,1 |
21,2 |
21,4 |
21,5 |
25 |
25,2 |
25,1 |
25,05 |
Miedź :
.
Czas[min] |
0' |
2' |
3' |
5' |
5'5” |
5'25” |
5'55” |
6'25” |
Temp.[oC] |
14,1 |
14,2 |
14,4 |
14,6 |
18 |
23,3 |
23,8 |
23,6 |
6'55” |
7'25” |
7'55” |
8'25” |
8'55” |
9'55” |
23,2 |
22,8 |
22,6 |
22,3 |
22 |
21,8 |
Żelazo :
.
Czas[min] |
0' |
2' |
3' |
4' |
5' |
5'5” |
5'30” |
6' |
Temp.[oC] |
13,8 |
14 |
14,1 |
14,2 |
14,3 |
16 |
19,3 |
21 |
6'30” |
7' |
8' |
8'30” |
9' |
9'30” |
10' |
10'30” |
11' |
21,7 |
21,9 |
21,8 |
21,6 |
21,4 |
21,3 |
21,2 |
21,1 |
21 |
Masa kalorymetru : 63 [g] .
Temperatury badanych ciał w chwili wkładania do kalorymetru wynosiły :
-aluminium TAl = 99 °C
-miedź TCu= 100 °C
-żelazo TFe= 90 °C
Ciepło właściwe aluminium :
Ciepło właściwe miedzi i żelaza :
Gdzie : - mAl , mCu , mFe - masy badanych ciał
- mw , cw - masa i ciepło właściwe wody
- mk - masa kalorymetru
- t1 , t2 , t3 - temperatury odpowiednio : początkowa układu woda-kalo- rymetr ; końcowa całego układu (woda , kalorymetr , badane ciało) ; początkowa badanego ciała .
4.Błędy i obliczenia .
Błędy względne ciepła właściwego badanych ciał wyznaczono metodą pochodnej logarytmicznej :
W oparciu o powyższe wzory wyliczono błędy bezwzględne Δcx :
|
Aluminium |
Miedź |
Żelazo |
cx [cal⋅g-1⋅K-1] |
0,227 |
0,149 |
0,167 |
Δcx [cal⋅g-1⋅K-1] |
0,072 |
0,023 |
0,028 |
5.Wnioski z ćwiczenia.
Uzyskane wartości ciepła właściwego dla aluminium i żelaza są bardzo bliskie wartościom odczytanym z tablic . Sugeruje to dość dobrą dokładność tej metody na miarę warunków . Z tego wnioskujemy , że poważne odchylenie pomiaru dla miedzi (w porównaniu z wartością tablicową - 0,09 cal⋅g-1⋅K-1 ) może być spowodowane tym , że badane ciało mogło nie być miedzią lub być miedzią domieszkowaną .
Ponadto na błędy pomiarów mogły wpłynąć następujące czynniki :
- ochłodzenie się badanego ciała przy jego przenoszeniu z cylindra do kalorymetru ,
- trudność w jednoczesnym wychwyceniu czasu i temperatury na odcinku gwałtownego skoku temperatury ,
- niedokładności w wyznaczeniu temperatur t1 i t2 spowodowana trudnością dobrania prostej dzielącej odcinek charakterystyki , odpowiadający wymianie ciepła badanego ciała z układem woda-kalorymetr , na dwa równe sobie pola .
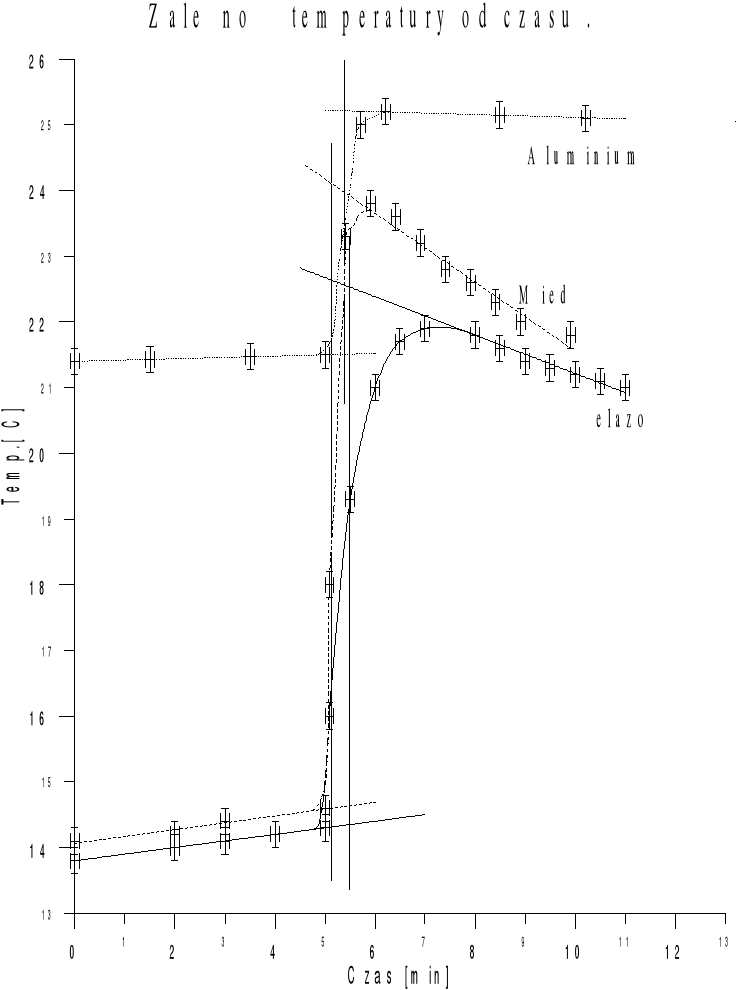
6.Charakterystyka .
Wyszukiwarka
Podobne podstrony:
065S~1, 1 STUDIA - Informatyka Politechnika Koszalińska, Labki, fizyka1, fiza, fizyka
kolos z inf, Studia, Rok I, Informatyka, semestr I
051C~1, 1 STUDIA - Informatyka Politechnika Koszalińska, Labki, fizyka1, fiza, fizyka
1 - wstep, CM UMK I rok, Informacja w zdrowiu publicznym
062C~1, 1 STUDIA - Informatyka Politechnika Koszalińska, Labki, fizyka1, fiza, fizyka
065A~1, 1 STUDIA - Informatyka Politechnika Koszalińska, Labki, fizyka1, fiza, fizyka
063A~1, 1 STUDIA - Informatyka Politechnika Koszalińska, Labki, fizyka1, fiza, fizyka
FERROREZ 4, II rok INFORMATYKA
071B~1, 1 STUDIA - Informatyka Politechnika Koszalińska, Labki, fizyka1, fiza, fizyka
Ćwiczenie2, geodezja, rok I, Informatyka
C & C++ Wyklady Politechnika Wroclawska 1 rok informatyki, W10 wskazniki na tablice wielowymiarowe i
Badanie ferrorezonansu prądów i napięć, Elektrotechnika- Ferrorezonans, II rok INFORMATYKA_
KONDES 2, I rok INFORMATYKA
więcej podobnych podstron