40697 scan001

imię i nizwisko grup*
Kolokwium — Kinetyko i*
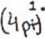
Wyprowadzić róivnanie kinetyczne dla reakcji kontaktowej A ♦ b —p zakłodojoc, źe adsorpcjo 0» A oraz B» P no jednorodnej powierzchni katalizatora. Etopon linitującym szybkość Jest adsorpcjo.
2. Badając spektroskopowo izomeryzację pierwszego rzędu chlorku cis-dwuctylenodwuaninodwuchlorokoboltu (lii) w metanolu, otrzymano następujące dane dotyczące szybkości znikania piku absorpcyjnego odpowiadającego długości fali 540 nn Jako funkcji czasu: czcs/min 0 10 • 20 33 47 62 60 93
ekstynkcja 0,119 0.115 0.108 0,102 0,096 0.0S9 0,081 0,075
Wykazać, źe reakcja Jest pierwszego rzędu i obliczyć dla niej okrc:, połowicznoj przemiany.
M 3. Podaj interpretację czynnika przedwykłcdniczcgo (a) w świetlo teorii zderzeń oraz teorii stanu przejściowego!
4. Wyprowadź równanie kinetyczne dlo reakcji gazowej:
A* -X P
stosując notodę stanu 3tacJonornego. Wyjaśnij mechanizm dla dużych i nolych clćnioń.
S . W temperaturze 414°C bodano rozkład termiczny tlenku etylenu w fazie gazowej:
CH0 - CH_ —> CH. ♦ CO
/ 2
0
mierząc ciśnienie całkowito (p) w różnych odstępach czasu, w.układzie o stałej objętości. Uzyskano następująco wyniki:
czas/min 0 5,0 7,0 9,0 12.0 oo
ciśn.całk. . 116,5 123,0 125.7 128,7 133,0 233
P/mraHg
Wykazać, źo reakcja Jest I rzędu oraz obliczyć stałą szybkości.
W
W
tenporaturzo 414°C bndono rozkład tornlczny tlenku etylenu fazie gazowej)
c„2- cti2 ch4 ♦ CO
X / o
mlerzgc ciśnienia cołkowlte (p) w różnych odstępach czasu, w układzie o 3tałeJ objętości. Uzyskano następujące wyniki:
czas/min 0 5,0 7,0 9,0 12,0 C/O
ciśn.całk. 116,5 123,0 125,7 *120,7 133,0 233
P/mmllg
Wykazać, żo reakcja Jest I rzędu oraz obliczyć stałą szybkości.
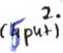
na powierzchni jednorodnej dla A —*- P produktu, gdy otapcm limitującym Jest
Podać równanie kinetyczne przy pomijalnoj adsorpcji etap powierzchniov/y.
d- Wyjaśnij na wykresach 1 wzorach zjawisko outokatalizy.
PołJdd definicję szybkości reakcji kontaktowej oraz definicję ogólny, zalecany przez IUPAC <1968).
czynnik A reakcji rozkładu eteru wlny1 owoety 1 owe go wynosi 11 s l. Obliczyć entropię aktywacji w temp. S30°C 1 skomentować
Ub p
2.7 10 otrzymany wartość.
vjh
Znano dq ntoln szybkoćcl rozkłodu pirydyny w roztworze wodnyn
(reakcjo
I rzędu) w funkcji temperatury
|
t/°c |
0 |
10 |
20 |
30 |
40 |
50 |
|
k/s-1 |
2.46-10_D |
10.0-10"5 |
47.5.10'5 |
163.10-5 |
576.10'5 |
1050.10"5 |
60
Obliczyć energię aktyuocjl.i
5430.10
Wyszukiwarka
Podobne podstrony:
015 4 1. Wyprowadzić równanie kinetyczne dla reakcji kontaktowej A + D
014 4 imię i nazwisko grapa Kolokwium - Klnę tyko 1 Wyprowadzić równanie kinetyczne dla reakcji kon
DSC02179 (2) 7. Rząd reakcji suma wykładników potęgowych stężeń substratu w równaniu kinetycznym, dl
Kolokwium 2. kinetyka 12.05.08 imię i nazwisko [ wt 12 wt 13 śr 10 śr 11
Kolokwium 1. kinetyka 11.04.07 imię i nazwisko grupa 1 2 3 4 1
Kolokwium 2. kinetyka 23.04.07 imię i nazwisko grupa 1 2 3 4 1
Kolokwium 1. kinetyka 21.04.08 1 2 1 3 4 1 5 6 7 L imię i nazwisko
jbgXdA (2) [ 9 06 11 Imię 1 Nizwisko_ Numer indeksu !>jIj Kolokwium z ćwiczeń z Podstaw hilynie
Scan0006 2 (imię nazwisko) (data egzaminu) T* i EGZAMINACYJNY NA PATENT STERAJ KA MOTOROWODNEGO
infa1 Imię i Nazwisko - Grupa Kolokwium z przedmiotu „Technologia Informacyjna” Kierunek: Budownictw
fizyka egzamin 1 Olsztyn 29 03 200/ Imię i nazwisko FIZYKA - KOLOKWIUM GRUPA III Zad 1 &
fizyka egzamin 3 Olsztyn 29 03 2007 Imię i nazwisko f IZYKA - KOLOKWIUM GRUPA II Zad 1 Prom ma przep
więcej podobnych podstron